pH 测量
在许多液体化学过程(工业、制药、制造、食品生产等)中,一个非常重要的测量是 pH 值:测量液体溶液中的氢离子浓度。 pH 值低的溶液称为“酸”,而 pH 值高的溶液称为“苛性碱”。常见的pH值范围从0(强酸)到14(强碱),中间的7代表纯水(中性):
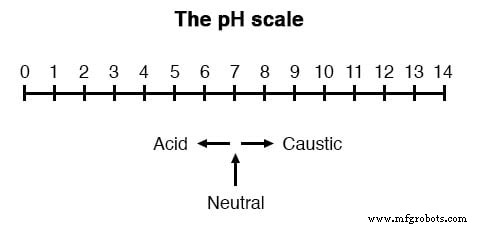
pH 的定义如下:pH 中的小写字母“p”代表负的常用(以十为底)对数,而大写字母“H”代表元素氢。因此,pH 值是每升溶液中氢离子 (H+) 的摩尔数的对数测量值。顺便提一下,“p”前缀也用于需要对数刻度的其他类型的化学测量,pCO2(二氧化碳)和 pO2(氧气)就是两个这样的例子。
对数 pH 值的工作原理如下:10 -12 的溶液 每升 H+ 离子的摩尔数的 pH 值为 12; 10 -3 的解决方案 每升 H+ 离子的摩尔数的 pH 值为 3。虽然非常罕见,但存在 pH 测量值低于 0 的酸和 pH 值高于 14 的苛性碱这样的东西。可以理解的是,此类溶液非常浓缩且 非常 反应式。
pH 电极
虽然可以通过某些化学粉末的颜色变化来测量 pH 值(“石蕊试纸”是高中化学课上常见的例子),但连续过程监测和 pH 值控制需要更复杂的方法。最常见的方法是使用专门制备的电极,旨在让溶液中的氢离子通过选择性屏障迁移,产生与溶液 pH 值成正比的可测量电位(电压)差:
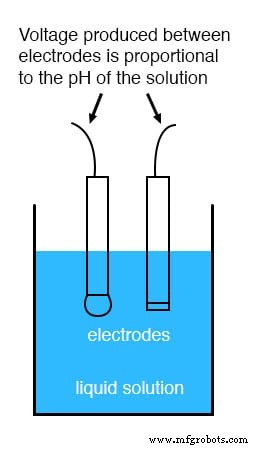
pH 电极的设计和操作理论是一个非常复杂的主题,在此仅作简要介绍。重要的是要了解这两个电极产生的电压与溶液的 pH 值成正比。在 pH 值为 7(中性)时,电极之间将产生 0 伏电压。在低 pH 值(酸性)时,会产生一种极性的电压,而在高 pH 值(腐蚀性)时,会产生相反极性的电压。
测量电极
pH 电极的一个不幸的设计限制是其中之一(称为测量 电极)必须由特殊玻璃制成,以形成离子选择屏障,以从溶液中漂浮的所有其他离子中筛选出氢离子。这种玻璃化学掺杂有锂离子,这使其与氢离子发生电化学反应。当然,玻璃并不完全是您所说的“导体”;相反,它是一种非常好的绝缘体。
如果我们的目的是测量两个电极之间的电压,这会带来一个主要问题。从一个电极触点,通过玻璃屏障,通过溶液,到另一个电极,再通过另一个电极触点返回的电路路径是非常 高电阻。
参比电极
另一个电极(称为参考 电极)由中性 (7) pH 缓冲溶液(通常是氯化钾)的化学溶液制成,允许通过多孔分离器与工艺溶液交换离子,从而与测试液体形成相对低电阻的连接。一开始,人们可能会问:为什么不直接将金属线浸入溶液中以实现与液体的电气连接?这行不通的原因是金属在离子溶液中往往具有高反应性,并且会在金属与液体接触的界面上产生显着的电压。
使用湿化学界面与被测溶液是必要的,以避免产生这样的电压,这当然会被任何测量设备错误地解释为指示 pH 值。
这是测量电极结构的图示。注意产生 pH 电压的掺锂玻璃薄膜:
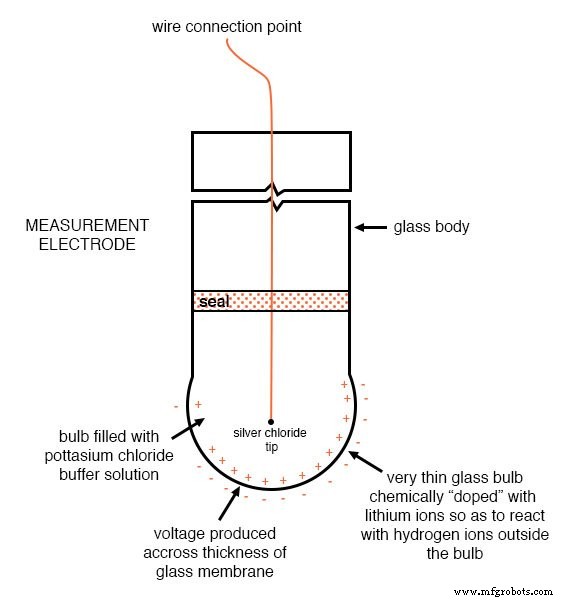
这是参考电极结构的图示。电极底部所示的多孔连接处是氯化钾缓冲液和工艺液体相互接触的地方:
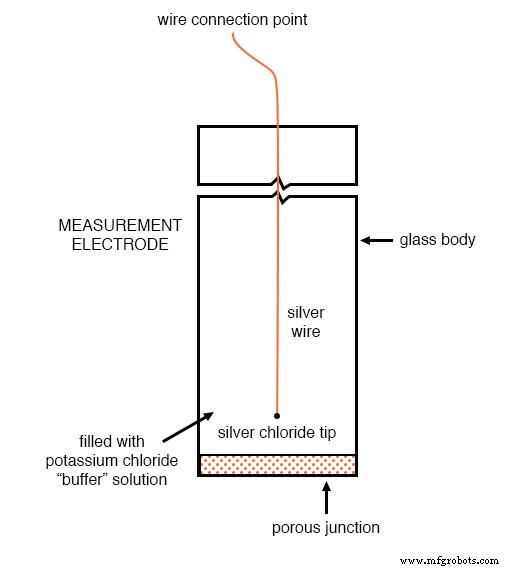
测量电极的目的是产生用于测量溶液 pH 值的电压。该电压出现在玻璃的整个厚度上,将银线放在电压的一侧,将液体溶液放在另一侧。参比电极的作用是为液体溶液提供稳定的零电压连接,从而形成一个完整的电路来测量玻璃电极的电压。
虽然参比电极与测试液体的连接可能只有几千欧,但玻璃电极的电阻可能在 10 到 900 兆欧之间,具体取决于电极设计!因为该电路中的任何电流都必须通过两者 电极的电阻(以及测试液体本身呈现的电阻),这些电阻彼此串联,因此相加以形成更大的总和。
普通的模拟甚至数字电压表的内阻太低,无法在如此高阻的电路中测量电压。典型pH探头电路的等效电路图说明了问题:
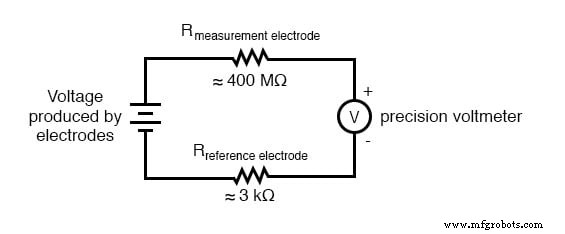
即使非常小的电路电流流经电路中每个组件的高电阻(尤其是测量电极的玻璃膜),也会在这些电阻上产生相对较大的电压降,从而严重降低仪表看到的电压。更糟糕的是,测量电极产生的电压差非常小,在毫伏范围内(理想情况下,室温下每个 pH 单位为 59.16 毫伏)。用于此任务的仪表必须非常灵敏并具有极高的输入电阻。
这个测量问题最常见的解决方案是使用具有极高内阻的放大表来测量电极电压,以便尽可能少地通过电路吸收电流。采用现代半导体元件,输入电阻高达 10 17 的电压表 Ω 可以很容易地构建。另一种在当代使用中很少见的方法是使用电位“零平衡”电压测量设置来测量该电压,而无需绘制任何 来自被测电路的电流。如果技术人员想要检查一对 pH 电极之间的电压输出,这可能是仅使用标准台式计量设备执行此操作的最实用方法:
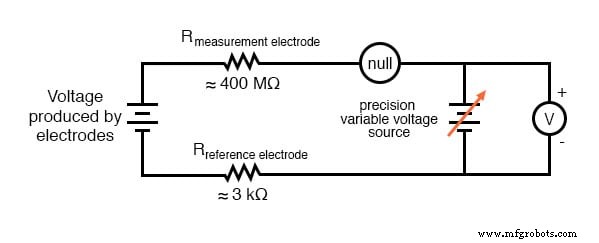
像往常一样,技术人员会调整精密电压电源,直到零位检测器记录为零,然后查看与电源并联的电压表以获得电压读数。当检测器“归零”(准确记录为零)时,pH 电极电路中的电流应该为零,因此任一电极的电阻上都没有电压下降,从而在电压表端子上给出真实的电极电压。
pH 电极的接线要求往往比热电偶接线更严格,需要非常干净的连接和短距离(10 码或更短,即使使用镀金触点和屏蔽电缆)以实现准确可靠的测量。然而,与热电偶一样,电极 pH 测量的缺点被以下优点所抵消:准确度高,技术相对简单。
很少有仪器技术能激发 pH 测量的敬畏和神秘感,因为它被广泛误解且难以排除故障。在不详细阐述 pH 测量的确切化学原理的情况下,这里可以给出一些关于 pH 测量系统的智慧词:
- 所有 pH 电极的寿命都是有限的,寿命在很大程度上取决于使用的类型和严重程度。在某些应用中,一个月的 pH 电极寿命可能会被认为很长,而在其他应用中,相同的电极可能会使用一年以上。
- 因为玻璃(测量)电极负责产生与 pH 成正比的电压,所以如果测量系统未能针对给定的 pH 变化(每个 pH 值大约 59 毫伏)产生足够的电压变化,则该电极被视为可疑单位),或者无法对测试液体 pH 值的快速变化做出足够快的响应。
- 如果 pH 测量系统“漂移”,产生偏移误差,则问题可能出在参比电极上,该电极应该为被测溶液提供零电压连接。
- 由于 pH 值测量是离子浓度的对数表示,因此看似简单的 0-14 pH 值范围代表了令人难以置信的过程条件范围。此外,由于对数标度的非线性特性,顶端 1 pH 值的变化(例如,从 12 到 13 pH 值)并不代表与底端 1 pH 值变化相同数量的化学活性变化(例如,从 2 到 3 的 pH 值)。如果希望控制,控制系统工程师和技术人员必须意识到这种动态 过程 pH 值稳定。
- 以下条件对测量(玻璃)电极有害:高温、极端 pH 值(酸性或碱性)、液体中的高离子浓度、磨损、液体中的氢氟酸(HF 酸会溶解玻璃!)、以及玻璃表面上的任何类型的材料涂层。
- 被测液体的温度变化会影响测量电极对给定 pH 水平(理想情况下为每 pH 单位 59 mV)的响应以及液体的实际 pH。可以将温度测量设备插入液体中,这些设备的信号用于补偿温度对 pH 测量的影响,但这只会补偿测量电极的 mV/pH 响应,而不是过程的实际 pH 变化液体!
pH 测量领域仍在取得进展,其中一些进展有望克服 pH 电极的传统局限性。其中一项技术使用一种称为场效应晶体管的设备 静电测量离子渗透膜产生的电压,而不是用实际的电压表电路测量电压。虽然这项技术有其自身的局限性,但它至少是一个开创性的概念,并且可能在以后证明更实用。
评论:
- pH 是液体中氢离子活性的表示。它是每升液体中氢离子数(以摩尔为单位)的负对数。因此: 10 -11 1 升液体中的氢离子摩尔数 =11 pH。 10 -5.3 1 升液体中的氢离子摩尔数 =5.3 pH。
- 基本 pH 值范围从 0(强酸)到 7(中性、纯水)再到 14(强腐蚀性)。 pH 值低于 0 和高于 14 的化学溶液是可能的,但很少见。
- 可以通过测量浸入液体溶液中的两个特殊电极之间产生的电压来测量 pH 值。
- 一个由特殊玻璃制成的电极称为测量 电极。其工作是产生一个与 pH 值成正比的小电压(理想情况下每个 pH 单位为 59.16 mV)。
- 另一个电极(称为参考 电极)使用被测液体和稳定的中性 pH 缓冲溶液(通常是氯化钾)之间的多孔连接来建立与液体的零电压电连接。这为整个电路提供了一个连续点,以便可以通过外部电压表测量测量电极中玻璃厚度上产生的电压。
- 测量电极的玻璃膜具有极高的电阻,因此必须使用具有极高内阻的电压表或零平衡电压表来测量电压。
工业技术


