硫酸根阴离子对超细二氧化钛成核的影响
摘要
研究了硫酸根阴离子对四氯化钛水解过程中纳米分散二氧化钛合成的影响的现象学模型。有人提出在硫酸根阴离子和八面体配位的 [Ti(OH)h(OH2)6−h] (4−h)+ 之间形成螯合和桥连双齿配合物 单体是锐钛矿相成核的决定因素。
背景
超细二氧化钛在许多不同领域都有广泛的应用前景——从环境导向的光催化系统,如有害有机化合物的降解 [1]、废水净化 [2]、NO x , 所以 x 和空气净化 [3] 到新的工业领域——传感器材料 [4] 和太阳能电池 [5]。相组成、粒径和表面状态是决定 TiO2 催化反应性、光敏性和吸附性能的最重要特征。例如,二氧化钛粒径的减小导致催化活性的迅速增加[6]。同时,二氧化钛的光催化性能对锐钛矿、板钛矿和金红石等TiO2多晶型物的相组成非常敏感[7]。
二氧化钛合成方法的选择及其物理和化学参数的控制是最终组成的至关重要的决定因素。纳米TiO2 的制备可以通过溶胶-凝胶[8]、化学沉淀[9]、微乳液[8] 和水热[10] 方法进行。溶胶-凝胶法是制备纳米氧化物最灵活的技术。主要前体类型、水解条件、反应介质的温度和 pH 值的变化允许控制纳米颗粒的成核和生长。获得的二氧化钛的溶胶-凝胶方法通常基于钛醇盐 Ti(OR)n 水解的反应。将这些昂贵的化学品换成更便宜的前体,如 TiCl4,对于大规模制造纳米尺寸的 TiO2 非常有希望。 TiCl4 应用的一个有前景的优势是通过使用二氧化钛特定相的预测成核,可以进行由附加离子控制的缩聚反应。
本文的目的是研究 SO4 2− 基于TiCl4水解的溶胶-凝胶过程中二氧化钛成核过程中低聚物缩聚和氧化物网络形成的阴离子。
方法
四氯化钛 TiCl4(默克,99.9%;比重 1.73 g/cm 3 在 20°C) 冷却至 0°C 并加入盐酸(36.0% 水溶液)并进一步蒸发氯化氢。 TiCl4与盐酸之比为2:1。在剧烈搅拌下,将碳酸氢钠水溶液滴加到氧氯化钛 TiOCl2 溶胶中,使 pH 值达到 5.0-5.5。在所有 pH 增加过程中观察到凝胶形成。纳米颗粒的悬浮液在 80°C 下保持 3 小时,然后用蒸馏水进一步洗涤以去除 Na + 和 Cl − 离子。沉淀的 TiO2 在 150°C 下干燥,得到的干凝胶标记为 S1。 S2材料合成过程同理,但在TiCl4水解阶段直接向四氯化钛中加入结晶干燥的Na2SO4。
衍射图是用配备 X 射线管 BSV28(Cu Kα 辐射,40 kV,30 mA)、Bragg-Brentano 几何型和 Ni Kβ 滤光片的衍射仪 DRON-4-07 获得的。使用 ICSD 结构模型进行定性分析。锐钛矿和金红石的结构模型分别基于 ICSD #92363 和 ICSD #24780。在真空中退火(850-900°C 4 小时)的平均晶粒尺寸约为 50 μm 的铜粉用作参考样品,以确定仪器的峰展宽。该参考样品在 2θ =43.38° 处的衍射峰的半峰全宽 (FWHM) 为 0.129°;因此,可以区分锐钛矿相和板钛矿相。相干散射域的大小由 Scherrer 方程计算:\( D=\frac{K\lambda}{\beta cos\theta} \),其中 K 是谢勒常数 (K =0.9), λ 是波长 (0.154 nm),β FWHM(以弧度为单位)和 θ 是峰值角位置。我们使用高斯和柯西(支配)函数的组合作为轮廓形状。
使用 Thermo-Nicolet Nexus 670 FTIR 光谱仪在 4000–400 cm -1 记录红外光谱 地区。将振动研磨后的TiO2/KBr混合物压成颗粒,并在透射模式下进行测量。
通过透射电子显微镜 (TEM) 和 100 kV 显微镜 JEOL JEM-100CX II 研究样品粉末的形态。薄透明碳膜覆盖的微观铜网格用作TEM研究的样品支架。
结果与讨论
反应介质中硫酸钠的存在显着影响了所得材料的相组成(图 1)。在不存在 Na2SO4 添加剂 (S1) 的情况下合成的材料是锐钛矿和金红石的混合物,相对相含量分别为 65 ± 4 和 35 ± 5wt%。锐钛矿的相干散射域 (CSD) 的平均尺寸约为 14 纳米,金红石为 9 纳米,因此两相都结晶良好。同时,由于XRD图谱上存在晕圈,2θ =16-32 o ,该部分材料接近于非晶态 很明显。根据合成条件,不太可能形成非二氧化钛相。结果,该材料由具有不同结晶度的分离区域组成。 S1 样品的比表面积约为 152 m 2 g −1 .材料S2接近于具有明显锐钛矿结构特征的无定形超细二氧化钛。在这种情况下也观察到 XRD 图案上的光晕,但它相对变窄并转移到更大的 2θ 值。 CSD 的平均尺寸约为 4-5 nm(由于材料结晶度低,分析变得复杂)。 S2 样品的比表面积增加到 328 m 2 g −1 .
<图片>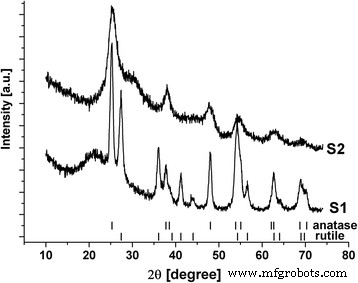
S1和S2材料的XRD图
S1 样品的 TEM 图像(图 2a)无法对其形态做出明确的结论,但观察到的附聚物由大小为 10-15 nm 的层状初级颗粒组成。此外,没有结晶区域边界的证据(图 2b)。 S2 样品具有附聚物的气泡状形态(图 2c、d)。 HR TEM 显示该材料的某些晶粒具有高结晶度(图 3),晶面间距为 0.34-0.37 nm。获得的晶面间距对应于锐钛矿的 (101) 面 (0.352 nm)。这表明CSD(微晶)的优选生长方向是[010]晶轴。该结果得出结论,具有氧化表面的锐钛矿纳米晶体在<010>方向上形成了小平面[11]。
<图片>
样品 S1 (a , b ) 和 S2 (c , d )
<图片>
具有 {101} 平面条纹的 S2 材料的 HR TEM 图像
通过 FTIR 光谱获得了有关合成材料的更多信息。 3400 cm −1 附近的广泛吸收区域 表明二氧化钛颗粒表面存在化学吸附的 OH 基团(ν-OH 模式)(图 4)[12]。 ν-OH 波段从典型的 3700–3600 到大约 3400 cm -1 可能是由氢键的存在引起的 [13]。 1600 cm −1 附近的波段 证明存在分子吸附水(δ-H2O 模式)[14]。 S1 样品较高的结晶度导致在二氧化钛特征区 (400–700 cm -1 ) [15]。
<图片>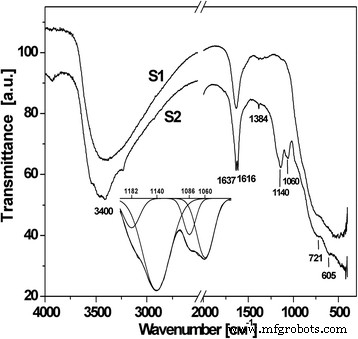
S1和S2材料的FTIR光谱
S2 材料在 1139 和 1060 cm −1 的 FTIR 图案上的附加吸收带 对应于化学吸附的 SO4 2− 离子 [16]。一个尖锐的低强度带 1384 cm −1 是典型的由硫酸根离子带改性的金属氧化物,并指定为 S=O 伸缩频率。同时,S=O-H 配位不太可能,因为吸收带将在低频区域移动到 1325 cm −1 在这种情况下。 SO4 2− 有两种不同的变体 在二氧化钛表面固定化——螯合双齿络合物通过两个氧与一个金属离子配位形成或通过两个金属离子键合形成桥连双齿络合物;两个复合体都属于 C2v 点群。桥接双齿 SO4 2− 阴离子与 Ti 4+ 协调 在 930–1200 cm −1 具有特征伸缩频率 1148 cm −1 处的主要吸收峰 归因于不对称伸缩振动 [17]。 1300–900 cm −1 中的波段 观察到 SO4 2− 的区域 /TiO2 系统,以及 1217、1134、1044 和 980 cm -1 处的峰 在 [18] 中被确定为桥双齿 SO4 2− 的特征频率 与金属相协调。根据 [19],桥接双齿复合物在 1195–1160、1110–1105、1035–1030 和 990–960 cm -1 有四个吸收带 , 分配给 S=O 和 S-O 键的不对称和对称伸缩频率。
SO4 2− 螯合络合物形成的能量有利性结论 在硫酸化二氧化钛研究的基础上,使用 DFT 计算 [20],使阴离子通过两个氧与 Ti 原子配位。螯合硫酸盐复合物的形成对应于 1201 cm −1 处的骨架 FTIR 波段 [21] 作为螯合双齿复合物在 1240–1230、1125–1090、1035–995 和 960–940 cm -1 有四个带 分配给 S=O 和 S-O 波段的非对称和对称伸缩频率 [19]。
1200–1000 cm −1 的解卷积 S2 材料 FTIR 光谱区域显示在 1182、1140、1086 和 1060 cm -1 处存在四个波段 . 1086 cm −1 处的吸收带 非常接近螯合二齿复合物。两条螯合和桥接双齿复合物的带相互重叠,因此带在 1182 cm −1 可以对应两种类型的复合物。 1060 和 1140 cm −1 处的波段 表明在S2样品表面形成了桥连双齿复合物。
我们可以推荐以下 SO4 2− 模型 考虑到 [22] 中显示的结果,在初级水络合物之间的水解相互作用阶段对二氧化钛成核的影响。 TiCl4水解生成[Ti(OH2)6] 4+ Ti 4+ 的地层 离子处于八面体配位中,接下来转化为 [Ti(OH)h(OH2)6−h] (4−h)+ 去质子化的结果是单体。水解比h 是 pH 值的函数,由部分电荷理论决定 [23]。在这些单体中,OH − 基团在八面体赤道平面中具有位置的热力学优势,H2O 分子主要占据“顶点”位置 [24]。水解产物为[Ti(OH)(OH2)5] 3+ 和 [Ti(OH)2(OH2)4] 2+ 当反应介质的 pH 值接近 1 时,单体。在 pH =3 时,[Ti(OH)2(OH2)4] 2+ 和 [Ti(OH)3(OH2)3] + 配合物共存于溶液中。在 pH =4 时,水解导致形成 [Ti(OH)3(OH2)3] + 络合物,在pH =6-8范围内,[Ti(OH)4(OH2)2] 0 形成单体。二氧化钛多晶型物形成的可能性由[Ti(OH)h(OH2)6−h] (4−h)+ 的空间组织定义 初级单体。 [Ti(OH)4(OH2)2] 0 单体(其中 OH 基团占据八面体赤道平面,H2O 分子位于顶点)在中性或碱性介质中形成 [20, 25]。二聚体是由于两种主要单体之间的缩合反应而形成的,其中八面体配位在八面体赤道面外有一个共同的边缘。进一步缩聚后,[Tin(OH)4n(OH2)2] 0 呈锯齿状或螺旋状链状 形成多面体,并创造锐钛矿相成核的条件。 [TimnOmn(OH)2mn(OH2)2m] 0 聚合物是由 m 形成的 [Tin(OH)4n(OH2)2] 0 的线性结构 关系互动。锐钛矿相的成核是八面体横向平面合并的结果 [26]。同时,反应介质的水合氢离子与八面体赤道面上的羟基相互作用。如果反应介质中的水合氢离子浓度增加,[Ti(OH)h(OH2)6−h] (4−h)+ 单体将在 h 下形成 <2 条件。它们之间的相互作用导致聚合物链的形成,其中单体通过八面体赤道面的联合边缘连接,从而定义了金红石相成核的前提[25]。
SO4 2− 的存在 在 pH 值约为 5.5 的反应介质中,离子会导致 Ti(SO4)(OH)2(H2O)2 螯合和 Ti2(SO4)(OH)6(OH2)2 桥接双齿复合物的形成(图 5)。这些复合物之间有两种不同的 olation 相互作用途径。两个单体相互连接或通过共享顶端边缘(螯合复合物影响)或在赤道面(桥接双齿复合物影响)与水分子脱水连接。在这两种情况下的下一阶段,随着两个水分子的脱水,形成倾斜的锯齿状四核钛配合物,并开始锐钛矿结构的成核。
<图片>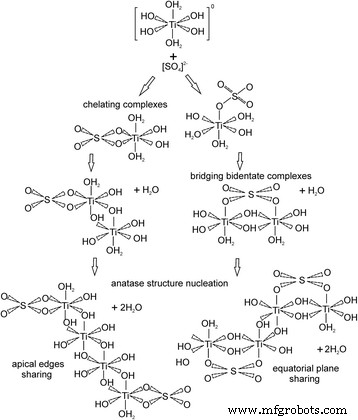
锐钛矿相成核与螯合和桥连双齿 SO4 2− 的形成机制 复合体
结论
SO4 2− 的作用 研究了四氯化钛水解过程中二氧化钛成核的阴离子。我们得出结论,成核过程主要受反应介质的 pH 值和 SO4 2− 控制 阴离子的存在。在四氯化钛水解阶段,硫酸根阴离子形成螯合 Ti(SO4)(OH)2(H2O)2 和桥连二齿 Ti2(SO4)(OH)6(OH2)2 络合物。当 SO4 2- 配体刺激螺旋聚合物链的形成和TiO2锐钛矿相的成核。
纳米材料


