二氧化硅气凝胶负载的水锌矿和碳酸盐插层水滑石通过沉淀转化反应高效去除 Pb(II) 离子
摘要
在这项工作中,水锌矿和 Zn/Al-CO3 2− 二氧化硅气凝胶负载的水滑石是通过简单经济的方法制备的,并用作吸附剂去除 Pb(II)。负载型水锌矿和 Zn/Al-CO3 2− 水滑石具有超薄的厚度、高的表面积和弱的结晶度。在批 Pb(II) 吸附实验中,Zn(II) 含量较高的吸附剂表现出较高的 Pb(II) 吸附容量,吸附数据与 Langmuir 等温线模型和准二级动力学模型拟合良好,表明表面化学吸附机理。基于 Langmuir 等温线模型计算的吸附容量分别为 684.9 毫克/克和 555.6 毫克/克,对于负载型水锌矿和 Zn/Al-CO3 2− 水滑石分别高于其他基于水滑石的吸附剂和之前报道的大多数其他无机吸附剂的吸附能力。水锌矿和Zn/Al-CO3的XRD衍射峰 2− 吸附后水滑石消失,Pb(II)物质以Pb3(CO3)2(OH)2形式均匀分散在吸附剂中,TEM、EDS图谱和XRD分析证明吸附的性质是沉淀水锌矿或 Zn/Al-CO3 2− 的转化 水滑石转化为 Pb3(CO3)2(OH)2。这些结果证明了 CO3 2− 的协同 Pb(II) 去除效果 和 OH − 衍生自水锌矿和 Zn/Al-CO3 2− 水滑石及其超薄的厚度和高的表面积有助于吸附剂的优异性能。
背景
配水系统和地表水中的重金属(例如 Pb、Cd 和 Hg)污染会导致严重的环境和生物体健康问题,多年来一直是全球关注的主要问题 [1, 2]。化学沉淀[3]、吸附[4、5]、离子交换[6、7]等多种技术已被用于去除水中高毒重金属离子,其中吸附是应用最广泛的一种。由于其操作简单、效率高[8, 9],对pH[10]等水生生物生存环境影响小,使用高浓度沉淀剂化学沉淀去除重金属离子时波动较大。试剂。由于这些原因,已经开发了许多吸收性材料,例如无机材料 [11,12,13,14,15]、聚合物 [16]、生物材料 [17, 18] 和吸附树脂 [7, 8],并且用于吸附废水中有毒金属离子。然而,仍然存在一些限制吸附方法的挑战,例如大多数吸附剂的表面积有限和相应的低吸附容量。因此,需要探索新型高表面积吸附材料以高效去除重金属离子。
水滑石(HTs,也称为层状双氢氧化物)由堆叠的水镁石型八面体层组成,由二价和三价金属氢氧化物组成,阴离子和水分子占据层间空间,已广泛用于通过离子交换吸附各种阴离子。 19,20,21]。近年来,这些材料也被研究作为水中重金属阳离子的吸附剂和清除剂 [22,23,24,25,26]。低成本、简单的制备和高吸附效率使这些材料适用于废水处理领域[27, 28]。 HTs本身可以通过三种途径吸附有毒金属阳离子:(1)HT晶体中二价金属离子被溶液中具有相似离子半径的有毒二价金属离子同晶取代[24, 27]; (2) HTs中的金属氢氧化物(主要是二价金属氢氧化物)组分与不同离子半径的有毒金属离子反应[29]; (3) 层间碳酸盐与有毒金属离子反应[29]。综上所述,层间碳酸盐和层内二价金属氢氧化物组分是HTs中吸附有毒金属离子的主要功能组分,因此含有这两种组分的碳酸盐插层HTs(carbonate-HTs)有望具有最佳的金属吸附性能。离子。然而,通过常规方法合成的 HT 粉末通常具有较低的比表面积 [30],这限制了它们的吸附性能。提高 HT 表面积的一个好方法是将它们支撑在具有高表面积的载体上。李等人。 [31] 通过对预先制备的 SBA-15 负载的混合金属氧化物进行长时间的水热处理,制备了具有高表面积的多孔材料 (SBA-15)。钟等人。 [32] 合成的碳纳米纤维支持具有小尺寸和增强表面积的 HT 薄片。但上述支撑方式有些复杂,支撑材料价格昂贵。此外,关于通过二价金属的碳酸盐氢氧化物盐吸附有毒金属离子的报道很少,其中也含有碳酸盐和二价金属氢氧化物,如碳酸盐-HTs。因此,开发低成本且易于制备的负载型碳酸盐氢氧化物和高表面积碳酸盐-HTs有望增强有毒金属离子的吸附。
二氧化硅气凝胶 (SAs) 由于其低堆积密度、高表面积和低热导率而在科学和技术领域引起了广泛关注 [33, 34]。此外,SA 价格低廉(2 至 3 美元/公斤),因为它的制造规模庞大,而且在隔热行业中需求量很大。因此,在目前的工作中,水锌矿 (Zn5(OH)6(CO3)2) 和 Zn/Al-CO3 2− 商业SA支撑的水滑石,为水锌矿和Zn/Al-CO3 2− 的加载和生长提供了密闭空间和成核位点 水滑石的制备方法简单。 SA负载水锌矿和Zn/Al-CO3的织构特性 2− 通过TEM、XRD、ICP和BET对水滑石进行了表征。特别评估了吸附剂合成中 Zn(II) 离子含量和 pH 值对吸附能力的影响。此外,研究了吸附平衡和动力学,并分别拟合了相应的等温线模型和动力学模型。吸附后的吸附剂通过TEM、XRD和EDS图谱进行表征。最后讨论了该吸附体系中可能的吸附机理。
方法
材料
硝酸锌、硝酸铝、碳酸氢钠、氢氧化钠和硝酸铅均为分析纯,购自阿拉丁试剂有限公司(中国上海)。盐酸(36-38%)为分析纯,购自国药集团化学试剂有限公司(中国上海)。 SA由纳米科技有限公司(中国绍兴)提供。
吸附剂的制备
SA 粉末在使用前在 823 K 下煅烧 2 小时以去除表面上的有机基团。通过超声将处理过的 SA(500 毫克)分散在 500 毫升的去离子水中 30 分钟。向得到的SA悬浮液中加入m的25mL混合溶液(A) mol Zn(NO3)2 和 n 加入 150 mL 去离子水中的 mol Al(NO3)3 并搅拌 5 分钟,然后交替滴加 125 mL 混合溶液 A 和另一种 NaOH/NaHCO3 (0.5 M/0.5 M) 混合溶液。改变 Zn:Al 比率,使得 m + n =0.0075 mol 和 m :n =3:0、3:1、2:1 和 0:1。用上述 NaOH/NaHCO 3 混合溶液将溶液的最终 pH 值调节至 8.8 或 9.5,然后在 80°C 下进行水热处理 24 小时。离心收集所得产物,用去离子水洗涤3次,真空干燥。 SA 负载水锌矿的最终样品(水锌矿,m :n =3:0) 和 Zn/Al 水滑石 (m :n =3:1 和 2:1) 表示为 SA-Zn-HZ 和 SA-Zn x 分别为 Al-HT,其中 x 表示前体溶液中二价金属/三价金属的摩尔比。 SA负载氢氧化铝的对照样品指定为SA-Al-H(m :n =0:1)。
特征化
使用在 80 kV 加速电压下操作的 JEM-1011 电子显微镜拍摄透射电子显微照片。使用配备 X-act 能量色散 X 射线 (EDX) 分析仪 (Oxford INCA) 的 JSM-6360LV 扫描电子显微镜获得扫描电子显微照片和能量色散光谱。在连续吸附条件下,使用 Micromeritics ASAP TriStar II 3020 孔分析仪在 77 K 下获得 N2 吸附-解吸等温线。样品在测量前在 150°C 下脱气 8 小时。通过Brunauer-Emmett-Teller方法计算比表面积,并使用Barrett-Joyner-Halenda分析从氮等温线的解吸分支测量孔径分布。使用 Empyrean XRD 衍射仪收集 X 射线衍射 (XRD) 图案。采用电感耦合等离子体原子发射光谱仪(Leeman Prodigy XP ICP-AES光谱仪)测定吸附剂中Zn、Si和Al的元素含量。
吸附实验
Pb(II) 水溶液 (1000 ppm) 是通过将 Pb(NO3)2 溶解在去离子水中制备的。然后用去离子水稀释至所需浓度。将不同浓度的 Pb(II) 溶液均调节至 pH 值约为 6.0,0.1 mol L -1 HCl 或 NaOH 水溶液。通常,将 50 毫克吸附剂分别放入锥形瓶中的 100 毫升不同浓度(100、200、300、400、500 和 1000 ppm)的 Pb(II) 水溶液中。然后,将锥形瓶在设定温度为 25°C 的培养摇床中振荡 (150 rpm) 24 小时以达到吸附平衡。在每个吸附过程结束时,将悬浮液离心并过滤上清液,并用于通过岛津 AA-6300 原子吸附分光光度计 (AAS) 测定 Pb(II) 的含量。根据下式计算吸附剂的吸附容量:q e =(C 0 - C e)V/m,其中 q e 表示平衡时的吸附量 (mg g -1 ), C 0 和 C e 是溶液中污染物的初始浓度和平衡浓度(mg L −1 ),V 是 Pb(II) 溶液的体积 (mL),m 是吸附剂的干重 (g)。对于吸附动力学分析,将 50 毫克吸附剂添加到 100 毫升浓度为 500 ppm 的 Pb(II) 溶液中。在 25°C 摇动 (150 rpm) 悬浮液。在 10、30、50、70、100、140、180、240、360、600 和 1440 分钟的特定反应时间间隔内,取 2 mL 悬浮液并通过 0.22 mL 膜过滤。用火焰原子吸附分光光度计(岛津AA-6300)分析滤液中Pb(II)浓度。
结果与讨论
综合参数优化
为了研究吸附剂的合成参数对其吸附性能的影响,在不同 Zn 条件下制备的 SA-Zn-HZ、SA-Zn3Al-HT、SA-Zn2Al-HT 和 SA-Al-H 的最大吸附容量测试了 /Al 前体比率(3:0、3:1、2:1 和 0:1)和 pH(8.8 和 9.5)(图 1)。最大吸附容量为 680.8 mg g −1 , 537.8 mg g −1 , 429.5 mg g −1 , 和 176.4 毫克 g −1 分别为在 pH 9.5 下制备的 SA-Zn-HZ、SA-Zn3Al-HT、SA-Zn2Al-HT 和 SA-Al-H,分别为 510.6、482.2、405.7 和 111.8 mg/g ,对于 SA-Zn-HZ、SA-Zn3Al-HT、SA-Zn2Al-HT 和 SA-Al-H,在 pH 值为 8.8 时制备。因此,可以得出结论,合成介质上的高二价金属含量和 pH 值(如 9.5)有利于促进吸附性能。以下部分以在pH 9.5下合成的具有高吸附容量的SA-Zn-HZ和SA-Zn3Al-HT进行结构特征、吸附平衡和动力学研究。
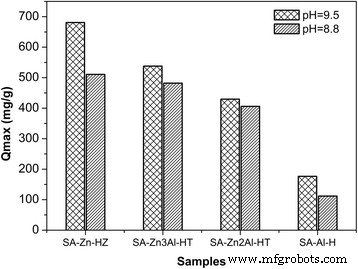
SA-Zn-HZ、SA-Zn x的最大吸附容量 Al-HT 和具有不同 Zn 含量的对照样品 SA-Al-H。从左到右,Zn元素含量逐步减少
SA-Zn-HZ和SA-Zn3Al-HT的织构特征
SA-Zn-HZ、SA-Zn3Al-HT 和载体 SA 的形态通过 TEM 表征,如图 2 和附加文件 1:图 S1。水锌矿 (HZ) 和 Zn/Al-CO3 2− SA-Zn-HZ 和 SA-Zn3Al-HT 复合材料中的 HT 分别显示出具有超薄厚度(<5 nm)的片状结构。 SA-Zn-HZ 和 SA-Zn3Al-HT 的结构参数列于表 1 中,由 N2 吸附-解吸等温线计算的 SA-Zn-HZ 和 SA-Zn3Al-HT 的表面积为(图 3a) 264.1 m 2 g −1 和 233.9 m 2 g −1 ,分别低于基材 SA(附加文件 1:表 S1 和图 S2),因为层状 HZ 和 Zn/Al-CO3 可能会阻塞 SA 的孔结构 2− HT 和 HZ 和 HT 的密度高于 SA。如图 3b 所示,XRD 谱显示 SA-Zn-HZ 的水锌矿结构(PDF#19-1458,Zn5(CO3)2(OH)6)和典型的碳酸盐插层水滑石结构(PDF#51- 1525) 分别用于 SA-Zn3Al-HT。然而,两种样品的特征衍射峰强度都很弱,表明复合材料中的超薄层状结构和相对较弱的HZ和HT结晶度。

SA-Zn-HZ (a , b ), SA-Zn3Al-HT (c , d ) 在 pH 9.5 下制备
<图>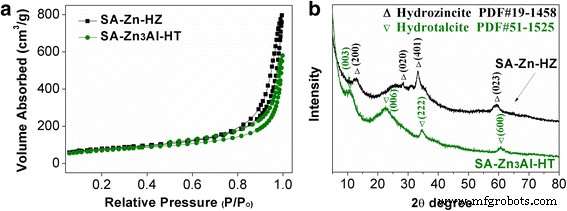
N2 吸附-解吸等温线 (a ) 和 XRD 图 (b ) SA-Zn-HZ 和 SA-Zn3Al-HT
SA-Zn-HZ 和 SA-Zn3Al-HT 上 Pb(II) 离子的吸附等温线
图 4a 包括了初始 Pb(II) 浓度(100、200、300、400、500 和 1000 ppm)对 SA-Zn-HZ 和 SA-Zn3Al-HT 吸附特性的影响。正如预期的那样,两种吸附剂的吸附容量都随着 Pb(II) 初始浓度的升高而增加。在 100、200 和 300 ppm 的低初始浓度下,Pb(II) 的吸附容量几乎与 SA-Zn-HZ 和 SA-Zn3Al-HT 的初始 Pb(II) 浓度成线性比例。然而,在 400、500 和 1000 ppm 的高初始 Pb(II) 浓度下,吸附容量缓慢增加并接近其最大吸附容量,这是由于吸附剂上缺乏可容纳更多 Pb( II) 离子。吸附等温线数据符合 Langmuir、Freundlich、Sips 和 Redlich-Peterson 模型,这些模型在数学上表示为方程。 (1), (2), (3), (4) [13, 24, 35,36,37] 分别为:
$$ {C}_e/{q}_e=1/\left({q}_m{K}_L\right)+{C}_e/{q}_m $$ (1) $$ \ln {q} _e=\ln {K}_F+\left(1/n\right)\ln {C}_e $$ (2) $$ {q}_e={q}_m{\left({K}_S{C} _e\right)}^{n{}_s}/\left\{1+{\left({K}_S{C}_e\right)}^{n{}_s}\right\} $$ (3 ) $$ {q}_e={q}_m\left({K}_{\mathrm{RP}}{C}_e\right)/\left\{1+{\left({K}_{\ mathrm{RP}}{C}_e\right)}^{n_{RP}}\right\} $$ (4)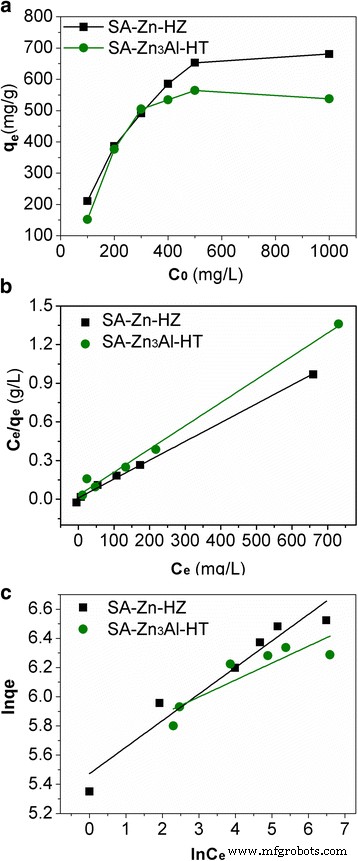
Pb(II) 在 SA-Zn-HZ 和 SA-Zn3Al-HT 上的吸附等温线 (a ), 朗缪尔 (b ) 和 Freundlich (c ) 吸附等温线模型拟合 Pb(II) 吸附。实验条件:初始 Pb(II) 浓度 100 ~ 1000 ppm;吸附剂剂量 0.5 g L −1 ;接触时间 24 小时,溶液 pH 值 6.0 ± 0.1;温度 30 °C
C 在哪里 e (mg/L) 是水相中的平衡浓度; q e(mg/g)为吸附剂吸附的平衡量; q m (mg/g) 表示理论饱和吸附容量; K L (L/mg) 是与吸附-解吸能和离子结合位点亲和力相关的朗缪尔常数; K F 粗略是吸附容量的一个指标,1/n 是吸附强度; K S (L/mmol) 是 Sips 等温线常数和 n S 是 Freundlich 异质性因子; K RP (L/mg) 和 n RP 是 Redlich-Peterson 常数。 Langmuir、Freundlich、Sips 和 Redlich-Peterson 模型在 SA-Zn-HZ 和 SA-Zn3Al-HT 上吸附 Pb(II) 的吸附数据和拟合图如图 4b、c 和附加文件 1 所示:图 S3 ,这些模型的计算参数在表 2 和附加文件 1:表 S2 中给出。对于四个研究模型,Langmuir 模型显示出更显着的相关系数(R 2 ≥ 0.99) 分别与 Freundlich、Sips 和 Redlich-Peterson 模型的实验数据相比,基于 Langmuir 模型的 SA-Zn-HZ 和 SA-Zn3Al-HT 对 Pb(II) 的最大吸附容量为 684.9分别为 mg/g 和 555.6 mg/g。
<图>Pb(II) 离子在 SA-Zn-HZ 和 SA-Zn3Al-HT 上的吸附动力学
研究吸附动力学以确定吸附平衡所需的时间并解释吸附剂上的 Pb(II) 吸附机制。图 5a 中显示了从 0 到 1440 分钟(24 小时)Pb(II)在 SA-Zn-HZ 和 SA-Zn3Al-HT 上的吸附动力学数据。可以看出,两种吸附剂的吸附速率在前 50 分钟内均较快,然后逐渐减慢,之后达到吸附平衡。初期 Pb(II) 的快速去除率可能归因于 Pb(II) 从本体溶液快速扩散到吸附剂的外表面以及在初始阶段吸附剂的大量可用位点。在后期,缓慢的吸附过程可能归因于 Pb(II) 在吸附剂上的扩散距离较长以及吸附剂的表面吸附位点有限。为了研究 Pb(II) 在 SA-Zn-HZ 和 SA-Zn3Al-HT 上的吸附机理,实验结果与方程 1 表示的拟一级和拟二级动力学模型拟合。 (5) 和 (6) [35, 38] 分别。
$$ \ln \left({q}_e-{q}_t\right)=\ln {q}_e-{k}_1t $$ (5) $$ t/{q}_t=1/\left( {k}_2{q_e}^2\right)+t/{q}_e $$ (6)其中 q t (mg/g) 是在时间 t 被吸附剂去除的吸附物的量 (分钟); q e (mg/g) 是平衡吸附容量; k 1 (min −1 ) 和 k 2 (g/(mg min −1 )) 分别是伪一阶和伪二阶模型的速率常数。 ln(q e-q t) 与 t 和 t 的图 /q t 对 t 对于伪一级和伪二级动力学模型,分别如图 5b、c 所示。吸附容量 (q e) 和速率常数 (k 1 和 k 2 ) 从曲线的斜率和截距计算得出的结果总结在表 3 中。显然,具有较高相关系数 (R 2 > 0.99) 可以比拟一级模型更好地拟合实验动力学数据。此外,吸附容量值 (q e , cal) 由伪二阶模型计算出的与实验 q 非常一致 e 值 (q e, exp)。这些结果表明,伪二级动力学模型吸附机制占主导地位,表明 Pb(II) 吸收的总体速率似乎受化学吸附过程控制 [13, 39]。
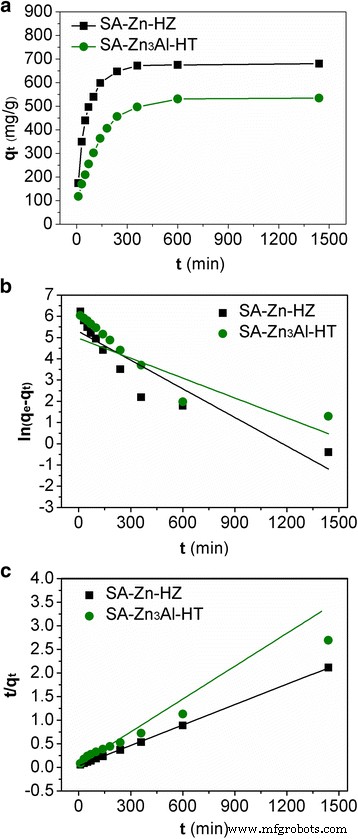
Pb() 的吸附动力学 二) SA-Zn-HZ 和 SA-Zn3Al-HT (a ) 和伪一阶 (b ) 和伪二阶 (c ) 适合 Pb(II) 吸附的吸附动力学模型。实验条件:初始 Pb(II) 浓度 500 ppm;吸附剂剂量 0.5 g L −1 ;接触时间 0 ~ 24 h,溶液 pH 6.0 ± 0.1;温度 30 °C
<图>吸附机理及性能评价
为了进一步探讨 Pb(II) 在 SA-Zn-HZ 和 SA-Zn3Al-HT 上的吸附机理,吸附后的样品 SA-Zn-HZ 和 SA-Zn3Al-HT(SA-Zn-HZ-Pb 和 SA- Zn3Al-HT-Pb) 通过 TEM、EDS 映射和 XRD 进行表征。 SA-Zn-HZ-Pb 和 SA-Zn3Al-HT-Pb(图 6)在 TEM 图像(图 2)中分别具有比 SA-Zn-HZ 和 SA-Zn3Al-HT 更高的对比度,表明高原子许多铅已从溶液中吸附到吸附剂上。在附加文件 1:图 S4 和图 S5 的 EDS 元素映射中,很明显 Pb 元素均匀分散在 SA-Zn-HZ-Pb 和 SA-Zn3Al-HT-Pb 中,间接表明 Pb 的异质成核(II) 吸附剂表面的物种。 XRD 分析(图 7)显示 SA-Zn-HZ-Pb 和 SA-Zn3Al-HT-Pb 中的 Pb(II) 物质均以 Pb3(CO3)2(OH)2(Hydrocerussite,PDF#)的形式存在13-0131),比 Pb(OH)2 或 PbCO3 更稳定,因为前者的溶度积常数较低 (3.16 × 10 −46 ) 与后者 (1.43 × 10 −15 对于 Pb(OH)2 和 7.9 × 10 −14 对于 PbCO3) [40, 41]。吸附过程中溶液pH值随时间的变化如图8所示。在初始接触时间(0~210分钟),溶液pH值不断升高,主要是由于氢氧化物组成的水锌矿和水滑石溶解达到沉淀-溶解在弱酸性 Pb 溶液中的平衡导致 OH − 的释放 .然而,随着接触时间(210~1440 min)的持续增加,溶液的pH值逐渐降低,这可能是因为吸附中产生的水蜡矿沉积在水锌矿和水滑石表面,阻止了两种吸附剂的进一步溶解和随后的释放OH − , 同时 OH − 依次消耗生成水蜡矿和 CO3 2− 和铅 2+ 在解决方案中。总体而言,在分别使用 SA-Zn-HZ 和 SA-Zn3Al-HT 作为吸附剂的吸附过程中,Pb(II) 溶液具有较低的 pH 波动,范围为 6.0 ~ 6.39 和 6.0 ~ 6.21,表明两种吸附剂均具有对水体pH值影响小。

SA-Zn-HZ-Pb (a ) 和 SA-Zn3Al-HT-Pb (b )
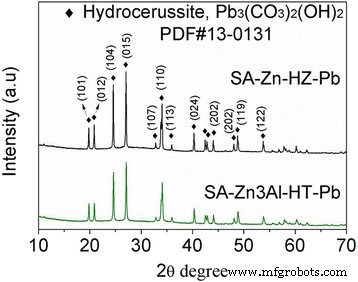
SA-Zn-HZ-Pb和SA-Zn3Al-HT-Pb的XRD图
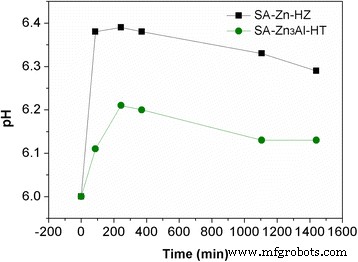
以SA-Zn-HZ和SA-Zn3Al-HT为吸附剂吸附Pb(II)溶液的pH值随时间变化
在该吸附系统中,由于 Pb(II) 的离子半径大得多 (0.119 nm),因此不可能用 Pb(II) 同构取代 SA-Zn-HZ 和 SA-Zn3Al-HT 中的二价 Zn(II)比 Zn(II) (0.074 nm)。因此,HZ或Zn/Al-CO3的反应 2− 带有有毒 Pb(II) 阳离子的 HT 可能对吸附做出了主要贡献,并导致水蜡矿沉淀。 HZ(或 Zn/Al-CO3 2− HT) 在含 Pb(II) 的水溶液中转化为水蜡矿可能是由于后者的溶度积常数低于前者 [42]。此外,在该吸附系统中,基于表面沉淀转化反应的吸附过程是不可逆的。在达到饱和吸附之前,催化剂可以重复使用,并且在每个循环中都表现出很高的去除效率(> 93.5%)(图 9)。一旦达到饱和吸附,吸附剂即使经过煅烧也不能重复使用,这是由于饱和吸附剂中的表面功能成分(水锌矿和水滑石)已转化为水蜡石,进一步吸附受到限制。
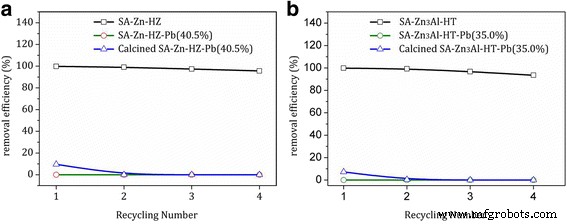
回收利用a去除Pb(II) 原始SA-Zn-HZ、饱和SA-Zn-HZ(SA-Zn-HZ-Pb(40.5%))和煅烧后的饱和SA-Zn-HZ; b 原始 SA-Zn3Al-HT、饱和 SA-Zn3Al-HT(SA-Zn-HZ-Pb (35.0%))和煅烧后的饱和 SA-Zn3Al-HT。初始 Pb(II) 浓度 100 ppm;吸附剂剂量 0.5 g L −1 ;接触时间 24 小时,溶液 pH 值 6.0 ± 0.1;温度 30 °C
基于 Langmuir 等温线模型的 SA-Zn-HZ 和 SA-Zn3Al-HT 对 Pb(II) 的最大吸附容量分别为 684.9 和 555.6 mg/g,高于其他基于水滑石的吸附剂和大多数其他吸附剂。无机吸附剂,如氧化石墨烯、碳纳米管和活性炭基吸附剂(表 4)。 SA-Zn-HZ和SA-Zn3Al-HT优异的吸附性能以及低成本和易于制备的特性使得SA-Zn-HZ和SA-Zn3Al-HT成为去除废水中Pb(II)的极具竞争力的清除剂。
<图>结论
我们已经证明了二氧化硅气凝胶负载的水锌矿和 Zn-Al-CO3 2− 的结构特性、Pb(II) 吸附特性、吸附动力学和可能的吸附机制 水滑石。负载水锌矿和 Zn/Al-CO3 2− 水滑石具有超薄的厚度(<5 nm)和高表面积。在批量 Pb(II) 吸附实验中,吸附数据与 Langmuir 等温线模型和准二级动力学模型非常吻合,表明存在表面化学吸附过程。负载型水锌矿和 Zn/Al-CO3 2− 基于 Langmuir 等温线模型计算的饱和吸附容量分别为 684.9 和 555.6 mg/g 水滑石分别接近实验值并高于其他基于水滑石的吸附剂和之前报道的大多数其他无机吸附剂的吸附能力。吸附后,吸附在吸附剂上的Pb(II)物质以水蜡矿形式存在,水锌矿或Zn/Al-CO3的XRD衍射峰 2− 水滑石消失,说明吸附性质可能是水锌矿或Zn/Al-CO3的沉淀转化 2− 将水滑石转化为在 Pb(II) 溶液中具有低溶度积常数的水蜡石。最后,该工作将为开发新型重金属离子吸收剂,例如、提供参考。 通过沉淀转化反应将有毒金属离子固定在吸附剂表面,形成溶度积常数低的特殊沉淀物。
纳米材料
- 为什么 3D 打印和软件对数字化转型至关重要
- 制造业的数字化转型——制造商的加速器和路线图
- 使用来自轧制废料的磁铁矿纳米吸附剂从水溶液中吸附去除铜 (II) 离子:合成、表征、吸附和动力学建模研究
- 用于高效偏振分束器和光学涡流发生器的高阶介电超表面
- 通过金属盐-聚合物纳米复合膜的相分离形成的表面纳米结构,用于抗反射和超疏水应用
- 单独用二氧化钛包覆二氧化硅并用海藻酸钠改性作为重金属离子吸附剂
- 用 Au 纳米粒子定制的二氧化硅硅藻壳可以对用于生物、安全和环境应用的分子进行灵敏分析
- 20 种适合初学者的基本焊接工具和设备
- 什么是适合您的金属去除和修整工作的磨料?
- 使用金属润滑剂的技巧:避免过度润滑等
- 冶金术语解释:制造商和机械师术语表
- 用于精密金属去除的 CNC 加工中心


