生物医学领域中与活性氧种类相关的纳米粒子毒性
摘要
纳米粒子独特的物理化学特性最近在各种应用中受到越来越多的关注,特别是在生物医学领域。然而,对纳米颗粒潜在毒理学影响的担忧仍然存在,因为它们更容易产生过量的活性氧 (ROS)。由于具有很强的氧化电位,纳米颗粒诱导的过量ROS会导致生物分子和细胞器结构的破坏,导致蛋白质氧化羰基化、脂质过氧化、DNA/RNA断裂和膜结构破坏,进而导致坏死、凋亡、甚至诱变。本综述旨在总结纳米粒子在细胞水平上产生 ROS 的机制和负责,并提供对 ROS 介导的生物毒性机制的见解。我们总结了有关纳米颗粒毒性的文献,并提出了优化纳米颗粒生物医学应用的策略。
介绍
纳米粒子 (NPs) 是一类尺寸 <100 nm 的新型合成粒子。根据它们的形状和大小,不同的物理和化学特性赋予 NPs 不同的功能。 NPs 广泛用于许多消费品,包括纺织品、化妆品、水净化和食品包装 [1, 2]。它们还用于光催化剂、能源和光电子工程[3,4,5,6]。
特别是,NPs 已成为生物医学材料中的首选材料,并广泛用于生物传感器、siRNAs 递送、靶向基因敲除、药物递送以及生物填充医学材料 [7,8,9,10,11]。 NP 的进一步用途仍在发现中。例如,段等人。 [12]表明Fe3O4-聚乙二醇-聚酰胺-胺-基质金属蛋白酶2@二氢卟酚e6(Fe3O4-PEG-G5-MMP2@Ce6)纳米探针显着抑制胃肿瘤生长。在另一种情况下,pDNA-聚乙烯亚胺 CeO 纳米颗粒(pDNA-PEI-CeO NPs)可以诱导更多的纤维肉瘤细胞凋亡 [13]。此外,中空二氧化硅-铁-聚乙二醇-人表皮生长因子受体 2 纳米粒子 (HS-Fe-PEG-HER2 NPs) 可以选择性地结合肿瘤细胞,并被用作区分正常组织和癌细胞的显像剂 [14]。最后,银纳米粒子(Ag NPs)作为纳米抗生素,可有效对抗耐药细菌生物膜相关感染[15]。
尽管 NPs 在各个领域具有积极应用的潜力,但越来越多的研究表明它们在 NP 暴露后对生物体 [16, 17] 和细胞产生不利影响 [18, 19]。 NPs 的潜在毒性取决于它们的大小和形状,这决定了它们诱导活性氧 (ROS) 产生的倾向 [20, 21]。过量产生的 ROS 可能会诱发一系列病理生理结果,包括遗传毒性、细胞凋亡、坏死、炎症、纤维化、化生、肥大和致癌作用 [18, 22, 23]。 NPs 的毒性也被证明会增强促炎细胞因子的表达并激活炎症细胞,如巨噬细胞,从而进一步增加 ROS 的产生 [23, 24]。暴露于 NPs 后 ROS 的增加也已被证明会诱导细胞功能的调节,在某些情况下会导致致命的结果 [17, 23, 25]。在这篇综述中,我们讨论了 NPs 诱导 ROS 爆发的主要机制,分析了 NPs 细胞毒性的主要原因,并总结了 NPs 的潜在致病作用。我们目前的审查提供了压倒性的证据,证明 ROS 的过度产生是 NP 生物毒性的主要原因。因此,新的研究应该旨在通过设计诱导低ROS产生的纳米颗粒来降低纳米颗粒的细胞毒性。
NPs在生物医学领域的应用
NPs 已被用于各种医学应用,并且一些新型 NPs 表现出有希望用于新型生物医学材料的特性。如表 1 所示,Nano-C60 可用作抗癌剂,在体内和体外抑制癌细胞增殖 [26]。 ZnO NPs 已被用作骨科和牙科植入物的填充剂 [38]。 TiO2 可用作抗菌剂,用于空气和水净化,以及用于假牙 [52,53,54]。达维法尔等人。据报道,藻蓝蛋白-ZnO 纳米棒可以通过减少内源性 ROS 的产生来保护细胞 [68]。帕库拉里等人。指出 SWCNT 可用作临床诊断剂和生物工程材料 [88]。除此之外,许多纳米颗粒可用作抗菌剂,通过诱导ROS爆发来杀死细菌(表1)。
细胞中NPs诱导ROS增加的机制
ROS 是含有氧的化学活性粒子,包括过氧化氢 (H2O2)、活性超氧阴离子自由基 (O 2- ) 和羟基自由基 (•OH) [92, 93]。 ROS 主要在细胞器中产生,例如内质网 (ER)、过氧化物酶体,尤其是线粒体 [94]。在氧化磷酸化过程中,氧气通过线粒体电子传递链 (ETC) 添加电子来合成水。其中一些电子被分子氧接受形成 O 2- , 可以进一步转化 H2O2 和 •OH [93]。
在生理环境中,ROS 是作为对正常氧代谢的自然反应而产生的 [95],并在各种细胞信号通路中发挥重要作用 [96, 97]。 Dröge 和 Holmstrom 等人。据报道,ROS 可以激活多种信号级联反应,包括表皮生长因子 (EGF) 受体、丝裂原活化蛋白激酶 (MAPK) 级联反应、转录因子激活蛋白-1 (AP-1) 和核因子-KB。 NF-κB),并进一步参与哺乳动物的生长、增殖和分化过程 [98, 99]。进一步的研究表明,ROS还调节伤口修复[100]、缺氧后存活[101]、细胞内pH稳态[102]和先天免疫[103]。
然而,暴露于 NPs 后,细胞内 ROS 的产生可能会通过诱导细胞中的 ROS 爆发而急剧增加 [20](表 1)。 ROS爆发的主要机制解释是NPs释放的金属离子通过损害线粒体呼吸促进ROS过度表达[30, 104]。
已证明纳米颗粒释放的金属离子通过芬顿反应 [H2O2 + Fe 2+ 混合到氧化还原循环和化学催化中 → Fe 3+ + HO − + •OH] 或类芬顿反应 [Ag + H2O2+H + =Ag + + •OH + H2O] [23, 105, 106]。解离的金属离子(即 Ag + ) 还会导致细胞酶失活、膜结构破坏 [31, 107]、电子穿梭过程受到干扰 [108]、氧化还原电位水平耗尽、线粒体膜电位 (MMP) 降低 [109],并进一步增强细胞内 ROS 的积累。据报道,NPs 还可以通过干扰电子转移过程来促进细胞内 ROS 的积累 [32, 110],增加 NADP + /NADPH 比率 [30] 和干扰线粒体功能 [18]。 NPs进一步干扰氧化应激相关基因的表达,如soxS , soxR , oxyR , 和 ahpC [58];抗氧化基因,如sod1 和 gpx 1 [111, 112];和NADPH产生相关基因met9 [30]。 NPs引起的氧化和抗氧化基因表达的不稳定加速了细胞内ROS的积累。
有趣的是,ROS 产生的增加与 NP 的特定大小和形状密切相关 [113, 114]。例如,TiO2 NPs 有助于细胞内 ROS 的产生,从而导致核酸和蛋白质损伤 [10]。廖等人。发现 10 nm TiO2 NPs 比其他尺寸的测试具有更高的遗传毒性,因此可以诱导更多的 ROS 产生 [115]。在另一种情况下,Se NPs促进细胞内ROS的产生,细胞内ROS的产量与Se NPs的直径高度相关。在这种情况下,81 nm 的直径比测试的其他尺寸诱导更多的 ROS 产生 [113]。 Cho 等人。进一步表明,NPs 的形状强烈影响其诱导 ROS 产生的能力。与夜花模拟金属纳米粒子 (N-NP) 相比,日花模拟金属纳米粒子 (D-NP) 产生显着更高的 ROS,从而增强细胞杀伤作用 [114](图 1)。 <图片>
在周围溶液和细胞中由纳米颗粒诱导产生 ROS [32]。 NPs产生的电子可以进入细胞并干扰呼吸链的功能,从而增加细胞内ROS的产生。电子也可以直接与O2反应,增加细胞外ROS的产生
NPs 可以在非常低的浓度下诱导细胞内 ROS 爆发(如表 1 所示),例如,1 μg/mL 的 Nano-C60 可以通过诱导氧化应激显着增加细胞凋亡 [26, 27]。值得注意的是,大多数 NPs 具有剂量依赖性效应,如已报道的 VO2 NPs [60, 61] 和 CuO NPs [74, 75]。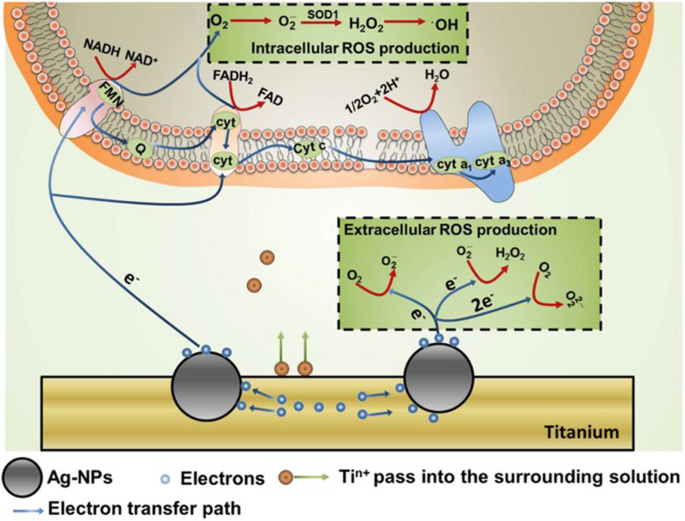
增加 ROS 产生的 NPs 对细胞的灾难性后果
进入细胞的纳米颗粒通常对其产生不利影响。对于 NPs 的细胞毒性,最受支持的解释是氧化应激是由 ROS 爆发引起的。由 NPs 引起的 ROS 爆发导致生物大分子的氧化修饰、细胞结构的破坏、耐药性的产生、基因突变和致癌作用 [116, 117]。此外,ROS 爆发改变了细胞的正常生理功能,就像触发炎症一样,最终会阻断细胞功能并损害生物体 [23, 118, 119]。通常,NPs 首先吸附在细胞表面,然后穿过细胞膜进入细胞,在那里它们诱导 ROS 的产生 [36]。由于其强大的氧化潜力,ROS 对细胞具有高度压力 [46] 并攻击细胞中几乎所有类型的生物分子,包括碳水化合物、核酸、不饱和脂肪酸、蛋白质和氨基酸以及维生素 [36、120、121 ](图2)。
<图片>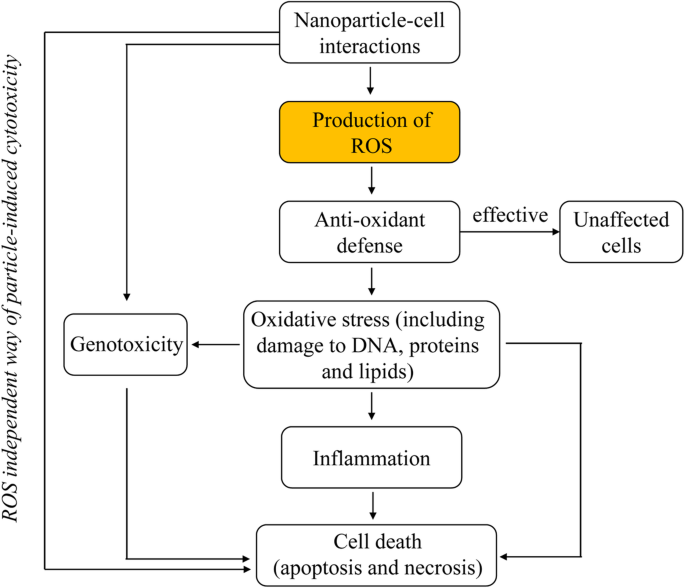
ROS 在 NPs 诱导的细胞毒性中的关键作用 [33]。 NPs与细胞内系统相互作用后可能发生的细胞事件
ROS 导致脂质过氧化物和膜结构损伤
脂质,尤其是不饱和脂肪酸,是重要的细胞内大分子,在细胞膜的结构和功能中起着关键作用。 NPs 被细胞膜强烈吸引,在那里它们可以产生 ROS 并导致外膜脂质过氧化。细胞膜中脂肪酸含量的改变可能导致细胞通透性增加,从而导致纳米颗粒不受控制地从细胞外环境转运到细胞质中,在那里细胞损伤可能进一步发展 [76, 122]。
细胞内 NPs 诱导下一轮 ROS 爆发。负荷过重的 ROS 会导致细胞器膜破裂、细胞器内容物泄漏 [52、123]、细胞受体失活 [124]、乳酸脱氢酶 (LDH) 释放,以及进一步不可逆的细胞损伤 [125] ].
ROS 攻击蛋白质并导致功能失活
ROS 攻击氨基酸的疏水残基,导致肽键断裂并干扰这些蛋白质的功能 [126,127,128]。羰基化是蛋白质遭受氧化损伤的另一个特征 [129]。羰基化蛋白质形成的聚集体在化学上是不可逆的,不能被蛋白酶体降解,导致这些蛋白质的功能永久丧失 [130, 131]。古鲁纳坦等人。 [132] 表明 PtNPs 可以增强 ROS 的产生并增加羰基化蛋白水平,从而抑制骨肉瘤增殖并促进细胞凋亡。在一个案例中,燃烧和摩擦衍生的纳米粒子 (CFDNPs) 在患有阿尔茨海默病的年轻人的大脑中积累,这可能促进了 ROS 的产生,导致蛋白质错误折叠、聚集和纤维化 [133]。此外,Pelgrift 等人。表明Mg NPs可能直接抑制基因转录或破坏蛋白质[10]。
ROS 诱导的基因突变
核酸,包括 DNA 和 RNA,对细胞功能、生长和发育至关重要,它们的组成核苷酸是 ROS 的脆弱靶点 [134,135,136]。由于它们的低氧化还原电位,ROS 可以直接与核碱基反应并对其进行修饰 [137]。例如,ROS 可以将鸟嘌呤氧化为 8-oxo-7,8 二氢鸟嘌呤 (8-oxoG) [138],将腺嘌呤氧化为 1,2-dihydro-2-oxoadenine (2-oxoA) [139]。这些碱基修饰会导致 DNA 损伤 [140]。由于它们的遗传毒性潜力和诱导 ROS 形成的能力 [141],NPs 显着诱导单链和双链 DNA 断裂 [142, 143]、染色体损伤和非整倍体基因事件 [144]。
ROS 产生的增加是基因错误编码、非整倍体、多倍体和暴露于 NPs 的细胞中诱变激活的主要原因 [145,146,147,148]。在核苷酸库中,鸟嘌呤是最脆弱的,很容易被 ROS 氧化为 8-oxoG [149]。 DNA 中 8-oxo-dG 水平的增加导致 DNA 碱基错配 [150]。类似地,A:8-oxoG 的掺入导致 G:C> T:A 有害颠换突变的发生率增加 [151, 152]。 G:C> T:A 颠换与 G:C> A:T 转换突变的比值也被用作量化 DNA 氧化损伤的指标 [153]。
由 NPs 诱导的 ROS 的产生导致 DNA 损伤的积累,从而推动致突变性 [154]、致癌性 [155]、多药耐药性 [156、157]、衰老和免疫逃逸 [158] 的发展。金等人。表明 ROS 的过度产生显着增加了 DNA 结合转录调节基因的诱变,导致抗生素外流加速 [159],进而促进细菌的多重抗生素耐药性 [34]。詹诺尼等人。报道线粒体DNA突变随着细胞内ROS的增加而发生,并进一步破坏ETC复合物I的活性并导致线粒体功能障碍[160, 161]。
由 NPs 诱导的 DNA 损伤已被证明会抑制氨基酸合成、复制 [162],并导致 p53 [163] 和 Rab51 蛋白的异常积累 [82, 142]。 DNA 损伤也可能延迟或完全阻止细胞 [164]。 DNA受损的细胞失去生长和增殖能力[165],最终可能导致细胞死亡[166](图3)。
<图片>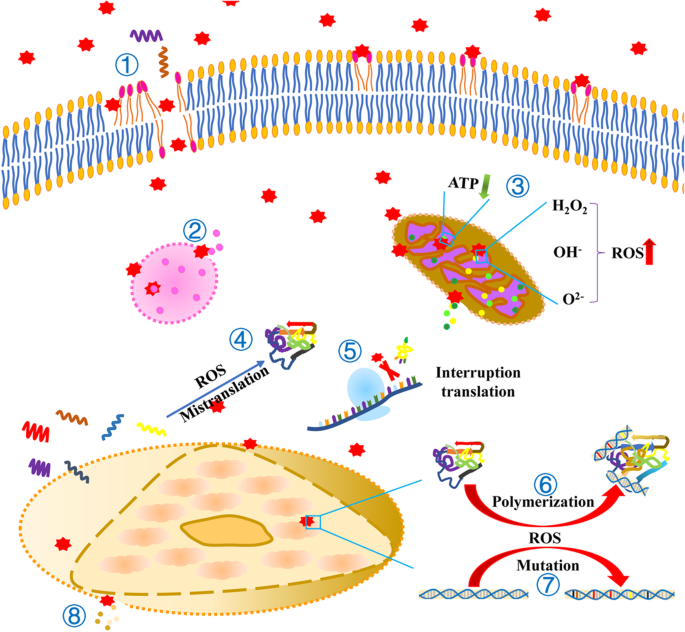
由 NPs 诱导的细胞事件。 ① NPs 有助于细胞膜的破坏和脂质过氧化。 ②溶酶体膜被NPs破坏并导致其内容物的释放。 ③ NPs损伤线粒体膜,导致内容物释放。 NPs 减少 ATP 的产生并增加 ROS 的产生。 ④ NPs 诱导的 ROS 导致 RNA 的错误翻译。 ⑤ NPs 阻止 tRNA 与核糖体结合。 ⑥ NPs 诱导的 ROS 导致蛋白质和 DNA 的聚合。 ⑦ NPs 诱导的 ROS 导致 DNA 突变 ⑧ NPs 破坏核膜,导致其内容物释放
ROS 的产生增加导致细胞损伤和疾病发生
NP 细胞毒性与氧化应激、内源性 ROS 产生和细胞内抗氧化剂库的消耗有关。氧化应激的增加导致生物大分子氧化损伤,进而影响细胞的正常功能,促进各种疾病的发生发展[167]。
NPs 诱导膜损伤并增强 NPs 向细胞质的转运。 NPs 集中在溶酶体、线粒体和细胞核中,这会给细胞带来灾难性的后果 [168, 169]。据报道,NPs 可以减少三磷酸腺苷 (ATP) 的产生 [89],消耗谷胱甘肽,诱导蛋白质错误翻译 [170],使溶酶体破裂 [171],并抑制核糖体亚基与转移 RNA (tRNA) 的结合。这些细胞事件表明细胞中基本生物过程的崩溃并导致细胞活力显着降低 [47]。 Singh 和 Scherz-Shouval 等人。报道NPs可通过诱导ROS产生干扰细胞骨架功能,激活细胞自噬和凋亡过程[89]。
NPs 通过不同途径进入人体,例如通过皮肤、肺或肠道(图 4a),并且可以产生多种毒理学效应并诱导生物学反应,例如炎症和免疫反应 [172,173,174]。在一种情况下,细胞暴露于二氧化硅纳米粒子导致巨噬细胞分泌大量白细胞介素-1β(IL-1β),最终导致细胞死亡[175]。 Gao 及其同事报告说,暴露于碳纳米管后,小鼠的肺部炎症明显更高,碳纳米管可以激活肺泡巨噬细胞并诱导强烈的炎症反应 [176]。在另一项研究中,暴露于 ZnO NPs 的豚鼠肺部受损,导致总肺活量和肺活量降低 [177,178,179]。
<图片>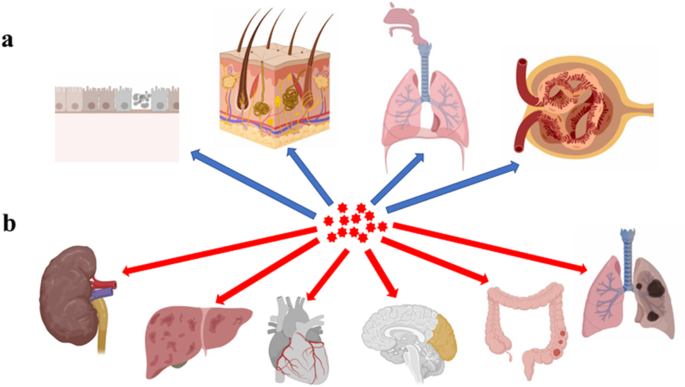
NP进入和器官损伤。 一 NPs可以通过口腔、鼻腔、呼吸道、肾脏和肠道进入机体; b NPs可通过体循环扩散并在肾脏、肝脏、心脏、大脑、肠道和肺部积聚,导致器官功能障碍(此图来自BioRender.com)。
ZnO NPs 还会引起肺泡上皮屏障的严重损伤,并引起人肺炎症 [180]。在另一种情况下,NPs 被吸收到肠道中会导致肠黏膜发炎和降解 [181]。舒巴耶夫等人。注意到 Mg NPs 通过以 MMP 依赖性方式降解血脑和血神经屏障来增强巨噬细胞向神经系统的迁移 [182]。此外,吸入碳纳米管的小鼠在幼稚脾细胞中表现出免疫抑制和抗体反应[183]。最后,Cd NPs 导致血液单核细胞活力严重下降,最终导致免疫缺陷[184]。
除了上述病理,高度可变的 ROS 水平已被确定为许多人类疾病发展的主要原因。 Tretyakova 和 Liou 等人。表明氧化的 DNA 倾向于形成 DNA-蛋白质结合物,其在心脏和大脑中积累并导致癌症、衰老相关疾病和慢性炎症的发生 [185, 186]。 Andersen [187] 得出结论,糖尿病以及心血管和神经退行性疾病与 ROS 的失衡密切相关。此外,Pérez-Rosés 等人。表明增加的 ROS 促进了阿尔茨海默病和帕金森病的发展 [188]。
有进一步报道,NPs通过促进ROS的产生促进乳腺癌细胞凋亡[35]并破坏恶性组织和病原体[189、190]。然而,也发现 ROS 可诱导正常细胞和癌细胞的增殖,刺激突变,并启动正常细胞的致癌作用和癌细胞的多药耐药性 [191, 192]。汉迪等人。发现暴露于碳纳米管的鱼在暴露时间延长后,肺部出现肉芽肿,肝脏出现肿瘤 [193]。一些 NPs 已导致多器官衰竭,主要影响心脏、肺、肾脏和肝脏。 TiO2 NPs 已被证明可促进体重减轻、脾脏损伤、呼吸系统凝血、肝细胞坏死和纤维化以及肺泡间隔增厚 [194, 195]。在一项研究中,NPs 还阻止了干细胞分化,从而加重了器官损伤 [196]。进一步的研究还报告说,NPs 会降低精子质量 [197],并且精子暴露于碳 NPs 会影响它们使卵子受精的能力并损害紫海胆胚胎的发育 [198]。越来越多的证据表明纳米颗粒对微生物、藻类、线虫、植物、动物和人类的毒理学影响 [22, 199, 200](图 4b)。
具有更少或无细胞毒性的新型纳米颗粒
NPs 具有一系列生物医学特性,使其具有价值(例如,作为抗菌剂和抗癌剂 [26,27,28])。它们的主要作用方式是能够增加细胞中 ROS 的产生;然而,这种特性也使这些颗粒具有毒性,导致基因突变、细胞凋亡,甚至致癌 [45, 49, 58]。因此,迫切需要开发新的 NPs,在不导致过量 ROS 产生的情况下保留其所需的特性。最近的研究报道了可以去除细胞内 ROS 的新型 NPs。这些类型分为两类:(1) 可以清除 ROS 的 NPs [77] 和 (2) 涂有额外材料以降低其细胞毒性的 NPs [87]。
Panikkanvalappil 及其同事表明,Pt NPs 通过降解 ROS 来抑制 DNA 的双链断裂 [201]。在另一种情况下,Mn3O4 NPs 调节细胞氧化还原,从而保护生物大分子免受氧化应激[77]。此外,CeO2 NP是一种新型试剂,具有清除自由基的能力,可保护细胞和组织免受氧化损伤[79, 202]。
H2O2 是 NP 细胞相互作用的主要副产品。 H2O2 会破坏重要的生物分子,包括蛋白质、脂质和核酸。然而,当细胞用涂有巯基丙酸 (MPA-NPs) 或胺化二氧化硅 (SiO2-MNPs) 的特化 MNPs 处理时,没有观察到这种损伤 [203, 204]。同样,用聚乙烯吡咯烷酮 (PVP) 包覆的 GO 对树突状细胞 (DC)、T 淋巴细胞和巨噬细胞的毒性作用比没有这种涂层的少。 PVP-GO 已被证明可以减少 T 淋巴细胞的凋亡,甚至增加巨噬细胞的活性 [205]。 Pt 包覆的 AuNRs (PtAuNRs) 保留了传统金纳米棒 (AuNR) 的功效,可以在清除 ROS 的同时触发所需细胞的细胞死亡,从而保护健康、未经处理的细胞免受 ROS 产生诱导的间接死亡 [87]。
结论和展望
NPs 具有独特的物理化学性质(例如超小尺寸、大表面积质量比和高反应性),使其在不同的应用中非常受欢迎。用于商业目的的工程纳米粒子一直在迅速增加。正因如此,纳米颗粒的生物安全性越来越受到公众的关注。在这篇综述中,我们总结了 NPs 在细胞水平上形成 ROS 的机制和原因,以及生物医学领域中 ROS 相关 NP 毒性的最新进展,并强调了细胞友好型 NPs 的新兴领域。由 NPs 诱导的 ROS 的产生与其大小、形态、表面积和成分有关。此外,ROS在细胞生物学和生物医学中具有生物多功能性,是细胞信号传导的关键介质,包括细胞凋亡、活力和分化。
然而,要提高纳米颗粒的生物安全性并加速其在生物医学领域的应用,还需要克服一些瓶颈,还需要做很多工作。首先,预计高通量方法 (HTM) 旨在有效检测 NPs 的体外和体内生物毒性。 HTM 可以节省时间和资源,在单个系统上组合多个参数,并最大限度地减少方法或系统错误。它还可以深入了解纳米颗粒特性与细胞反应之间的关系,有助于我们确定最佳条件。
其次,与 NP 诱导的 ROS 的生物毒性相关的分子和细胞机制尚不清楚。需要进一步探索与 NPs 形成 ROS 相关的机制,这将为修改 NPs 的化学物理特性以控制 ROS 生成提供更多信息。这可以帮助研究人员制定新的策略来降低工程化纳米颗粒的危害,从而加速其在生物医学领域的临床和商业转化。
最后,由于其结构特性,NPs可以通过多种途径自由进入体内,NPs在体内的积累会诱发炎症和免疫反应,导致细胞损伤或死亡、器官功能障碍,最终刺激炎症的发生。许多疾病,如阿尔茨海默氏症、帕金森氏症、肝脏炎症和胚胎发育不良。随着NPs的广泛使用,这些问题变得更加紧迫。
数据和材料的可用性
本研究期间生成或分析的所有数据均包含在这篇已发表的文章 [及其补充信息文件] 中。
缩写
- •OH:
-
羟基
- 2-oxoA:
-
1,2-二氢-2-氧代腺嘌呤
- 8-oxoG:
-
8-oxo-7,8 二氢鸟嘌呤
- Ag NP:
-
银纳米粒子
- AP-1:
-
转录因子激活蛋白-1
- ATP:
-
三磷酸腺苷
- AuNR:
-
金纳米棒
- CFDNP:
-
燃烧和摩擦衍生的纳米粒子
- DC:
-
树突状细胞
- D-NP:
-
仿天花金属纳米粒子
- EGF:
-
表皮生长因子
- ER:
-
内质网
- ETC:
-
线粒体电子传递链
- Fe3O4-PEG-G5-MMP2@Ce6:
-
Fe3O4-聚乙二醇-聚酰胺-胺-基质金属蛋白酶2@二氢卟酚e6
- H2O2:
-
过氧化氢
- HS-Fe-PEG-HER2 NP:
-
空心二氧化硅-铁-聚乙二醇-人表皮生长因子受体2纳米粒
- LDH:
-
乳酸脱氢酶
- MMP:
-
线粒体膜电位
- MPA-NP:
-
巯基丙酸包覆的MNPs
- NADP + /NADPH:
-
氧化/还原磷酸烟酰胺腺嘌呤二核苷酸
- NF-κB:
-
核因子-κB
- N-NP:
-
仿夜花金属纳米粒子
- NP:
-
纳米粒子
- O 2- :
-
反应性超氧阴离子自由基
- pDNA-PEI-CeO NP:
-
pDNA-聚乙烯亚胺CeO纳米颗粒
- PtAuNR:
-
铂包覆AuNRs
- PVP:
-
聚乙烯吡咯烷酮
- ROS:
-
活性氧
- SiO2-MNP:
-
含胺化二氧化硅的 MNPs
- tRNA:
-
转移RNA
纳米材料


