从含铬氧化铝污泥制备氧化铝纳米棒
摘要
以含铬氧化铝污泥为原料制备氧化铝纳米棒,并研究了掺杂铬、铁、镁等元素的影响。结果表明,氧化铝的晶体转变受到掺杂Cr的限制,而掺杂的Fe和Mg促进了氧化铝的晶体转变,后者由θ转变 -Al2O3 到 α -Al2O3 在煅烧过程中。同时,含铬氧化铝污泥中的共掺杂元素强烈抑制了氧化铝的晶体转变。掺杂元素改变了相结构转变的过程,并略微改变了氧化铝纳米棒的化学键。杂质元素掺杂在氧化铝晶体中,并按规律抑制氧化铝纳米棒的晶体生长。含铬氧化铝污泥制备的样品中,Cr和Mg掺杂较多,Fe掺杂较少,大部分Cr以Cr(III)形式存在。 Fe 掺杂可能受到 Cr 和 Mg 竞争的限制。此外,氧化铝的晶格缺陷是由掺杂的离子,如铬、铁和镁引起的,并影响氧和铝的化学状态。这些实验结果为消除污染和促进含铬氧化铝污泥的综合利用提供了重要信息。
背景
低维纳米氧化铝,如氧化铝纳米纤维[1,2,3]和氧化铝纳米棒[4],具有强度高、弹性模量高、化学稳定性好、隔热性能好、导热系数低等优越性能[5, 6,7,8,9],因此它被广泛应用于各个领域,如陶瓷基复合材料和金属基复合材料的增强以及催化剂、催化剂载体、吸附剂、膜反应器、涂层和阳极材料 [4, 10, 11、12、13、14、15]。然而,高昂的生产成本限制了它的应用。一些作者报道了成功的低维纳米氧化铝的合成方法,主要有固相法、气相法[16]和液相法[17、18]。其中,液相法以其反应条件温和、产物均一、生产成本低而得到广泛应用。关于溶胶-凝胶法[5, 19,20,21]、微乳液法[22]、水热法[23]、沉淀法[23]、化学气相沉积法[16]、和静电纺丝 [1, 3, 24, 25]。但沉淀法能耗低、产品均一、尺寸和形状可控,适合实验室和工业应用。
含铬氧化铝污泥是一种危险的固体废物,是在铬制品生产过程中采用无钙焙烧法产生的。每吨铬产品产生七千公斤含铬氧化铝污泥。由55 ~ 65%的Al2O3、7 ~ 13%的铬和少量的硅、铁、镁、钠的化合物组成。含铬氧化铝污泥的成分如表1所示,由制造商(中国中信锦州金属有限公司)提供。
铬作为主要有害物质,以Cr(III)或Cr(VI)形式存在于含铬氧化铝污泥中,Cr(VI)因其致癌性而被认为是主要污染物[26]。目前,含铬氧化铝污泥的溶液污染主要是脱毒利用。前者将 Cr(VI) 转化为低毒 Cr(III),并将其作为废渣储存。张大磊 [27] 提到了一种利用秸秆将 Cr(VI) 转化为 Cr(III) 的热解方法。段素华[28]指出,含铬渣可用工业酒精处理。但是,上述方法不仅占用土地,而且造成了极大的资源浪费。更有什者,可能会出现意想不到的二次污染。后一种方法是对含铬氧化铝污泥中的有用成分进行分离利用。薛文东 [29] 报道,含铬氧化铝污泥可用于制备耐火材料。然而,上述方法可能因其附加值低而受到限制。因此,应提出一些新的方法来消除污染,促进含铬氧化铝污泥的综合利用,既可以解决环境问题,又可以带来巨大的经济效益。
本文以含铬氧化铝污泥为原料,采用沉淀-煅烧法制备氧化铝纳米棒。同时,为了研究单掺杂离子对氧化铝纳米棒的影响,制备并表征了非掺杂或单掺杂的氧化铝纳米棒。研究结果将为消除污染、促进含铬氧化铝污泥的综合利用提供技术支持。
方法
材料
本研究中使用的试剂(例如,十八水硫酸铝、硫酸铬、硫酸铁、硫酸镁、氢氧化钠、硫酸和十二烷基苯磺酸钠)为分析纯化学品。含铬氧化铝污泥由中信锦州金属有限公司(中国)提供。所有溶液均用去离子水配制。
含铬氧化铝污泥的处理
首先,将含铬氧化铝污泥按固液比1:5(g/mL)用去离子水洗涤过滤。因此,大部分 Cr 6+ 从含铬氧化铝污泥中分离出化合物。然后将滤饼按1:3(g/mL)的固液比用硫酸溶解,然后用H2O2转化残留的Cr 6+ 到 Cr 3+ .最后成功得到含铬氧化铝污泥酸溶液,并用化学滴定和可见光分光光度计(VIS,721N,美国瓦里安)进行成分分析,见表2。
氧化铝纳米棒的合成
在85℃磁力搅拌下,将每升2mol NaOH溶液和十二烷基苯磺酸盐溶液缓慢加入0.25mol/L Al2(SO4)3溶液中,用NaOH或H2SO4将混合溶液的pH值调至9.0解决方案。搅拌 5 小时并老化 20 小时后,分离沉淀物并用去离子水和乙醇洗涤数次。随后,将样品在 40°C 下真空干燥 15 小时,然后制备前体。最后,将样品在 250°C 煅烧 1 小时、400°C 1 小时、770°C 1 小时、900°C 1 小时和 1050°C 2 小时连续煅烧,然后收集样品用来。未掺杂氧化铝由纯 Al2(SO4)3 溶液制备,离子掺杂样品采用与上述相同的方法制备。同时,根据含铬氧化铝污泥中掺杂元素的含量(表2),在Al2(SO4)3溶液中加入Cr、Fe和Mg的氯酸盐,Cr掺杂、Fe掺杂、制备了掺镁氧化铝。以含铬氧化铝污泥酸溶液为原料,以含铬氧化铝污泥为原料制备氧化铝,命名为氧化铝。
纳米氧化铝棒的特性
使用 D/MAX-RB X 射线衍射仪(日本理学)通过 X 射线粉末衍射(XRD)对样品的晶相进行表征,Cu K 辐射在 10°–70° 的 2θ 范围内进行扫描2°/分钟的速度。样品的傅里叶变换红外光谱 (FT-IR) 使用 Scimitar 2000 Near FT-IR Spectrometer (Thermoelectron, USA) 进行表征,光谱记录范围为 4000-400 cm -1 .前驱体的热稳定性通过热重分析仪(TG-DSC,STA449F3,NETZSCH,德国)在空气气氛中以 30 mL/min 的流速和 15–1200 °C 的温度和 10 °C 的加热速率进行检测℃/分钟。通过场发射透射电子显微镜(FETEM,Jem-2100F,JEOL,日本)检查样品的形态、晶体结构和元素分布。样品的 X 射线光电子能谱 (XPS) 光谱记录在配备半球形电子分析仪和 Al Kα 的 XPS (ESCAMABMKLL, VG, UK) 上 X射线源。
结果与讨论
氧化铝纳米棒的 XRD 表征
记录 XRD 图案以确认样品的晶体结构,如图 1 所示。对于未掺杂的氧化铝纳米棒,XRD 结果显示存在不同的氧化铝晶体结构,包括刚玉 (α -Al2O3,syn)(JCPDS No. 46–1212)和氧化铝(θ -Al2O3, JCPDS No. 35–0121),以及 θ 的衍射峰 -Al2O3 较弱(图 1(a))。一般来说,氧化铝从过渡态θ转变 -Al2O3 到稳态 α -Al2O3 在 1000 ~ 1200 °C。与未掺杂的样品相比,Cr掺杂的氧化铝纳米棒具有相对更强的θ峰 -Al2O3 和相对较弱的 α 峰 -Al2O3(图 1 (b))。这意味着在煅烧过程中掺杂的 Cr 限制了晶体转变,所以 θ -Al2O3 转化为 α -Al2O3 在 1050°C 下煅烧后。从图 1 (c) 可以看出,α 的峰值 -Al2O3 比 (a) 和 (b) 中的更强和更锋利,表明更大的晶体尺寸和更好的结晶度。同时,θ的峰值 -Al2O3 甚至更弱,这表明掺杂的 Fe 促进了晶体转变。可能是因为更多的θ -Al2O3 转化为 α -Al2O3 煅烧后。图 1 (d) 表明掺杂 Mg 的氧化铝纳米棒具有相对更强和更尖锐的 α 峰 -Al2O3 和相对较弱的 θ 峰 -Al2O3。建议样本中含有更多的α -Al2O3 及以下 θ -Al2O3,这可能是由于掺杂的Mg促进了氧化铝在煅烧过程中的晶体转变。对于由含铬氧化铝污泥制备的氧化铝纳米棒,α -Al2O3 几乎消失,而 θ 的峰 -Al2O3 变得更强但不够锋利(图 1 (e))。表明 θ -Al2O3 结晶度差,晶体尺寸较小。这可能是因为氧化铝中掺杂了较多的含铬氧化铝泥中的杂质元素,在煅烧过程中限制了氧化铝的晶态转变。所以,θ -Al2O3 很少转化为 α -Al2O3。
<图片>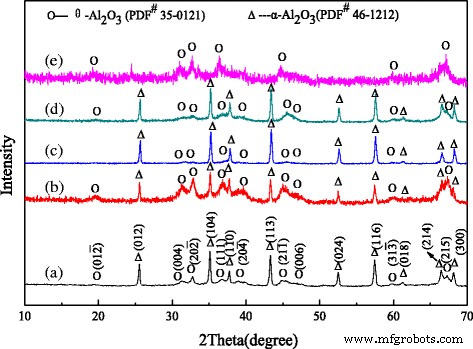
掺杂不同离子的氧化铝纳米棒的XRD图谱:a 未掺杂氧化铝,b Cr掺杂氧化铝,c 铁掺杂氧化铝,d Mg掺杂的氧化铝和e 含铬氧化铝污泥制备氧化铝
氧化铝纳米棒的 FT-IR 光谱
氧化铝纳米棒在 4000-400 cm -1 范围内的 FT-IR 光谱 如图 2 [27] 所示。吸收峰位于 3500–3300 和 1635 cm -1 出现在所有光谱中的振动分别归因于 OH 基团的非化学键缔合的伸缩振动和 H-O-H 弯曲振动,表明样品中存在孔隙水和吸附水 [30]。 2360 cm −1 处的峰值 归因于二氧化碳的存在。图 2 (2) 显示了样品的 FT-IR 光谱的指纹区域。如图 2 (2a) 所示,对于未掺杂的样品,峰值在 829、589 和 449 cm -1 归因于 AlO6 振动,表明 α 的形成 -Al2O3 [1]。同时,在 762 cm −1 处的峰值 归因于 Al-O-Al 的弯曲振动,以及 663 和 488 cm -1 分别归因于Al-O的伸缩振动和弯曲振动,表明形成了θ -Al2O3。图 2 (2b) 显示 α 的峰 -Al2O3 比图 2(2a) 中的弱,表明 Cr 掺杂阻止了 α 的形成 -Al2O3 在煅烧过程中。对于 Fe 和 Mg 掺杂的氧化铝,θ 的峰 -Al2O3 变弱,α 的峰 -Al2O3 变化很小(图 2 (2c,d))。与图 2(2a) 相比,峰略有红移或蓝移,说明掺杂的 Fe 和 Mg 有利于 α 的生长 -Al2O3 并略微改变氧化铝纳米棒的化学键。图 2 (2e) 是由含铬氧化铝污泥制备的氧化铝纳米棒的 FT-IR 光谱指纹区。低于 500 cm −1 的峰值 消失,表示没有α 样品中的 -Al2O3。此外,900–500 cm -1 处的峰值 分散,这可能是 M-O 和 M-O-M 振动的结果(M 是 Al 或含铬氧化铝污泥中的氧化铝掺杂元素)。以上结果与XRD结果一致。
<图片>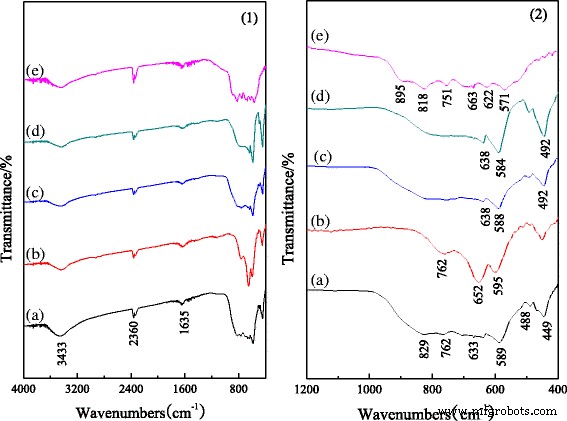
掺杂不同离子的纳米氧化铝棒的红外光谱:a 未掺杂氧化铝,b Cr掺杂氧化铝,c 铁掺杂氧化铝,d Mg掺杂的氧化铝和e 含铬氧化铝污泥制备氧化铝
氧化铝纳米棒的 TG-DSC
氧化铝纳米棒前驱体的热重分析仪 (TG) 和差示扫描量热法 (DSC) 曲线如图 3 所示。XRD 结果表明氧化铝纳米棒前驱体为 Al2O(OH) (JCPDS No. 49–0133)。如图 3a 所示,在空气中,未掺杂的样品只能看到三个阶段。低于 250°C,TG 曲线上约 40% 的质量损失和 DSC 曲线上 50 和 150°C 处的相应吸热峰与水分蒸发和吸附水解吸有关。第二阶段在 250 到 730°C 之间,总质量损失约为 35%,两个吸热峰位于 320 和 694°C。在 320 °C 的温度下,吸热峰是由于 AlO(OH) 转变为非晶 Al2O3。同时,694°C 处的弱吸热峰归因于非晶 Al2O3 向 θ 的转变 -Al2O3。在730°C以上的第三阶段,在980°C处有少量质量损失和强吸热峰,这主要是θ转化的结果 -Al2O3 到 α -Al2O3。与未掺杂的样品相比,金属离子掺杂使吸热峰发生偏移。图 3b-e 显示吸热峰转移到更高的温度并变宽。可能是因为掺杂离子改变了相结构转变的过程,所以θ的转变程度 -Al2O3 到 α 每个样品的 -Al2O3 都不同。结果与XRD和FT-IR一致。
<图片>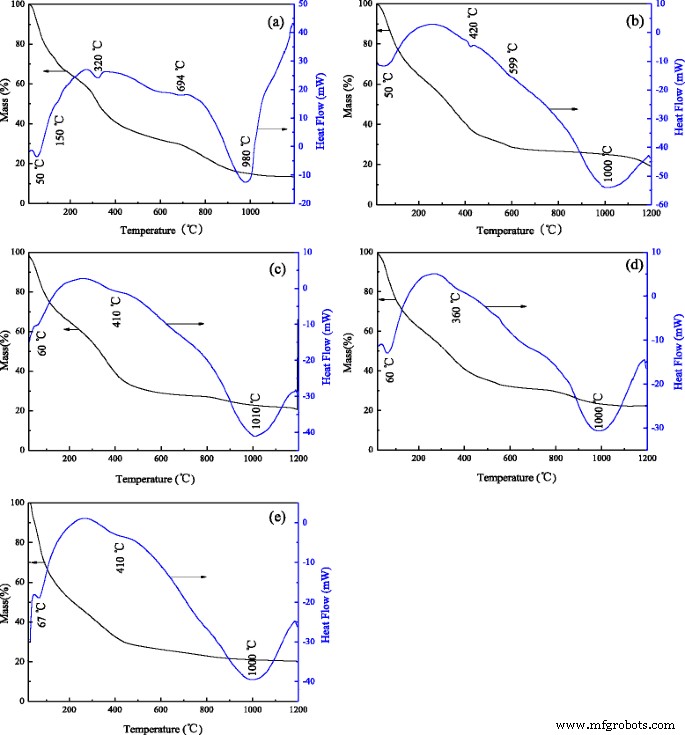
掺杂不同离子的纳米氧化铝棒前驱体的TG和DSC:a 未掺杂氧化铝,b Cr掺杂氧化铝,c 铁掺杂氧化铝,d 掺镁氧化铝和e 含铬氧化铝污泥制备氧化铝
氧化铝纳米棒的 TEM、SAED 和 HRTEM 图像
图 4 给出了 TEM、选区电子衍射 (SAED) 和高分辨率透射电子显微镜 (HRTEM) 结果。如图 4 (a1-a3) 所示,未掺杂的氧化铝是分散的纳米棒,直径为 4-6 nm,长度为 20-60 nm。同时,(215), (006), (21 \( \overline{1} \)) 和 (20 \( \overline{4} \)) 平面符合 θ -Al2O3 (JCPDS No. 35–0121),以及 (300)、(214)、(113) 和 (104) 平面与 α 相关 -Al2O3(JCPDS 编号 46–1212)。此外,观察到的 0.273 和 0.284 nm 的面间距可以分配给 θ 的 (20 \( \overline{2} \)) 和 (004) 平面 -Al2O3,0.255 和 0.348 nm 的晶格间距可以对应于 α 的 (104) 和 (012) 面 -Al2O3。与未掺杂的样品相比,Cr 掺杂的样品是直径为 4-6 纳米、长度为 50-120 纳米的纳米棒(图 4(b1))。图 4 (b2) 表明 (215)、(21 \( \overline{1} \))、(20 \( \overline{2} \)) 和 (111) 平面符合 θ -Al2O3,(300)、(214)、(113)、(104)面与α一致 -Al2O3。如图 4 (b3) 所示,0.202 nm、0.273 nm、0.284 nm 和 0.454 nm 的面间距分配给 (21 \( \overline{1} \)), (20 \( \overline{ 2} \)), (004), 和 (10 \( \overline{2} \)) θ 平面 -Al2O3,以及 0.209 和 0.238 nm 的晶面距离分配给 α 的 (113) 和 (110) 平面 -Al2O3。图 4 (c1) 显示 Fe 掺杂样品是直径为 5-10 nm 和长度为 30-100 nm 的纳米棒和约 10 nm 纳米颗粒的混合物。图 4 (c2) 显示 (20 \( \overline{2} \)) 平面与 θ 一致 -Al2O3,且(300)、(214)、(024)、(113)、(104)和(116)面与α一致 -Al2O3,与XRD结果一致。同时,观察到的 0.284 和 0.454 nm 的面间距被分配给 θ 的 (004) 和 (10 \( \overline{2} \)) 平面 -Al2O3,0.238 和 0.255 nm 的晶面距离分配给 α 的 (110) 和 (104) 平面 -Al2O3(图 4 (c3))。
<图片>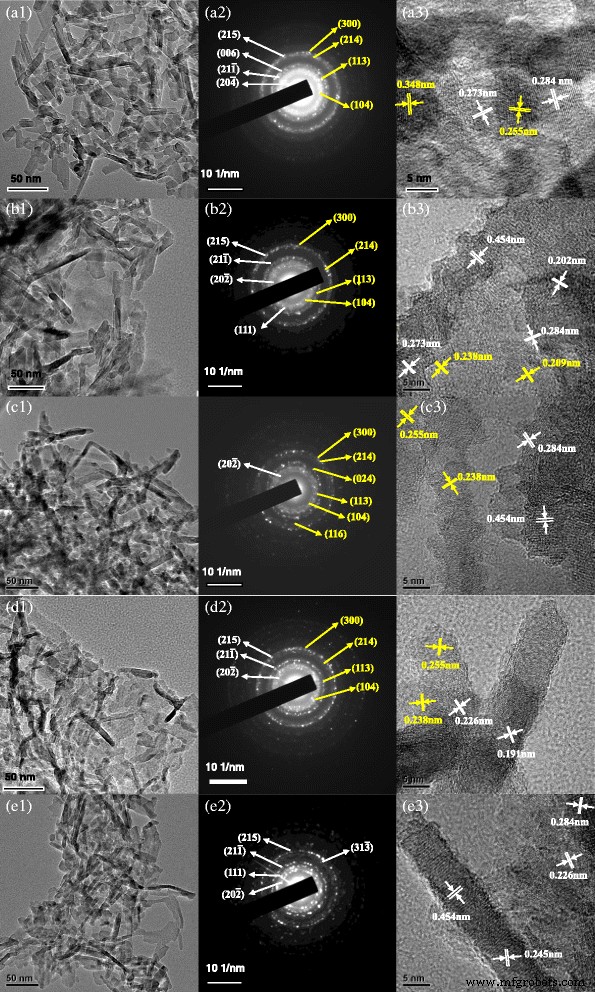
掺杂不同离子的氧化铝纳米棒的TEM、SAED和HRTEM:a 未掺杂氧化铝,b Cr掺杂氧化铝,c 铁掺杂氧化铝,d Mg掺杂的氧化铝和e 由含铬氧化铝污泥制备的氧化铝。 (1) 透射电镜; (2) 萨德; (3) 人力资源管理
如图 4 (d1-d3) 所示,Mg 掺杂样品是分散良好的纳米棒,直径为 5-10 nm,长度为 20-50 nm,同时存在约 10 nm 的纳米颗粒。 SAED 结果表明 (215)、(21 \( \overline{1} \)) 和 (20 \( \overline{2} \)) 平面符合 θ -Al2O3,(300)、(214)、(113)、(104)面与α一致 -Al2O3。 HRTEM 结果表明,观察到的 0.226 和 0.191 nm 的面间距分配给 θ 的 (20 \( \overline{4} \)) 和 (006) 平面 -Al2O3,0.255 和 0.238 nm 的晶面距离分配给 α 的 (104) 和 (110) 平面 -Al2O3。图 4 (e1-e3) 表明,由含铬氧化铝污泥制备的样品是分散良好的纳米棒,直径为 4-6 纳米,长度为 50-100 纳米,同时存在约 5-10 纳米的纳米颗粒。 SAED 和 HRTEM 结果表明 (215), (111), (21 \( \overline{1} \)), (31 \( \overline{3} \)) 和 (20 \( \overline{2 } \)) 平面符合θ -Al2O3,观察到的 0.226、0.245、0.284 和 0.454 nm 的晶面间距被分配给 (20 \( \overline{4} \))、(111)、(004) 和 (10 \( \overline {2} \)) 它的平面。然而,没有平面符合α -Al2O3。因此,未掺杂的氧化铝纳米棒比其他纳米棒分散性好,颗粒形状规则。可能是杂质元素掺杂在氧化铝晶体中,按规律抑制了氧化铝纳米棒的晶体生长。因此,氧化铝纳米棒的形状和分散性受掺杂元素的影响。
掺杂不同离子的氧化铝纳米棒前驱体的 EDS 表征
EDS 结果表明,Cr、Fe 和 Mg 分别以 2.06、0.99 和 0.58% 的摩尔量掺杂在氧化铝纳米棒前体中(表 3)。该掺杂量接近于杂质元素的添加量(表 2),说明大部分杂质元素都掺杂在氧化铝纳米棒前驱体中。同时,对于由含铬氧化铝污泥制备的样品,Cr、Fe和Mg的掺杂摩尔量分别为2.11、0.14和0.96%。结果表明,大部分Cr和Mg掺杂在样品中,少量Fe掺杂在样品中。 Fe的掺杂可能受限于Cr和Mg的竞争。
掺杂不同离子的纳米氧化铝纤维的 XPS 表征
图 5 显示了 O1s 的 XPS 光谱 和 Al 2p .如图 5a 所示,531.90、531.85、531.15、531.20 和 532.00 eV 处的峰归因于未掺杂、Cr 掺杂、Fe 掺杂和 Mg 掺杂的氧化铝纳米棒和由含铬制备的样品氧化铝污泥,分别。峰值分配给 O 2− Al2O3 [31]。图 5b 显示了 Al 2p 在 74.00、74.25、74.75、74.38 和 73.90 eV 处的峰 分别归因于上述样本。峰归因于 Al 3+ 的 Al2O3。同时,高斯拟合证明了曲线的良好对称性,表明样品中形成的其他氧和铝较少。 O1s 未掺杂和 Cr 掺杂的氧化铝纳米棒和由含铬氧化铝污泥制备的样品的结合能 (BE) 接近并高于 Fe 和 Mg 掺杂的样品。最小的 O1s BE 的顺序如下:Fe 掺杂、Mg 掺杂、Cr 掺杂、未掺杂的氧化铝纳米棒,以及由含铬氧化铝污泥制备的样品。然而,Al2p BE 则相反。 XRD结果表明,更多的瞬态θ -Al2O3 存在于未掺杂和 Cr 掺杂的氧化铝纳米棒和由含铬氧化铝污泥制备的样品中,并且更多 α -Al2O3 存在于 Fe 掺杂和 Mg 掺杂的氧化铝纳米棒中。由于 θ 的配位形式 [AlO4] -Al2O3 和 [AlO6] 用于 α -Al2O3,有可能是 O1s [AlO6] 的 BE 更大,Al 2p BE 小于 [AlO4]。此外,Al2O3 的晶格缺陷是由 Cr、Fe 和 Mg 离子进入 Al2O3 晶格引起的。因此,O和Al的化学态受晶格缺陷的影响,结合能发生变化。
<图片>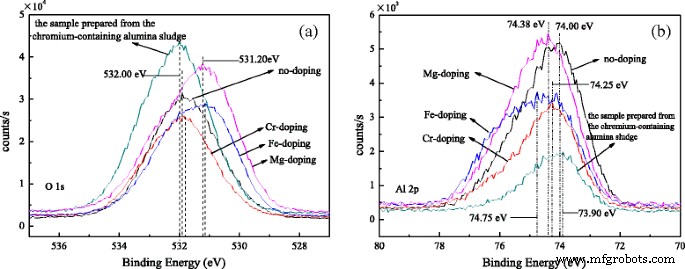
a 的 XPS 光谱 O1s 和 b Al 2p 掺杂不同离子的氧化铝纳米棒
图 6 显示了掺杂离子的 XPS 光谱。如图 6a 所示,589.80 eV 和 578.52 eV 处的峰被指定为 Cr 2p 1/2 和 Cr 2p Cr(VI) 的 3/2,587.53 和 577.39 eV 处的峰归属于 Cr 2p 1/2 和 Cr 2p 3/2 的 Cr(III)。这表明Cr以Cr(VI)和Cr(III)的形式存在于Cr掺杂的氧化铝纳米棒中。然而,在由含铬氧化铝污泥制备的样品中,大部分 Cr 以 Cr(III) 的形式存在。表明Cr掺杂样品在煅烧过程中部分Cr(III)被氧化,而由含铬氧化铝污泥制备的样品中Cr(III)被氧化较少。对于由含铬氧化铝泥制备的样品,由于 Cr-O 与杂质金属元素形成化学键结合,Cr 6+ 的电极电位 /Cr 3+ 在高温下增加,因此样品中很少有 Cr(VI)。如图 6b 所示,724.45 和 711.30 eV 处的峰归属于 Fe 2p 1/2 和 Fe 2p Fe2O3 的 3/2,以及 722.38 和 710.44 eV 分配给 Fe 2p 1/2 和 Fe 2p 3/2 的 Fe3O4。结果表明,Fe以Fe(II)和Fe(III)的形式存在于Fe掺杂样品中。这表明Fe元素进入氧化铝前驱体的晶格,并在合成过程中发生在晶格铝处。在随后的煅烧过程中,少量的Fe(III)被空气中的还原物质还原为Fe(II)。然而,由于样品中的 Fe 很少,因此在由含铬氧化铝污泥制备的样品中没有 Fe 峰(表 3)。如图 6c 所示,50.20 到 50.34 eV 的峰被指定为 Mg 2p MgO,表明 Mg 以 MgO 的形式存在于 Mg 掺杂的样品中。然而,Mg 2p 的峰值 在由含铬氧化铝污泥制备的样品中非常弱。 Mg 含量可能很少。结果与 EDS 一致。 XRD、FT-IR和XPS结果表明,单元素掺杂样品的晶格缺陷是由于金属元素的杂质进入氧化铝晶格而形成的。但由于多种元素的竞争,含铬氧化铝污泥制备的氧化铝晶格中Cr较多,Fe、Mg元素较少。
<图片>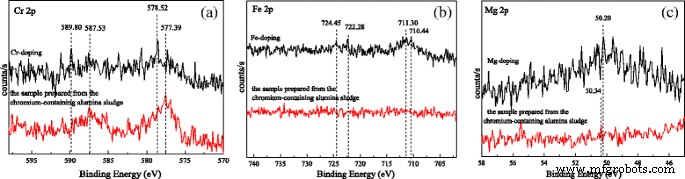
a 的 XPS 光谱 Cr 3+ 2p , b Fe 3+ 2p , 和 c 镁 2+ 2p
结论
总之,杂质元素掺杂在氧化铝纳米棒中,例如 Cr、Fe 和 Mg。氧化铝的晶体转变受到掺杂Cr的限制,并受掺杂的Fe和Mg促进,由θ转变 -Al2O3 到 α -Al2O3 在煅烧过程中。此外,氧化铝的晶体转变受到来自含铬氧化铝污泥的共掺杂元素的强烈抑制。掺杂元素会影响氧化铝纳米棒的相结构转变过程、化学键、微观结构以及O和Al的化学状态。在由含铬氧化铝污泥制备的样品中,Fe 掺杂受到 Cr 和 Mg 竞争的限制。本研究表明,可以利用含铬氧化铝污泥制备氧化铝纳米棒,以降低成本和消除污染。
缩写
- BE:
-
结合能
- DSC:
-
差示扫描量热分析
- EDS:
-
能量色散光谱仪
- FETEM:
-
场发射透射电子显微镜
- FT-IR:
-
傅里叶变换红外光谱
- HRTEM:
-
高分辨透射电子显微镜
- SAED:
-
选区电子衍射
- TEM:
-
透射电子显微镜
- TG:
-
热重分析仪
- XPS:
-
X射线光电子能谱
- XRD:
-
X射线粉末衍射
纳米材料


