纳米技术:从体内成像系统到受控给药
摘要
科学和技术一直是人类奋斗的生命线,专门用于开发从微米级到纳米级的新型工具和产品。纳米技术因其在生物医学中的广泛应用而受到广泛关注,特别是与生物成像和药物输送有关。各种纳米器件和纳米材料已被开发用于诊断和治疗不同的疾病。在此,我们描述了纳米医学的两个主要方面,即体内成像和药物递送,突出了最近的进展和未来的探索。最近观察到用于成像的纳米技术工具,特别是癌细胞的巨大进步。纳米粒子提供了一种合适的介质来进行分子水平的修饰,包括位点特定的成像和靶向。放射性核素、量子点、磁性纳米粒子和碳纳米管的发明以及金纳米粒子在生物传感器中的使用已经彻底改变了成像领域,从而使人们更容易了解疾病的病理生理学,提高诊断能力并增强治疗效果。纳米药物的这种高特异性和选择性很重要,因此,需要了解该领域的最新进展,才能更好地把握今天和更繁荣的未来。
评论
简介
事实上,纳米技术正在工程和科学的所有必要领域取得进步,科学家们正在通过设计能够在最小尺度长度上工作的东西,一个原子一个原子地彻底改变所有行业和人类生活[1]。纳米技术涉及对非常小的结构的研究。纳米技术可以概括地定义为通过在纳米尺度上将物质控制在 1-100 nm 的尺寸范围内来研究、创造、设计、合成和实现功能材料、系统和设备。此外,在这个纳米尺度上操纵创新现象和改善物质特性,也称为分子纳米技术,是尺度长度上的一个神奇点,最小的人造器具在这里遇到了宇宙的分子和原子 [2,3,4 ].
纳米技术和纳米医学概念的早期提出源于费曼的敏锐想法,即可以开发、制造微型纳米机器人和相关设备并将其引入人体以在分子水平上修复细胞。尽管在 1980 年代和 1990 年代后期,这种创新理念在 Drexler 的著名著作中得到了倡导[5, 6],在 1990 年代和 2000 年代在 Freitas 的流行著作中得到了倡导 [7, 8]。费曼提出了第一个已知的纳米医学程序来治疗心脏病的提议。总的来说,医疗工具的小型化将为提高人类生活质量提供更准确、可控、可靠、通用、经济高效和快速的方法[9]。 2000 年,第一次启动了国家纳米技术计划;从那时起,新材料的电子学和分子结构的建模、纳米级光子和电子器件的建立 [10, 11]、3D 网络的发展、纳米机器人 [12] 以及多频力显微镜 [13] 的出现都铺平了道路分子纳米技术的出现途径。
纳米粒子被认为是纳米技术的基本组成部分。强化学键的存在、随尺寸变化的价电子的广泛离域以及纳米粒子的结构改变导致不同的物理和化学性质,包括熔点、光学性质、磁性、比热和表面反应性。由于特定特征的变化,例如尺寸、分布和颗粒的变化,这些超细纳米颗粒与它们的大量对应物相比,表现出全新和改进的特性,从而产生更大的表面积与体积比 [14,15,16]。随着纳米结构材料领域的发展,正在使用许多不同的标签和术语,包括 3D 纳米粒子、纳米晶体、纳米薄膜、纳米管、纳米线和量子点,具有无限数量的潜力[17]。由于潜在应用的多样性(包括工业和军事),政府已在纳米技术研究上投入了数十亿美元。美国通过国家纳米技术计划投资37亿美元,欧盟也补贴12亿美元,日本投资7.5亿美元[18]。
今天,纳米技术是科学研究中最具创新性、最前沿的领域之一,它继续以惊人的速度发展 [19]。通过纳米技术的进步,许多最先进的技术可用于药物输送。研究人员广泛研究了纳米器件在多种生物医学应用(如癌症 [20, 21]、疫苗接种 [22])中靶向特异性和受控递送各种微分子和大分子(包括药物、蛋白质、单克隆抗体和 DNA(脱氧核糖核酸))的潜力、牙科 [23]、炎症 [24] 和其他健康障碍。因此,现在需要证明纳米技术应用的有效利用,从体内成像系统到受控药物递送,以标记当前的进展并为即将到来的医学领域的研究指明方向。
药物纳米系统
药物纳米技术可分为两大类纳米工具,即纳米材料和纳米器件。纳米材料可以根据三个基本参数进一步分类,包括结构、尺寸和相组成。纳米结构进一步分为聚合物和非聚合物结构,包括纳米颗粒、胶束、树枝状聚合物、药物偶联物、金属纳米颗粒和量子点 [25]。根据它们的尺寸,纳米材料分为四组,即零、一、二和三纳米材料。根据相组成,这些纳米材料可以分为三组。纳米设备细分为三组,包括微机电系统/纳米机电系统 (MEMS/NEMS)、微阵列和呼吸细胞。这些结构和设备可以制造出具有高度功能特性的药物,用于在分子水平上与细胞相互作用,从而实现生物系统和最新技术之间的整合,这是以前无法实现的 [26]。药物纳米工具的详细分类见表1。
制造方法
纳米尺寸技术对于难溶于水的药物的配方具有重要意义。根据 Noyes-Whitney 方程 [27],通过将粒径减小到纳米级范围,由于表面积增加,溶出率和生物利用度增加。用于制造材料的方法分为自下而上技术、自上而下技术以及自下而上和自上而下技术的组合。自下而上的技术涉及分子的构建。一些遵循自下而上方法制造纳米级材料的技术包括基于反胶束的液相技术、化学气相沉积 (CVD)、溶胶-凝胶处理和分子自组装。由于将它们结合在一起的共价力,自下而上产生的组件明显强于宏观组件。在自上而下的技术中,材料通过切割、雕刻和成型进行微粉化,以制造纳米材料。例子包括铣削、物理气相沉积、皮下注射技术电镀和纳米光刻 [28]。不同的制造方法及其各自的类型如表 2 所示。
先进纳米技术的生物医学应用
成像
在过去十年中报告了巨大的进步,使用纳米技术工具进行成像和治疗,特别是针对癌细胞的研究。大小为 10-100 nm 的纳米颗粒提供了一种非常适合进行分子水平修饰的介质,例如在癌细胞中进行位点特异性成像和靶向 [29]。以下部分总结了成像技术的一些最新进展。
放射性核素成像
由于无创技术无法观察小分子,因此采用定点造影剂来识别无法与正常周围组织分离的选定生物标志物 [30]。放射性核素成像的发展理念是用放射性药物或同位素标记的试剂或细胞探测表达的蛋白质,并在体内进一步跟踪 [31]。正电子发射断层扫描 (PET) 成像已成功用于癌症患者,使用 99 m tetrofosmin 和 sestamibi 作为 P-糖蛋白的放射性标记底物,通过 P-糖蛋白转运对多药耐药性进行成像 [32, 33]。成像机制由用于成像的模态类型决定,例如纳米载体,包括脂质体 [34]、树枝状聚合物 [35]、巴基球 [36] 和众多聚合物和共聚物 [37]。它们可以填充大量的成像粒子,例如光学活性化合物和放射性核素,以便用成像设备进行检测。 BODIPY(硼二吡咯甲烷)标记的 jasplakinolide 类似物已被用于观察活细胞内长寿命的肌动蛋白丝 [38, 39]。
纳米技术的巨大发展引领着许多造影剂的分子成像研究。为了获得适当的成像,所选的造影剂应具有更长的半衰期、低背景信号、特异性表位结合和增强的噪声对比度增强。大量的载体可用性能够定义成像方面的更多进步,特别关注疾病的分子和细胞机制;这将为成像和给药系统的合理发展创造更多机会[30]。
量子点
半导体量子点现在被用作一类新的荧光标记。由于这些半导体纳米晶体易于表面化学,因此它们是生物细胞可视化的有前途的工具,允许生物相容性并与荧光时间的延长结合 [29, 40]。量子点的可视化特性(荧光波长)与尺寸密切相关。量子点的光学特性取决于它们的结构,因为它们由外壳和金属核组成。例如,石墨烯量子点(GQD)是一种绿色荧光碳纳米材料,通过溶剂热法切割氧化石墨烯制成,并被发现在可视化性能中占主导地位[41]。
量子点核心通常由硒化镉、硫化镉或碲化镉组成。外壳在具有高带隙能量的核上制造,以提供电绝缘并保留量子点的荧光特性。具有特定波长可视化特性的不同尺寸和成分的微调核和壳提供了大量的生物标志物 [40]。量子点与不同的配体结合以获得与生物受体的特异性结合。肿瘤靶向配体与两亲聚合物量子点相连,用于在小鼠中进行前列腺癌的成像研究 [42]。类似地,量子点与传统染料相比具有显着优势,例如窄带宽发射、更高的光稳定性和单一激发源的扩展吸收光谱。此外,量子点疏水性的挑战已经通过使它们溶于水来克服。在生物体液中具有长保留时间的水性量子点的一个例子是用含硫醇的带电基团制造的高荧光金属硫化物 (MS) 量子点的开发 [43]。此外,量子点独特的荧光特性使其成为癌细胞的合适成像工具 [42]。与多柔比星 (QD-Apt-Dox) 偶联的 A10 RNA 适体连接的量子点是靶向癌细胞成像的示例 [44]。然而,由于掺入了重金属,已经观察到量子点的毒性增加,导致它们在体内成像中的应用受到限制。然而,最近的方法侧重于降低毒性和增强量子点对体细胞的生物相容性。还值得一提的是,直径小于 5.5 nm 的量子点可以快速有效地从尿液中排出,从而降低毒性。这种现象表现在合成无镉 CulnS2/ZnS(硫化铜铟/硫化锌)作为量子点的核和壳,从而增强了活细胞的淋巴结成像稳定性,并明显减少了急性局部毒性[45, 46].
生物传感器
近几年来,纳米材料取得的最大成就之一是生物传感器的发展。生物传感器是包含连接或集成在换能器中的生物传感元件的设备。生物传感器根据其结构,包括抗体抗原、酶底物和受体激素,通过识别体内特定分子来发挥其作用。生物传感器的两个主要特性包括它们的特异性和选择性取决于该识别系统。生物传感器的这些基本特性最重要的是用于与信号成正比的浓度[47,48,49]。
为了高效地生产生物传感器,选择用于传感材料分散的基板是先决条件。不同类型的纳米材料,包括量子点 [50]、磁性纳米粒子 [51]、碳纳米管 (CNT) [52] 和金纳米粒子 (GNP) [53] 被应用于生物传感器。纳米材料独特的化学、物理、磁性、光学和机械特性导致其检测的特异性和灵敏度增加。含有 GNP 的生物传感器为生物分子提供了一个兼容的环境,增加了电极表面固定化生物分子的浓度。它提高了生物传感器的灵敏度 [54, 55]。生物传感器中使用最广泛的电极表面是玻璃碳电极 (GCE),它是由 GNP 修饰而成的。此外,它们显示出最佳的灵敏度和电化学稳定性。在这方面,亚甲蓝 (MB) 和 GNP 很容易通过逐层 (LBL) 技术在 GCE 上以薄膜的形式组装和修饰,以检测人绒毛膜促性腺激素 (HCG) 的浓度 [56]。由于纳米颗粒含有较大的表面积以加载抗 HCG,这些免疫传感器有可能用于检测人血或尿样中的 HCG 浓度。同样,碳纳米管在生物医学工程、生物分析、生物传感和纳米电子学中也有很大的应用 [57,58,59]。此外,聚合物的生物纳米复合层形式的多壁碳纳米管 (MWNT) 有可能用于 DNA 检测 [60]。此外,磁性纳米粒子也因其磁性而得到广泛应用,包括磁共振成像 (MRI) 造影剂 [61]、热疗 [62]、免疫测定 [63]、组织修复 [64]、细胞分离 [65]、 GMR-sensor [66],药物或基因传递[67]。
同样,一种新型磁性壳聚糖微球 (MCMS) 也已通过简单地使用壳聚糖和碳包覆的磁性纳米粒子制备而成 [68]。在这项研究中,通过使用戊二醛作为交联剂,血红蛋白也成功地固定在 MCMS 修饰的 GCE 表面上。生物传感器的另一个重要应用是在光学技术中,包括使用 SsDNA-CNT 探针作为生物传感器检测各种 DNA 寡核苷酸 [69]。同样,基于脂质体的生物传感器也得到了相当多的关注,因为它们已被用于有机磷农药的监测,包括最低水平的对氧磷和敌敌畏[70]。
磁性纳米粒子
磁性纳米粒子 (MNP) 具有独特的磁性,因为它们能够在生物相互作用的分子或细胞水平上发挥作用,这使它们成为 MRI 中作为造影剂和药物输送中的载体的最佳化合物。纳米技术的最新进展引起了人们的关注,因为它有助于修改 MNP 的性质和特征以用于生物医学应用。在这方面,通过 RES 介导的超顺磁性氧化铁 (SPIO) 摄取的肝脏肿瘤和转移成像已被证明能够区分小至 2-3 毫米的病变 [70, 71]。此外,这些超小超磁性氧化铁 (USPIO) 在对直径仅 5 至 10 毫米的淋巴结转移成像方面也非常有效 [72]。此外,这种非侵入性方法在检测淋巴播散方面的重要性也已被证明,因为它被认为是乳腺癌分期和确定乳腺癌结肠癌和前列腺癌治疗方法的重要组成部分 [73]。
药物递送
由于纳米技术具有不同的物理、光学和电子特性,因此对于从材料科学到生物医学的各个学科来说都是一种有吸引力的工具。纳米技术最有效的研究领域是应用纳米技术原理治疗、预防和诊断疾病的纳米医学。此外,由于过去几十年来纳米医学研究在全球范围内激增,许多纳米医学产品已经上市。目前,纳米医学受药物输送系统的影响,占总销售额的 75% 以上 [74]。在这方面,基于纳米颗粒的药物递送平台已获得科学家的信任,因为它是解决与传统药物制剂相关的药代动力学缺陷的最合适的载体 [75]。因此,已尝试使用各种纳米形式作为药物递送系统,例如脂质体、固体脂质纳米粒子、树枝状聚合物和含固体金属的纳米粒子,以提高药物的治疗效果 [76, 77]。下面讨论了一些主要的兴趣领域。
眼科
通过眼科途径递送药物对制药科学家来说极具吸引力,但也极具挑战性。眼睛是一个微小而复杂的器官,有多个隔室。它的生物化学、生理学和解剖学使其对异生物质最不渗透。需要眼部给药的常见病症包括眼部感染,例如结膜炎以及青光眼等角膜疾病。眼部给药中最常见的药物类别包括散瞳药或散瞳药缩瞳药、抗感染药、抗炎药、诊断药和手术辅助药。对于小的眼球不规则,也需要基因治疗,在这方面正在进行大量的工作。纳米载体支持的方法因其适用性和特异性而受到科学家的关注。据报道,微粒递送系统如微球和纳米粒子以及囊泡载体如脂质体、niosomes、药效体和 discomes 改善了各种类型药物分子的药代动力学和药效学特性 [76]。已经出现了许多新的受控药物递送系统,包括水凝胶、粘膜粘附聚合物、微乳液、树枝状聚合物、离子电渗药物递送、基于 siRNA 的方法、干细胞技术、非病毒基因治疗和巩膜塞激光治疗 [78] .用于药物递送的不同系统被装扮成通过眼部途径递送药物。所有给药系统的主要目标是改善滞留时间,增强角膜通透性,并在眼后房释放药物,从而提高生物利用度并改善患者依从性[79]。
阿布雷戈等人。制备了普拉洛芬的 PLGA(聚乳酸共乙醇酸)纳米颗粒,用于水凝胶形式的眼科给药。这种水凝胶制剂具有合适的流变学和物理化学特性,可用于普拉洛芬的眼部递送,并具有改进的药物生物制药轮廓。此外,它加强了药物的局部抗炎和镇痛效果,从而提高了患者的依从性[80]。在另一项研究中,使用双乳液双交联技术开发了负载头孢呋辛的壳聚糖纳米颗粒。推论指出壳聚糖-明胶颗粒是眼内水平 DD 的有效实用候选物 [81]。此外,开发了负载双氯芬酸的 N-三甲基壳聚糖纳米颗粒 (DC-TMCN) 用于眼科,以提高药物的眼部生物利用度 [82]。此外,基于壳聚糖的地塞米松磷酸酯的纳米级超分子组装体已被开发用于改善角膜前药物的停留时间,因为它具有黏膜粘附特性。这些纳米颗粒与眼表和药物强烈相互作用,并保护药物免于代谢降解,导致角膜前停留时间延长 [83]。青光眼是一种眼科疾病,使用单硬脂酸甘油酯作为固体脂质,使用基于溴莫尼定的负载缓释固体脂质纳米颗粒进行治疗 [84, 85]。同样,载有达托霉素的壳聚糖包被海藻酸盐 (CS-ALG) 纳米颗粒被开发出来,具有适合眼部应用的合适尺寸和高封装效率(高达 92%)。该研究表明,未来可使用达托霉素纳米载体系统将这种抗生素直接输送到眼内,从而作为一种针对细菌性眼内炎的前瞻性治疗方法和壳聚糖纳米颗粒的有效替代品[86]。
角膜移植中移植物短期和长期失败的主要原因之一是免疫移植排斥。为此,制备了基于 PLGA 的地塞米松磷酸钠 (DSP) 的可生物降解纳米颗粒系统,导致皮质类固醇的持续释放,以防止角膜移植物的排斥反应 [87]。此外,还报道了姜黄素的 MePEG-PCL(聚乙二醇 - 聚己内酯)纳米颗粒,它们显示出更高的效率,增强了姜黄素在角膜中的保留,并且与游离姜黄素相比,在预防角膜新生血管方面有显着改善 [88]。同样,银纳米颗粒注入的组织粘合剂(氰基丙烯酸 2-辛酯)被开发出来,具有增强的机械强度和抗菌功效。这些掺杂的粘合剂(银纳米粒子)支持使用组织粘合剂作为缝合线的可行补充或替代品[89]。
肺病学
肺部疾病可能是哮喘、慢性阻塞性肺疾病 (COPD) 和肺癌的发生率很高,并且常常危及生命。例如,描述COPD是第四大死亡原因,而肺癌是全世界癌症死亡的最常见原因。纳米颗粒被视为改善这些严重疾病治疗的一种选择 [90]。各种载药纳米颗粒因其局部和全身作用而被用于治疗肺部疾病。将治疗剂输送到肺部疾病的作用部位可能允许有效治疗慢性肺部感染、肺癌、肺结核和其他呼吸道疾病 [91]。用于此目的的纳米载体包括脂质体、基于脂质或聚合物的胶束、树枝状聚合物和聚合物纳米颗粒 [92]。聚合物 NPs 具有重要意义,因为聚合物可以共聚、表面改性或生物共轭,以改善包封剂的靶向能力和分布。肺部给药常用的纳米载体包含天然聚合物如明胶、壳聚糖和海藻酸盐以及合成聚合物如泊洛沙姆、PLGA和PEG[93]。
据观察,PLGA NPs 作为肺蛋白质/DNA 传递的载体表现出最方便的一组特征,而明胶 NPs 是一种令人满意的互惠选择 [94]。同样,阿霉素和姜黄素的各向异性或 Janus 颗粒被配制为装载抗癌药物,用于通过吸入治疗肺癌。通过使用生物相容性和生物可降解材料二元混合物配制颗粒。这些颗粒没有表现出基因和细胞毒性后果。癌细胞将这些 Janus 颗粒内化,并将它们聚集在细胞核和细胞质中,从而导致滞留时间延长。此外,聚酰胺胺 (PAMAM) 树枝状大分子被评估为纳米载体,用于使用 G3、G4 和 G4 [12] 树枝状大分子对模型弱溶性抗哮喘药物二丙酸倍氯米松 (BDP) 进行肺部递送。该研究表明,BDP 树枝状聚合物具有使用喷气和振动网状雾化器进行肺部吸入的潜力。此外,据观察,气溶胶特性受雾化器设计而非树枝状聚合物的影响 [95]。此外,由无机金属、金属氧化物、准金属、有机可生物降解和无机生物相容性聚合物组成的工程纳米粒子 (ENP) 被有效地用作疫苗和药物递送的载体,以及用于管理各种肺部疾病。 ENP 对肺的特性和有效作用如图 1 所示。无机 ENP(银、金和碳 ENP)、金属氧化物 ENP(氧化铁、氧化锌和二氧化钛)和有机 ENP(基于脂质,基于多糖、基于聚合物基质)被开发和评估用于肺免疫止血。除了作为相对安全的载体外,现代研究表明 ENP 电缆具有抗炎特性(例如银和聚苯乙烯)和肺印记(例如,聚苯乙烯)的维持的有益结果。进一步了解这些机制可能有助于更好地理解 ENP 对肺免疫稳态和/或炎症性肺病管理的有用作用 [96]。
<图片>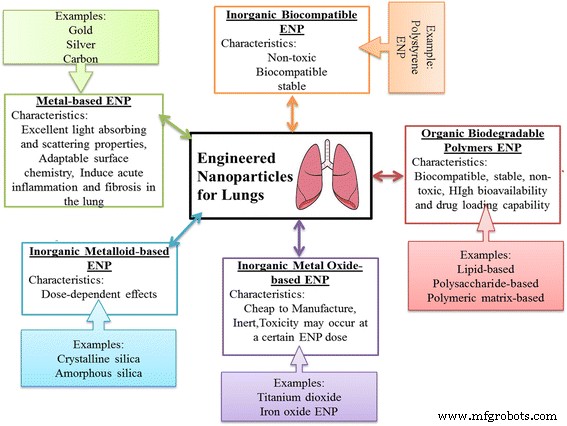
ENPs对肺的性质及疗效
重要的是要说明功能化的阳离子脂多胺(星号:Star-mPEG-550)最近已被开发用于将 siRNA(短干扰 RNA)体内递送至肺血管细胞。这种平衡的脂质配方加强了 siRNA 在小鼠肺中的保留,并实现了目标基因的显着分解。结果发现,通过使用功能化阳离子脂多胺纳米颗粒来招募肺动脉病变并纠正患有严重肺动脉高压 (PAH) 的大鼠的心脏功能 [97]。 /P>
心血管系统
心血管疾病是影响心血管系统、脑和肾脏血管疾病以及外周动脉疾病的疾病。尽管在药理学和临床管理方面取得了所有进展,但心力衰竭是世界范围内发病的首要原因。许多新的治疗策略,包括细胞移植、基因递送或治疗,以及细胞因子或其他小分子,已被研究用于治疗心力衰竭 [98]。发展中国家受影响的人数不足;超过 80% 的心血管疾病导致的死亡发生在不发达国家,并且几乎均匀地发生在男性和女性中 [99]。马瑟斯等人。 2008 年估计每年有 940 万人死亡 [100]。由此得出结论,45% 的死亡是由冠心病引起的,51% 的死亡是由心脏病引起的 [101]。药物载体的种类很多,如聚合物胶束、脂质体、树枝状大分子、脂蛋白负载型药物载体和纳米颗粒药物载体。
开发了包封率≥83% 的基于壳聚糖的西罗莫司脂质体,用于治疗再狭窄,并已被证明是一种有效靶向递送的新平台 [102]。同样,卡维地洛富含胆汁盐的 niosomes 具有 85% 的包封率,提高了药物的生物利用度,从而获得了更好的治疗效果 [103]。通过开发包裹 AGL 2043 和 AG1295(血小板衍生生长因子 (PDGF) 受体的选择性阻滞剂)的基于 PLGA 的纳米颗粒,可以抑制大鼠球囊损伤颈动脉的再狭窄 [104]。 Angiogenic therapy of myocardial ischemia with vascular endothelial growth factor (VEGF) is a favorable approach to overcome hypoxia and its sequel effects. Polymeric particles loaded with VEGF have been proved a promising system for delivery of cytokines to rat myocardial ischemic model. This approach could be further explored for clinical studies [105]. Coenzyme Q10 (CoQ10) owing to its role in mitochondrial electron transport chain appears to be a reliable candidate to treat myocardial ischemia (MI) but its poor biopharmaceutical characteristics needed to be addressed by developing promising delivery approaches. Polymeric nanoparticles were developed to encapsulate CoQ10 to overcome its poor pharmaceutical properties and administered to MI-induced rats. Cardiac function was analyzed by determining ejection fraction before and after 3 months of therapy. Results showed significant betterment in the ejection fraction after 3 months [106].
Oncology
Cancer is a prime cause of mortality around the globe. The World Health Organization determines that 84 million people die of cancer between 2005 and 2015. The eventual target of cancer therapeutics is to increase the life span and the quality of life of the patient by minimizing the systemic toxicity of chemotherapy [107]. Chemotherapeutic agents have widely been studied in oncology for the past 25 years, but their tumor specificity is unsatisfactory and therefore exhibit dose-dependent toxicity. To overcome this limitation, recent interest has been centered on developing nanoscale delivery carriers that can be targeted directly to the cancer cell, deliver the drug at a controlled rate, and optimize the therapeutic efficacy [108, 109]. Passive and active targeting is used to deliver the drug at its tumor site. The passive phenomenon called the “enhanced permeability and retention (EPR) effect,” discovered by Matsumura and Maeda, is the dominated pathway used for chemotherapeutics [110, 111]. Active targeting is achieved by grafting ligand at the surface of nanocarriers that bind to receptors or stimuli-based carriers, e.g., dual reverse thermosensitive [112], photo-responsive [113], magnetic nanoparticles [114], and enzymatically activated pro-drugs [115]. Nanoparticles (NPs) can be conjugated with various smart therapeutic carriers like polymeric nanoparticles [116], micelles [117], liposomes [118], solid lipid nanoparticles (SLNs) [119], protein nanoparticles [120], viral nanoparticles [121], metallic nanoparticles [122], aptamers [123], dendrimers [124], and monoclonal antibody [125] to improve their efficacy and decrease the systemic toxicity. Table 3 summarizes the different approaches for drug deliveries which are widely studied to target the tumor with maximize therapeutic response and minimum toxicity.
Biodegradable poly (o-caprolactone) nanocarriers loaded with tamoxifen were developed for the management of estrogen receptor-specific breast cancer [126]. This study suggested that the nanoparticle preparations of selective estrogen receptor modulators deliver the drug in the specific estrogen receptor zone resulting in enhanced therapeutic efficacy. Similarly, a nanoconjugation of doxorubicin and cisplatin was developed by Chohen et al. [127], which have exhibited enhanced efficiency and reduced side effects of the loaded drugs in the treatment of localized progressive breast cancer. Likewise, chemotherapeutic drug oxaliplatin-loaded nanoparticulate micelles were prepared by Cabral et al. [128], with sustained release of loaded drug in the tumor microenvironment, resulted in enhanced antitumor effect [128]. Furthermore, SLN loaded-5-FU resulted in enhanced bioavailability and sustained release of the encapsulated anticancer drug, leading to enhanced antitumor effect [129].
Conclusions
Nanotechnology is subjected to inordinate progress in various fronts especially to make innovations in healthcare. Target-selective drug delivery and approaches for molecular imaging are the areas of prime importance for research where nanotechnology is playing a progressive role. This review provides readers with a wide vision on novel ongoing potentialities of various nanotechnology-based approaches for imaging and delivery of therapeutics. In order to obtain effective drug delivery, nanotechnology-based imaging has enabled us to apprehend the interactions of nanomaterials with biological environment, targeting receptors, molecular mechanisms involved in pathophysiology of diseases, and has made the real time monitoring of therapeutic response possible. Development of analytical technologies to measure the size of particles in nanometer ranges, and advent of latest manufacturing approaches for nanomaterials, has resulted in establishment of more effective methods for delivery of therapeutics for the treatment of ophthalmological, pulmonary, cardiovascular diseases, and more importantly cancer therapy. These new drug therapies have already been shown to cause fewer side effects and be more effective than traditional therapies. Furthermore, the imaging techniques have enhanced the determination of tumor location in human bodies and their selective targeting. Altogether, this comparatively new and thriving data suggest that additional clinical and toxicity studies are required further on the “proof-of-concept” phase. Nanomedicine cost and manufacturing at larger scale is also a matter of concern that needs to be addressed. Notwithstanding, future of nanomedicines is propitious.
缩写
- AIE:
-
Aggregation-induced emission
- BDP:
-
Beclometasone dipropionate
- BODIPY:
-
Boron dipyrromethane
- CNTs:
-
碳纳米管
- COPD:
-
Chronic obstructive pulmonary disease
- CulnS2/ZnS:
-
Copper indium sulfide/zinc sulfide quantum dots
- CVD:
-
化学气相沉积
- DNA:
-
Deoxyribonucleic acid
- ENPs:
-
Engineered nanoparticles
- EPR:
-
Enhanced permeability and retention
- GCE:
-
玻碳电极
- GNPs:
-
金纳米粒子
- GQD:
-
Grapheme quantum dots
- HCG:
-
Human chorionic gonadotrophin
- MEMS:
-
Microelectromechanical systems
- MI:
-
Myocardial ischemia
- MNPs:
-
Magnetic nanoparticles
- MSNs:
-
Mesoporous silica nanoparticles
- MWNT:
-
Multi-walled carbon nanotubes
- NEMS:
-
Nanoelectromechanical system
- PAH:
-
Pulmonary arterial hypertension
- PCL:
-
Poly caprolactone
- PDGF:
-
Platelet-derived growth factors
- PEG:
-
Poly ethylene glycol
- PET:
-
Positron emission tomography
- PLGA:
-
Poly lactic-co-glycolic acid
- ROS:
-
活性氧
- SiRNA:
-
Short interference RNA
- SLNS:
-
Solid lipid nanoparticles
- SPIOs:
-
Superparamagnetic iron oxides
- VEGF:
-
Vascular endothelial growth factor
纳米材料
- Raspberry Pi 控制的鱼菜共生
- 用于增强药物递送的纳米纤维和细丝
- 生物相容性 FePO4 纳米颗粒:药物递送、RNA 稳定和功能活性
- 环境响应金属-有机框架作为肿瘤治疗的给药系统
- 用于癌症应用的基于细胞的药物递送
- 斑马鱼:一种用于纳米技术介导的神经特异性药物递送的有前景的实时模型系统
- 131I 追踪的 PLGA-脂质纳米颗粒作为靶向化疗治疗黑色素瘤的药物递送载体
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 基于纳米脂质体的双重给药系统的理化特性研究
- 纳米粒子和超声波控制的水过冷
- 氨基末端 HBP 修饰的 rGO 的光热/pH 双响应给药系统和肿瘤细胞的化学光热疗法
- 紧凑型 3D LiDAR 成像系统


