在短波红外区域发射的纳米探针的高光谱复用生物成像
摘要
在短波红外光谱区(SWIR,~ 1000–1700 nm)中发射外源性发光团的光学生物成像是一个快速发展的领域,最近报道了多个 SWIR 光致发光纳米探针的开发。在这方面,高光谱成像 (HSI) 与分离算法相结合,是一种很有前途的工具,它可以通过光致发光 (PL) 光谱分布对发射 SWIR 的纳米试剂进行有效的多路复用。此处报道的 SWIR HSI 技术被开发用于多路复用两种类型的纳米探针:掺杂有机染料 (PNP) 的聚合物纳米粒子和掺杂稀土的氟化物纳米粒子 (RENP)。两种类型的纳米探针都在相同的光谱范围内(~ 900-1200 nm)表现出 PL,这阻碍了 PL 与滤光片的光谱分离,并限制了它们在生物组织中进行多重成像的可能性。通过应用 SWIR HSI,我们利用了 PL 光谱轮廓的差异,并实现了来自每种类型纳米粒子的 PL 信号的光谱选择性和敏感成像。分离获得的数据允许通过其 PL 轮廓对光谱重叠的纳米探针进行多路复用。每种类型的纳米粒子的定量和空间分布均从它们的混合悬浮液中获得。最后,将具有分离协议的 SWIR HSI 技术应用于皮下注射 PNPs 和 RENPs 的小鼠体内成像。成功证明了高光谱技术在体内成像中多重纳米探针的适用性。
介绍
近几十年来,生物医学成像技术发展迅速,可以对各种疾病和病理进行早期检测和评估。在不同的成像方式中,光学成像因其高时空分辨率和相对较低的成本而占有独特的地位。基于光致发光(或更具体地说,荧光)的多种光学成像方法正在开发和临床转化。例如,淋巴系统成像和术中荧光成像引导的手术已显示出可促进医疗保健的有希望的结果 [1, 2]。另一方面,针对特定感兴趣区域(例如肿瘤)的外源性光致发光探针正在积极开发用于体内和体外成像。除了对光致发光 (PL) 探针的通常要求(即高吸光度、发射量子产率和光稳定性)之外,PL 发射的光谱位置和形状也是需要考虑的重要参数。由于已知生物组织对光的衰减在近红外 (NIR) 光谱范围 (~ 700–950 nm) 中低于可见光范围,因此存在生物组织的 NIR 透明窗口 (~ 700– 950 nm) 已经被引入,并且大量的努力致力于 NIR 发射探针的开发和应用 [3,4,5,6]。此外,最近的进展导致在 ~ 1000–1700 nm 的光谱范围内引入了第二和第三个 NIR 窗口(NIR-II 和 NIR-III),这通常被称为短波红外(SWIR),尤其是通过快速发展的红外成像领域的制造商 [7,8,9]。尽管与传统的 NIR 窗口相比,SWIR 范围内的吸水率更高,但生物组织的较低自发荧光和散射允许 SWIR PL 生物成像中的卓越成像分辨率和更高的成像深度 [10,11,12]。例如,在淋巴管和脑血管系统的 SWIR PL 成像中,使用新型 SWIR 荧光染料 CH1055-PEG,与使用 NIR-I 荧光染料、吲哚菁绿的常规 NIR PL 成像相比,分辨率和信号与背景比显示出更好[13]。此外,使用短波发射纳米探针(单壁碳纳米管)和短波红外成像相机使戴的团队能够在小鼠脑血管系统的非侵入性(无开颅)成像中观察> 2 mm 深度的亚 10 μm 血管,这是在可见光或 NIR-I 范围内无法进行 PL 成像的 [8]。
有机染料和染料配合物在第一个 NIR 窗口中具有强吸收和 NIR-II 窗口中的荧光可被认为是有前途的 NIR-SWIR 探针;它们被证明是血管和淋巴结成像、肿瘤勾画和图像引导手术的特殊造影剂 [13,14,15,16]。值得注意的是,有机染料吲哚菁绿 (ICG) 是目前美国食品和药物管理局批准用于人体的唯一 NIR 荧光造影剂 [17]。同时,分子成像探针(即染料或染料复合物)具有局限性,需要修改其分子结构以改变其生物探针特性(例如水溶性、细胞渗透性等)或为其提供其他成像或定位方式。相比之下,包含 PL 中心的纳米粒子 (NP) 可以用不同的部分共价修饰其表面,以提高水分散性和稳定性、控制表面电荷或靶向目的。此外,NIR-SWIR PL 纳米平台的引入允许将 PL 成像与其他成像、诊断或治疗方式相结合。最近的研究报告了使用 SWIR 发射纳米制剂进行深部组织、全身、肿瘤或经颅成像,用于监测体内的各种过程 [14, 18,19,20,21]。在各种报道的用于体内成像的 NIR-SWIR 发射纳米探针中,可以区分两种类型:NIR-SWIR 荧光来自有机部分(即共轭聚合物)或陶瓷(例如氟化物)纳米晶体掺杂稀土离子。由于合成和化学功能化相对容易,以及优异的生物相容性和生物降解性,基于聚合物的纳米粒子 (PNP) 是临床转化中最成功的纳米药物之一 [22]。当装载 NIR-SWIR 荧光团时,PNP 可以作为有前景的成像探针或成像引导的药物输送载体 [23, 24]。另一方面,稀土离子掺杂纳米粒子 (RENP) 是一类众所周知的纳米探针,它具有独特的光致发光特性,可通过上转换(反斯托克斯位移)和下转换(斯托克斯位移)过程获得[25,26,27,28,29,30]。最近,RENP 已被翻译用于 NIR-SWIR 成像。与基于有机部分的 NIR-SWIR 探针相比,它们在整个 NIR-SWIR 光谱区域具有高量子产率、出色的光稳定性和窄发射带,可以通过掺杂各种离子进行调节 [20, 31, 32]。 RENPs被应用于小动物血管和器官成像、肿瘤检测、多路复用和多光谱成像[3, 19, 20, 33,34,35]。
随着 PL 生物成像的新兴发展,不同目的可能需要同时跟踪体内多个 PL 部分的能力(例如,选定细胞或器官的靶向成像以及成像引导的药物递送)。为了应对这一挑战,开发了多路成像方法。多重成像是指成像生物系统中解剖和功能信息的互补性;它的应用可以结合成像生物标志物、对比度和模式,以增加成像在研究和临床应用中的效用 [36]。多路 PL 成像可以增强纳米医学的治疗诊断维度,提供引入多种 PL 成像对比以及治疗方式的能力。最常用的多路成像方法使用适当的滤光片,通过 PL 发射的光谱位置来区分 PL 探针 [37,38,39]。然而,在这种方法中适当的多路复用需要利用光谱窄、不重叠的 PL 光谱的纳米探针。在这方面,高光谱成像 (HSI) 与光谱混合分析算法相结合是 PL 多路复用的有前途的工具。然而,PL HSI 的生物医学应用主要限于荧光显微镜,用于多路复用不同类型的纳米探针并消除背景和自发荧光 [40, 41]。关于体内 HSI,它最常用于通过组织反射光谱的采集和顺序分析的反射成像模式 [42],尽管也报道了体内 HSI 成像(也称为多光谱成像)用于可见光中的 PL。和 NIR 范围 [3, 5]。然而,文献中没有关于短波红外发射纳米探针的HSI的报道。
最近,我们报道了波段序列 HSI 系统与用于 SWIR PL 成像的光谱解混软件的开发 [43]。波段顺序 HSI 程序基于通过具有光谱变化透射率的元件(即液晶可调滤波器,LCTF)连续获取 2D 图像。从 RENPs 悬浮液获得的 SWIR PL 数据呈现为三维光谱数据立方体(超立方体),包括两个空间维度和一个光谱维度。将光谱解混程序进一步应用于获取的超立方体的每个空间像素,允许计算 PL 混合分量中的丰度。在此,我们应用 HSI 来解决用于体内 SWIR PL 生物成像的纳米探针的多重化。我们使用了两种类型的 SWIR 发射纳米粒子,它们的发射光谱重叠,尽管它们的光谱轮廓不同,但在使用滤光片的传统 PL 成像中无法轻易区分。图 1 说明了这些纳米粒子中 PL 的光谱混合问题以及使用 HSI 带序解混合克服该问题的方法。
<图片>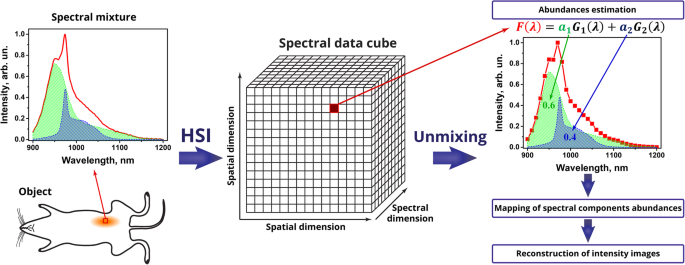
HSI在复合光致发光纳米探针中的应用示意图
应用 HSI 来获取两种类型的纳米粒子的光谱选择性和灵敏的 PL 成像。为了分离 SWIR PL 光谱剖面,开发了分离协议,使我们能够获得混合物中成分的定量和空间映射,除了丰度外,还可以确定强度分布。 SWIR HSI技术和开发的分离协议进一步应用于皮下注射纳米颗粒的小鼠体内成像,以证明HSI在体内成像中多重SWIR PL纳米探针的适用性。
方法
纳米制剂制备和表征
载有有机荧光 NIR-SWIR 染料的聚合物核壳纳米粒子的合成
聚苯乙烯 (PS)-poly-N -异丙基丙烯酰胺 (PNIPAM) 核壳纳米粒子是通过微乳液聚合合成的,并修改了之前描述的方法 [44, 45]。首先,如下制备PS-co-PNIPAM(PNIPAM的10 wt.%)核纳米颗粒。将 NIPAM (0.1 g)、十二烷基硫酸钠 SDS (0.1 g) 和 0.005 g NaH2PO4 × H2O 溶解在 45 ml H2O 中。当温度升至 60 °C 时,在剧烈搅拌下滴加苯乙烯 (1 g)。随着下一步将 Ar 鼓泡到混合物中 30 分钟,温度升至 70 °C,并注入溶解在 1 ml H2O 中的 0.08 g K2S2O8 以引发聚合。其次,PNIPAM 壳层层叠在 PS-co-PNIPAM 核上。为此,在反应器中加入单体 NIPAM (1.8 g) 和交联剂 N 的水溶液 ,N '-亚甲基双丙烯酰胺 (BIS) (0.18 g) 使用注射器溶于 4 ml H2O。使反应在 70 °C 下继续进行 4 小时。将混合物冷却至室温并使用具有 MWCO 3500 Da 的纤维素膜透析 74 小时。结果,制备了 PS-PNIPAM 纳米颗粒的悬浮液;透射电子显微镜 (TEM) 图像清楚地揭示了纳米粒子的核壳结构(图 3a)。为了获得NIR-SWIR荧光PNP,2-丁基-6-[5-(2-丁基-1,3-二甲基环庚[c]吡咯-6(2H)-亚基)penta-1,3-dien -1-基]-1,3-二甲基环庚[c]吡咯鎓四氟硼酸盐(标记为JB9-08)荧光染料[46]被后载[47]到PS-PNIPAM纳米颗粒。将8微升1 mM JB9-08染料的DMF溶液加入2 mL 0.25 wt% PNPs水悬浮液中,放置24 h后使用。
核壳 RENP 的合成
RENP 是按照其他地方报道的修改方案合成的 [48]。一、α-NaYF4:10%Yb 3+ , 30% Nd 3+ 核心纳米粒子是通过金属三氟乙酸盐在高温下分解制备的。在典型的程序中,将 0.05 mmol Yb2O3、0.15 mmol Nd2O3 和 0.25 mmol Y2O3 装入含有 5 ml 去离子水和 5 ml TFA 的 250 ml 烧瓶中,并加热至 90 °C 保持 1 小时得到澄清溶液。在此温度下在氩气吹扫下蒸发所得澄清溶液,得到泥状粉末状 RE(TFA) 3 。随后,将8 ml OA、8 ml OM、12 ml ODE和2 mmol NaTFA加入烧瓶中。将溶液加热至120 °C并在该温度下保持30 分钟,然后加热至300 °C并保持30 分钟,然后自然冷却至室温。在整个合成过程中采用氩气环境。通过向冷却的反应烧瓶中加入20 mL乙醇来沉淀所得纳米颗粒。用乙醇离心洗涤3次后,最后将收集的白色粉末分散于10 ml正己烷中备用。
二、α-NaYF4:10%Yb 3+ , 30% Nd 3+ @CaF2 核壳 RENP 是通过种子介导的外延生长过程制备的,涉及使用 α-NaYF4:10% Yb 3+ , x% Nd 3+ 核作为种子和相应的壳前体溶液中的生长。为了制备壳前体,首先,将 2 mmol CaO 与 5 ml 去离子水和 5 ml TFA 加入到 250 毫升烧瓶中,并在 90 °C 下加热 1 小时以产生澄清溶液。然后在该温度下蒸发该溶液以产生三氟乙酸钙(Ca(TFA) 2 )的壳前体。接下来,0.5 mmol NaYF4:10% Yb 3+ , 30% Nd 3+ 将核心纳米颗粒、7 ml OA 和 7 ml ODE 都添加到烧瓶中。然后将溶液加热至 120 °C 30 分钟,然后加热至 300 °C 60 分钟,然后自然冷却。整个过程在氩气环境下进行。通过向冷却的反应烧瓶中加入20 mL乙醇来沉淀所得核-壳纳米颗粒。用乙醇离心洗涤 3 次后,将收集到的核壳 NPs 最后分散在 10 ml 己烷中备用。为制备水分散体,制备的α-NaYF4:10%Yb 3+ , 30% Nd 3+ @CaF2 核壳 RENPs(5 mL 己烷分散体)首先与 5 mL N 混合 ,N -四氟硼酸亚硝基 (NOBF4) (0.1 M) 在室温下的二甲基甲酰胺 (DMF) 溶液。对混合物轻轻摇动直至观察到 RENP 沉淀。随后,将甲苯和己烷(1:1,体积)加入混合物中,然后以10000 rpm离心10 分钟。收集沉淀物并分散在5 mL DMF中。其次,将 250 mg 聚(丙烯酸)(PAA,MW =18,000)加入到 5 mL 经 NOBF4 处理的 RENP 的 DMF 溶液中,加热至 80 °C,并在剧烈搅拌下在该温度下保持 30 分钟。之后,通过加入丙酮沉淀纳米颗粒,用乙醇洗涤,最后分散在蒸馏水中。
透射电子显微镜
使用透射电子显微镜 (TEM) 评估 PNP 和 RENP 的形态。为了用 TEM 成像,将 10 μL 的纳米颗粒悬浮液滴在用 formvar 稳定的碳支撑膜上。为了使 PNP 的核壳结构可视化,在滴到支持膜上之前,用 1% 的磷钨酸水溶液对它们进行负染色。将碳载体膜风干并用5 μL纯水洗涤。图像是通过在 TEM(JEM-1230,JEOL)上在 100 kV 的加速电压下操作获得的。
光致发光光谱
使用配备有适用于 NIR-SWIR 范围的 iHR320 光谱仪(Horiba)的 Fluorolog-3 分光光度计在 NIR 和 SWIR 范围内测量两种类型的纳米粒子的 PL 光谱;使用发射波长为 808 nm 的光纤耦合激光二极管 (QSP-808-4, QPhotonics) 激发 PNPs 和 RENPs 的 PL。
高光谱成像系统
自制 SWIR HSI 系统采用波段顺序采集方法(图 2),包括 NIR 相机(Xeva-1.7-320,Xenics,比利时)、聚焦光学器件(TEC-M55MPW,Computar,美国)和液晶可调滤光片(Varispec LNIR 20-HC-20, PerkinElmer, USA) 作为分散元素。该系统具有 340 × 258 像素分辨率,可在 900-1700 nm 光谱范围内运行。系统中的照明源包括白炽灯(用于图像对准、聚焦和明场成像)和 808 nm 光纤耦合激光二极管(QSP-808-4,QPhotonics,美国),由激光电源(Laser Source 4308)供电, Arroyo Instruments, USA),用于 PL 成像中的 PL 激发。通过在 900 至 1200 nm 范围内以 10 nm 步长顺序调谐 20 nm 光谱宽度的 LCTF 透射率并捕获相应图像来执行光谱数据立方体采集。 HSI 采集期间 NIR 相机的曝光时间设置为 200 ms。样品上的激光功率密度固定在~ 100 mW/cm 2 .为了获取整个 NIR-SWIR 范围内的 PL 图像,LCTF 被 850 nm 长通滤波器(Edmund Optics,USA)取代。
<图片>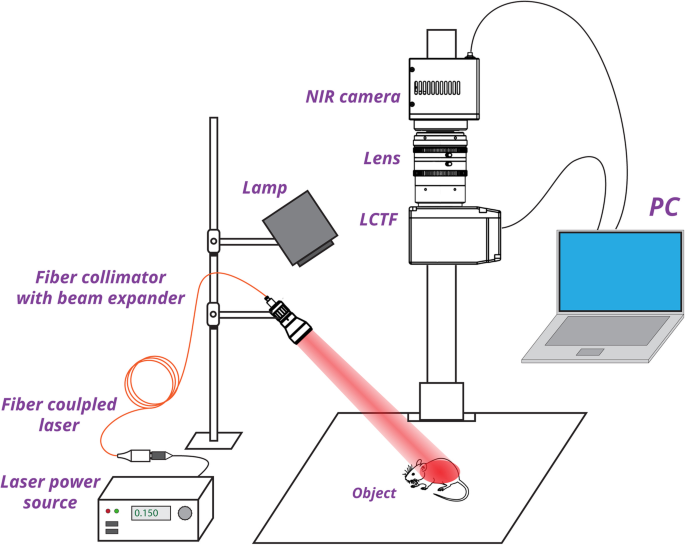
NIR-SWIR高光谱成像系统示意图
光谱分离软件
为了分析获得的光谱数据立方体,我们使用MATLAB环境开发了光谱分离算法。每个像素的光谱被认为是已知端元的线性混合:\( F\left(\lambda \right)=\sum \limits_i{a}_i{G}_i\left(\lambda \right) \),其中 F (λ )——像素谱,G 我 —— 端元光谱和a 我是大量的终端成员。解混软件的目的是通过解决获取的光谱数据立方体的每个像素中的线性光谱混合分析 (LSMA) 问题来估计已知端元的丰度。假设,L 是光谱带的数量,p 是混合物中存在的端元数。那么,LSMA 问题可以表示为 F =Ga + n , 其中 F 是 L × 1 个像素强度向量,G 是 L × p 包含所有端元向量的矩阵,a 是 p × 1 个未知丰度向量,以及 n 是 L × 1 误差向量。解决 LSMA 问题的基于最小二乘误差 (LSE) 的方法可以形成为以下优化任务: mina {(F − Ga ) T (F − Ga )},经典的解决方案是 a (r ) =(G T G ) −1 G T F .然而,这样的解可能包含丰度的负值,这没有物理意义。为了解决这个障碍,必须修改 LSE 优化任务:mina {(F − Ga ) T (F − Ga )}, 服从 a ≥ 0. 为了解决这个任务,我们利用迭代算法,基于非负约束线性光谱混合分析(NC-LSMA),在[49, 50]中有详细描述。在计算每个成分的丰度后,它们被映射为 2D 颜色图。最后,解混软件根据获得的丰度产生相应成分的强度图像:\( {I}_i\left(x,y\right)={a}_i\left(x,y\right)\sum \limits_ {\lambda}{G}_i\left(\lambda \right) \),其中 I 我(x , y )——i的积分强度 -th endmember 以像素为单位,和 a 我 (x , y )—i -th 丰度。
动物实验
BALB/c 裸鼠(来源:美国杰克逊实验室)是在一个小动物设施中在黑暗和无菌条件下饲养的。所有动物实验均按照《国家实验动物护理和使用条例》的标准进行。在成像之前,雄性裸鼠(6 周龄,20 ± 2 g)通过腹膜内注射用5%水合氯醛(每克小鼠体重0.06 ml)麻醉。对于体内 SWIR PL 成像,将纳米颗粒悬浮在 10x 磷酸盐缓冲盐水 (PBS) 中,然后将 100 μL 的 PNPs、RENPs 或其混合物的每种 PBS 悬浮液皮下注射到小鼠体内。
结果与讨论
制备了两种类型的 SWIR 光致发光 NPs 用于 HSI:(1) 后加载 JB9-08 染料的 PNPs,它在水溶液中几乎不发荧光 [46] 但是,如我们 [51] 所示,恢复通过后加载到 PNP 的聚合物基质中(图 3a 和 b)和(2)PAA 包覆的 NaYF4:10%Yb 3+ 使其在水中的荧光 ,30%Nd 3+ @CaF2 核壳稀土离子掺杂纳米粒子(RENP,图 3c 和 d)。钕 3+ RENPs核心中的离子可以被~ 808 nm的光激发( 4 I9/2 → 4 F5/2 跃迁)并将能量转移到 Yb 3+ 离子,在 950–1100 nm 范围内发射,峰值在 ~ 975 nm ( 2 F5/2 → 2 F7/2 过渡)。 RENPs 核涂有惰性 CaF2 壳,以减少通过表面缺陷和与周围环境相互作用造成的非辐射损失 [48]。两种纳米制剂在 808 nm 激发下均表现出 900-1200 范围内的光致发光(图 3e)。
<图片>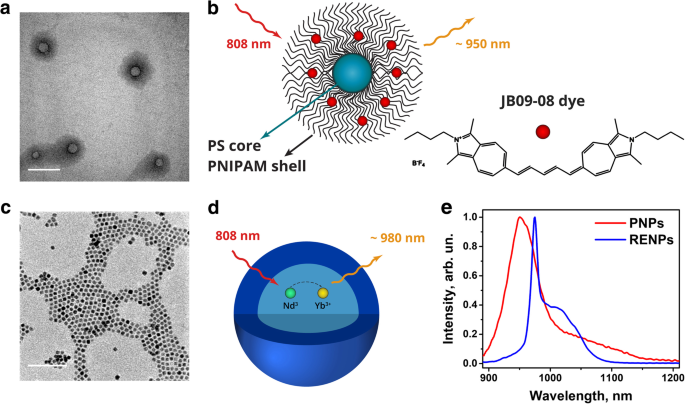
PNP 和 RENP 的表征。 TEM 图像 (a ) 和示意图结构 (b ) 加载了 JB9-08 染料的 PNP。 TEM 图像 (c ) 和示意图结构 (d ) 的 RENP。 e PNPs-JB9-08 和 RENPs 悬浮液在 808 nm 激发下的归一化 PL 发射光谱。比例尺,100 nm
应该注意的是,由于两个原因,用荧光分光光度计获得的纳米粒子的 PL 发射光谱不能用作光谱解混软件中的端元。首先,与传统的荧光分光计不同,HSI 系统的灵敏度没有经过光谱校正,因此两种采集方法获得的发射光谱轮廓是不同的。其次,虽然 LCTF 的光谱带宽为 20 nm,但 HSI 帧以 10 nm 的步长收集。这导致信号在相邻帧中重叠,导致与使用分光光度计测量的光谱轮廓相比失真。为了克服这些障碍,使用 HSI 系统获取端元(PNP 和 RENP 样品的光谱图)。为此,将两种类型的纳米探针悬浮在 PBS 中,并将它们的 PBS 悬浮液置于微量离心管中(图 4a)。很难用传统的 PL 成像区分两个样品,因为它们的 PL 发射光谱重叠(图 4b 和 3e)。使用 HSI 系统,在 900 到 1200 纳米的光谱范围内以 10 纳米的步长收集了 31 张 PL 图像(图 4c)。 PNPs、RENPs 和背景 (BG) 的光谱分布是通过光谱数据立方体的光谱维度通过平均由红色、蓝色和绿色方块标记的区域中的信号来计算的,相应地(图 4b)。发现获得的 PNP 和 RENP 的光谱分布(图 4d)与荧光分光计测量的相似,后来用作光谱分离的端元。此后,以 PNP、RENP 和 BG 光谱轮廓作为端元,计算相应的组分丰度并将其映射为二维颜色图(图 4e)。计算超立方体的每个空间像素的丰度,并表示为从 0 到 1 的值,0 和 1 分别表示该成分的完全缺失和完全丰度。每个像素中所有分量的丰度总和等于1。需要注意的是,解混软件使用了信号强度的阈值来消除低强度像素引起的误差。如果一个像素沿光谱维度的最大强度小于整个超立方体最大值的 5%,则认为该像素完全含有噪声成分。此外,考虑到相应的丰度和消除背景成分,计算了 PNP 和 RENP 的积分强度图像(图 4f)。正如预期的那样,丰度映射和积分强度图像都表明右管中的 PNPs 和左管中的 RENPs 完全丰度,由于 PL 发射散射和解混合算法的不完善导致了轻微的误差。
<图片>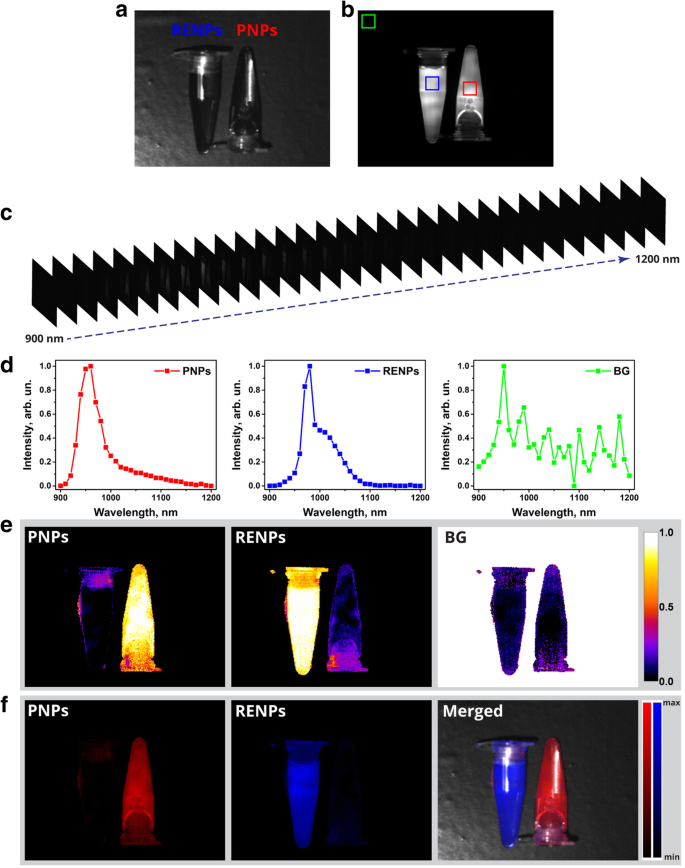
含有 RENP 和 PNP 的微量离心管的 HSI。 一 PNP 和 RENP 悬浮在 PBS 中的微量离心管的明场图像。 b 用 808 nm 激发的 PNP 和 RENP 样品的 PL 图像(850 纳米长的通滤波器用于图像采集)。 c 说明由 HSI 帧组成的超立方体的方案。 d 从 b 中显示的 ROI 中平均得到的 PNP、RENP 和背景 (BG) 的光谱图 相应地显示为红色、蓝色和绿色方块。 e 组分丰度的颜色图。 f PL分量重建强度图像和PL/明场合并图像
光谱分离还能够区分 PNPs、RENPs 的混合物。为了证明这一点,三个微量离心管中装有 PNP、RENP 及其混合物的溶液。在获得超立方体和光谱分离程序后,丰度图表明第一个微量离心管中完全存在 PNP,第二个中存在 RENP,第三个中存在两者的混合物(图 5a)。进一步重建强度图像以揭示样品中PNPs和RENPs PL信号的强度分布(图5b)。
<图片>
含有(从左到右)RENP、PNP 和两者混合物的微量离心管的 HSI。 一 大量的 PNP、RENP 和背景 (BG)。 b 重建PL强度图像和PL/明场合并图像
我们进一步证明了我们的 HIS 方法在体内 SWIR PL 成像中复用光谱重叠纳米探针的适用性。裸鼠被麻醉并皮下注射 PNP、RENP 和两者的混合物。使用 850 nm 长通滤波器的 NIR 成像显示三个无法区分的光致发光点(图 6a)。在执行 HSI 和分析后,丰度图分别显示顶部和底部注入位点的 PNPs 和 RENPs 的完整丰度,而在左侧注入位点识别出两者的混合物(图 6b)。此外,为了获得 PL 强度分布,进行了强度重建(图 6c)。通过将解混软件中的阈值调整为 15%(根据经验估计),可以去除与排放点相邻的区域的噪声(图 6d)。这些结果表明,与使用长滤光片或带通滤光片的传统 PL 成像模式不同,HSI 不仅能够绘制样本中的强度分布图,而且还可以通过识别样本中强度的光谱分布来对混合物中存在的成分进行多路复用。图像的每个像素。
<图片>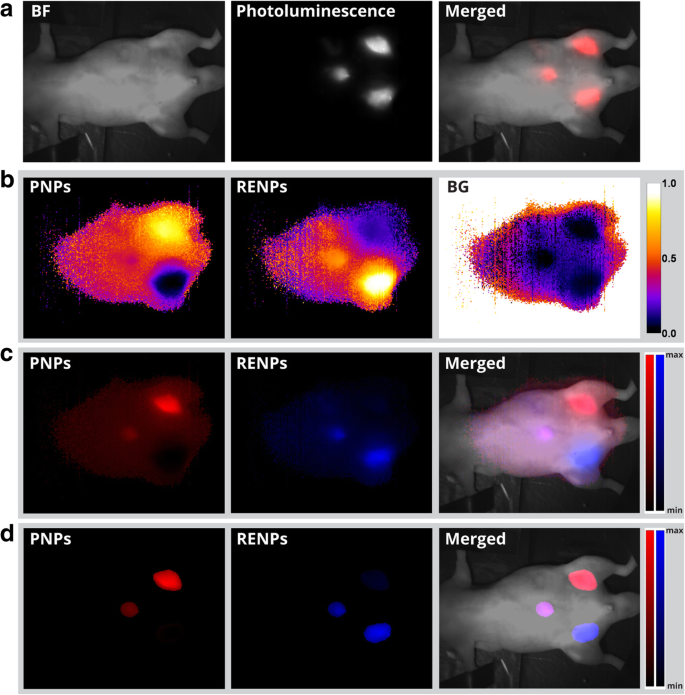
皮下注射 PNP(右上注射部位)、RENP(右下)和 RENP/PNP 混合物(左)的小鼠 HSI。 一 明场 (SWIR)、SWIR PL 和使用 850 纳米长通发射滤光片获取的合并图像。 b 大量的 PNP、RENP 和背景 (BG)。 c 相应的重建强度图像。 d 阈值为15%的丰度重建PL强度图像和PL/明场融合图像。
因此,在这项工作中应用了 HSI 采集和光谱分离处理的组合,以获得光谱重叠 SWIR PL 纳米探针的多路复用成像。然而,在 HSI 模式的适用性方面,应考虑一些问题。首先,由于光谱窄采集,每个 HSI 帧处理相对较低的信号强度(特别是在光谱宽的 PL 发射来自有机部分的情况下)。此外,生物成像中 PL 激发激光功率的增加受到组织损伤(或光毒性)危险的限制。 This results in higher requirements for the brightness of the PL probes and their photostability, as HSI can require order of magnitude longer acquisition time in comparison with conventional PL imaging. It should also be noted that the linear mixture analysis and spectral unmixing algorithm can work satisfactorily for multiplexed PL imaging of biological tissues in the spectral range where tissue transmittance does not change much. In contrast, if tissue transmittance has distinctive features in the spectral range of HSI, linear spectral mixture model may be hardly applicable (especially in case of deeper tissues) and nonlinear models can be considered.
结论
In conclusion, we developed a hyperspectral SWIR bioimaging technique and applied it for multiplexing of nanoparticles emitting in SWIR spectral range. Two types of nanoparticles with overlapping PL spectra, which are undistinguishable in conventional imaging, were successfully multiplexed by their PL spectral profiles using hyperspectral acquisition along with the linear spectral mixture analysis algorithm. The developed method was successfully employed for multiplexed imaging of SWIR PL nanoparticles both in sample suspensions and injected in small animals. With SWIR bioimaging having superior resolution at higher imaging depth, SWIR HSI approach holds a great potential for use in various applications requiring multiplexed imaging with NIR-SWIR PL nanoprobes. Furthermore, as SWIR bioimaging is at a very early stage, there is plenty of room for the development of biomedical applications of PL probes in a combination with HSI.
数据和材料的可用性
本研究期间生成或分析的所有数据均包含在这篇已发表的文章中。
缩写
- BG:
-
Background
- HSI:
-
Hyperspectral imaging
- LCTF:
-
Liquid crystal tunable filter
- 近红外:
-
近红外
- NP:
-
纳米粒子
- PL:
-
光致发光
- PNIPAM:
-
Poly-N -isopropylacrylamide
- PNPs:
-
Polymeric nanoparticles
- 附注:
-
聚苯乙烯
- RENPs:
-
Rare-earth doped fluoride nanoparticles
- SWIR:
-
Short-wave infrared
- TEM:
-
透射电子显微镜
纳米材料


