药物再利用
抑制 SARS-CoV-2 主蛋白酶
新药的开发是一个昂贵且漫长的过程。今天,由于世界正面临大流行,因此迫切需要快速确定阻止病毒扩散的药物。通过尝试确定已知对人体安全的药物是否可用于治疗新疾病,药物再利用为这一漫长过程提供了一种有吸引力的替代方案。
虽然单独使用这种重新定位的药物最终可能不会带来显着的临床益处,但针对几种对病毒复制和增殖至关重要的蛋白质的药物的仔细组合可能非常有效,就像 1990 年代的 HIV 一样。紧迫的问题是哪种组合更有效?
在这里,我们尝试了解 SARS-CoV-2 蛋白酶活性位点的结构,将其与与微摩尔抑制剂复合的 SARS-CoV 蛋白酶的现有结构进行比较,以便我们更好地了解创建良好抑制剂所需的关键相互作用SARS-CoV-2蛋白酶。
然后,我们使用 FDA 批准的药物库进行了虚拟筛选实验,以查看其中一些是否预计会与蛋白酶结合。我们研究了它们如何被预测与 SARS-CoV-2 蛋白酶结合,从而可用于联合治疗。
SARS-CoV-2 蛋白
来自患病患者的 SARS-CoV-2 基因组被快速分离和测序,提供了可能的蛋白质靶标的序列。这些蛋白质与 SARS-CoV 蛋白质具有高度的序列相似性,最初研究小组开始建立同源模型。现在我们看到越来越多的这些通过实验获得的(X 射线和冷冻电镜)结构变得可用。
冠状病毒中表征最好的药物靶点之一是主要蛋白酶:Mpro,也称为 3CL 蛋白酶。 1 与木瓜蛋白酶样蛋白酶一起,这种酶对于加工从病毒 RNA 翻译而来的多蛋白至关重要。 2 它在大多聚蛋白 1ab 的 11 个切割位点切割氨基酸骨架(图 1)。
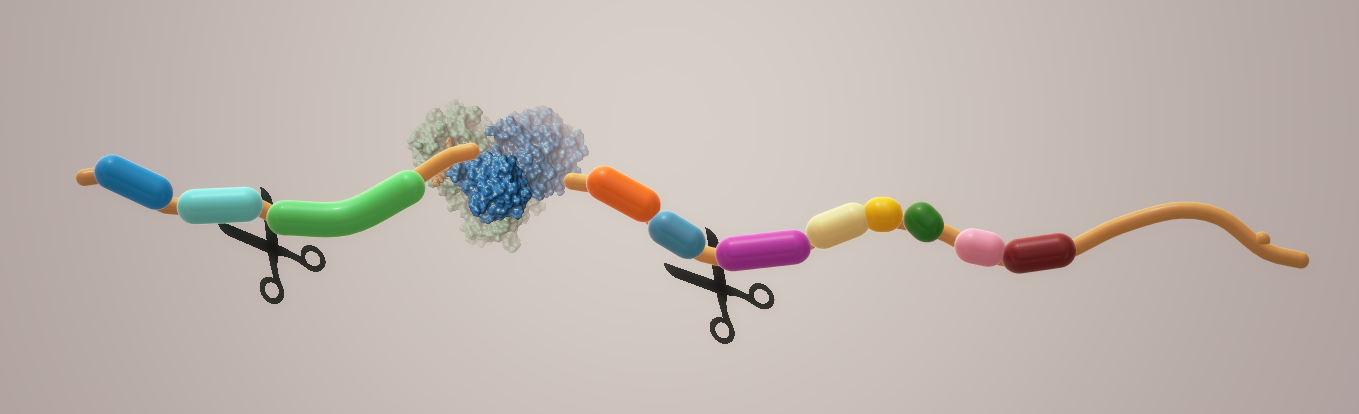
抑制这种酶的活性会阻止病毒复制。由于没有已知具有类似切割特异性的人类蛋白酶,因此该靶标的抑制剂毒性和引起副作用的可能性要小得多。
用于药物再利用的基于结构的药物设计:主蛋白酶
该主要蛋白酶是同源二聚体(图 2),每个亚基包含一个 His41/Cys145 催化二元组。
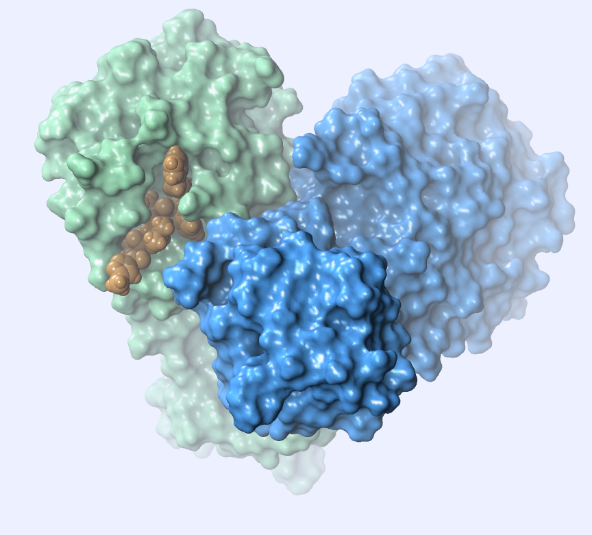
SARS-CoV-2 与 SARS-CoV 蛋白酶具有 96.1% 的同一性和 99% 的相似性。 (图3)活性位点只有一个氨基酸差异:SARS-CoV-2中的第46位残基是丝氨酸,而不是SARS-CoV中的丙氨酸。
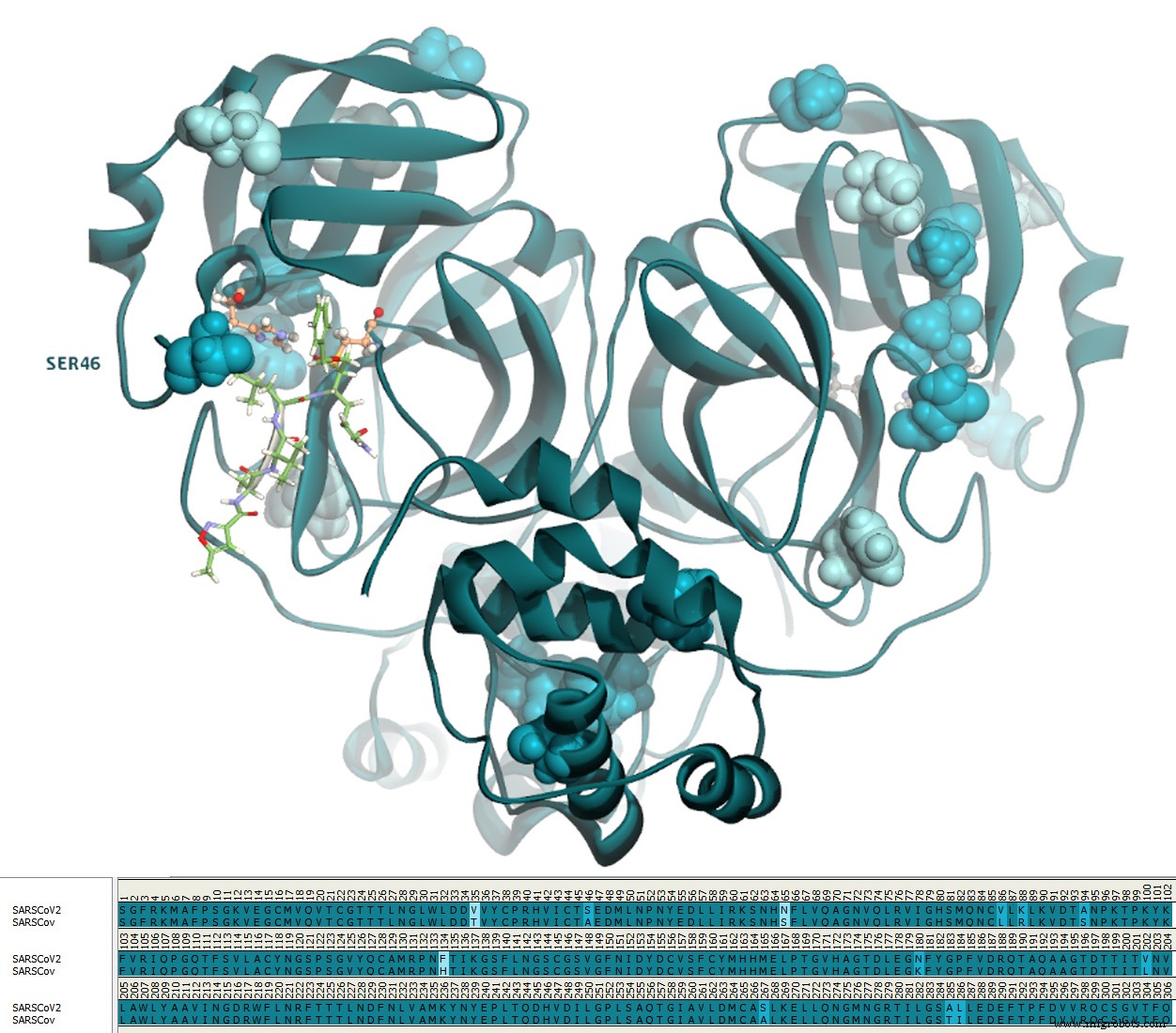
SARS-CoV Mpro与PDB上可用的配体复合的结构很多,具有微摩尔结合亲和力的配体都是共价配体。
主要蛋白酶的活性位点在冠状病毒中高度保守,通常由四个位点(S1'、S1、S2 和 S4)组成 3 (图4)。
在 PDB 结构 2ZU4 和 2GX4 的情况下,配体的 Ki 值分别为 0.038 μM 和 0.053 μM,S1' 位点中的半胱氨酸 145 的硫醇以共价键接触抑制剂。与其他亲和力较低的抑制剂相比,这似乎对较高亲和力很重要。
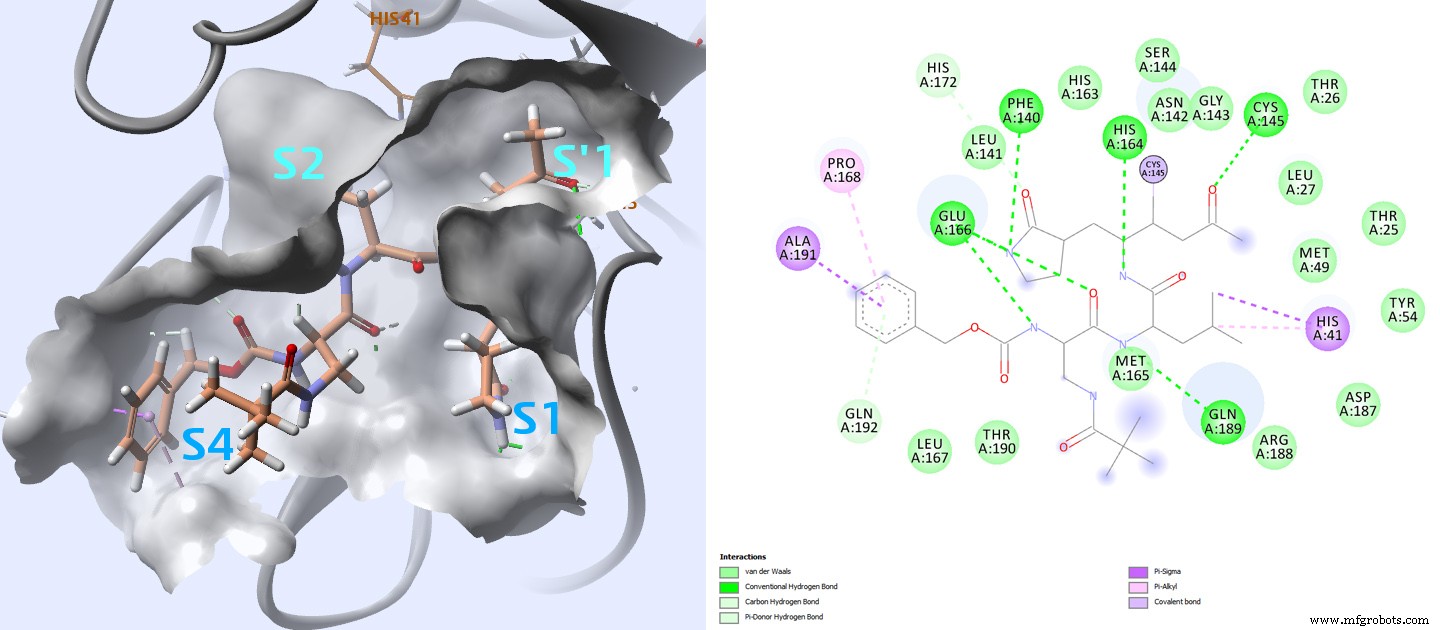
仔细检查所有这些配体如何与这种蛋白酶相互作用可能会提供有关关键相互作用的信息,以便在分析对接结果时进行监测。
虚拟筛选
利用 SARS-COV-2 蛋白酶二聚体与 2 月份发布的共价键合肽样抑制剂 N3 复合物的高分辨率晶体结构 (6LU7) 4 ,我们使用这种结构进行了虚拟筛选实验。共结晶的抑制剂 N3 以扩展构象结合在底物结合袋中。 (图5)
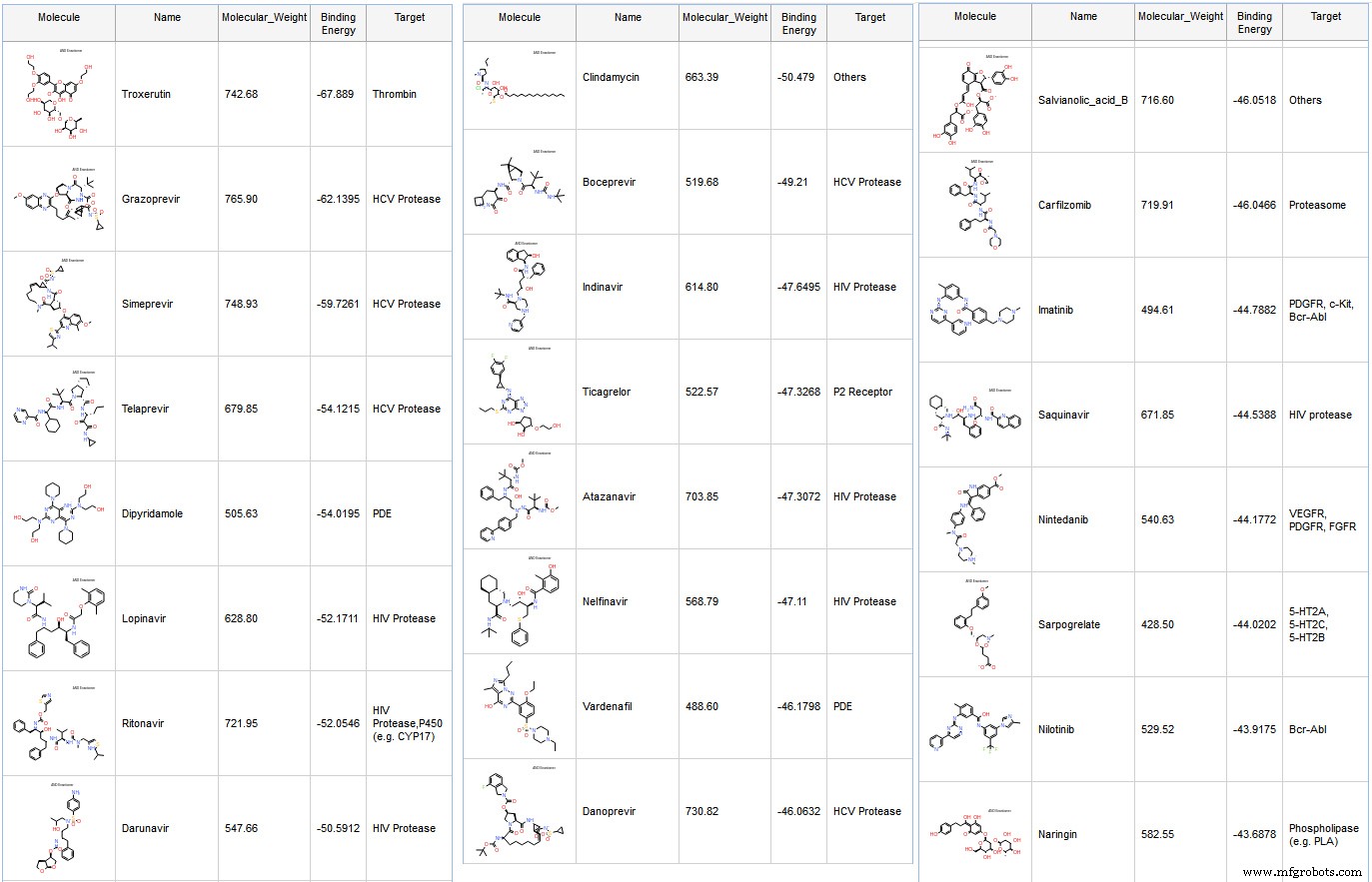
我们从一个包含 FDA 批准的药物和 2,684 种化合物的库开始。我们保留了分子量低于 800 kDa 的化合物,并与来自 CCDC 的 GOLD 进行对接。后来,我们用 CHARMM 和 GBMV 隐式溶剂计算了结合自由能。对于每个姿势,我们首先使用 14 Å 直径的球体进行原位配体最小化以提高残基灵活性,并在计算结合自由能时估计配体熵。大多数对接的化合物是已知的 HCV 和 HIV 蛋白酶药物。 (图6)
许多化合物在 4 个亚位点:S1、S'1、S2、S4 以及一些与 HIS 41 和 CYS 145 发生接触,尤其是 HIV 蛋白酶抑制剂。
得分最高的化合物是曲克芦丁,它是一种黄酮类化合物。
- 黄酮类化合物已被证明可以抑制某些蛋白酶 5 最近,IC50 值是根据草本素、红叶黄素和果胶苷对 SARS-CoV 的剂量依赖性抑制曲线计算得出的。测量值分别为 33.17、27.45 和 37.78 μM。
双嘧达莫(图 7)是排名第五的化合物,最近在预印本中提到双嘧达莫对具有凝血功能障碍的 COVID-19 患者的治疗作用,并显示以 100 nM 的 EC50 抑制 HCoV-19 复制体外。
图 7 :主要蛋白酶中双嘧达莫的 3D 渲染和 2D 相互作用图。存在与催化残留物的相互作用,以及与前面提到的 SARS-CoV 抑制剂的一些残留物的相互作用。
最近的一份预印本报告了几种 HIV 蛋白酶抑制剂的细胞分析:“奈非那韦在体外抑制严重急性呼吸系统综合症冠状病毒 2 的复制 .”
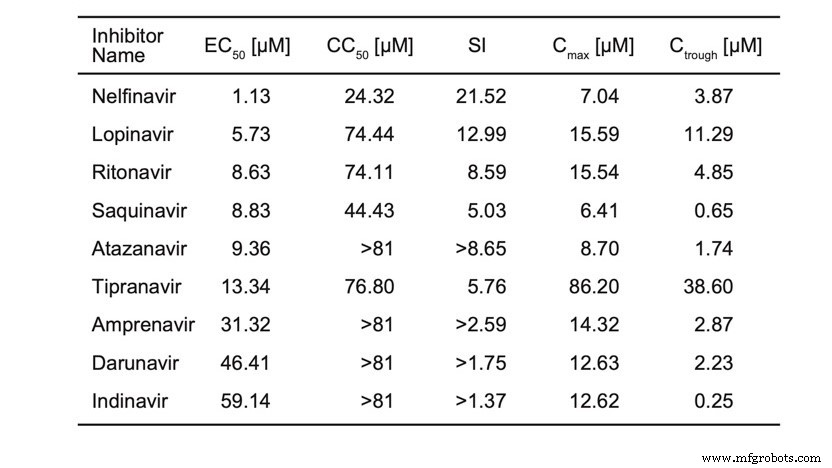
我们正在报告预印本中的表格(表 1)。这些不是 IC50,而是 EC50,因此它不能说明这些分子与蛋白酶的结合情况。然而,这表明所有这些化合物都在抑制 SARS-CoV-2 的复制,并且有些化合物比其他化合物更活跃。
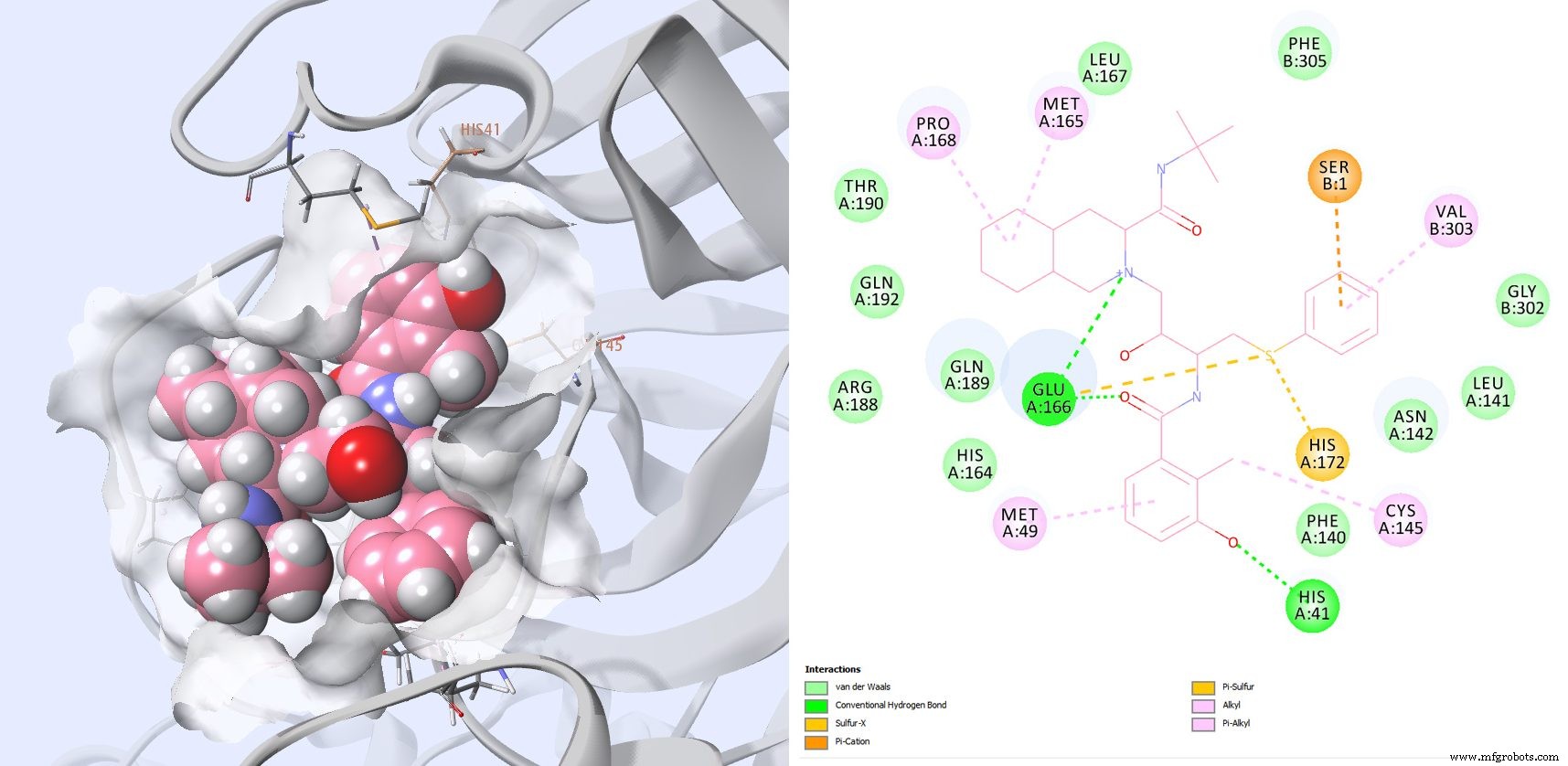
利托那韦和洛匹那韦正在与以前在其他靶向 SARS-CoV 蛋白酶的化合物中看到的许多残基相互作用(图 8 和 9)。尽管正在对这两种分子的组合进行多项临床试验,但遗憾的是,尚无利托那韦或洛匹那韦对 SARS-CoV-2 的 IC50 数据。
图 8 :利托那韦的最佳得分姿势:以及显示利托那韦与两个催化残基相互作用的二维相互作用图:CYS145 和 HIS41,以及其他已知的 SARS-CoV 抑制剂所见的 GLU166、PRO168 和 GLN189。
图 9 :洛匹那韦的最佳得分姿势:以及显示洛匹那韦与两个催化残基相互作用的二维相互作用图:CYS145 和 HIS41,以及 GLU166、PRO168 和 GLN189,如其他已知的 SARS-CoV 抑制剂。 em>
奈非那韦(图 10)在我们的计算中具有很高的预测结合亲和力,并且在最近的预印本中也对 COVID19 进行了表征:“奈非那韦对 Vero E6 细胞中的 SARS-CoV-2 具有活性。”
第二份预印本显示阿扎那韦对 SARS-CoV-2 感染细胞具有活性:“阿扎那韦抑制 SARS-CoV-2 复制和促炎细胞因子的产生。”
在我们开始这项工作后,发表了一种 PDB 结构 6W63,其中包含一种新的 SARS-CoV-2 抑制剂(图 11)。没有关于该化合物与 SARS-CoV-2 Mpro 的结合亲和力的公开信息。结合位点中的侧链与 6LU7 的方向几乎相同。我们对接我们的化合物,并像以前一样使用 MMGBSA 方法对它们重新评分,并发现了非常相似的结果。
图 11 :PDB结构6W63:SARS-CoV-2主要蛋白酶与抑制剂X77复合。
观点
SARS-CoV-2蛋白酶的结合位点非常大,包含四个亚位点,可以容纳许多不同的配体,结合亲和力适中。正如此处所解释的,虚拟筛选是识别可能的抑制剂的有用工具,并且能够为我们提供一些关于可能的抑制剂如何与蛋白酶相互作用的结构解释。
然而,所有这些假设都需要通过实验证据来证实,比如 IC50 的测量,以建立更稳健的模型。
在这里,我们没有进行共价对接,但由于对抗 SARS-CoV 蛋白酶最活跃的化合物是共价的,这可能是强抑制剂的要求。与可逆抑制剂相比,共价抑制剂还显示出优势,例如具有很强的靶点亲和力和延长患者的作用寿命。
为了使药物在患者体内具有活性,我们需要考虑其他药理学方面,例如药代动力学。有必要评估这些药物在人体批准给药后达到目标血浆和肺浓度的能力。
评论其他基于结构的设计研究不在这项工作的范围内,因为这对于当前的流行病来说并不及时。我们的目的是评估针对 COVID19 的潜在候选药物的易于使用的疗法。
我们要感谢剑桥晶体数据中心 (CCDC) 允许在这项工作中使用 GOLD 进行虚拟筛选。 GOLD 在虚拟筛选、先导优化和识别活性分子的正确结合模式方面取得了成功。 Discovery Studio 中提供了 GOLD 的界面。
生物制品


