核壳异质结构 CNT@Li2FeSiO4@C 作为锂离子电池的高稳定性阴极材料
摘要
纳米结构的合理设计是解决Li2FeSiO4正极材料固有缺陷和实现高性能的关键。在这项工作中,设计并合成了一种新型异质结构 CNT@Li2FeSiO4@C,并将其用作锂离子电池的正极材料。结果表明,产物具有均匀的核壳结构,Li2FeSiO4层和外碳层的厚度分别约为19 nm和2 nm。合理的设计有效地加速了锂离子的扩散,提高了电导率,缓解了充放电过程中的体积变化。 CNT@Li2FeSiO4@C凭借其特定结构的优势,成功克服了Li2FeSiO4的固有缺点,表现出良好的可逆容量和循环性能。
介绍
锂离子电池(LIBs)具有能量转换效率高、循环寿命长、能量密度高、自放电小等优点,被广泛应用于便携式电子设备和电动汽车中[1,2,3]。然而,迫切需要具有更高能量密度、更高倍率能力和更高循环性能的新一代LIBs来满足电动汽车的发展[4,5,6]。由于LIBs的性能与正极材料的性能密切相关,因此开发新型正极材料对于新一代LIBs的发展具有重要意义。近年来,Li2FeSiO4正极材料以其价格低廉、化学稳定性好、环境友好等优点引起了人们的广泛关注。特别是,每个分子单元有可能嵌入/脱嵌两个锂离子,容量为 332 mAh g -1 理论上 [7, 8]。然而,由于电导率低(~ 6 × 10 − 14 S cm −1 ) 和锂离子扩散系数 (~ 10 − 14 厘米 2 s −1 ) Li2FeSiO4 [9,10,11,12]。因此,提高Li2FeSiO4正极的电子电导率和锂离子传输能力对优化LIBs的性能非常重要。为了解决这些问题,人们做出了许多努力,例如合成纳米级 Li2FeSiO4 [13,14,15] 和用碳材料涂覆表面 [16,17,18]。但是,它在合成过程中经常会遇到两个问题。一个问题是难以合成纯相的Li2FeSiO4产物,而且一些伴随的杂质如Fe3O4或Li2SiO3往往是不可避免的,这不利于实践能力[19, 20]。另一个问题是Li2FeSiO4的纳米结构在退火处理过程中经常受到损伤。
本研究合成了一种核壳异质结构CNT@Li2FeSiO4@C正极材料。与已报道的 Li2FeSiO4 正极材料工作相比,CNT@Li2FeSiO4@C 材料通过调节化学试剂计量比和反应条件,展现出无杂质相和结构完整的优点。此外,CNT的内层可以增加导电性。中间层的 Li2FeSiO4 厚度仅为 20-25 nm,有利于 Li + 扩散。并且外层无定形碳层可以提高导电性并保护内部框架结构。因此,核壳异质结构CNT@Li2FeSiO4@C在比容量、循环稳定性和倍率性能方面都有显着提高。
方法
材料与合成
CNT@Li2FeSiO4@C 是通过逐步制备过程制造的。首先,CNT@SiO2 同轴结构是通过溶胶-凝胶涂层工艺制备的 [21, 22]。通常,将 8 mg CNT 分散在 80 mL 乙醇和 30 mL 去离子水的混合物中,然后将该混合物超声处理 30 分钟以形成均匀溶液。然后,将 2 mL NH3·H2O(25-28 wt.%)和 0.16 g 十六烷基三甲基溴化铵(CTAB)加入上述溶液中,超声处理并保持 20 分钟。将含有0.45 mL四乙氧基硅烷(TEOS)和40 mL乙醇的混合溶液在磁力搅拌40 min以上滴入上述溶液中,然后搅拌10 h。通过离心和去离子水和乙醇清洗获得 CNT@SiO2 产品。接下来,通过固相烧结获得CNT@Li2FeSiO4。将0.334 g LiAc·2H2O和0.734 g Fe(NO3)3·9H2O的水溶液连续溶解在30 mL乙醇中,搅拌20 分钟。将得到的 CNT@SiO2 加入溶液中,超声处理 40 min,磁力搅拌 20 min。然后,将其转移到80 °C的真空干燥器中12 小时。得到的干粉首先在400 ℃下煅烧2 h,然后在氩气气氛中650 ℃下加热10 h;结果,制备了 CNT@Li2FeSiO4。以葡萄糖为碳源制备了 CNT@Li2FeSiO4@C。将 0.2 g CNT@Li2FeSiO4 通过超声波分散在 40 mL 乙醇中 40 分钟。然后,将含有0.1 g葡萄糖的溶液加入到溶液中。将所得溶液置于真空干燥器中,在 80 °C 下保持 6 小时。然后将产物在氩气气氛中400 °C煅烧4 h,得到CNT@Li2FeSiO4@C正极材料。
材料表征
CNT@Li2FeSiO4@C 和 CNT@Li2FeSiO4 的晶体结构通过 X 射线衍射(XRD,D2 PHASER Bruker)在 Cu-Kα 辐射(λ =1.5418 Å) 辐射,电压为 30 kV 和 10 mA。材料的化学元素通过X射线光电子能谱(XPS,K-ALPHA 0.5EV)系统验证。使用扫描电子显微镜(FESEM,S-4800)和透射电子显微镜(TEM,Tecnai G2 F 20)观察材料的结构和形貌。通过能量色散 X 射线光谱 (EDX) 揭示复合材料中元素的分布。通过热重分析仪(TGA)曲线(STD Q600 TA)以10 °C min -1 的速度检测复合材料的碳含量 从室温到 800 °C。
电化学测量
阴极由 10 wt.% 的聚偏二氟乙烯 (PVDF)、20 wt.% 的乙炔黑和 70 wt.% 的活性材料分散在 N 中制成 -甲基-2-吡咯烷酮 (NMP) 以形成一致的浆液。然后将浆液涂在铝箔上,并在 80 °C 下真空干燥 12 小时以上。 CNT@Li2FeSiO4@C和CNT@Li2FeSiO4电极活性材料的质量负载约为1.5 mg/cm 2 .最后,将半电池组装在充满氩气的手套箱中。使用 Neware 电池系统在 1.5~4.8 V 的电压窗口内对电池进行充电和放电测试。循环伏安 (CV) 测量在 VMP3 多通道电化学工作站(法国,Bio-logic)上以不同的扫描速率进行。
结果与讨论
CNT@Li2FeSiO4@C材料的制备过程示意图如图1所示。首先,通过简单的溶胶-凝胶法制备CNT@SiO2。通过控制CNT和TEOS的用量,达到精确控制Li2FeSiO4层厚度的目的。其次,通过在氩气气氛中在 650 °C 下退火 10 h 获得具有良好结晶度的 CNT@Li2FeSiO4。最后,仅在 400 °C 下用无定形碳包覆 CNT@Li2FeSiO4 以实现核壳异质结构 CNT@Li2FeSiO4@C。
<图片>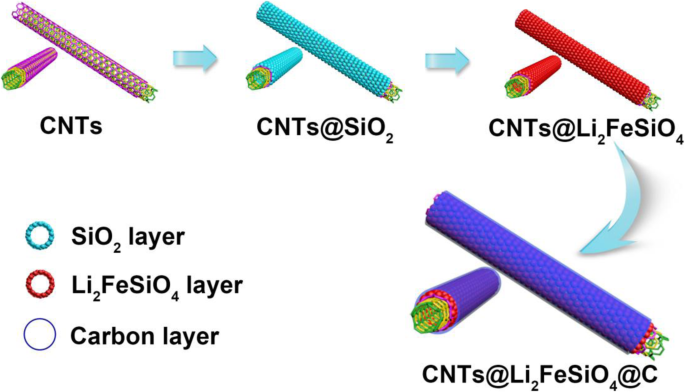
核壳异质结构CNT@Li2FeSiO4@C合成示意图
图2a描绘了CNT@Li2FeSiO4和CNT@Li2FeSiO4@C的XRD图谱。 Li2FeSiO4 的衍射峰与具有 p21/n 空间群的单斜结构一致。此外,没有观察到杂质(如 Fe3O4 和 Li2SiO3)的 XRD 衍射峰,这证实了所得产品的纯度。 XPS 研究了 CNT@Li2FeSiO4@C 的主要元素和表面价态(图 2b-d)。图 2b 显示了 Li2FeSiO4 的全光谱,包括 Li 1s、Si 2p、Si 2s、C 1s、O 1s 和 Fe 2p。图 2c 显示了 Fe2p 光谱,710.3 eV 和 723.8 eV 处的两个峰归因于 Fe 2+ 的 Fe 2p3/2 和 Fe 2p1/2 , 分别。 710.4 eV处的结合能卫星峰比715.0 eV处的结合能卫星峰低4.6 eV,进一步说明只有Fe 2+ 存在于 Li2FeSiO4 纳米晶体 [23]。图 2d 表明 Si 2p 处的峰在 101.8 eV 处的峰与 Si 4+ 处的峰基本一致 在聚硅氧烷中,证明了正交硅酸盐结构[SiO4]的形成[24, 25]。
<图片>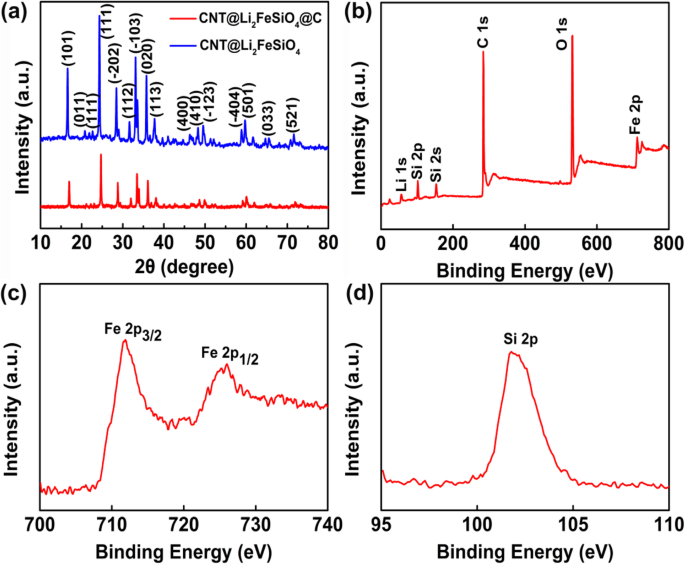
一 CNT@Li2FeSiO4 和 CNT@Li2FeSiO4 的 XRD,b CNT@Li2FeSiO4@C的XPS全光谱和c的高分辨率光谱 Fe 2p 和 d 硅2p
扫描电子显微镜 (SEM) 揭示了 CNT(附加文件 1:图 S1A)、CNT@SiO2(附加文件 1:图 S1B)、CNT@Li2FeSiO4(图 3a、b)和 CNT@Li2FeSiO4@的形态和结构C(图 3c、d)。值得注意的是,CNT@Li2FeSiO4 和 CNT@Li2FeSiO4@C 的一维纳米结构都被保留下来,没有观察到游离的 Li2FeSiO4 颗粒。 TG结果证实CNT@Li2FeSiO4和CNT@Li2FeSiO4@C的碳含量分别为16.93%和22.69%(附加文件1:图S2)。
<图片>
一 , b CNT@Li2FeSiO4,c的SEM图像 和 d CNT@Li2FeSiO4@C 的 SEM 图像。 e 和 f CNT@Li2FeSiO4 的TEM图像,h 和 i CNT@Li2FeSiO4@C的TEM图像; j 和 k 分别为 CNT@Li2FeSiO4@C 和 CNT@Li2FeSiO4@C 的 HRTEM; 我 –o Fe、Si和O的EDX元素映射
通过透射电子显微镜 (TEM) 进一步证实了 CNT@Li2FeSiO4 和 CNT@Li2FeSiO4@C 的结构。从图 3e 和 f 中可以直观地看出 CNT@Li2FeSiO4 的核壳结构。 CNT@Li2FeSiO4 的总直径约为 70 nm,外层 Li2FeSiO4 的厚度为 20 nm。 CNT@Li2FeSiO4@C 的核壳异质结构可以在图 3h 和 i 中清楚地证实。此外,图 3i 进一步显示了直径约为 85 nm 的 CNT@Li2FeSiO4@C 的一维纳米结构。 CNT内层直径约40 nm,Li2FeSiO4中间层厚度约16-22 nm。外层碳层的厚度约为 2 nm。图 3j 和 k 分别显示了 CNT@Li2FeSiO4 和 CNT@Li2FeSiO4@C 的 HR-TEM。距离为 0.27 nm 的晶格条纹与正交 Li2FeSiO4 的 (- 103) 晶格间距重合。图 3k 还显示外部无定形碳的厚度约为 1.5 nm。图3l-o是CNT@Li2FeSiO4的元素映射分析,表明Fe、Si和O元素共存且分布均匀。
CNT@Li2FeSiO4 和 CNT@Li2FeSiO4@C 的循环性能在 Neware 电池测试系统上进行测试,电压窗口为 1.5-4.8 V,电流密度为 0.2 C。如图 4a 所示,首次放电比容量CNT@Li2FeSiO4 为 100.8 mAh g −1 2、10、50和150次循环后的容量保持率分别为95.2%、92.8%、91%和78.2%。相比之下,CNT@Li2FeSiO4@C 的充电容量为 207 mAh g −1 放电容量为 178 mAh g −1 在初始循环中(图 4b)。在 2、10、50 和 150 次循环后,CNT@Li2FeSiO4@C 电极的放电容量保持率分别保持在 95.5%、93.3%、92.4% 和 89.3%。显然,与 CNT@Li2FeSiO4 相比,CNT@Li2FeSiO4@C 具有更高的容量和更好的循环性能,这应该是由于其更高的导电性 [26, 27]。据我们所知,与之前的报道相比,这项工作中 CNT@Li2FeSiO4@C 的循环特性表现出更好的循环性能。例如,酒石酸辅助溶胶-凝胶法制备的多孔Li2FeSiO4/C纳米复合材料的初始放电容量为176.8 mAh g -1 在 0.5 C 和 132.1 mAh g −1 的可逆容量 在 50 次循环后在 1°C [28]。采用柠檬酸基溶胶-凝胶法合成还原氧化石墨烯改性Li2FeSiO4/C复合材料,可逆容量为178 mAh g -1 在 0.1 C 下,40 次循环后容量保持率为 94.5% [29]。电化学性能更好的原因可以概括为以下三个部分。首先,CNT和Li2FeSiO4的结合可以提高材料的导电性。其次,厚度仅为 20-25 nm 的 Li2FeSiO4 有利于锂离子的扩散。最后,涂覆在 Li2FeSiO4 外部的碳层可以保护内部结构并进一步提高导电性。此外,图 4c 中 CNT@Li2FeSiO4 和 CNT@Li2FeSiO4@C 的循环性能图进一步验证了上述说法。可以看出,在0.2 C的电流密度下,CNT@Li2FeSiO4@C比CNT@Li2FeSiO4具有更高的循环性能和容量。CNT@Li2FeSiO4和CNT@Li2FeSiO4@C的倍率性能如图4d所示.可以观察到CNT@Li2FeSiO4的放电容量为98.8 mAh g -1 , 81.3 mAh g −1 , 78.6 mAh g −1 , 和 62.4 mAh g −1 分别在 0.2、0.5、1 和 2 C。虽然 CNT@Li2FeSiO4@C 正极表现出更好的倍率性能,但放电容量为 167.7 mAh g −1 , 125.8 mAh g −1 , 94.6 mAh g −1 , 和 70.6 mAh g −1 分别在 0.2、0.5、1 和 2 C 下实现。这些性能优于其他类似报告中描述的性能[30,31,32]。
<图片>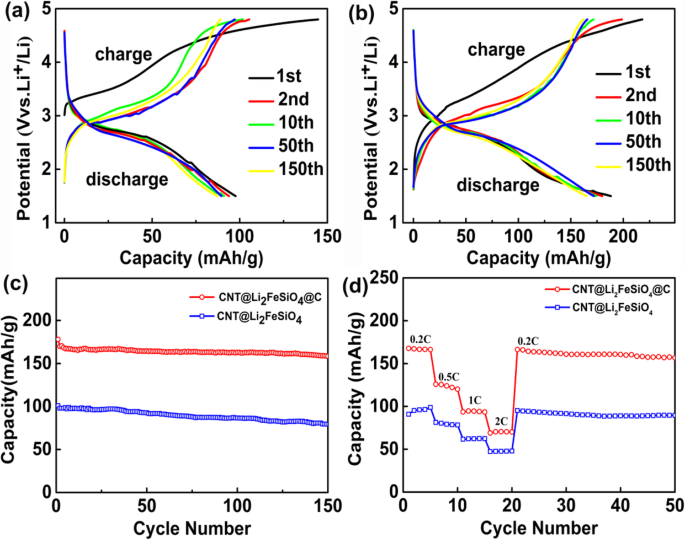
一 CNT@Li2FeSiO4电极在0.2 C倍率下的充放电曲线,b CNT@Li2FeSiO4@C电极在0.2 C倍率下的充放电曲线,c CNT@Li2FeSiO4和CNT@Li2FeSiO4@C电极的循环性能,以及d CNT@Li2FeSiO4和CNT@Li2FeSiO4@C电极的倍率性能
进一步应用CV曲线来分析CNT@Li2FeSiO4@C正极材料的动力学特性。图 5a 显示了 CNT@Li2FeSiO4@C 在 0.1 到 1.0 mV s −1 不同扫描速率下的 CV 曲线 .
<图片>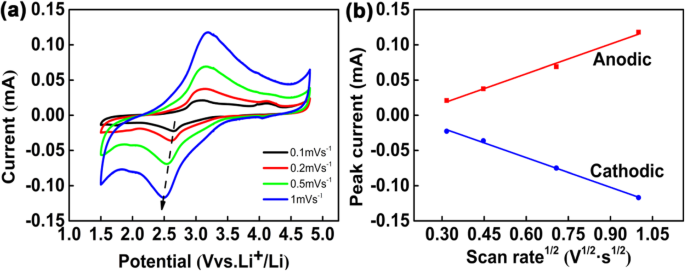
使用 CV 对 CNT@Li2FeSiO4@C 进行动力学分析。 一 各种扫描速率下的 CV 配置文件。 b 作为扫描速率平方根的函数的峰值电流
Fe 2+ 引起的主要氧化还原对电位 /Fe 3+ 反应分别为 3.1 V(阳极)和 2.7 V(阴极),这与恒电流平台曲线一致。值得注意的是,在 3.1 V(阳极)和 2.7 V(阴极)处只有一个主要的氧化还原电对电位对应于 Fe 2+ /Fe 3+ 观察到反应,Fe 3+ /Fe 4+ 氧化还原对被证实不存在。并且 CV 结果与 dQ/dV 与电压数据(附加文件 1:图 S3)一致。所以我们可以得出结论,只有一个 Li + 在充放电过程中,每个配方单位被插入和提取。
此外,随着扫描速率的增加,氧化还原峰的峰位变化很小,表明CNT@Li2FeSiO4@C正极材料的极化反应很小[28]。锂离子在CNT@Li2FeSiO4@C中的扩散系数可通过峰值电流Ip(A)与扫描速率平方根v的线性关系计算 1/2 (v 1/2 s -1/2 )来自 CV(图 5b)。通过下面的等式[33, 34],
$$ \mathrm{Ip}=2.69\times {10}^5{n}^{3/2}{\mathrm{AD}}_{\mathrm{Li}}^{1/2}{\mathrm{ C}}_{\mathrm{Li}}^{\ast}{v}^{1/2} $$在这里,n 是参与反应的电子数,A 指电极面积,C ∗ Li代表Li + 的体积浓度 在电极中。图 5b 说明了 Ip 和 v 之间良好的线性关系 1/2 .在阳极和阴极反应过程中,锂离子的扩散系数为7.32 × 10 -11 和 0.64 × 10 −12 厘米 2 s −1 ,并且这些系数优于之前的实验结果 [35, 36]。这一优势可归因于 CNT@Li2FeSiO4@C 在充放电过程中优异的导电性和离子传输效率。电化学阻抗谱 (EIS) 用于研究 CNT@Li2FeSiO4@C 和 CNT@Li2FeSiO4 的电化学性能。附加文件 1:图 S4 显示了 CNT@Li2FeSiO4@C 和 CNT@Li2FeSiO4 电极的奈奎斯特图。奈奎斯特图由与锂离子迁移阻力相关的高频半圆组成 (R SEI)通过固体电解质界面(SEI),由阴极电解质界面电荷转移电阻(R)引起的中频半圆 ct),以及对应于阴极中锂离子扩散的低频区域倾斜线(Warburg 区域)[36]。 CNT@Li2FeSiO4@C的电荷转移电阻(76.5 Ω)明显低于CNT@Li2FeSiO4(193.4 Ω),说明CNT@Li2FeSiO4@C的电子转移速度更高。
结论
总之,我们通过非常有效的逐层堆叠策略制备了 CNT@Li2FeSiO4@C。核壳异质结构CNT@Li2FeSiO4@C提高了导电性,实现了锂离子的快速提取/嵌入,并减轻了结构损伤。因此,它表现出高容量、循环和倍率性能。因此,CNT@Li2FeSiO4@C正极材料在锂离子电池应用中具有广阔的应用前景。
数据和材料的可用性
所有数据和材料均不受限制地完全可用。
缩写
- CNT:
-
碳纳米管
- CTAB:
-
十六烷基三甲基溴化铵
- 简历:
-
循环伏安法
- EDX:
-
能量色散X射线光谱
- EIS:
-
电化学阻抗谱
- HR-TEM:
-
高分辨透射电子显微镜
- LIB:
-
锂离子电池
- NMP:
-
N -甲基-2-吡咯烷酮
- PVDF:
-
聚偏二氟乙烯
- SEI:
-
固体电解质界面
- SEM:
-
扫描电镜
- TEM:
-
透射电子显微镜
- TEOS:
-
四乙氧基硅烷
- TGA:
-
热重分析仪
- XPS:
-
X射线光电子能谱
- XRD:
-
X射线衍射
纳米材料
- Scalmalloy:用于金属 3D 打印的最新高性能材料
- IBM 和 Warwick Image 首次获得高反应性三角形分子
- 用于金属 X 打印机的 H13 工具钢材料
- 用于锂离子电池的可再生 PVDF 等级
- 锂离子电池用Cr3+和F-复合掺杂LiNi0.5Mn1.5O4正极材料的合成及电化学性能
- 少层二硫化钼/乙炔黑复合材料作为锂离子电池的高效阳极材料
- 用于高效光催化制氢的 ZnO@TiO2 空心球的分级异质结构
- 不同粘合剂对锂离子电池金属氧化物阳极电化学性能的影响
- Na4Mn9O18/碳纳米管复合材料作为水性钠离子电池的高电化学性能材料
- 下一代智能传感器材料
- 问答:优化锂离子电池以实现极速充电
- 摩擦力最好的离合器材料是什么?


