用于蛋白质亲和分离的功能化纳米吸附剂
摘要
通过水热途径合成了平均直径为 460 nm 的硫醇官能化二氧化硅纳米球 (SiO2-SH NSs)。随后,制备的 SiO2-SH NSs 被 SnO2 量子点修饰,得到具有明显荧光的 SnO2/SiO2 复合 NSs,可用于追踪目标蛋白质。 SnO2/SiO2 NSs通过还原型谷胱甘肽(GSH)进一步修饰得到SnO2/SiO2-GSH NSs,可特异性分离谷胱甘肽S -转移酶标记(GST 标记)蛋白。此外,还评估了体外从 SnO2/SiO2-GSH NSs 中分离的谷胱甘肽过氧化物酶 3 (GPX3) 的过氧化物酶活性。结果表明,制备的 SnO2/SiO2-GSH NSs 表现出可忽略不计的非特异性吸附、高浓度的蛋白质结合 (7.4 mg/g) 和良好的再利用特性。同时,被这些 NS 分隔的 GST 标记的 GPX3 可以保留其氧化还原状态和过氧化物酶活性。因此,所制备的SnO2/SiO2-GSH NSs在GST标签蛋白的快速分离和纯化中具有广阔的应用前景。
背景
蛋白质的容易分离和纯化在异生物质的生物转化、药物代谢、前列腺素和类固醇激素的生物合成以及芳香族氨基酸的降解中非常重要[1,2,3,4,5,6]。分离的蛋白质可用于抗原和疫苗生产、分子免疫学和结构以及生化和细胞生物学研究。谷胱甘肽S -转移酶(GST)代表了一类主要的解毒同工酶,可用于GST基因融合系统和药效靶向领域或作为肿瘤标志物[7, 8]。目前可采用沉淀、层析、超滤、透析等多种方法纯化各种蛋白质,尤其是基于生物大分子与互补配体之间天然亲和性的亲和分离具有非凡的意义[9,10,11,12 ,13,14]。然而,全长、可溶性和天然融合蛋白的成功生产和纯化仍然受到各种障碍的阻碍,例如需要预处理以去除细胞碎片和胶体污染物、相对较长的操作时间和蛋白质溶解度。幸运的是,这些缺点可以通过应用纳米材料来帮助目标蛋白质的分离和纯化得到克服 [15,16,17,18,19]。例如,磁性 SiO2-NiO 纳米复合材料能够分离带有 His 标签的蛋白质 [20]。然而,纳米材料在分离各种蛋白质方面仍然存在不足,因为它们通常对可视化和荧光技术无效,可用作敏感的生物分子和医学诊断工具来对抗生物战 [21,22,23]。因此,寻找具有荧光响应的纳米材料以促进其在谷胱甘肽过氧化物酶3(GPX3)等重组蛋白的分离纯化中的应用势在必行。
我们特别关注纳米级 SnO2 量子点 (QD),因为作为具有良好化学稳定性和生物相容性的 n 型宽带隙 (3.6 eV) 半导体,SnO2 在可见光谱区表现出吸光度。在此,我们建立了一种将荧光 SnO2 QD 引入二氧化硅纳米球 (NSs) 表面的智能途径,希望开发出所需的 SnO2/SiO2 纳米结构,并在 GST 标记蛋白质的分离和纯化中具有潜在应用。首先,通过水热途径制备了硫醇官能化二氧化硅纳米球(SiO2-SH NSs)。所得的 SiO2-SH NSs 与 SnO2 量子点复合得到具有明显荧光吸收的 SiO2/SnO2 复合 NSs。通过还原型谷胱甘肽 (GSH) 进一步修饰 SiO2/SnO2 NSs,以获得具有亲和性分离 GST 标签蛋白潜力的 SiO2/SnO2-GSH NSs。采用SDS-PAGE分析制备的SnO2/SiO2-GSH NSs对GST标签蛋白的分离能力和过氧化物酶活性。
实验
材料和方法
十六烷基三甲基溴化铵 (CTAB)、氯化锡 (IV) (SnCl4)、三乙胺 (TEA) 和异丙醇由天津 Kermel 化学试剂公司(中国天津)提供。 AgNO3 购自天津富臣科技发展有限公司(中国天津)。 3-巯基丙基三甲氧基硅烷 (MPS) 由 Alfa-Aesar(中国上海)提供。原硅酸四乙酯 (TEOS) 由天津富臣化工(中国天津)提供。二氢烟酰胺腺嘌呤二核苷酸磷酸 (NADPH)、硫氧还蛋白和硫氧还蛋白还原酶购自 Sigma(中国北京)。 Glutathione Sepharose 4B (Stockholm, USA) 来自 GE Healthcare。二硫苏糖醇(DTT)可从阿拉丁工业公司(Inalco SPA,意大利)获得。所有化学试剂均为分析纯,未经进一步纯化直接使用。
SnO2 量子点的制备
在典型的合成中 [24],将 3.5 g SnCl4·5H2O 加入 50 mL H2O 中,然后在搅拌下将 5 mL 氨加入溶液中。随后,将离心得到的沉淀用去离子水洗涤数次以除去过量的Cl - 离子。将所得沉淀加入去离子水30毫升,然后用2mol/L氨水将溶液pH调至12。将混合溶液转移到衬有聚四氟乙烯的不锈钢高压釜中,密封并在 150°C 下加热 24 小时。加热完成后,将混合溶液冷却,离心,用乙醇-异丙醇(体积比1:1)充分洗涤,得到SnO2量子点。
SnO2/SiO2-SH NSs 的制备
在典型的合成中,将 0.2 g SnO2 QD 和 0.09 g CTAB 在磁力搅拌(200 G,r)下溶解在 H2O(42.5 mL)和无水酒精(7 mL)的混合溶剂中 =180 毫米)。在另外的 20 分钟搅拌下向所得溶液中加入 2.7 mL TEA。将混合溶液在 60°C 加热 5 小时,同时缓慢滴加 3.5 mL TEOS 和 0.35 mL MPS,然后离心(12,800 G,r =180 mm) 并用 HCl-乙醇 (30 mL) 和水 (30 mL) 充分洗涤以获得 SnO2/SiO2-SH NSs 3 次,将其分散在水中 (0.12 g/mL)。
SnO2/SiO2-SH NSs 的表面改性
将四毫升 0.12 g/mL SnO2/SiO2-SH NSs 用 PBS (0.01 mol/L, pH =7.4) 洗涤 3 次。将这些 SnO2/SiO2-SH NS 添加到 30 mL 16.7 mg/mL GSH 溶液中,并在 37°C 下用恒温振荡器振荡 24 小时(120 转/分钟)。在振荡结束时,将混合溶液离心以提供SnO2/SiO2-GSH NSs;然后,将沉淀物用30 mL PBS(0.01 mol/L,pH =7.4)充分洗涤3次以通过物理吸附去除过量的GSH,从而得到所需的SnO2/SiO2-GSH NSs。将得到的 SnO2/SiO2-GSH NSs 添加到酒精 (25%, v /v ) 并在 4°C 下储存。
GST 标记蛋白质的分离
从大肠杆菌细胞裂解液中收集混合蛋白 ,这是通过水裂解(浓度 0.01 mol/L,pH 7.4)。对于体外蛋白质表达,在
用 PBS 溶液(0.01 mol/L,pH =7.4)洗涤后,将制备的 SnO2/SiO2-GSH NSs 直接引入 1000 μL E。大肠杆菌 裂解物并在 4°C 下振荡 2 小时(转速:90 转/分钟),使 SnO2/SiO2-GSH NSs 捕获 GST 标记的蛋白质。摇动完成后,通过离心从溶液中分离这些 NSs,并用 PBS 溶液充分洗涤以去除任何残留的未捕获的蛋白质。 GST 标记的蛋白质结合的 SnO2/SiO2-GSH NSs 用 300 μL 和 0.5 mol/L GSH 溶液洗涤 3 次,以将 GST 标记的蛋白质与其表面分离。通过十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE)检测单独收集的蛋白质溶液。分离的蛋白质的浓度由BCA蛋白质测定试剂盒测定。 SnO2/SiO2-GSH NSs可以重复使用多次,以相同的方法分离目标蛋白质。
谷胱甘肽过氧化物酶活性的测量
如 Delaunay 等人所述,通过光谱测定法测定 340 nm 处的 NADPH 消耗来测量分离的 GPX3 活性。 [25]。通过PreScission 蛋白酶从GST 标记的GPX3 上切下GST 标签,然后将GPX3 用于活性分析。首先,98 μL 反应缓冲液(包括 100 mmol/L Tris-Cl、0.3 mmol/L NADPH、1.34 μmol/L 硫氧还蛋白和 0.18 μmol/L 硫氧还蛋白还原酶来自E.coli lysate)加入管中;完全混合后,将 1.35 μmol 纯化的 GPX3 添加到所得反应缓冲溶液中。然后,将混合溶液加入到 2 μL H2O2 (5 mmol/L) 中以引发反应,并通过光谱测定收集 340 nm 处的 NADPH 消耗量。
纯化 GPX3 的氧化还原状态分析
GST 标签是由 PreScission 蛋白酶从 GST 标签的 GPX3 上切下的。分离的 GPX3 用 5 mmol/L H2O2 和 1mmol/L DTT 处理 10 分钟,以改变纯化 GPX3 的氧化还原状态。所得 GPX3 用于氧化还原状态的体外分析。提取物经非还原性15% SDS-PAGE凝胶检测。
特征化
通过透射电子显微镜 (TEM, JEM-2010, Japan)、扫描电子显微镜 (SEM, JSM 5600LV, Japan)、X 射线衍射 (XRD, X' Pert Philips,Holland)和荧光光谱仪(FL,FluoroSENS,英国,激发波长为 260 nm)。分离的GST标签蛋白用十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE,Power PAC 300,China)检测,预浓缩电压70 V,分离电压120 V。恒温振荡器来自上海ChemStar Instruments , 有限公司(ATS-03M2R,中国)。分离后的蛋白浓度采用BCA蛋白检测试剂盒(北京科威生物技术有限公司)测定。
结果与讨论
SnO2 QD 和 SnO2/SiO2-GSH NSs 的 TEM、SEM、XRD 和荧光分析
图 1 给出了合成的 SnO2 QD 的高分辨率 TEM (HRTEM) 图像和 XRD 图案。可以看出,合成的 SnO2 QD 为球形,平均直径为 5 nm,粒径分布较窄(图 1a),(110)面的晶格间距为 0.29 nm(图 1a)。 1b)。解析良好的晶格图像表明制备的 SnO2 QD 具有高度有序的晶体结构。 SnO2 QD 的相应选区电子衍射图(图 1c)可以归为单一锡石相,这与相关的 XRD 图(图 1d)一致。即2θ =26.6°(110)、33.9°(101)、38.0°(200)、51.8°(211)、65.9°(301)和78.7°(321)处的特征峰与标准一致锡石 SnO2 的 XRD 数据(JCPDS 卡号 41-1445)。此外,强烈的XRD峰表明制备的SnO2 QDs结晶良好,没有其他特征峰表明它们不含赤铁矿或氢氧化物杂质。
<图片>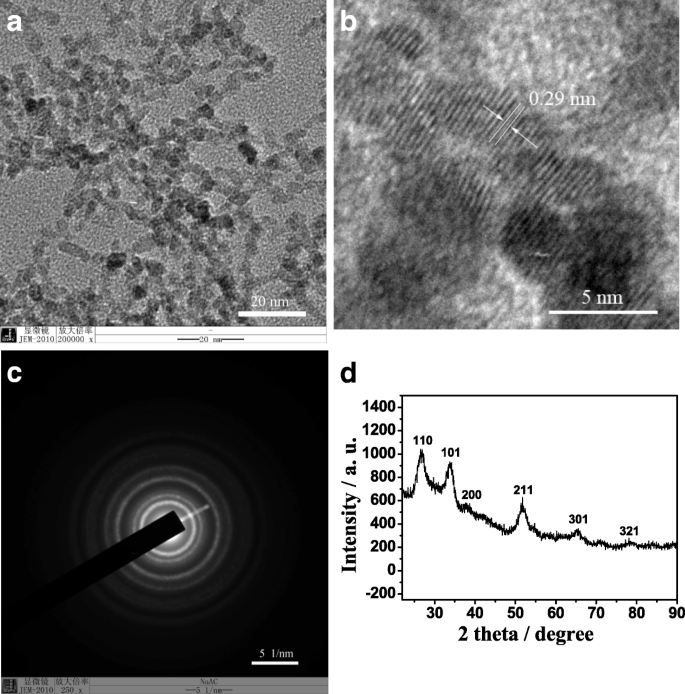
透射电镜 (a ), HRTEM (b ) 图像,选区电子衍射图 (c ) 和 XRD 图 (d ) 制备的 SnO2 QDs
图 2 给出了 SnO2/SiO2-GSH NSs 的 SEM 和 TEM 图像。可以看出,制备的 SnO2/SiO2-GSH NSs 呈球形,平均直径约为 430 nm,表面看起来有些粗糙(图 2a、b)。同时,可以看到 SnO2 QD(约 5-15 nm)在 SiO2 微球表面发生了改性(图 2c、d),这与相应的 SEM 图像一致。表明SnO2和二氧化硅NSs已经聚集。
<图片>
SEM (a , b ) 和 TEM (c , d ) 制备的 SnO2/SiO2-GSH NSs 的图像
图 3a 给出了合成的 SnO2/SiO2-GSH NSs 的 XRD 图。 2 theta =110°、101°、200°、211°、301°和321°的主峰与SnO2的主峰一致(图1d)。此外,SnO2/SiO2-GSH NSs 在 23° 附近显示出强烈的无定形二氧化硅特征峰(JCPDS 卡号 76-0933),这表明具有可见光响应的 SnO2 已成功引入到 SiO2 NSs 表面。图 3b 显示了 SnO2/SiO2-GSH NSs 在 368 nm 处的荧光光谱。可以看出,SnO2/SiO2-GSH 显示出强烈的荧光发射,这归因于 SnO2 的氧空位。图 3c 给出了 SnO2/SiO2-GSH NSs 的荧光成像,当这些 NSs 用于分离 E 中的 GST 标记的 GPX3 时。线圈 裂解液。可以看出,使用制备的 SnO2/SiO2-GSH NSs 有明显的绿色荧光。表明在SiO2表面修饰了SnO2,SnO2/SiO2-GSH NSs具有良好的荧光性能。
<图片>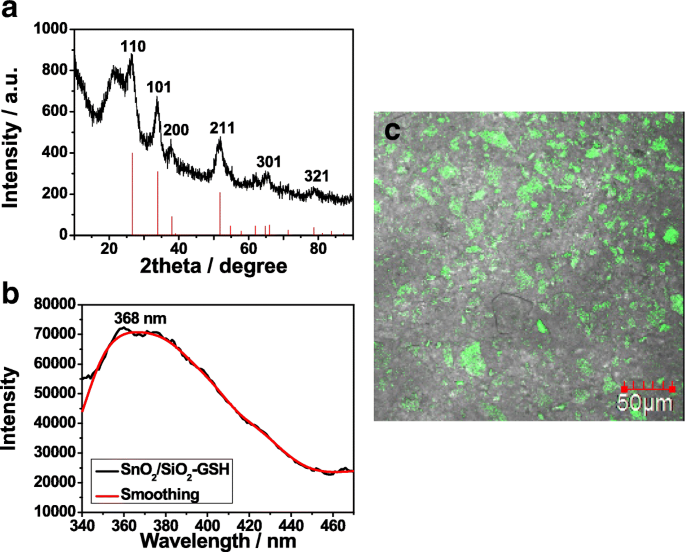
XRD 图 (a )、荧光光谱(b ) 和荧光成像 (c )制备的SnO2/SiO2-GSH NSs
SDS-PAGE 分析
为了评估制备的 SnO2/SiO2-GSH NSs 在分离 GST 标签蛋白方面的能力,我们进行了 SDS-PAGE 分析。图 4 显示了被 SnO2/SiO2-GSH NSs 分离的 GST 标记的 GPX3 的 SDS-PAGE 分析结果。可以看出,SnO2/SiO2-GSH NSs 可以有效地从E 中富集目标蛋白。大肠杆菌 裂解物,特别是,随着 GSH 浓度在 10-100 mmol/L 范围内的增量,解离蛋白的数量趋于增加(图 4a 中的第 3-6 道)。很明显,目标蛋白质可以通过制备的 SnO2/SiO2-GSH NSs 从 E 中特异性分离。大肠杆菌 裂解物,几乎没有任何非特异性。
<图片>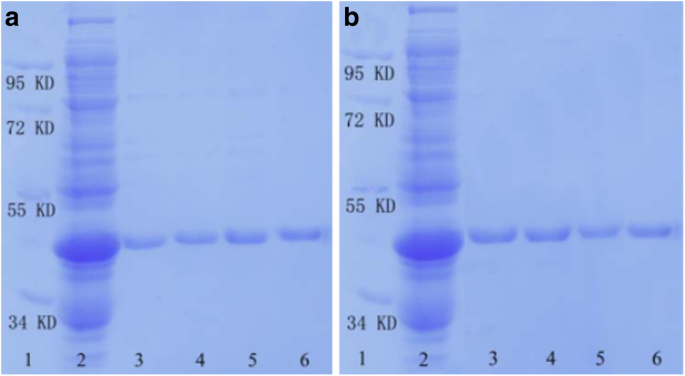
由 SnO2/SiO2-GSH NSs 分离的纯化 GST 标记蛋白的 SDS-PAGE 分析。 一 泳道 1,标记;泳道 2,E。大肠杆菌 裂解液;泳道 3-6 是指用不同浓度的 GSH 溶液(泳道 1,10 mmol/L;泳道 2,20 mmol/L;泳道 3,50 mmol/L;泳道)从 SnO2/SiO2-GSH NSs 洗掉的部分4, 100 毫摩尔/升)。 b 泳道 1,标记;泳道 2,E。大肠杆菌 裂解液;车道 3,第 1 分隔;车道 4, 2nd 分离;车道 5,第 3 分隔;泳道6,从Glutathione Sepharose 4B中洗掉的馏分
为了研究制备的 SnO2/SiO2-GSH NSs 的重复使用特性,我们反复使用它们来分离 GST 标记的 GPX3。如图 4b 所示(第 1 道指标记,第 2 道指含有 GST-GPX3 的大肠杆菌 裂解液,第 3 道指第 1 次分离,第 4 道指第 2 次分离,第 5 道指第 3 次分离,第 6 道指从谷胱甘肽琼脂糖凝胶 4B 中洗掉的馏分),合成的 SnO2/SiO2-GSH NSs 对从 E 中提取的带有 GST 标签的 GPX3。大肠杆菌 裂解液经过三个循环的重复分离后,其特异性和亲和力不受影响。
为了测试合成的 SnO2/SiO2-GSH NSs 纯化 GST 标签蛋白的通用性,我们选择了三种 GST 标签蛋白(GST 标签 GPX3、GST 标签 OST1 和 GST 标签 ABI2)进行实验。如图 5 所示,带有 GST 标签的 GPX3、OST1 和 ABI2 蛋白可以通过 SnO2/SiO2-GSH NSs 从 E 中特异性分离。大肠杆菌 裂解物(泳道 3、6、9);然后,我们可以得到 GPX3(从 SnO2/SiO2-GSH NSs 中切断 GST 标签结合 GST 标签 GPX3)和从 SnO2/SiO2-GSH NSs 洗脱的 GST 标签(13 道,GPX3;14 道,GST 标签),它与谷胱甘肽琼脂糖凝胶 4B 具有相似的效果(泳道 2、5、8、11、12)。 SnO2/SiO2-GSH NSs 纯化的蛋白质浓度为 7.4 mg/g(GST 标记的 GPX3)、7.1 mg/g(GST 标记的 OST1)和 6.8 mg/g(GST 标记的 ABI2),这表明SnO2/SiO2-GSH NSs 可以很好地从 E 中纯化带有 GST 标签的蛋白质。大肠杆菌 裂解液。为了比较制备的SnO2/SiO2-GSH NSs与其他材料的结合能力,使用Glutathione Sepharose 4B(购自美国斯德哥尔摩)作为对比实验材料。通过谷胱甘肽琼脂糖凝胶 4B 纯化的总蛋白质分别为 7.1 mg/mL(GST 标记的 GPX3)、6.9 mg/mL(GST 标记的 OST1)和 5.6 mg/mL(GST 标记的 ABI2)。可见,所制备的SnO2/SiO2-GSH NSs的结合能力高于商品4B。
<图片>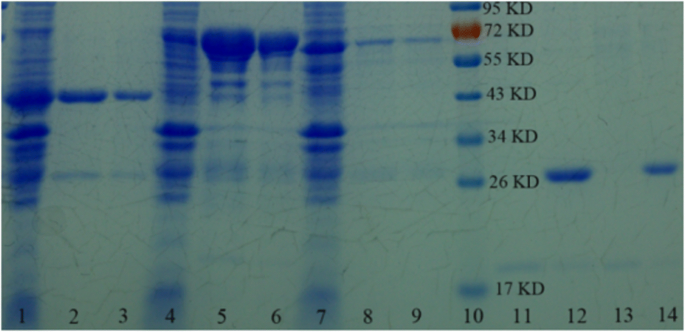
纯化的重组 GPX3、OST1 和 ABI2 蛋白的 SDS-PAGE 分析。泳道 1、4 和 7,E。大肠杆菌 裂解液;泳道 2、5 和 8,从商业 Glutathione Sepharose 4B(GE Healthcare,美国)洗脱的蛋白质;泳道 3、6 和 9,从 SnO2/SiO2-GSH NSs 洗脱的蛋白质;车道10,标记;泳道11和13,从谷胱甘肽琼脂糖凝胶4B结合的GST-GPX3和SnO2/SiO2-GSH NSs结合GST标记的GPX3切断GST标签后获得的GPX3;泳道12和14,GST标签从谷胱甘肽琼脂糖凝胶4B和SnO2/SiO2-GSH NSs洗脱
GST 标记 GPX3 的氧化还原状态和过氧化物酶活性分析
为了分析由制备的 SnO2/SiO2-GSH NSs 分离的 GST 标签 GPX3 的氧化还原状态和活性,我们切断 GST 标签以获得分离的 GPX3。图 6a 显示给定的 GPX3 氧化还原状态的体外测定(对应于来自三个独立实验的代表性凝胶)。 1、2道是GST标签从Glutathione Sepharose 4B结合的GST-tagged GPX3上切下GST标签后得到的GPX3(1道是氧化的GPX3,2道是还原的GPX3);第3和第4道是指从SnO2/SiO2-GSH结合的GST-tagged GPX3上切断GST标签后得到的GPX3(第3道是氧化的GPX3,第4道是还原的GPX3);车道 5 是指标记。如图 6a 所示,从 Glutathione Sepharose 4B(泳道 1 和 2)和 SnO2/SiO2-GSH NSs(泳道 3 和 4)中分离出来的纯化 GPX3 具有氧化和还原状态,并且还原的 GPX3 迁移比氧化对应物。这与我们之前的研究结果非常一致,即 GPX3 在体外以氧化和还原状态存在,并且可以通过修饰还原的 Cys 残基将其还原和氧化形式分开 [26,27,28]。
<图片>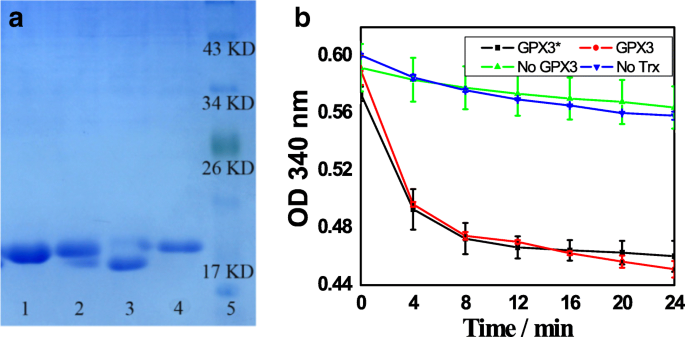
一 GPX3 氧化还原状态的体外测定:泳道 1 和 3(氧化的 GPX3)和泳道 2 和 4(还原的 GPX3)是指从谷胱甘肽琼脂糖凝胶 4B 和 SnO2/SiO2-GSH 结合 GST-切断 GST 标签后获得的 GPX3。分别标记为GPX3;车道 5,标记。 b GPX3过氧化物酶活性测定
图 6b 显示了 GPX3 过氧化物酶活性的测定:线 GPX3*,在谷胱甘肽琼脂糖凝胶 4B、硫氧还蛋白、硫氧还蛋白还原酶、NADPH 和 H 2 O 2 存在下对纯化的 GPX3 的完整测定;线 GPX3,SnO2/SiO2-GSH NSs 之间的完全反应分离 GPX3、硫氧还蛋白、硫氧还蛋白还原酶、NADPH 和 H2O2;线没有GPX3,在没有GPX3的情况下完全反应;和线 No Trx,在没有硫氧还蛋白的情况下完成反应。图 6b 显示了从谷胱甘肽琼脂糖凝胶 4B 和 SnO2/SiO2-GSH NSs 分离的纯化 GPX3 在体外的谷胱甘肽过氧化物酶活性。可以看出,以硫氧还蛋白为底物,纯化的GPX3表现出显着的过氧化物酶活性,表明从SnO2/SiO2-GSH NSs中分离出来的GPX3以天然状态存在。
结论
建立了一种简单的方法来制造二氧化硅保护的 SnO2 QD 纳米球 (SnO2/SiO2 NSs)。 SnO2/SiO2 NSs 被谷胱甘肽进一步修饰,得到 SnO2/SiO2-GSH NSs 用于亲和分离谷胱甘肽 S -转移酶标记(GST 标记)重组蛋白。研究结果表明,在分离 GST 标记的 GPX3、GST 标记的 LOV 和 GST 标记的 ABI2 的能力方面,制备的 SiO2/SiO2-GSH NSs 表现出特定的分离、高浓度的蛋白质结合和良好的重复利用特性。此外,与 GST 标记的 GPX3 分离的 GPX3 在体外保持其氧化还原状态和 GPX 活性,这意味着制备的 SnO2/SiO2-GSH NSs 可能具有快速分离和纯化 GST 标记的蛋白质的潜力.
缩写
- ABI2:
-
ABA不敏感2
- CTAB:
-
十六烷基三甲基溴化铵
- DTT:
-
二硫苏糖醇
- GPX3:
-
谷胱甘肽过氧化物酶3的过氧化物酶活性
- GSH:
-
还原型谷胱甘肽
- GST 标签:
-
谷胱甘肽S -转移酶标记
- MPS:
-
3-巯基丙基-三甲氧基硅烷
- NADPH:
-
二氢烟酰胺腺嘌呤双核苷酸磷酸
- OST1:
-
打开气孔1
- 量子点:
-
量子点
- SDS-PAGE:
-
十二烷基硫酸钠聚丙烯酰胺凝胶电泳
- SEM:
-
扫描电镜
- SiO2-SH NSs:
-
巯基功能化二氧化硅纳米球
- 氯化锡:
-
氯化锡(IV)
- TEA:
-
三乙胺
- TEM:
-
透射电子显微镜
- TEOS:
-
原硅酸四乙酯
- XRD:
-
X射线衍射
纳米材料


