Ag 修饰的 SnO2 微球的一锅绿色合成:一种用于还原 4-硝基苯酚的高效且可重复使用的催化剂
摘要
在本文中,通过简便的一锅水热法合成了分级 Ag 修饰的 SnO2 微球。所得复合材料通过 XRD、SEM、TEM、XPS、BET 和 FTIR 分析进行表征。以硼氢化钾 (KBH4) 将 4-硝基苯酚还原为 4-氨基苯酚作为模型反应,评估样品的催化性能。时间依赖性实验表明,当反应时间小于 10 小时时,可以形成由 SnO2 和 Ag 纳米颗粒组装的分级微球。随着水热时间的增加,SnO2纳米颗粒会自组装成SnO2纳米片,得到Ag纳米颗粒修饰的SnO2纳米片。当评估为催化剂时,制备 36 h 所得的 Ag 修饰的 SnO2 微球表现出优异的催化性能,归一化速率常数 (κ 也) 6.20 分钟 −1 g −1 L,这比之前报道的一些催化剂要好得多。此外,这种银装饰的 SnO2 微球在前五个循环后表现出良好的可重复使用性。此外,我们推测了分级Ag修饰的SnO2微球的形成机制,并讨论了其优异催化活性的可能来源。
背景
SnO2 是一种重要的 n 型半导体,具有大带隙(Eg =3.6 eV,在 300 K 时)、高电子迁移率和低成本,使其在气体传感 [1]、锂离子电池 [2]、光电器件和染料敏化太阳能电池 [3,4,5,6,7,8]。在过去的 20 年中,坚固的 SnO2 材料引起了相当多的关注,并且已经报道了各种纳米结构 [9, 10]。其中,由纳米片积木自组装的三维(3D)层次结构由于其特殊的结构和迷人的特性而更加有趣[11, 12]。然而,关于SnO2催化性能的报道很少,催化效率相对较低[13,14,15]。因此,合成分级的 SnO2 结构并研究其催化性能非常重要。特别是,正如我们所知,贵金属纳米粒子 (NPs),如 Au-、Ag-、Pt- 和 Pd 修饰的 3D 分层结构将显示出大大增强的催化性能 [16]。然而,上述贵金属改性氧化物的合成过程大多是较为复杂的多步过程,通常对环境有毒有害[17]。因此,开发简便高效的贵金属NP修饰多级SnO2的制备方法并对其催化性能进行研究是非常必要的。
由于各种工业染料、重金属离子和其他芳香族污染物的广泛分布,我们有限的水资源受到越来越多的污染,正在危及我们的星球 [18]。 4-硝基苯酚 (4-NP) 是一种众所周知的有毒污染物,广泛存在于工业废水和农业废水中 [19]。在各种处理技术中,如膜过滤[20]、光降解[21]、吸附[22]和化学还原[23、24、25、26、27、28、29、30],4 -NP 制 4-氨基苯酚 (4-AP) 是一条有利的路线,因为该产品 (4-AP) 是制造镇痛和解热药物、照相显影剂、缓蚀剂、防腐润滑剂和头发的重要中间体。 - 染色剂 [31, 32]。因此,将4-NP还原为4-AP对于污染减排和资源再生具有重要意义[33]。
在本文中,我们报道了一种在温和温度下通过简单的一锅水热路线合成贵金属 Ag 纳米颗粒 (NP) 修饰的 SnO2 分层结构的绿色合成方法,无需任何模板和表面活性剂的辅助。研究了反应时间对Ag修饰的SnO2微球形貌的影响,并提出了Ag修饰的SnO2分级结构的可能生长机制。催化结果表明,合成的产物对 4-NP 还原为 4-AP 表现出优异的催化性能,具有归一化速率常数 (κ 也) 6.20 分钟 −1 g −1 L. 此外,Ag 修饰的 SnO2 分级结构在 10 次循环中保持高催化效率,并在前 5 次循环后表现出稳定性。这种获得的银修饰的 SnO2 分级结构可能具有处理水污染物的潜在应用,这种简单的一步水热路线可以扩展到设计其他贵金属 NP 修饰的复合材料,在未来具有广泛的实际应用。
方法
材料
硝酸银(AgNO3, 99.8%)、尿素(CO(NH2)2, 99%)、氨溶液(NH3·H2O, 25~28%)、硼氢化钾(KBH4, 97%)购自国药集团化学试剂有限公司. Ltd.复水锡酸钠(Na2SnO3·3H2O, 98%)和4-硝基苯酚(C6H5NO3, 98%)由阿拉丁试剂有限公司提供,所有原料未经进一步纯化直接使用。
Ag 修饰的 SnO2 微球的合成
用一锅水热法合成了Ag修饰的SnO2粉体(Ag:SnO2 =1:1的摩尔比)。在典型的程序中,将 2.67 g 锡酸钠再水合物和 0.2 g 尿素溶解在 25 mL 超纯水中并剧烈搅拌 30 分钟以形成混合物。然后,将 1.69 g 硝酸银分散在 25 mL 超纯水中,然后将 2.4 mL 氢氧化铵加入硝酸银溶液中形成银-氨溶液。搅拌 5 分钟后,在磁力搅拌下将新制备的银-氨溶液加入混合物中 1 小时。随后,将所得混合物迁移到 50 毫升特氟龙衬里的高压釜中,并在 150°C 下加热 5、10、24 和 36 小时。水热程序后,将高压釜自然冷却至室温,离心收集 SnO2/Ag 产物,然后用去离子水和乙醇冲洗,并在 60°C 的真空烘箱中干燥。除了 AgNO3 和 NH3·H2O 的用量不同外,Ag 与 SnO2 的摩尔比不同(1.5:1、1:1、0.5:1、0.01:1)的 SnO2/Ag 微球的合成方法类似。为了比较,在不添加AgNO3和Na2SnO3的情况下,也通过类似的方法合成了纯SnO2和Ag。
样本特征
通过X射线粉末衍射(XRD,Cu Kα辐射(λ =1.5418 Å))。扫描电子显微镜 (SEM) 测量在 SU-70 场发射 SEM 显微镜上进行,加速电压为 20 kV。透射电子显微照片 (TEM) 和高分辨率透射电子显微镜 (HRTEM) 在 Tecnai G2 F20 S-TWIN 透射电子显微镜上拍摄,加速电压为 200 kV。在 MARK II X 射线光电子能谱仪上使用 Mg Kα 辐射进行 X 射线光电子能谱 (XPS) 以鉴定催化剂的表面化学成分和化学状态。样品的比表面积通过Langmuir模型和Brunauer-Emmett-Teller(BET)模型基于V-sorb X2008系列获得的氮吸附等温线进行评估,而孔径分布由Barrett-Joyner-Halenda估算(BJH) 理论。
Ag 修饰的 SnO2 微球的催化活性
用 KBH4 溶液还原 4-NP 作为模型反应来研究 Ag 修饰的 SnO2 复合材料的催化活性。催化还原过程在具有 1 cm 路径长度和约 4 mL 体积的标准石英池中进行,其中包含 0.3 mL 新鲜制备的 4-NP (20 mg/L) 和 KBH4 (1.5 mg) 水溶液。 KBH4 与 4-NP 的高摩尔比确保了前者的过量,因此,在还原反应过程中其浓度基本保持恒定。将 KBH4 加入 4-NP 溶液后,由于 4-硝基苯酚离子(由 KBH4 的高碱度形成)的形成,其颜色立即从浅黄色变为深黄色。后来,在添加 1.5 毫克 Ag 修饰的 SnO2 杂化物后,深黄色随着时间的推移而褪色(由于 4-NP 转化为 4-AP)。 UV-Vis 吸收光谱由 UV-Vis 光谱仪在室温下以 1 分钟的时间间隔在 250-500 nm 的扫描范围内记录。连续进行几轮反应以确定催化剂的稳定性。
结果与讨论
Ag 修饰的 SnO2 微球的表征
通过XRD研究了不同时间合成的Ag修饰的SnO2粉末的组成和相结构,相应的图案如图1所示。可以看出特征衍射峰与四方金红石相SnO2匹配良好( JCPDS 文件编号 41-1445,a =4.738Å 和 c =3.187 Å) 和面心立方 (fcc) 相 Ag(JCPDS 文件编号 04-0783)。没有检测到来自任何其他杂质的衍射峰,表明粉末是纯 SnO2 和 Ag 的混合物。对于反应 5 小时的样品,在 38.12° 和 44.2° 处的特征衍射峰,对应于 Ag 的 (111) 和 (200) 面,相对较弱。随着水热时间的增加,Ag 的峰强度增加,衍射峰的全宽也减小,表明 Ag 纳米颗粒的结晶度增强或 Ag 的重量增加。这可以通过在不同温度和不同Ag和SnO2摩尔比下获得的样品的XRD图进一步验证(附加文件1:图S1)。
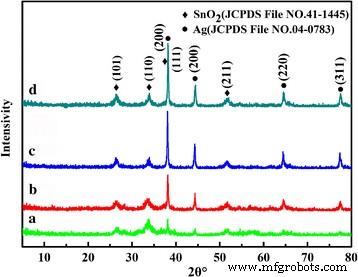
在 150°C 下制备不同时间的 Ag 修饰的 SnO2 微球的 XRD 图 (a ) 5 小时,(b ) 10 小时,(c ) 24 小时,和 (d ) 36 小时
图 2 中的 SEM 图像显示了在 5 至 36 小时的不同水热时间制备的样品的有趣形态演变。制备 5 小时的样品是不规则的微球,插图中微球表面的放大图说明微球是由纳米颗粒组装的(图 2a)。随着水热时间的增加,微球变得更加规则。水热时间增加到 24 小时后(图 2c),微球变大,但纳米颗粒变小,表面纳米颗粒自组装成纳米片。这些纳米片组装起来形成分层的微球结构。当水热时间进一步增加到 36 小时时,粗纳米片变得平滑,直径在 2 到 4 微米之间的微球更加均匀。水热时间的进一步增加导致形态和结晶没有明显变化(本文未显示)。通过 TEM 和 HRTEM 进一步观察制备 36 小时的样品的形态。如图 2e 所示,获得的 SnO2/Ag 具有直径约 5 μm 的微球形态,微球由纳米片组装而成。在典型的 HRTEM 图像(图 2f)中,形成了平均尺寸约为 5 nm 的 Ag NPs 并均匀分布到 SnO2 中。 d 的晶格条纹 =0.26 nm 间距可以分配给 Ag (111) 平面,而 d 的晶格条纹 =0.33 nm 可以分别分配给 SnO2 的 (110) 平面。为了进一步说明 Ag 纳米粒子在微球中的均匀分布,进行了 SnO2/Ag 微球的元素映射分析(图 3)。如图 3 所示,Ag、Sn 和 O 元素的分布图与样品形貌相吻合,表明 Ag 纳米颗粒均匀地分散在微球中。
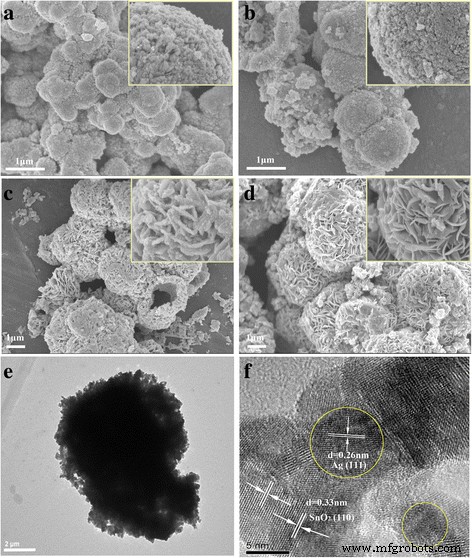
在 150°C 下制备的不同水热时间下 Ag 修饰的 SnO2 微球的代表性 FESEM 图像和 TEM 图像a 5 小时,b 10 小时,c 24 小时和 d 36h 和 e , f 制备 36 h 的样品的低倍率 TEM 图像和高分辨率 TEM (HRTEM)
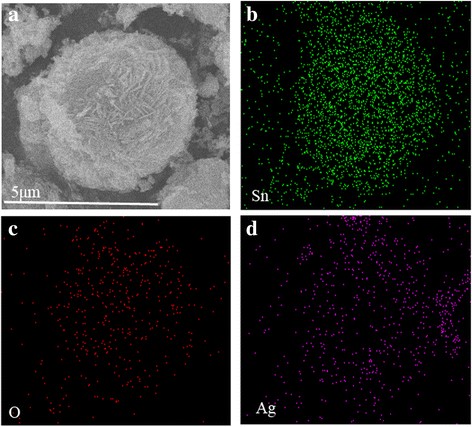
SnO2/Ag 微球的 EDS 元素映射。 一 b的SEM图像和元素图 Sn,c O 和 d 银
样品的 N2 吸附-解吸等温线及其相应的孔径分布如图 4 所示。所有样品均表现出具有 H3 滞后回线的 IV 型等温线,表明具有均匀孔径的典型介孔结构 [34]。 BET 比表面积确定为 21.8、22.4、24.6。和 25.7 m 2 g −1 , 分别。插图描绘了样品的孔径分布。所有样品的孔径分布都是单峰的。分级 Ag 装饰的 SnO2 粉末的平均孔径为 ~2 nm。注意到计算得到的BET表面积和平均孔径随着水热时间的增加没有明显变化。
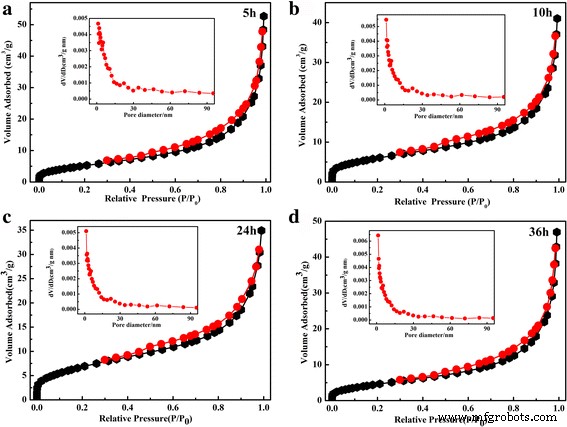
在150°C下制备的不同水热时间下制备的SnO2/Ag微球的典型氮吸附-解吸等温线a 5 小时,b 10 小时,c 24 小时和 d 36 小时
XPS 用于检查 Ag 装饰的 SnO2 微球的化学状态和表面组成。首先记录宽测量扫描,然后详细扫描每个元素的边缘,例如 Sn 3d、Ag 3d 和 O 1s(图 5)。值得一提的是,通过将碳 (C 1s) 的结合能设置为 284.6 eV 来校正对样品的充电效应,并将该碳峰用作缩放所有其他峰的参考位置。如图 5b 所示,对于 Ag 0 ,峰在 369.1 eV (Ag 3d5/2) 和 375.2 eV (Ag 3d3/2) 处表现为自旋轨道双峰 [35, 36] 在产品中。 366.5 和 372.3 eV 的两个卫星峰可以解释 Ag 装饰的 SnO2 纳米复合材料中的 Ag 3d [37]。此外,位于 488 和 496.7 eV 的两个 XPS 峰与 Sn 3d5/2 和 Sn 3d3/2 相关,表明存在 Sn 4+ 在 SnO2 中。 485.7 和 494.7 eV 附近的峰值可能是由 Sn 和 Ag 之间的结合引起的 [38, 39]。这些元素在 Ag 装饰的 SnO2 微球中的轻微结合能转移意味着电子可以在 Ag 和 SnO2 之间转移,这表明 Ag 纳米颗粒和 SnO2 纳米片之间存在强相互作用,而不是简单的物理接触。强相互作用有利于相邻粒子之间的电子转移,可以提高催化活性并有利于一些类似现象,这在其他文献中观察到[38,39,40]。在图 5d 中,530.5 eV 处的 O 1s 光谱对应于晶格氧,而 532.6 eV 处的峰对应于化学吸附的氧或氢氧根离子,例如 O - , O2 − , 或 OH − 在SnO2表面[41,42,43,44]。
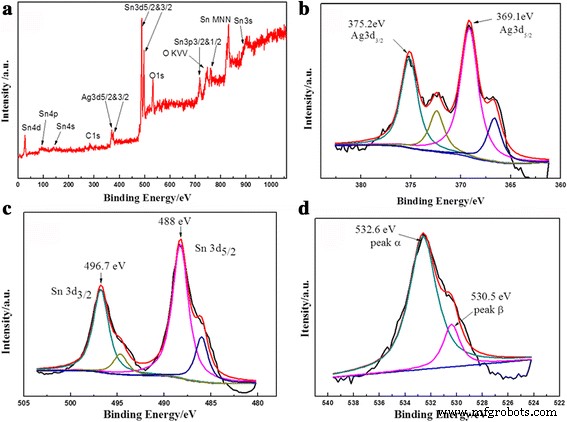
在 150°C 下制备 36 小时的 SnO2/Ag 微球的代表性 XPS 光谱。 一 XPS 全光谱。 b 元素的高分辨率光谱 银,c Sn 和 d 哦
4-NP 的催化还原
在催化剂存在下 KBH4 还原 4-NP 是一个经过充分研究的绿色化学反应,并被选为模型反应来研究所制备的 Ag 装饰的 SnO2 复合材料的催化活性。由于硝基化合物,在 400 nm 处形成了最大吸收的 UV-Vis 吸收光谱。添加 Ag 修饰的 SnO2 催化剂后,归因于硝基化合物的 400 nm 吸收峰在 1 分钟内急剧下降,并在 300 nm 处出现对应于 4-AP 的新峰,表明 4-NP 的催化还原已经进行成功(图 6a)。考虑到过量的 KBH4,可以假设其浓度在反应过程中是一个常数。因此,可以应用伪一级动力学方程来评估催化速率。还原的动力学方程可写为:
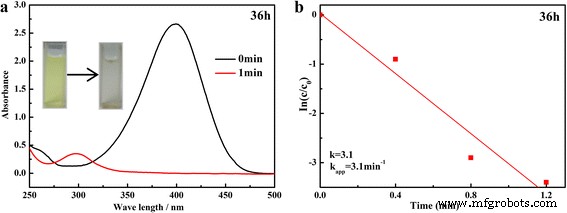
一 , b 随时间变化的 UV-Vis 吸收光谱和 ln(C t /C 0) 与在 150 °C 下制备 36 h 的样品的 4-NP 还原反应时间对比
$$ \frac{dC}{dt}={\kappa}_{\mathrm{app}}{C}_t\;或\;\mathrm{In}\left(\frac{C_t}{C_0}\right)=\mathrm{In}\left(\frac{A_t}{A_0}\right)=-{\kappa}_{ \mathrm{app}} t $$ (1)其中 4-NP 浓度的比率 C t (在时间 t ) 到它的初始值 C 0 (t =0) 由各自吸光度的相对强度 At/A0 直接给出,κ app 对应于表观速率常数。表观速率常数,κ 应用程序,计算为 3.10 分钟 −1 用于在 150°C 下将制备的 Ag 装饰的 SnO2 微球的 4-NP 还原 36 小时(图 6b)。为了进一步评估Ag修饰的SnO2的催化性能,对不同水热时间制备的所有样品进行了4-NP的催化还原。还原的紫外-可见吸收光谱显示在附加文件 1:图 S2-S5 中,以及相应的 ln(C t /C 0) 与时间的关系如图 7 所示。很明显,在第一个循环的 1 分钟内可以减少几乎 100% 的 4-NP。随着循环次数的增加,时间变长。然而,超过 80% 的 4-NP 可以在 8 分钟内重复使用。可以看出,ln(C t /C 0) 值与所有催化剂的反应时间显示出良好的线性相关性,表明还原遵循一级反应规律。计算的表观速率常数κ 所有样品不同循环的应用见表1。
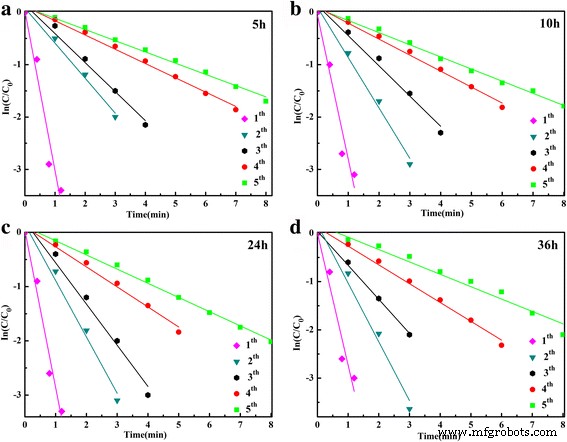
ln(C t /C 0) 与在不同水热时间制备的银修饰的 SnO2 微球存在下的反应时间 a 5 小时,b 10 小时,c 24 小时和 d 36 小时
<图>如图 7 和表 1 所示,表观速率常数 (κ app)随着热液时间的延长而增加,随着循环次数的增加而减少,尤其是在第一次和第二次循环中。速率常数的降低可能是由于离心过程中 Ag NPs 从微球上的剥离和凝结所致。为了证明工作中制备的样品的稳定性,将分离的催化剂(制备 36 h)重新用于催化还原 4-NP 超过 5 个循环。第 6 次循环至第 10 次循环的时间相关 UV-Vis 吸收光谱显示在附加文件 1:图 S6 中。相应的表观速率常数 (κ app) 如图 8 所示,κ 仅略有下降 app 值随着连续循环次数的增加而增加,表明在前五个循环后,催化剂比新制备的样品稳定得多。这证明所制备的 Ag 修饰的 SnO2 样品对 KBH4 将 4-NP 催化还原为 p-AP 具有良好的稳定性,可作为替代的活性和稳定的催化剂用于催化还原 4-NP。
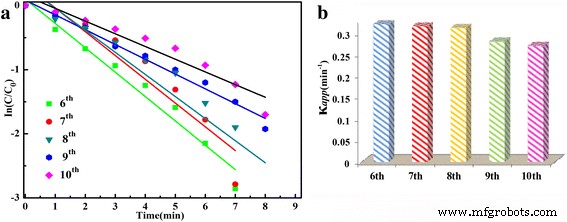
一 , b ln(C t /C 0) 对 36 小时样品的第六至第十次循环的反应时间
此外,在 ESI 中显示了催化剂在五次循环和十次催化还原循环前后的 FTIR 光谱。如附加文件1:图S7所示,经过5次和10次催化还原循环后,样品的主峰与制备的样品几乎相同,这说明催化剂非常稳定。
为了将我们的结果与文献中的其他催化剂进行比较,我们通过标准化 κ 来评估 Ag 修饰的 SnO2 的催化能力 κ 的应用值 也不是 [45, 46]。归一化速率常数κ 也不是 (κ nor =κ 应用程序/c 猫,其中 c cat 是催化剂的浓度)是估计催化活性的关键指标。归一化速率常数κ 也没有计算为 6.20、0.64 和 0.54 min -1 g −1 SnO2/Ag 微球的第一个循环、第五个循环和第十个循环的 L 分别反应了 36 小时。 κ的比较 SnO2/Ag (36 h) 和文献中的其他催化剂也见表 2。从表 2 中可以明显看出归一化表观速率常数 κ 本工作中的样品也远高于文献报道的一些催化剂[47,48,49,50,51,52,53,54,55,56,57,58],如核壳银@Pt (0.92 min −1 g −1 L), AgNPs/GR-G3.0PAMAM (0.78 min −1 g −1 L), rGO/Fe3O4/Au (0.52 min −1 g −1 L)。此外,对于第五个和第十个循环,计算的 κ 也 (0.64 和 0.54 min −1 g −1 L) 甚至高于这些催化剂 [51,52,53,54,55,56,57,58]。这些结果表明所制备的SnO2/Ag微球可作为一种潜在的4-NP还原催化剂。
<图>基于以往的研究结果和贵金属催化还原 p-NP 的传统理论,推测了分级 Ag 修饰的 SnO2 微球的形成机理和优异催化效率的来源,示意图如图 1 和图 5 所示。 9 和 10。在简便的一锅水热法中,Ag 和 SnO2 NPs 在溶液中同时形成,新生成的表面倾向于相互结合。随着水热时间的增加,SnO2 纳米粒子组装成纳米片[59],Ag 纳米粒子分散在微球中。在催化还原过程中,Ag 纳米粒子通过传递来自供体 BH4 − 的电子开始催化还原 到样品吸附位点上的受体 4-NP,这被 SnO2 和 Ag NP 之间的紧密结合加速。此外,由于空间位阻效应,分散在微球中的Ag NPs可以避免催化反应过程中的团聚。此外,Ag NPs 和 SnO2 纳米片的协同作用共同促成了 Ag 修饰的 SnO2 复合材料的优异催化活性。为了验证这一假设,在不添加 AgNO3 和 Na2SnO3 的情况下,分别通过类似的程序合成了纯 SnO2 和 Ag NPs,然后用于催化还原 4-NP。随时间变化的紫外-可见光谱和 ln(C t /C 0) SnO2 和 Ag NPs 与时间的关系显示在附加文件 1 中:图 S8 和图 S9。可以观察到,还原也遵循一级反应规律。速率常数 (κ app) 发现从线性区域的斜率计算的值为 1.24 min -1 , 和 1.16 分钟 −1 对于 SnO2 和 Ag,低于 SnO2/Ag。因此,SnO2/Ag 的优异催化活性可能源于 Ag 纳米颗粒和 SnO2 纳米片之间的协同作用。但具体机制有待进一步探索。
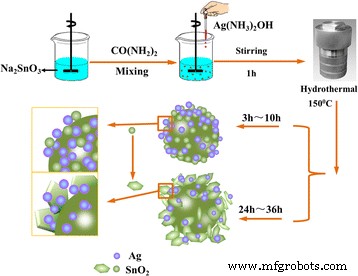
Ag修饰SnO2微球的合成示意图
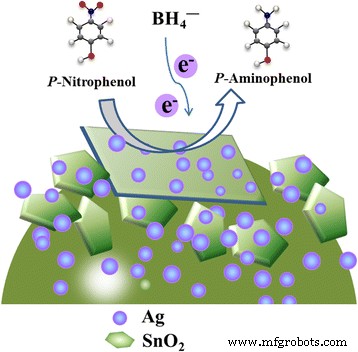
Ag修饰的SnO2微球上4-NP催化还原为4-AP的示意图
结论
总之,通过简便的一锅法成功制备了具有均匀 Ag 纳米粒子和 SnO2 纳米片的分级 Ag 修饰的 SnO2 微球。通过这种简单而有效的方法制备的催化剂在用κ将4-NP还原为4-AP方面表现出优异的催化性能 也不是 6.20 分钟 −1 g −1 L. 此外,该催化剂在前五次循环后仍能保持较高的催化性能,有望成为还原 4-NP 的高效催化剂。此外,我们相信该方法可作为制备其他金属颗粒改性半导体复合材料的新策略。
纳米材料
- 用于合成和生物医学应用的荧光纳米材料的进展和挑战
- 用于细胞内蛋白质递送的二氧化硅纳米颗粒:一种使用绿色荧光蛋白的新型合成方法
- 基于三苯基膦的功能性多孔聚合物作为一种高效的多相催化剂,用于从 CO2 合成环状碳酸酯
- 用于最大太阳能收集的高效且有效的 InP 纳米线设计
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- Cu2ZnSnSe4 纳米片的一锅法合成及其可见光驱动的光催化活性
- 铜纳米粒子合成和稳定方面的环保能力:催化、抗菌、细胞毒性和抗氧化活性
- 桔梗皂苷(桔梗)用于金和银纳米颗粒的绿色合成
- 掺杂 Sb2O3 纳米晶体:一种用于有机降解的高效可见光催化剂
- 支持直接甲醇燃料电池的新型阳极催化剂:表征和单电池性能
- 分层多孔 Silicalite-1 封装的 Ag NP 的制备及其对 4-硝基苯酚还原的催化性能
- 金属和金属氧化物纳米粒子的绿色合成及其对单细胞藻类莱茵衣藻的影响


