Fe3O4@C 混合纳米粒子的水热合成和磁性吸附性能以去除水溶液中的重金属离子
摘要
具有高比表面积的先进核壳材料被认为是去除水溶液中重金属的有效材料。在研究中,核壳 Fe3O4@C 杂化纳米颗粒聚集在一起,具有环保通道。此外,更高的Brunauer-Emmet-Teller (BET)表面积达到238.18 m 2 的特殊配置可以实现更高的吸附位点暴露 g −1 .因此,获得了更有效的重金属离子去除效果,Pb (II)、Cd (II)、Cu (II) 和 Cr (VI) 分别高达 100、99.2、96.6 和 94.8%。此外,由于亚微米尺寸相对较大,铁基核引入的外部磁场增强,吸附后的产物很容易从水溶液中分离出来。我们提供了一种在水处理条件下使用核壳 Fe3O4@C 去除重金属离子的理想模式。阐明了一种新的途径,可以很好地大规模合成核壳纳米/微功能材料,用于环境修复、催化剂和能源等多个领域。
背景
随着环保的呼声不断高涨,其毒性作用也越来越受到重视,即重金属污染对人体健康和环境造成的污染[1,2,3]。在排放之前从工业废水中去除重金属元素变得至关重要 [4]。迄今为止,在过去的几十年中,离子交换、混凝沉淀等一系列传统技术被应用于去除废水中的重金属[5, 6]。认识到传统技术为人类创造了显着的好处,但它也暴露了管理和技术方面的缺点,即昂贵的运行成本、额外的有毒污泥产生和金属去除不完全 [7,8,9]。另一方面,控制粒径、吸附材料的形态已被证明是克服这些问题的有效和创新的解决方案之一。参考文献[10,11,12,13]中空心球、纳米线和纳米管具有更好的吸附性能,有助于去除重金属。此外,研究集中在具有核-空-壳特征的核-壳结构的新材料上。与相同尺寸的固体对应物相比,它的优点得到了证明,例如在表面积、折射率、较低的密度和容纳体积的变化方面的有效性,这在两个方面都有很大的贡献。属性和功能 [14, 15]。因此,这种具有可调节形状、组成和内部结构的独特结构是追求环境修复的一个令人兴奋的方向。
许多文献都涉及核壳结构材料。郭 [16] 制作了笼罩型 Ag@TiO2 材料,该研究表现出更好的光催化和电化学性能。 Liu [17] 制备了核壳型 Fe3O4 聚多巴胺纳米粒子,在药物载体、催化剂载体和碳吸附剂领域表现出良好的潜力。据我们所知,所需壳的可移除或牺牲模板(例如,聚合物二氧化硅 [18]、球体 [19]、碳 [20] 和离子液体 [21])的帮助在核的一般合成中很重要。壳杂化纳米颗粒结构。然而,最可用的核壳结构材料是通过多模板工艺合成的,主要集中在相对简单的配置上,例如单壳颗粒中的一种组合。此外,还缺乏具有通用方法的重金属离子去除方法,进一步加强具有核壳结构的先进材料的制备可行性,包括受合成模板限制的复杂纳米结构的构建过程中的时间和成本和多模板路线,无论是从技术还是生态效益上都成为人们的愿望。
磁性功能纳米复合材料的合成是解决吸附剂与溶液分离的有效且简便的方法,以扩大磁分离[22]。在这个过程中,越来越多的共价固定聚合物、新型分子和无机材料被放入磁性纳米粒子的表面;它们也是有毒重金属离子废水处理的有用技术路线 [23]。例如,报道了新型合成的壳聚糖改性磁性纳米复合材料 [24] 和单分散 Fe3O4@二氧化硅核壳结构复合磁性纳米颗粒核壳微球 [25]。尽管这些磁性纳米复合材料通过基于外磁的吸附过程很容易从溶液中分离出来,但仍需要进一步考虑强酸性废水的适用性等特殊条件。
最近有很多关于碳基纳米结构材料的研究。 Wildgoose [26] 提出这些材料在成本、耐碱腐蚀、比表面积和吸附能力方面具有明显的优势。 Uchida [27] 指出羧基官能团很容易在碳表面生成,从而进一步增强对重金属离子的吸附能力。然而,由于碳颗粒尺寸小导致难以从溶液中去除它们的致命缺陷限制了其在重金属废水处理中的应用。考虑到碳包覆磁性纳米颗粒是废水处理中的一种介质,它在外部磁场中对吸附能力和分离性能产生了先进的影响。更多的关注增加了 [28,29,30,31,32,33,34,35]。张[36]制备了磁性空心碳纳米球,用于铬离子去除。为了去除重金属,Wang 小组 [37] 报道了 Fe 纳米颗粒材料的案例研究。这些先前的研究表明,相应的未来工作必须涉及高效的重金属离子吸附剂,易于分离和吸附容量大。同时需要指出的是,目前关于核壳Fe3O4@C杂化纳米粒子聚集体的研究还很少。
在这项研究中,我们制备了具有磁芯的碳微球。此外,还提出了一种简洁的策略来合成核壳 Fe3O4@C 杂化纳米粒子聚集体,这是一种具有强度纯度、表面积和吸附能力的先进重金属离子去除材料。与传统的Fe3O4材料生产工艺相比,优势明显。它不仅表现出更大的表面积和稳定的构型,而且还表现出不受产品形态影响的去除模板。我们的研究提供了更高程度的活性位点 [38, 39]。当引入外部磁场时,吸附剂可以很容易地分离,这是由铁基纳米粒子引起的 [40, 41]。因此,所获得的核壳Fe3O4@C杂化纳米粒子聚集体对重金属离子表现出优异的吸附能力,且路线环保、量产、成本效益高。
实验
材料与合成
核壳 Fe3O4 杂化纳米粒子聚集体的合成
在典型的合成步骤中,将 0.72 g Fe(NO3)3·9H2O、0.0086 g NH4H2PO4、0.008 g Na2SO4·10H2O 和 3 g 葡萄糖分别溶解在蒸馏水中,混合在一起,体积为 90 mL,添加向混合物中加入蒸馏水,并用基本磁力搅拌器连续混合 10 分钟。然后,将混合物转移到 100 mL 内衬聚四氟乙烯的不锈钢高压釜中,温度为 180 °C,48 小时。反应完毕自然冷却至室温后,取黑脚,用去离子水和无水乙醇洗涤数次,然后在真空条件下65℃干燥一整夜,最后得到前体通过在 450°C 下以 3°C min -1 的速率煅烧 然后用连续的一氧化碳/氩气流保持加热(4 小时)并冷却至环境温度。得到 Fe3O4@C 样品。如方案 1 所述,Fe 3+ 的水解 导致纳米级精度的氧化铁层。同时,蔗糖被碳化。之后,Fe-C-O复合材料微球将在浴加热反应过程中通过煅烧部分原位产生,然后获得核壳Fe3O4@C杂化纳米颗粒。
<图片>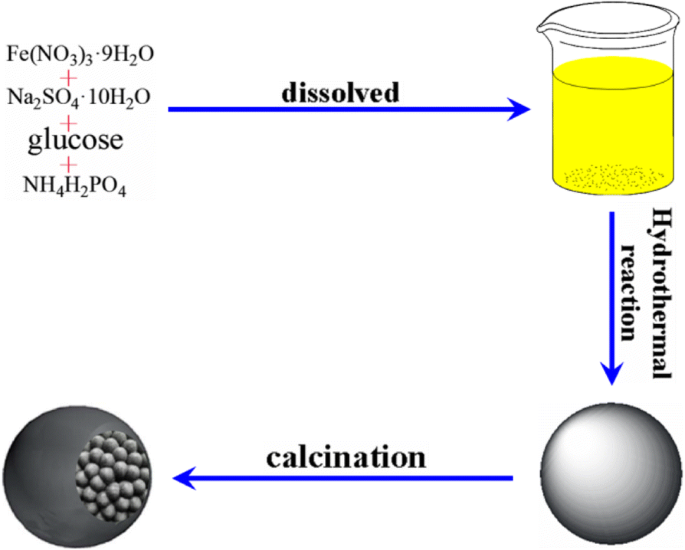
核壳Fe3O4@C杂化纳米粒子的合成路线
特征化
通过X射线衍射(XRD)分析制备材料的相组成,在2θ =20°–90°,由 Rigaku D/max-A 衍射仪测得,Co Kα 辐射。 FTIR(傅里叶变换红外光谱,Thermo Nicolet AVATARFTIR 360)用于记录样品在 400-4000 cm -1 范围内的 FTIR 特征 以及。使用 AMRAY 1000B SEM(扫描电子显微镜)、HR-TEM(高分辨率透射电子显微镜,JEOL JEM-2100)(200 Kv)和选区电子衍射(SAED)来描述样品的形态、微观结构特征、和晶格结构。此外,采用Micromeritics Tristar装置在350.15°C下测量氮吸附和解吸过程; Brunauer-Emmet-Teller (BET) 用于讨论比表面积;原子吸收光谱(AAS)定量分析将由日立Z2000分光光度计实现,该分光光度计配备空心阴极灯和乙炔-空气火焰。用振动样品磁强计(VSM)测量制备材料的磁性能。
重金属离子去除实验
在室温下,进行一系列实验被认为是去除重金属离子。首先在四个密闭容器中加入Pb(II)、Cd(II)、Cu(II)和Cr(VI);之后,使用0.1 M HCl和0.1 M NH3•H2O调节pH至3,然后得到终体积为50 mL、浓度为10 mg L -1 的吸附溶液 获得了。随后,在连续搅拌条件下,将 20 mg 制备的 Fe3O4@C 样品加入上述溶液中。在吸附反应过程中,几乎 1.0 mL 每种上述溶液在不同时间段(分别为 0、0.5、1、1.5、2、4、6、10 和 24 小时)通过针管使用浸出,配备膜过滤器,最终衰减用于AAS测量。
结果与讨论
核壳Fe3O4@C纳米球的理化特性
合成的核壳 Fe3O4@C 杂化纳米粒子聚集体及其前驱体的 XRD 谱如图 1 所示,明显表明该生产工艺在 450°C 下煅烧具有比前驱体更高的结晶度。制备的样品显示出对应于面心立方 (f c c) Fe3O4 的复合材料(JCPDS(粉末衍射标准联合委员会)卡片编号 75-0033)。图中21.5°的衍射峰应归属于石墨碳的(002)面,SEM和TEM也可直接发现。
<图片>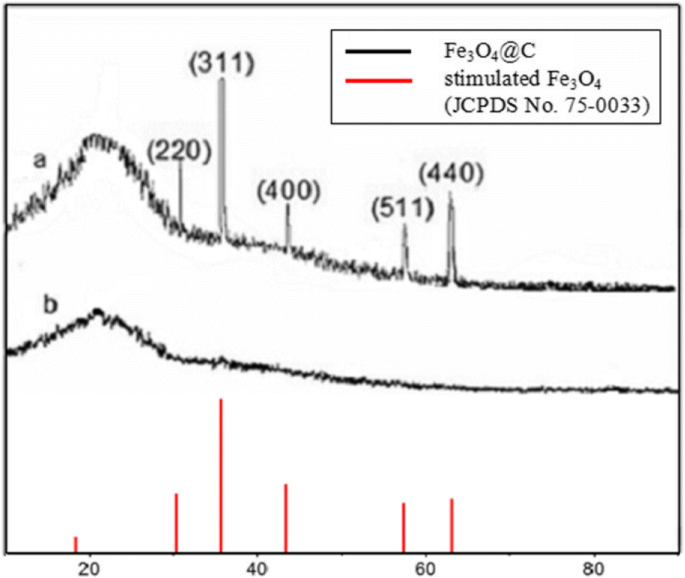
核壳Fe3O4@C杂化纳米粒子聚集体及其前驱体的XRD图谱(a—Fe3O4@C杂化纳米粒子聚集体;b—前驱体)
前体和核壳 Fe3O4@C 杂化纳米颗粒合成的 SEM 图像在 450°C 下以不同放大倍数煅烧产生,如图 2a-c 所示。显然,除了尺寸略小之外,合成的 Fe3O4@C 保留了制备的前体的形态,即大约为微球。大小均匀为 700 nm。图 2b、c 清楚地描述了 Fe3O4@C 的混合核壳结构;中间层可以证明这一点。图 2c 还显示了合成的粉末是由纳米尺寸的颗粒制成的,这是基于部分颗粒壳部分破裂的结果。上述裂隙微球可能来自于通过壳的快速传质。图 2d、e 还描述了 Fe3O4@C 的结构。图 2d 中可见核壳内部结构,说明 Fe3O4 纳米颗粒明显分布在无定形碳中。这与SEM结果一致。另一方面,HRTEM(图 2e)和 XRD 也有很好的一致性,这表明晶格间距(0.297 nm)与面心立方 Fe3O4 的(220)面间距一致。其 SAED 结果表明 Fe3O4 纳米颗粒是高度结晶的单晶。因此,独特的混合核壳样品可能对目标吸附物具有更高的吸附位点响应效率,可用于环境保护领域。
<图片>
制备的前驱体 (a )。 SEM 图像 (b , c ), TEM 图像 (d ), HRTEM 显微照片 (e ) 和选区电子衍射 (f ) 合成的核壳型 Fe3O4@C 杂化纳米颗粒聚集体在 450 °C 下煅烧
使用 VSM 评估制备的磁性能,结果如图 3 所示。与裸 Fe3O4 微球 (67.55emu/g) 相比,磁饱和值达到 53emu/g。可以清楚地看出制备的材料的高磁化值。图 3 中的插图显示当施加外部磁场时,颗粒被磁铁吸引,使水溶液清澈透明。
<图片>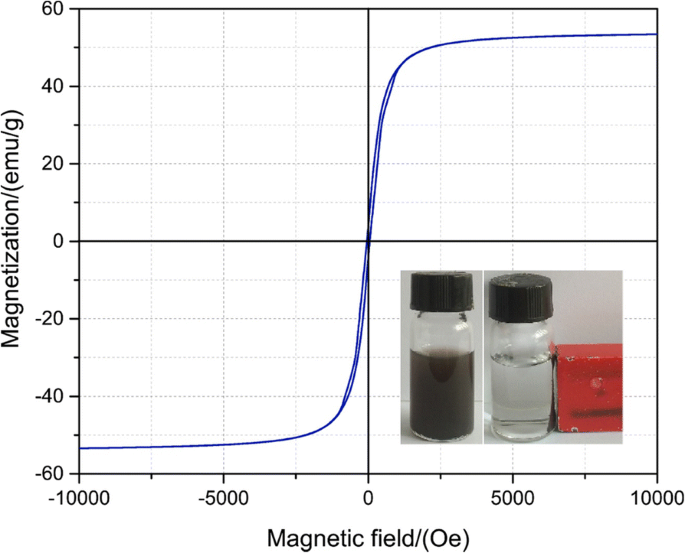
磁化回路测量
图 4a 显示了样品的吸附和解吸等温线,而图 4b 显示了所得样品的孔径分布,它们分别来自煅烧前后。等温线是基于经典IV型的介孔材料的代表性等温线。通过煅烧的孔径分布清楚地显示了 7.5 到 9.1 nm 的平均孔径,小于前体。同时,样品的 BET 表面积在煅烧后从 9.74 显着增加到 238.18,高于大多数报告 [36, 37]。上述结果也表明,被弃置的 Fe3O4@C 样品是一种松散的介孔结构材料,有利于提高吸附性能。
<图片>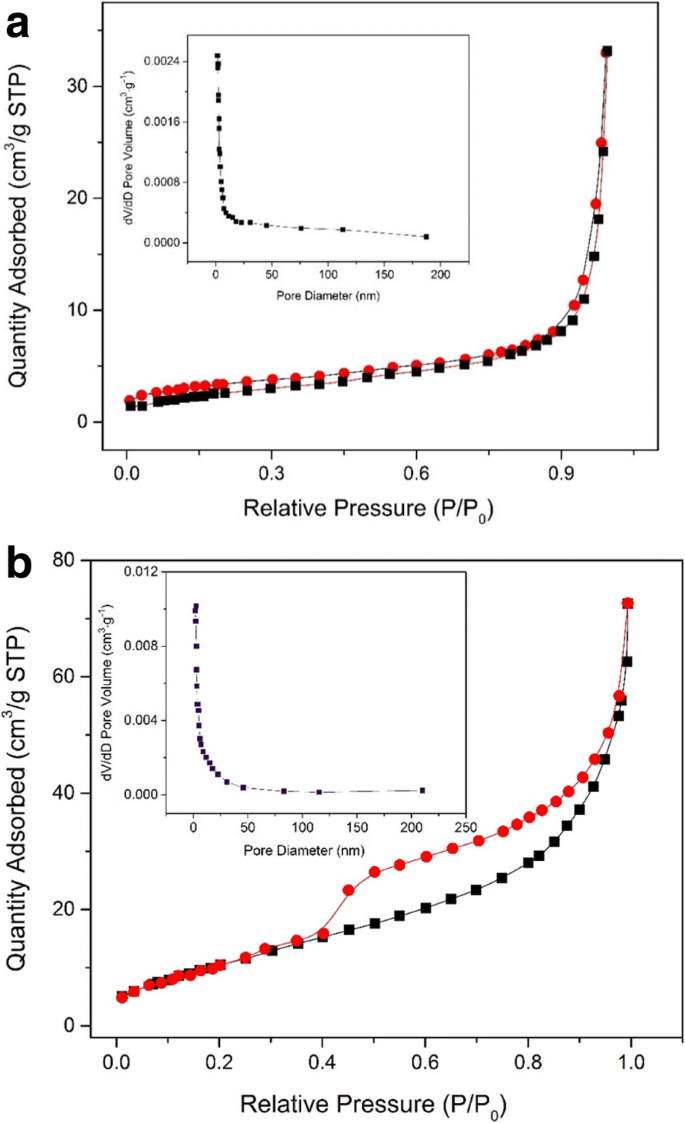
(a之前制备的样品的氮吸附-解吸等温线和Barrett-Joyner-Halenda (BJH)孔径分布图(插图) ) 和之后 (b ) 煅烧
Fe3O4@C 对重金属离子的吸收
选择 Pb (II)、Cd (II)、Cu (II) 和 Cr (VI) 作为吸附质研究制备的 Fe3O4@C 的吸附能力,并将它们置于室温下 pH =3 进行动力学实验。如图 5 所示,制备的样品成功吸附了所有吸附离子,Pb (II) 的效率达到了 100%,Cd (II) 的效率达到了 99.2%,Cu(II) 的效率达到了 96.6%,Cu(II) 的效率达到了 94.8%。 Cr (VI),分别。与之前的研究[42]相比,它具有更广泛的应用和更高的去除效率。这种高吸收效率可归因于具有高比表面积的核壳混合结构的内在优势,这为 Fe3O4@C 样品提供了更多活性位点用于去除过程。此外,由于相对较大的亚微米颗粒结构,吸附后很容易回收。还可以很容易地看出,由于通常通过离子交换进行吸附,Pb(II)表现出最高的速率是合理的,并且游离金属离子与吸附剂表面存在静电相互作用。因此,Cd、Cu、Cr离子交换后轻而易解吸,Pb(II)则相反[43,44,45,46,47,48,49]。
<图片>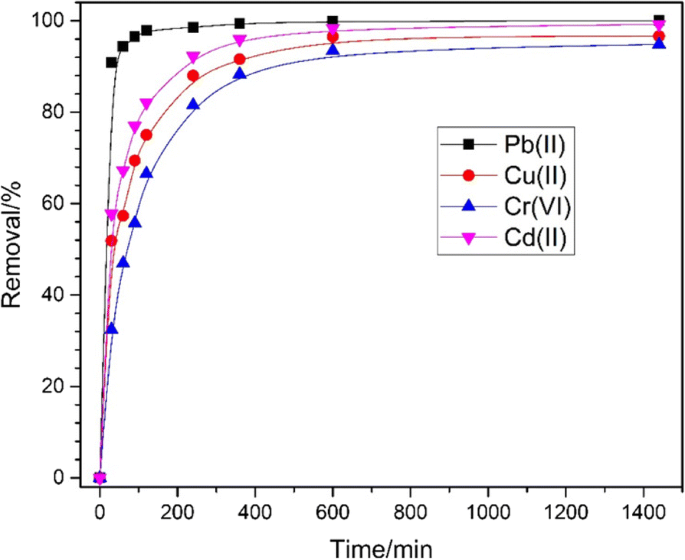
Fe3O4@C (400 mg L −1 ) 吸附 Pb (II)、Cd (II)、Cu (II) 和 Cr (VI) 的去除效率与时间的关系 ) 重金属离子初始浓度为 10 mg L −1 的样品 , 分别
载有 Fe3O4@C 的重金属的 FTIR 光谱
图 6 显示了具有最高 Pb 2+ 的样品 吸附开始和结束时的吸收,用于研究发现 Fe3O4@C 与重金属离子之间的相互作用。此外,-OH 基团从 H3O + 的前后振动 通过离子交换或物理吸附水分子,导致在 3475.26 cm −1 处的宽振动带 . 2304.20 cm −1 处的峰值 归因于 CO2 的振动范围,而峰值在约。 1625 厘米 −1 通常是由 O-H 曲线引起的。 1605.45 cm −1 处的峰值 来自羧基(-C=O-)。 400-1000 cm范围内其他峰的主要贡献 − 1 通常与 O 金属键相关。 Pb 2+ 吸附开始和结束时金属O峰位置和强度的差异 暗示 Pb 2+ 强烈负载在 Fe3O4@C 样品上。
<图片>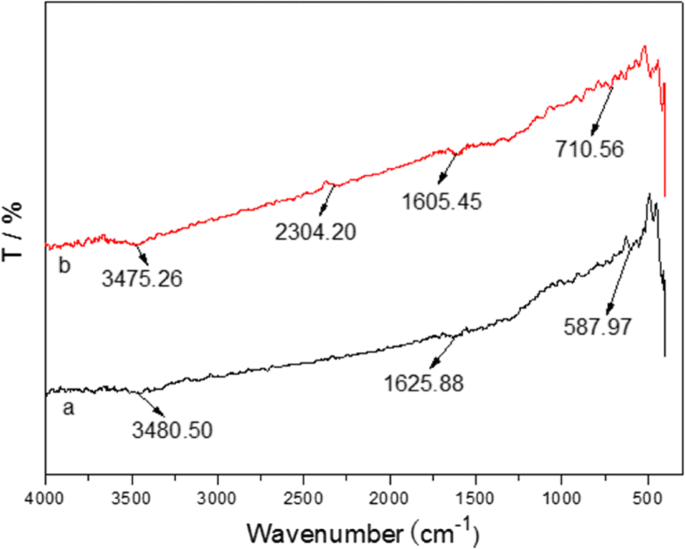
之前制备的 Fe3O4@C 样品的 FTIR 光谱 (a ) 和之后 (b )吸附Pb(II)
吸附动力学
在本节中进行了各种文本来讨论 Fe3O4@C 杂化纳米颗粒聚集体的吸附能力和动力学。铅 2+ 制备用于从 pH =3 的水溶液中去除实验。之后,制备体积为 50 mL 的 10、30 和 50 mg L -1 初始溶液,20 毫克吸附剂,添加到 Pb 2+ 100 mL 锥形瓶中的溶液分别在 30 °C 下吸附。随着不同时间段(0、7、14、21、28、35、60、180、480 和 1440 分钟),从每种溶液中提取约 1 mL,将用于 AAS 分析。等式(1) 显示了准二级动力学速率模型[50]:
$$ \frac{t}{q_t}=\frac{1}{k_2{q}_e^2}+\frac{1}{q_e}t $$ (1)其中 q e 是 Pb 2+ 当吸附剂处于平衡状态时每单位质量的吸附量,q t (mg g −1 ) 表示 Pb 2+ 在 t 时间内吸附在单位质量上 (分钟); k 2 (g mg −1 min −1 ) 是动力学模型的速率常数,它是伪二级。图 7a 显示了 Fe3O4@C 样品在 Pb 2+ 中的反应时间 在不同的初始浓度(10、30 和 50 毫克 L -1 ),那么很容易找出效率差异。结果表明,Fe3O4@C 样品表现出更高的吸附性能,并且易于分离。图 7b 描述了不同浓度 Pb 2+ 下的吸附率 (10、30 和 50 毫克 L −1 )。吸附率与初始浓度呈负相关。这种趋势可以揭示如下,在吸附过程中只有部分表面活性位点被使用。即随着Pb 2+ 的浓度 增加,吸附首先从高能量位点开始,然后是低能量位点饱和,最终导致吸附率下降[51]。表 1 显示了相关系数 (R 2 ) 在本研究中达到 0.999;清楚地表明吸附过程符合伪二级模型。
<图片>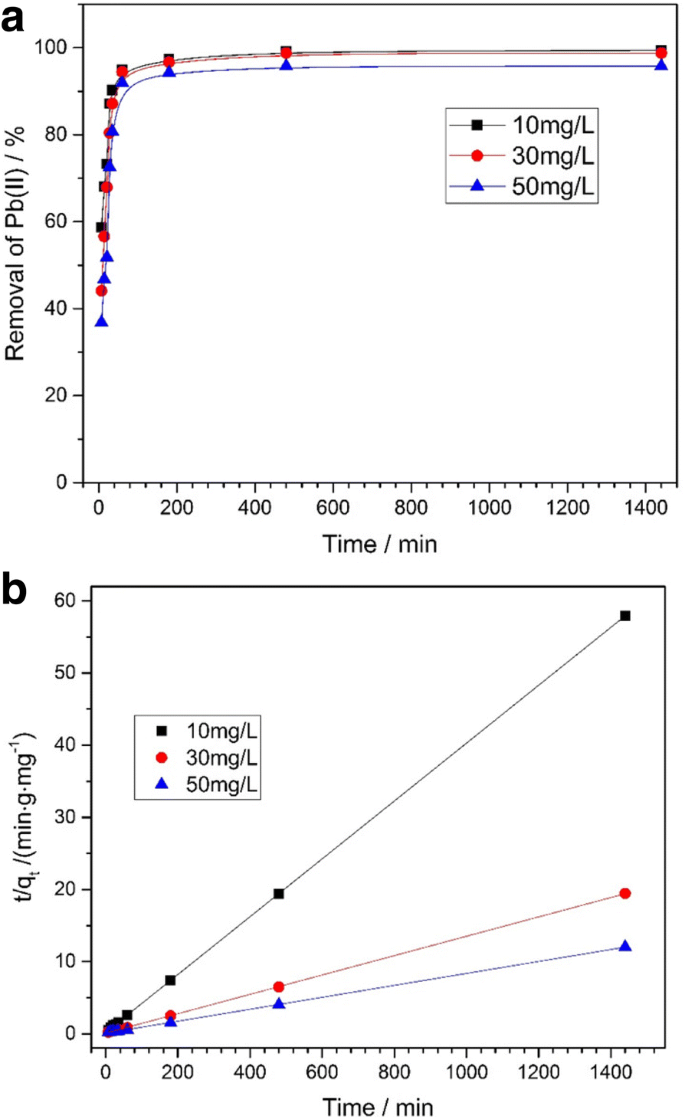
一 在初始 Pb2+ 浓度为 10、30 和 50 mg L -1 时,Fe3O4@C(20 mg)吸附 Pb(II) 的效率与时间之间的关系 , 分别。 b Fe3O4@C 样品 (T) 上吸附 Pb2+ 的伪二级动力学 =30℃;吸收剂量 =400 毫克 L −1 ; Pb2+ 浓度:a =10 mg L −1 , b =30 mg L −1 , c =50 mg L −1 )
吸附等温线
在这部分中,向 100 mL 锥形瓶中加入 20 mg 吸附剂,Pb 2+ 还制备了溶液样品(10-60 毫克 L -1 , 50 mL, pH =3)。在30°C下,将上述锥形瓶样品保持在密封条件下,置于恒温摇床(24小时,150转/分)中,然后通过离心得到AAS测量的上清液。图 8a 显示了制备的 Fe3O4@C 对 Pb 2+ 的吸附能力 . Langmuir 和 Freundlich 等温线用于解释研究中的吸附过程。该过程发生在局部单层中,吸附分子之间没有相互作用 [52]。此外,吸附物分子的位点是先到先得,同一位点不再吸附。朗缪尔等温线描述如下:
<图片>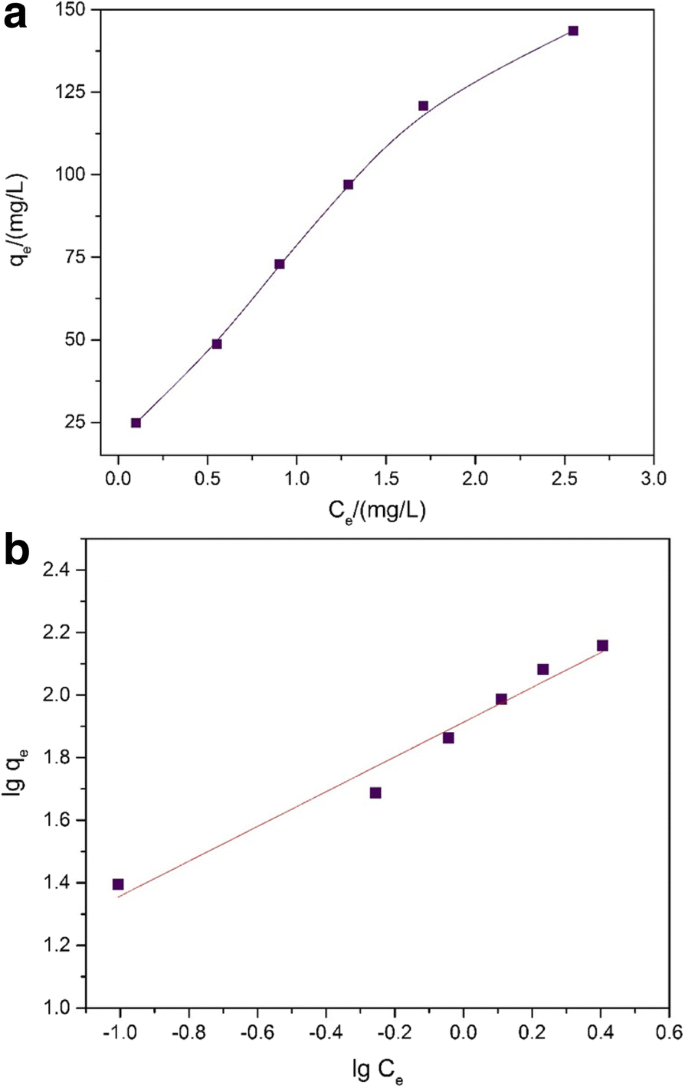
一 Fe3O4@C 样品上 Pb2+ 的吸附等温线 (T =30℃;吸附剂剂量 =400 mg L −1 ; Pb2+ 浓度 =10–60 mg L −1 )。 b Fe3O4@C 样品在 30°C 下去除 Pb2+ 时吸附等温线的 Freundlich 线性图
$$ \frac{C_e}{q_e}=\frac{C_e}{q_{\mathrm{max}}}+\frac{1}{k_L{q}_{\mathrm{max}}} $$ (2 )其中理论最大单层吸附容量表示为 q 最大值 (mg g −1 ),取 k L 表达朗缪尔常数 (L mg −1 ) 和 C e 是最初的 Pb (II) 浓度。然而,朗缪尔等温线没有达到我们研究的理想结果,这意味着它不太合适。对应于方程的线性形式。 (3) 是另一种常见的经验模型,即 Freundlich 等温线,它假设随着位点占有度的升高,更多坚固的结合位点被提前捆绑,其意图相应降低[52]。
$$ \lg {q}_e=\lg {k}_F+\frac{1}{n}\lg {C}_e $$ (3)在这里,k F 表示 Freundlich 常数 (mg g −1 )(L mg −1 ) 1/n , 和 1/n 表示异质性因子。 k的具体内容 F 和 1/n , 用 lg q 的图标识 e 与 lg C e ,如图 8b 所示。表 2 显示了有利的吸附条件 [52、53]。它说明了 Freundlich 指数 n 大于1,可以得出Pb 2+ 的吸附效果 取决于 Fe3O4@C 样品表面的混合核壳结构或异质性。与此同时,R 2 ,样品的相关系数达到0.9712,表明Freundlich等温线模型非常适合实验平衡分析。
热力学分析
将孤立系统作为相关假设,采用阿伦尼乌斯方程(方程(4))进行热力学分析。通常,在恒温摇床的某些特殊条件下,原始浓度为 30 mg L -1 吸附体积为50毫升,然后将20毫克吸附剂放入容量为100毫升的锥形瓶中,并加入Pb 2+ 在五种分类温度条件下的溶液,包括 30、40、50、60 和 70°C。在吸附过程中,水样经过不同时间段采样;在此期间,Pb 2+ 也将基于 AAS 进行测量,该 AAS 用于根据上述不同温度情况分析其吸附动力学。此外,利用前面给出的Arrhenius方程来评估活化能,这是吸附研究的前提。
$$ \ln {k}_2=1n\kern0.5em A-\frac{E_a}{RT} $$ (4)在这里,E 一 是阿伦尼乌斯活化能 (kJ mol −1 )。 A 代表阿累尼乌斯的因数;气体常数 (8.314 J mol −1 K −1 ) 用 R 表示 , 和 T 指绝对温度 (K)。对应的斜率是-Ea /R , 基于 lnk 的图 2 对 1/T (图 9)得到直线。
<图片>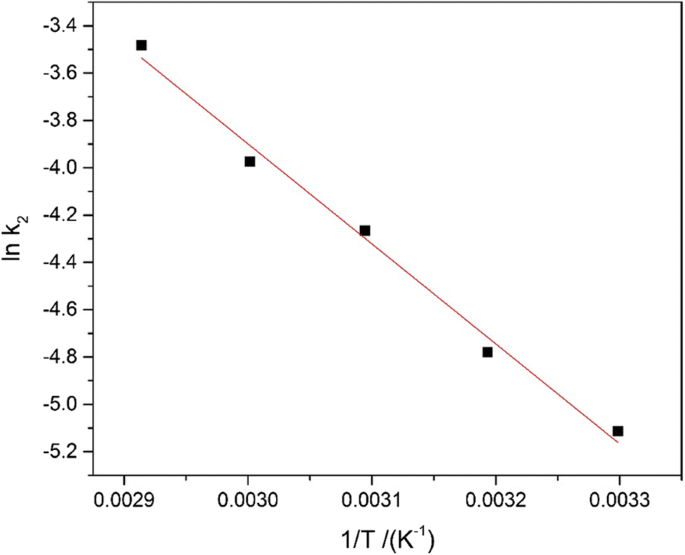
lnk2 与 1/T 的图 Fe3O4@C样品(TOC)上的Pb2+吸附
活化能的维度被用来确定吸附的形式。通常具有特定的范围 (0–40 kJ mol −1 ) 对于物理吸附过程中的活化能 [54],相比之下,化学吸附过程需要更长的范围。活化能为 34.92 kJ mol -1 这里。表明Pb 2+ 的吸附过程 Fe3O4@C上的吸附分为物理吸附。
结论
核壳Fe3O4@C杂化纳米粒子聚集体的复合是基于溶剂热合成法,采用和平温和的环保步骤实现的,最终在450°C下煅烧获得。通过碳基混合核壳纳米结构,与固体相比,吸附质可以有效地实现更高程度的吸附位点暴露效率,这将提供更好的吸附性能以消除重金属离子。此外,铁基芯使吸附剂很容易从水溶液中分离出来。在该装置(更便宜、更少复杂性和更高生产率)下,阐明了一种新方法,可以很好地大规模合成核-壳纳米/微功能材料,用于环境修复、催化剂、和能源。
缩写
- AAS:
-
原子吸收光谱
- 赌注:
-
布鲁诺尔-埃米特-特勒
- FTIR:
-
傅里叶变换红外光谱
- HR-TEM:
-
高分辨透射电子显微镜
- JCPDS:
-
粉末衍射标准联合委员会
- SAED:
-
选区电子衍射
- SEM:
-
扫描电子显微镜
- TEM:
-
透射电子显微镜
- VSM:
-
振动样品磁力计
- XRD:
-
X射线衍射
纳米材料
- Vodcast:OEE 和实时绩效管理
- 使用来自轧制废料的磁铁矿纳米吸附剂从水溶液中吸附去除铜 (II) 离子:合成、表征、吸附和动力学建模研究
- 通过溶胶-凝胶工艺制备的纳米结构二氧化硅/金-纤维素-键合氨基-POSS 混合复合材料
- 使用铁改性生物炭纳米复合材料研究重金属离子吸附
- 通过激光脉冲和溅射技术合成导电二氧化硅纳米纤维/金纳米粒子复合材料
- 接触非平衡等离子体对 Mn Х Fe3 − X О4 尖晶石结构和磁性能的影响
- 水热合成 In2O3 纳米颗粒混合孪晶六边形圆盘 ZnO 异质结构以提高光催化活性和稳定性
- 二氧化硅气凝胶负载的水锌矿和碳酸盐插层水滑石通过沉淀转化反应高效去除 Pb(II) 离子
- 钯(II)离子印迹聚合物纳米球的制备及其从水溶液中去除钯(II)
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- 改性 BiOCl 的合成和表征及其在从水溶液中吸附低浓度染料中的应用
- 使用声悬浮快速合成 Pt 纳米晶体和 Pt/微孔 La2O3 材料


