纳米硫化铜的制备及其对 17α-乙炔雌二醇的吸附性能
摘要
在目前的工作中,通过水热法成功合成了管状纳米硫化铜。通过XRD、SEM、TEM和BET对制备的材料的物理和化学性质进行了表征。合成的硫化铜用作吸附剂去除 17α-乙炔雌二醇 (EE2) 并表现出优异的吸附性能。在25 ℃下,对50 mL 5 mg/L EE2溶液施加15 mg吸附剂,180 min后达到吸附平衡,吸附率接近90%。此外,在理论计算和实验结果的基础上讨论了吸附过程的动力学、等温吸附和热力学。硫化铜的理论最大吸附容量经计算为147.06 mg/g。研究结果表明,硫化铜是一种稳定高效的吸附剂,具有良好的实际应用前景。
介绍
近年来,随着社会产业的不断发展壮大,人类活动对环境造成了严重污染,全球环境问题日益严重。其中,环境内分泌干扰物(EDCs)主要是持久性有机污染物(POPs),具有生物蓄积性、高毒性、低浓度、潜伏性等特点。它们可以通过食物链直接或间接进入人体,并在生物体内被丰富和扩增[1, 2]。因此,对EDCs治理的研究成为环境领域广泛关注的问题。在众多内分泌干扰物中,生活中广泛使用雌激素和双酚类化合物,其中17α-乙炔雌二醇(EE2)是典型的一种。 EE2 常用于避孕药和激素替代疗法。然而,研究表明,EE2 会给生物和人类带来严重危害,并导致生殖系统疾病、不孕症和癌症等疾病 [3,4,5,6,7].. 因此,如何有效且廉价地去除水中的EE2尤为紧迫。
目前,去除EE2的方法很多,如物理方法(吸附和膜分离)、生物降解方法和化学方法(氧化方法和光催化方法)[8,9,10,11]。在这些方法中,吸附法具有成本低、操作简单、无二次污染等优点,具有广阔的应用前景。迄今为止,研究人员已经使用生物炭、活性炭、碳纳米管、石墨烯和粘土来吸附 EE2 [12,13,14],但整体吸附效果较差且耗时。尹等人。用活性炭吸附水中浓度为100 nmol/L的EE2;当活性炭用量为9 mg/L时,EE2完全吸附需要24 h[8]。
硫化铜是一种重要的过渡金属硫化物,极难溶于水,是最难溶的物质之一[15, 16]。纳米硫化铜具有成本低、步骤简单、形貌易控制、粒径小、比表面积大、光热转化率高等优点,被广泛用作光电导材料。它还在光催化剂、热电偶、过滤器、太阳能电池和生物医学中具有潜在的应用[17]。在碱性环境下,硫化铜的等电点(IEP)大,其表面易带正电荷[18,19,20],而EE2结构中存在酚羟基[21],在水溶液中呈弱酸性,表面带负电荷,使它们之间有很强的化学吸附作用。因此,硫化铜有可能吸附EE2。
本研究采用水热法合成了管状纳米硫化铜。合成的纳米硫化铜比表面积为16.94 m 2 /g,EE2的最大吸附量为147.06 mg/g。详细研究了制备的纳米硫化铜的晶相组成、形貌和比表面积。通过优化溶液pH值、吸附剂用量、吸附时间、吸附温度和EE2初始浓度,研究了硫化铜对EE2的吸附性能。并通过实验数据研究了硫化铜在EE2上的动力学吸附、等温吸附和热力学吸附。
材料和方法
硫化铜吸附剂的合成
所有化学试剂均为分析纯,无需进一步纯化即可使用。采用水热法合成了管状纳米硫化铜。在典型的程序中,将 4.8 mmol CuCl2·2H2O 和 4.8 mmol CH3CSNH2 溶解在 40 mL 去离子水中并磁力搅拌直至形成澄清溶液。然后,将20 mL 0.4-mol/L NaOH水溶液缓慢加入上述溶液中。搅拌5 分钟后,将混合溶液转移到100毫升内衬聚四氟乙烯的不锈钢高压釜中,然后在160 ℃加热6 小时。随后,将高压釜自然冷却至室温。最后将固体产物离心,用乙醇和去离子水交替洗涤3次,然后在60 ℃下干燥6 h即得材料。
特征化
使用 TTRIII X 射线衍射仪(日本理学)在 40 kV 和 200 mA 的 CuKα 辐射下通过 X 射线衍射(XRD)表征材料的晶体结构。通过QUANTA 200扫描电子显微镜(SEM,FEI,USA)在约20 kV和Tecnai-G20透射电子显微镜(TEM,FEI,USA)下研究材料的形貌。利用N2吸附等温线的Brunauer-Emmett-Teller图求得纳米硫化铜的表面积。
吸附测量
吸附实验
在装有50.00 mL一定浓度EE2溶液的碘量瓶中加入一定量的吸附剂。然后,将碘量瓶放入摇床中。在一定温度和200 rpm/min的振荡速度下,将混合溶液振荡一定时间。然后用0.4um混合纤维素滤膜快速过滤溶液,测定溶液中残留EE2的浓度。
EE2浓度采用超高效液相色谱法(UPLC,Waters,USA)检测,检测波长210 nm。使用 C18 色谱柱(1.7 μm,2.1 × 50 mm)和乙腈/水 (55/45 v/v),流速为 0.35 mL/min,进样量为 7 μL。
吸附模型
吸附效率
吸附效率表示吸附剂对EE2的去除率。表达式如下:
$$ \mathrm{吸收}\left(\%\right)=\frac{C_0-{C}_e}{C_0}\times 100\% $$ (1)C 0 和 C e 分别代表EE2的初始浓度(mg/L)和达到吸附平衡时的浓度(mg/L)。
吸附能力
平衡吸附量q e 表示达到吸附平衡时单位质量吸附剂的吸附量,单位为mg/g,计算公式为:
$$ \kern0.5em {q}_e=\frac{\left({C}_0-{C}_e\right)V}{m} $$ (2)V 和 m 分别代表EE2的体积(mL)和吸附剂用量(mg)。
吸附动力学
利用准一级动力学模型和准二级动力学模型对实验数据进行线性拟合,可以对硫化铜对EE2的吸附进行简单的动力学分析。准一级动力学模型[22]方程如下(3):
$$ \ln {q}_e=\ln \left({q}_e-{q}_t\right)+{K}_1t $$ (3)q t 为吸附剂在 t 时刻吸附 EE2 溶液的吸附量 ,单位为 mg/g,K 1为准一级动力学吸附速率常数,单位为min −1 .准二级动力学模型[23]方程如下:
$$ \frac{t}{q_t}=\frac{1}{K_2{q}_e^2}+\frac{1}{q_e}t $$ (4)K 2为准二次吸附速率常数,单位为g/(mg·min)。
等温吸附模型
等温吸附模型通常用于研究吸附过程中吸附剂与被吸附质的相互作用。常见的等温吸附模型有两种:Langmuir模型[24]和Freundlich模型[25]。
Langmuir 模型假设吸附剂表面的吸附位点分布均匀,被吸附物在吸附剂表面形成单分子吸附层。表达公式如下:
$$ \frac{1}{q_e}=\frac{1}{q_m{k}_L}\ \frac{1}{C_e}+\frac{1}{q_m} $$ (5)q 米 表示吸附剂对EE2的最大吸附量(或饱和吸附量),单位为mg/g,k L 为朗缪尔常数,即吸附速率与解吸速率的比值,可反映吸附剂对被吸附质的吸附强度,单位为L/mg。
友好吸附模型是用于研究多层吸附模型的经验公式。其表达式为:
$$ \ln {q}_e=\ln {K}_F+\frac{1}{n}\ln {C}_e $$ (6)K F 是用来表征吸附剂性能的 Freundlich 常数,n 是吸附难度的反映。
吸附热力学
吸附热力学研究是通过研究温度对 EE2 去除的影响进行的,这提供了对吸附过程中内部相关能量变化的更深入的了解(图 1)。吸附过程的热力学描述由三个参数组成:标准吉布斯自由能(ΔG θ ), 标准热力学焓 (ΔH θ ) 和标准热力学熵变 (ΔS θ ) [26]。三者关系如下:
$$ \Delta {G}^{\theta }=\Delta {H}^{\theta }-T\Delta {S}^{\theta } $$ (7)
EE2的化学结构
进一步推导上式可表示为:
$$ \Delta {G}^{\theta }=- RT\ln {K}_C $$ (8)其中 R 是气体常数,值为 8.314 J/(mol K); T 为吸附温度,单位为K;和 K C 是热力学平衡常数。计算公式如下:
$$ {K}_C=\frac{C_0-{C}_e}{C_e} $$ (9)综上所述,我们可以得到汇总公式:
$$ \ln {K}_C=-\frac{\Delta {H}^{\theta }}{RT}+\frac{\Delta {S}^{\theta }}{R} $$ (10)可以通过绘制 lnK 来获得线性函数 C 相对于 − 1/T . ΔH 的值 θ 和 ∆S θ 可以从拟合线的斜率和截距计算。
结果和讨论
特征化
XRD 分析
使用XRD技术研究了材料的化学成分和相结构。如图2所示,硫化铜在2θ处的衍射峰 观测到的值分别为 28、30、32、33、43、53 和 59°,与(101)、(102)、(103)、(006)、(110)、(108)和(116) 硫化铜的晶面 (JCPDS No. 06-0464) [27],分别。实验证明合成了纯相纳米硫化铜;未观察到其他衍射峰,表明该材料纯度高。
<图片>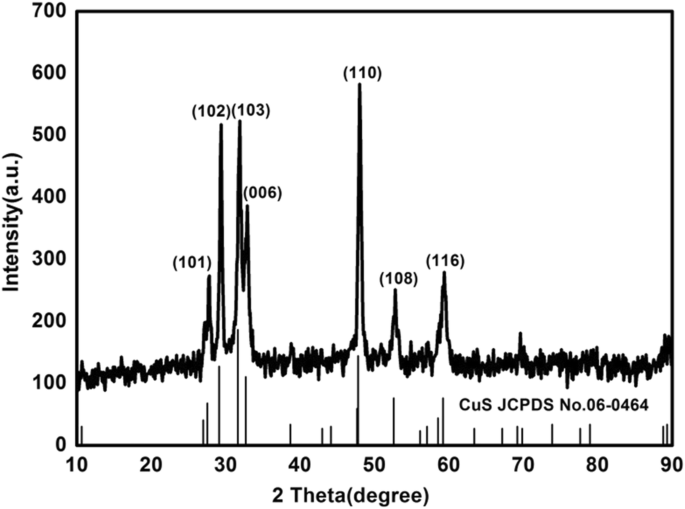
纳米硫化铜的XRD图
SEM 分析
使用扫描电子显微镜(SEM)来研究纳米硫化铜的形貌。图 3a、b 显示了硫化铜在不同放大倍数下的 SEM 图像。图 3a 显示在低放大倍数下,硫化铜具有中空管状结构,长度为 0.4-8.8 μm,宽度为 0.1-0.9 μm。图 3b 显示了在更高放大倍数下硫化铜的微观形态;从图中可以看出,管状结构上有一些颗粒沉积。
<图片>
纳米硫化铜的SEM照片
TEM 分析
图 4 显示了纳米硫化铜的透射电子显微照片。从图 4a 可以看出,管状硫化铜相对均匀,管径为 0.2-0.7 μm。从图 4b、c 中可以明显看出,除了合成管状硫化铜之外,颗粒(球形)硫化铜沉积在管状硫化铜上。这些结果与SEM的结果一致。从 SEM 和 TEM 图像可以知道合成的硫化铜具有管状和颗粒(球形)两种形状。两种形状中,管状硫化铜占主要部分,颗粒状(球状)硫化铜数量较少,但两种形状的硫化铜都吸附了EE2。
<图片>
硫化铜的TEM图像
投注分析
N2吸附-解吸曲线的取向和形状可用于确定材料的孔结构和孔径分布。硫化铜材料的N2吸附-解吸曲线如图5所示,根据Brunauer-Deming-Teller(BDDT)[28]吸附等温线分类,属于IV型等温线;该材料为介孔结构。一般来说,介孔结构的存在可以为活性物质和反应物分子的吸附提供更多的表面活性位点,有利于吸附性能。 BET测试结果表明硫化铜的孔径为18.16 nm,比表面积为16.94 m 2 /g,孔体积为0.083 m 3 /G。这种结构和比表面积有利于吸附 EE2。结合SEM和TEM图像可知,合成的硫化铜具有管状和颗粒(球形)两种形状。因此,硫化铜的两种形状都会影响BET测量。
<图片>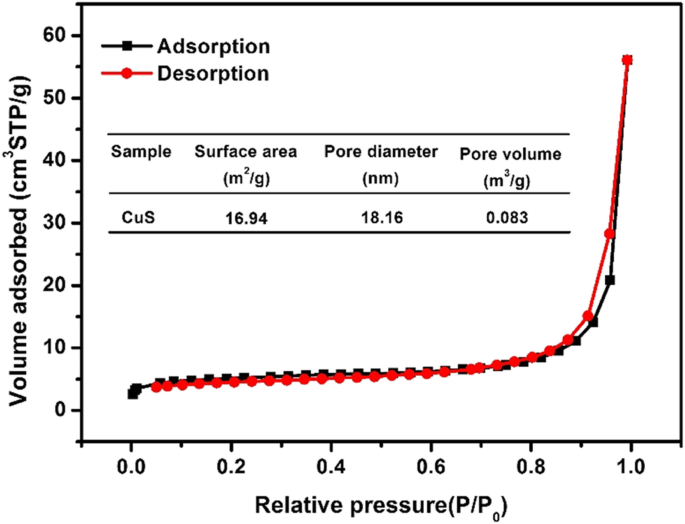
硫化铜的N2吸附-解吸曲线
吸附实验
pH 对吸附的影响
通过用NaOH和HCl调节溶液的pH值,研究了溶液pH值对EE2吸附的影响。 EE2吸附实验在pH值2.0~10.0范围内进行,吸附剂用量10 mg,EE2初始浓度5 mg/L,摇床温度25 ℃,吸附时间3 h。如图 6 所示,pH 从 2 增加到 6,硫化铜对 EE2 的吸附率变化不大,吸附率约为 40-45%。令人惊讶的是,当pH值变为8时,吸附率急剧上升,达到77.1%。
<图片>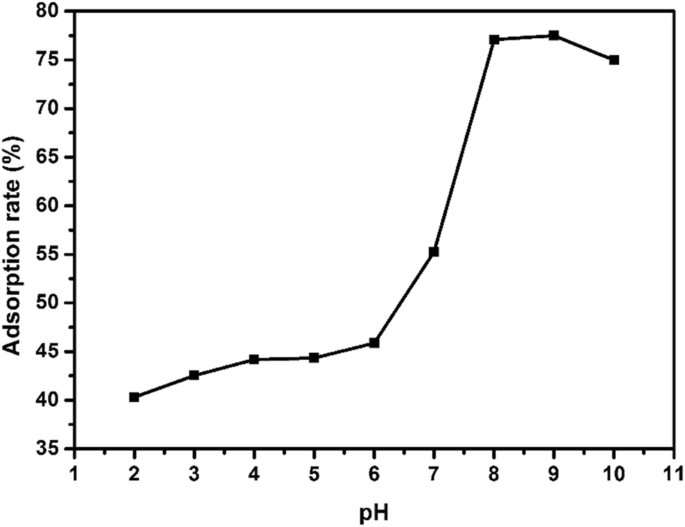
不同pH值对纳米硫化铜吸附EE2的影响
然而,当 pH 值进一步增加到 10 时,吸附率下降到 74.9%。吸附率随pH值变化而不同的一个可能原因是在碱性环境中硫化铜的等电点(IEP)向氢氧化铜的等电点(IEP =9.5)转移[16,17,18];此时硫化铜的等电点(IEP)较大,表面容易带正电荷[18,19,20],而EE2的结构中存在酚羟基[21],在水溶液中呈弱酸性,表面带负电荷,使它们之间有很强的化学吸附作用。当溶液pH值高于9.5时,化学力降低,吸附速率相应降低,与实验数据一致。
根据实验数据,选择pH =8作为后续实验的最佳pH值。
吸附剂用量对吸附的影响
为了研究不同吸附剂剂量对硫化铜吸附EE2的影响,使用不同剂量的硫化铜(5 mg、7.5 mg、10 mg、12.5 mg、15 mg、17.5 mg和20 mg)吸附EE2。 EE2吸附实验在pH =8条件下进行,EE2初始浓度为5 mg/L,吸附温度为25 ℃,吸附时间为3 h。如图 7 所示,随着吸附剂用量从 5 增加到 20 mg,吸附率从 54% 增加到 98%。在低剂量下,由于吸附位点不足,吸附率较低,随着吸附剂量的增加,吸附位点增加,吸附率增加。当吸附量为15 mg时,吸附率接近90%,与吸附剂量为20 mg时的吸附率非常接近。考虑到经济和环境问题,吸附剂的最佳用量选择为15 mg。
<图片>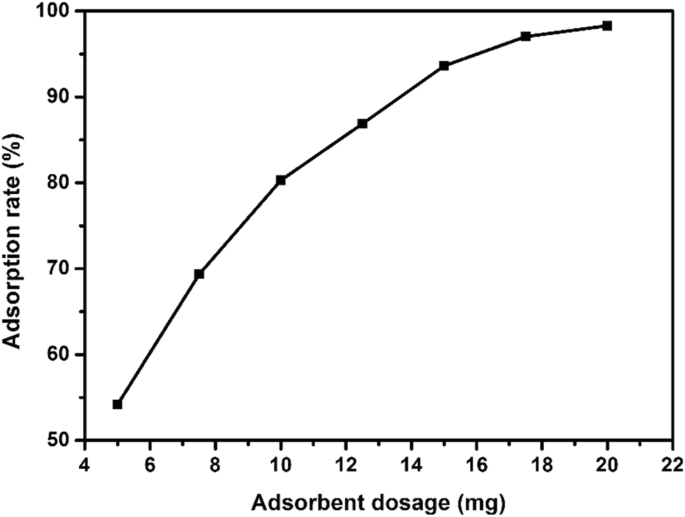
不同硫化铜吸附剂用量对吸附的影响
吸附时间对吸附的影响
为了研究吸附时间对硫化铜吸附EE2速率的影响,振动筛的吸附时间分别为0、10、30、60、90、120、150和180 min。 EE2吸附实验在pH =8条件下进行,吸附剂量为15 mg,EE2初始浓度为5 mg/L,吸附温度为25 ℃。如图 8 所示,吸附 3 h 后,硫化铜对 EE2 的吸附率达到 89%。随着硫化铜与EE2接触时间的增加,吸附去除率增加。
<图片>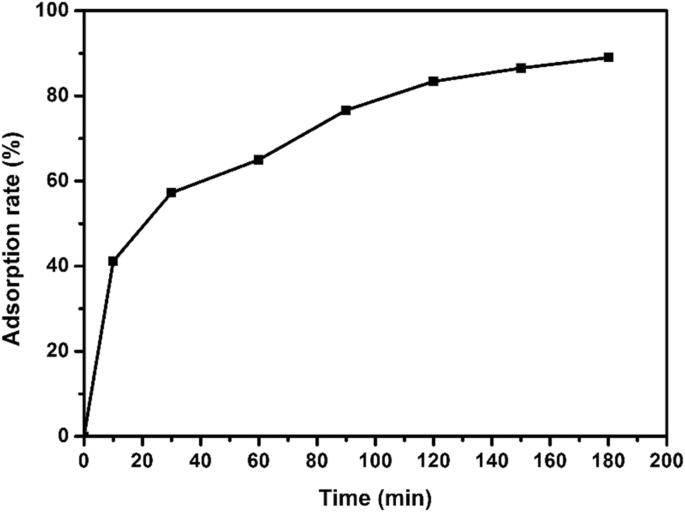
纳米硫化铜对EE2的吸附速率随时间的变化
温度对吸附的影响
为了讨论吸附温度对硫化铜吸附EE2的影响,分别在25 ℃、35 ℃和45 ℃下进行了EE2吸附实验。其他实验条件不变:pH为8,吸附剂量为15 mg,EE2初始浓度为5 mg/L,吸附时间为3 h。从图 9 中可以看出,随着温度从 298 上升到 318 K,吸附率从 68.32% 增加到 97.25%。结果表明该反应为吸热反应。
<图片>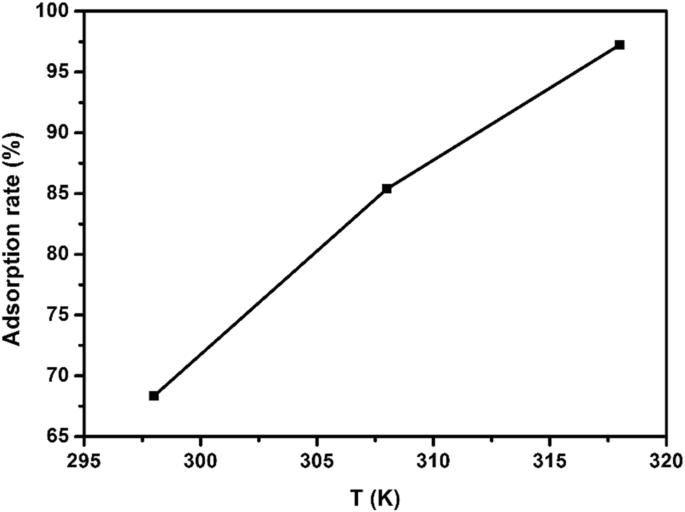
不同温度与吸附速率的关系
EE2 初始浓度对吸附的影响
图10为在吸附剂用量为15 mg、pH =8、25 ℃、吸附时间为3的条件下,不同初始浓度(1、3、5、7、9 mg/L)的EE2与吸附速率的关系图H。从图中可以看出,当EE2的初始浓度为1 mg/L、3 mg/L、5 mg/L、7 mg/L和9 mg/L时,硫化铜对EE2的吸附去除率分别为 100%、100%、89.68%、78.69。 % 和 68.32%。随着EE2初始浓度的增加,硫化铜对EE2的吸附去除率逐渐降低。当EE2的初始浓度高于3 mg/L时,由于催化剂用量有限,EE2的吸附率下降,无法为高浓度的EE2提供足够的活性位点。
<图片>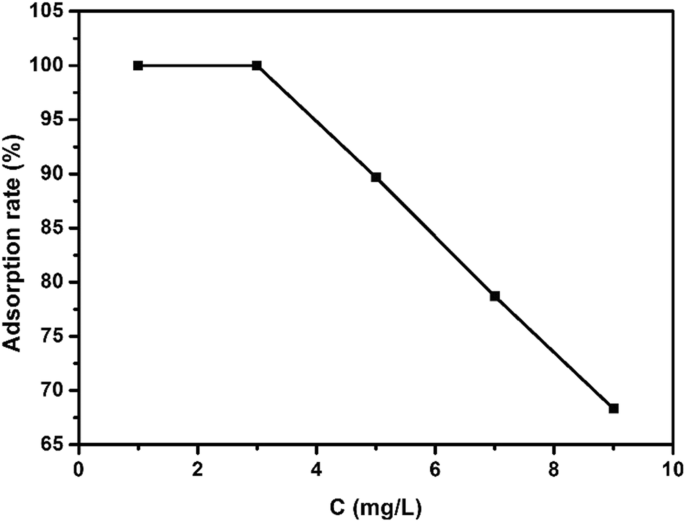
EE2初始浓度对吸附速率的影响
吸附稳定性
为探究合成的纳米硫化铜的稳定性,以EE2初始浓度5 mg/L、吸附量15 mg、pH 8、温度25 °进行EE2吸附在硫化铜上的循环实验C,吸附时间为3 h。每次吸附循环后,将吸附剂用EE2水溶液离心,乙醇和水交替洗涤6次,干燥后重新用于下一个循环。从图 11a 可以看出,随着重复次数的增加,吸附率略有下降,但吸附率仍超过 85%。图 11b 是五次循环前后硫化铜的 XRD 谱。从图中可以看出,循环前后硫化铜的相组成略有变化,图案中标记处有两个杂质峰,这可能是循环后吸附率下降的原因.从图11c、d硫化铜的SEM和TEM照片可以看出,经过5次循环后硫化铜的形貌没有变化,仍然呈现管状和粒状(球状)形状。
<图片>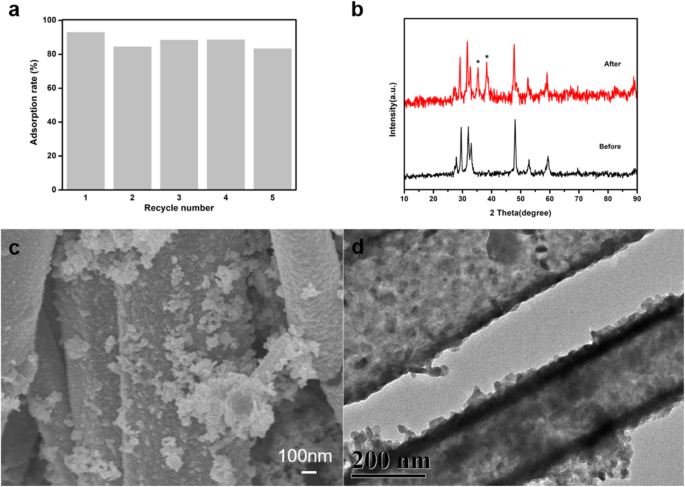
硫化铜吸附EE2(a ); CuS 的 XRD 图,使用 CuS (b );使用过的 CuS (c );和使用过的 CuS 的 TEM 图像 (d )
吸附机制
动力学实验
图 12a 显示了硫化铜吸附 EE2 的吸附量随时间增加的变化。可以看出,随着时间的推移,吸附量逐渐增加,但变化程度逐渐减小。图 12b、c 显示了硫化铜吸附 EE2 的一级和二级动力学拟合。表 1 显示了动力学模型的相关参数。通过绘制ln(q e -q t ) 与 t , 和 K 1 是斜率。通过绘制t得到二级动力学方程 /q t 对比 t , 和 K 2 可以通过截距计算。如表 1 所示,R 2 准一级动力学的 0.9784,而准二级动力学模型的 R 2 0.9916 表明更好的线性关系。因此,硫化铜对EE2的吸附更符合准二级动力学模型。此外,比较理论平衡吸附量(q e ,cal) 由理论方程和实验得到的吸附量 (q e ,exp),它们在准二级动力学模型中的值更接近。综上所述,硫化铜吸附EE2的过程遵循准二级动力学模型。
<图片>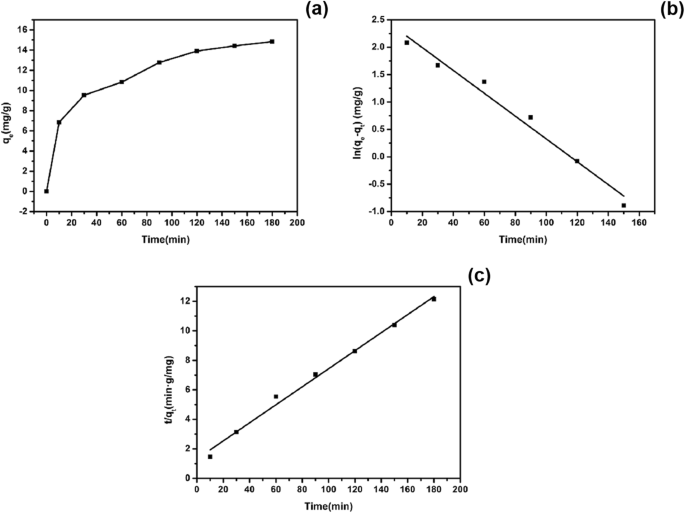
硫化铜吸附随时间的变化(a ), 硫化铜吸附 EE2 的准一级动力学模型 (b ), 以及硫化铜吸附 EE2 的准二级动力学模型 (c )
等温吸附实验
图13a为硫化铜在298 K处的等温吸附曲线,从图中可以看出,EE2浓度越高,吸附量越大。图 13b、c 显示了硫化铜吸附 EE2 的 Langmuir 和 Freundlich 等温拟合曲线。表 2 显示了 Langmuir 和 Freundlich 模型的相关参数。 Langmuir 模型绘制了一条 1/q 的线 e 与 1/C e , q 米 可以从拟合线的截距得到,K L 是斜坡。 Freundlich 模型由 lnC 线绘制 e 与 lnq e, K F 是线截距,1/n 是斜坡。从表2相关参数可以看出,Langmuir模型线性相关系数较好,说明硫化铜对EE2的吸附更符合Langmuir模型,理论最大吸附量 米 硫化铜可达147.06 mg/g。
<图片>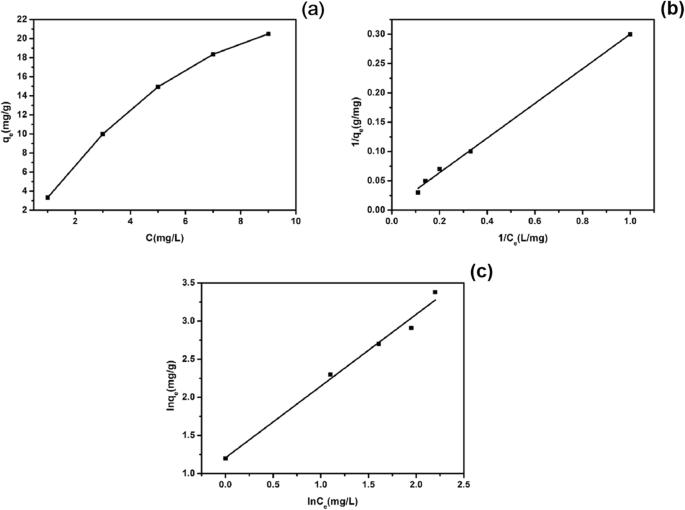
298 K硫化铜吸附EE2的等温线(a ),硫化铜吸附EE2的Langmuir等温线拟合(b ),以及吸附在硫化铜上的 EE2 的 Freundlich 等温线拟合 (c )
热力学实验
如图 14 所示,在实验中,线性拟合由 lnK C 到 − 1/T , 等式 lnK C =1268.1 (− 1/T ) + 43.37,ΔH θ 由拟合线的斜率获得,ΔS θ 是通过拦截获得的。那么,ΔG θ 在298 K、308 K和318 K按式(7)计算,实验结果如表3所示。> θ ) 的硫化铜吸附 EE2 为负,热力学焓 (ΔH θ ) 为正,熵 (∆S θ ) 为正,表明吸附是自发吸热过程,熵增加。根据文献,ΔG的吸附过程 θ - 20 和 0 kJ/mol 之间是物理吸附,而 ∆G θ - 400 和 - 80 kJ/mol 之间是化学吸附过程 [29]。在表 3 中,我们可以看到 ∆G θ 根据热力学实验数据计算的值为- 1.84 kJ/mol (298 K)、- 5.44 kJ/mol (308 K)、- 9.04 kJ/mol (318 K)。因此,硫化铜对EE2的吸附属于物理吸附。在吸附过程中,各种吸附力引起的吸附热的绝对值为[30, 31]:范德华力4-10 kJ/mol,疏水相互作用力5 kJ/mol,2-40 kJ/mol mol 表示氢键相互作用力,大于 60 kJ/mol 表示化学吸附相互作用力。热力学焓 (∆H θ =105.44 kJ/mol)表明硫化铜在EE2上的吸附具有化学吸附特性。从表 3 可以看出,ΔS θ > 0,说明硫化铜在EE2上的吸附过程是一个增加溶液体系混沌度的过程。
<图片>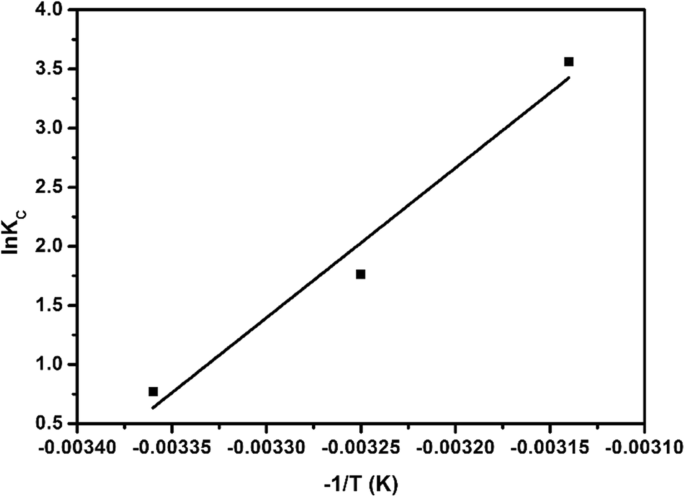
硫化铜吸附EE2的热力学拟合
Conclusion
In this paper, the tubular nano-copper sulfide was synthesized by hydrothermal method. The synthesized copper sulfide was used as an adsorbent for 17α-ethynyl estradiol (EE2) and exhibited excellent adsorption properties. At 25 °C, 15 mg of adsorbent was applied for 50 mL of 5 mg/L EE2 solution, in which adsorption equilibrium was achieved after 180 min, and the adsorption rate reached nearly 90%. The adsorption mechanism of copper sulfide material was found to be consistent with the quasi-secondary kinetic model. The isothermal adsorption model was accorded with the Langmuir model, and the maximum theoretical adsorption capacity of copper sulfide was up to 174.06 mg/g. The thermodynamic model study found that the Gibbs free energy ∆G θ of copper sulfide adsorption EE2 was less than 0, the thermodynamic enthalpy ∆H θ was greater than 0, and the thermodynamic entropy ∆S θ was greater than 0, indicating that the whole adsorption process was a spontaneous endothermic process with increased entropy. By studying the values of thermodynamic enthalpy change ∆H θ and thermodynamic entropy change ∆G θ , it was found that there were chemical adsorption and physical adsorption in the adsorption process. Moreover, the synthesized nano-copper sulfide adsorbent was quite stable under the conditions studied. It is feasible and efficient to absorb EE2 by the nano-copper sulfide adsorbent.
数据和材料的可用性
All data supporting the conclusions of this article are included within the article.
缩写
- BDDT:
-
Brunauer-Deming-Teller
- 赌注:
-
Brunauer-Emmett-Teller measurements
- EDCs:
-
Environmental endocrine disruptors
- EE2:
-
17α-Ethynyl estradiol
- IEP:
-
Isoelectric point
- POPs:
-
Persistent organic pollutants
- SEM:
-
扫描电子显微镜
- TEM:
-
透射电子显微镜
- UPLC:
-
Ultra-high performance liquid chromatography
- XRD:
-
X射线衍射
纳米材料
- 铝的 10 大特性及其应用
- 铝的特性和合金特性
- 钴掺杂 FeMn2O4 尖晶石纳米粒子的制备和磁性
- 走向 TiO2 纳米流体——第 1 部分:制备和性质
- 通过溶胶-凝胶工艺制备的纳米结构二氧化硅/金-纤维素-键合氨基-POSS 混合复合材料
- SrTiO3 改性金红石型 TiO2 纳米纤维的一步静电纺丝路线及其光催化性能
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- Au@TiO2 蛋黄-壳纳米结构的制备及其在亚甲基蓝降解和检测中的应用
- 钯(II)离子印迹聚合物纳米球的制备及其从水溶液中去除钯(II)
- 水溶性硫化锑量子点的合成及其光电特性
- 使用分子束外延法制备锗铋薄膜及其光学特性
- Fe3+ 的可恢复荧光探针 BHN-Fe3O4@SiO2 混合纳米结构及其在生物成像中的应用


