Fe3+ 的可恢复荧光探针 BHN-Fe3O4@SiO2 混合纳米结构及其在生物成像中的应用
摘要
Fe 3+ 的多功能荧光探针BHN-Fe3O4@SiO2纳米结构 被设计和开发。对Fe 3+ 有很好的选择性响应 具有荧光猝灭功能,可以使用外部磁场进行回收。添加 EDTA (2.5 × 10 −5 M) 到随后的产品 Fe 3+ -BHN-Fe3O4@SiO2, Fe 3+ 可以从复合物中去除,其荧光探测能力恢复,这意味着这种构成的开关型荧光探针可以逆转和重复使用。同时,该探针已成功应用于定量检测Fe 3+ 在线性模式下,检测下限为 1.25 × 10 −8 M. 此外,BHN-Fe3O4@SiO2纳米结构探针成功用于检测Fe 3+ 活HeLa细胞,显示其在生物成像检测方面的巨大潜力。
背景
开发检测各种小分子和离子的新方法已成为科研人员的一项重要任务。作为代谢过程中不可缺少的重要金属离子之一,Fe 3+ 在大脑功能和病理学、基因转录、免疫功能和哺乳动物繁殖等各种生物过程中发挥着重要和关键的作用 [1,2,3,4,5,6,7,8,9]。医学研究表明,只有当 Fe 3+ 浓度在合适的范围内。当 Fe 3+ 当生物体内的浓度偏离其适宜范围时,代谢或生物过程中会诱发某些疾病或严重障碍[10,11,12]。尽管已经开发了多种检测方法来检测 Fe 3+ [13,14,15],荧光技术具有操作简单、灵敏度和选择性高、检出限低等优点,是更有效、更有效的方法[16,17,18,19,20]。
在这些基于分子的荧光探针中,与安全性、可回收性和可重复使用性相关的一些问题尚未得到解决。例如,如参考文献 [21] 所指出的,所采用的小分子是有毒的。基于分子的荧光探针所表现出的这些缺陷完全限制了探针进入实际应用。克服上述 Fe 3+ 荧光探针的安全性挑战 ,另一种技术方法是通过使用掺入小分子荧光探针的无机载体。在这种新方法中,已知磁性纳米粒子、金属纳米粒子、纳米管和介孔二氧化硅等无机材料可用于设计荧光探针[22,23,24]。在所有这些无机材料中,磁性二氧化硅核壳Fe3O4@SiO2纳米颗粒具有毒性低、生物相容性高、外磁场分离简单、比表面积大等优点,可以通过荧光探针接枝在分子内或其他材料上。离子识别和分离领域 [25,26,27]。因此,这种新方法为我们实现检测Fe 3+ 的应用提供了可能的途径。 ,尤其是在安全性方面具有低毒和高生物相容性。
在这项工作中,一种用于Fe 3+ 的多功能磁性BHN-Fe3O4@SiO2纳米结构荧光传感器 被设计和合成。对Fe 3+ 有很好的敏感和选择性反应 在 CH3CN/H2O (1:1, v /v ) 在室温下。通过施加外部磁场,可以将探针与溶液分离。加入EDTA时,Fe 3+ 可以通过荧光强度恢复从复合物中去除。此外,使用HeLa细胞的共聚焦荧光成像表明该探针可用于检测Fe 3+ 在活细胞中。因此,获得的BHN-Fe3O4@SiO2表现出优异的选择性、水溶性、可逆性和可回收性,有利于Fe 3+ 的检测。 .
方法/实验
Fe3O4@SiO2纳米颗粒的合成
Fe3O4 磁铁矿纳米颗粒是根据参考文献[28]合成的。通过改进的 Stöber 方法 [29] 将它们进一步涂上一层薄薄的二氧化硅层,以获得稳定的 Fe3O4@SiO2。将原硅酸四乙酯 (TEOS) 与作为种子的磁铁矿纳米颗粒在乙醇/水混合物中水解。所得平均直径为50-60 nm的Fe3O4@SiO2纳米颗粒被用作荧光传感器纳米颗粒的载体。
BHN-Fe3O4@SiO2纳米结构的合成
N -丁基-4-双(2-羟乙基)氨基-1,8-萘二甲酰亚胺(BHN)根据之前报道的方法合成[30, 31]。第一个中间体由4-溴-1,8-萘酐与n反应合成 -丁胺。然后,中间体与二乙醇胺反应得到 BHN。 ESI-MS:m/z 357.3 (M + H + )。 1 H NMR(CDCl3,400 MHz):δ (ppm):0.95 (t, 3H, J =8.0 赫兹); 1.41(米,2H); 1.66(米,2H); 2.69(米,2H); 3.60 (t, 4H, J =5.0 赫兹); 3.86(t, 4H, J =5.0 赫兹); 4.08 (t, 2H, J =8.0 赫兹); 7.33 (d, 1H, J =8.0 赫兹); 7.58 (t, 1H, J =8.0 赫兹); 8.38(d, 1 H, J =8.0 赫兹); 8.41 (dd, 1H, J =8.0 赫兹); 8.84 (dd, 1H, J =8.0 赫兹)。
BHN(356 毫克,1 毫摩尔)和 3-异氰酸根合丙基三乙氧基硅烷(IPTES,494 毫克,2 毫摩尔)在室温下在无水 THF(15 毫升)中混合。然后将溶液在 N 2 下回流 48 小时。之后,蒸发溶剂,粗产物通过快速柱色谱法(硅胶,石油醚/CH2Cl2/甲醇 50/50/1)进一步纯化,得到 255mg(30%)黄色 BHN-IPTES粉末。 ESI-MS:m/z 851.5(M + H + )。 1 H NMR:(400 MHz,CDCl3):δ (ppm) 0.60 (t, 4H, J =8.0 赫兹); 0.98 (t, 3H, J =8.0 赫兹); 1.21(米,18小时); 1.45(米,2H); 1.58(米,4H); 1.70(米,2H); 3.13(米,4H); 3.73 (t, 2H, J =5.0 赫兹); 3.82(米,12H); 4.16(米,4H); 4.24(米,4H); 4.94(米,2H); 7.38 (d, 1H, J =8.0 赫兹); 7.70 (t, 1H, J =8.0 赫兹); 8.45 (d, 1H, J =8.0 Hz); 8.50 (dd, 1H, J =8.0 赫兹); 8.58 (dd, 1H, J =8.0 赫兹)。
将 100 毫克干燥的 Fe3O4@SiO2 纳米粒子和 300 毫克(0.35 毫摩尔)的 BHN-IPTES 悬浮在无水甲苯(15 毫升)中。将溶液在 N2 下于 110°C 回流 12 小时以获得 BHN-Fe3O4@SiO2。通过离心(10,000 rpm)收集纳米颗粒并用无水乙醇反复彻底洗涤。通过监测上层液体的荧光,可以完全去除未反应的有机分子。然后,BHN-Fe3O4@SiO2纳米结构最终在真空下干燥过夜。
结果与讨论
BHN-Fe3O4@SiO2的设计
Fe3O4@SiO2纳米颗粒是构建安全、可回收和可重复使用的Fe 3+ 的有希望的候选者 荧光传感器由于其毒性低、生物相容性高、可通过外部磁场方便地回收利用。与其他荧光团相比,1,8-萘二甲酰亚胺具有较大的斯托克斯位移、较长的发射波长、不同侧链修饰的方便性和较高的量子产率。因此,通过引入合适的侧链,它可以接枝在Fe3O4@SiO2纳米颗粒上,获得安全、可回收、可重复使用的Fe 3+ 具有显着荧光响应的荧光传感器。
众所周知,Fe 3+ 可以很容易地与O和N原子配位,因此我们用二乙醇胺修饰1,8-萘酰亚胺,使1,8-萘酰亚胺具有检测Fe 3+ 的能力 如图 1a 所示。在二乙醇胺中,羟乙基和酯-酰胺部分用作受体单元。最后,修饰的 1,8-萘二甲酰亚胺通过 Si (OEt)3 与 Fe3O4@SiO2 表面羟基的水解缩合反应接枝到 Fe3O4@SiO2 上,如图 1b 所示。
<图片>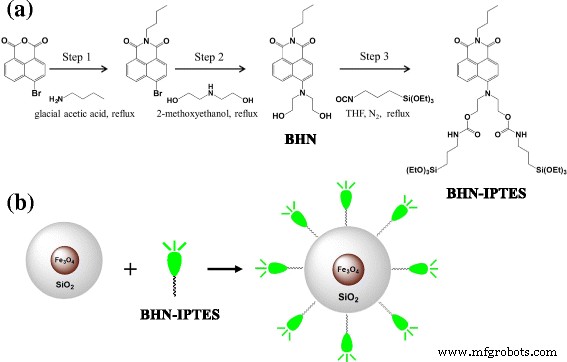
一 BHN的合成。 b BHN-Fe3O4@SiO2的合成
BHN-Fe3O4@SiO2的结构
从图 2a 所示的 TEM 图像中,可以清楚地显示 BHN-Fe3O4@SiO2 的典型核/壳结构。虽然裸磁核在液体中容易聚集,但磁性纳米粒子表面的二氧化硅壳会阻止聚集并提高分散性。氧化铁纳米颗粒已经成功地被包裹在二氧化硅壳中并且分散良好。还可以看出,核/壳结构的总直径在50-60 nm的狭窄分布中,氧化铁核为10 nm,低于其超顺磁性临界尺寸,适合用作荧光探针的载体纳米颗粒。
<图片>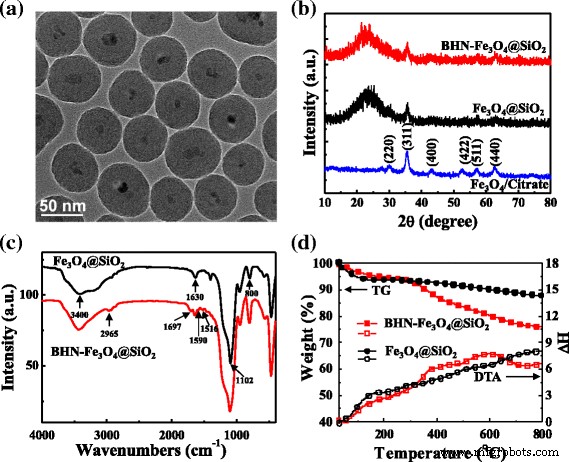
一 BHN-Fe3O4@SiO2 的 TEM 图像(比例尺为 50 nm。)。 b Fe3O4/柠檬酸盐、Fe3O4@SiO2 和 BHN-Fe3O4@SiO2 的 XRD 谱。 c Fe3O4@SiO2 和 BHN-Fe3O4@SiO2 的 FT-IR 光谱。 d Fe3O4@SiO2和BHN-Fe3O4@SiO2的TG和DTA曲线
图 2b 显示了 Fe3O4、Fe3O4@SiO2 和 BHN-Fe3O4@SiO2 的 XRD 粉末衍射图。裸 Fe3O4 的六个特征衍射峰可以索引到磁铁矿的 220、311、400、422、511 和 440 次反射。然而,归因于 Fe3O4 的 XRD 峰在 Fe3O4@SiO2 和 BHN-Fe3O4@SiO2 中具有低强度,这意味着 Fe3O4 纳米颗粒被无定形二氧化硅壳包覆。二氧化硅壳可能会降低 Fe3O4 核的相对含量,进而影响峰强度。此外,在 Fe3O4@SiO2 和 BHN-Fe3O4@SiO2 中,在 20° 至 30° 的低衍射角处发现了广泛的 XRD 封装,这对应于围绕 Fe3O4 纳米颗粒的非晶态 SiO2 壳。
为了研究 BHN-IPTES 在 Fe3O4@SiO2 纳米粒子表面的改性条件,测量了其傅里叶变换红外 (FT-IR) 光谱。如图 2c 所示,两条曲线都表现出典型的 -OH 在 3400 到 3500 cm -1 处在硅烷醇上拉伸的振动带 和 1000 到 1200 厘米 −1 [32]。这表明并非 Fe3O4@SiO2 纳米颗粒上的所有硅烷醇都被共价改性。 1630 cm −1 处的波段 表示 -OH 振动的弯曲模式 [33]。带中心在 1109 (νas ) 和 800 cm −1 可归因于硅氧烷 (-Si-O-Si-) [34]。上述峰表明二氧化硅壳的存在。 2965 和 2934 cm −1 处的附加峰 在 BHN-Fe3O4@SiO2 中发现,对应于脂肪族和芳香族基团的 -CH 振动 [32, 35]。 1697、1590 和 1516 cm −1 处的波段 BHN-Fe3O4@SiO2 来自 BHN 部分的 -CH3 弯曲振动 [36]。这些结果证明了磁性材料BHN-Fe3O4@SiO2中存在有机分子。
磁性纳米粒子的超顺磁性对其生物应用起着至关重要的作用。附加文件 1:图 S1 显示了 BHN-Fe3O4@SiO2 的磁化曲线,该曲线是通过振动样品磁力计在 - 15,000 到 15,000 Oe 范围内在 300 K 下测量的。结果与磁性 Fe3O4 的直径的结论一致小于 30 nm 的纳米粒子在室温下通常是超顺磁性的 [37]。合成的 BHN-Fe3O4@SiO2 的饱和磁化强度值约为 4.02 emu/g。更重要的是,从BHN-Fe3O4@SiO2纳米结构的磁滞回线可以发现它表现出超顺磁性,磁滞回线中没有观察到矫顽力。这种现象是由于磁铁矿芯的直径很小,约为 10 纳米。同时,二氧化硅壳阻止了磁铁矿核的聚集。因此,BHN-Fe3O4@SiO2纳米结构可以进一步表现出良好的分散性。
BHN-Fe3O4@SiO2的荧光响应
为了验证 BHN-Fe3O4@SiO2 对各种金属离子的荧光响应,在 CH3CN/H2O 1:1 (v /v ) 在 HEPES 缓冲液中 pH 7.36 的溶液。 BHN-Fe3O4@SiO2的浓度为0.2 g/L(对应的游离有机分子约为3.34 × 10 -5 M,根据 TGA,见图 2d),以及各种金属离子 Ag + , 铝 3+ , Ca 2+ , Cd 2+ , Co 2+ , Cr 3+ , 铜 2+ , 汞 2+ , K + , 李 + , Mg 2+ , Mn 2+ , Na + , Pb 2+ , Zn 2+ , 和 Fe 3+ (全部为高氯酸盐)为 5.0 × 10 -5 M. 如图 3a 所示,加入 Fe 3+ 时观察到明显的荧光猝灭 , 但在相同条件下加入除 Cu 2+ 以外的其他金属离子,荧光强度没有明显降低 .铜 2+ 会在 20 分钟内引起轻微的荧光猝灭和响应。然而,在相同的检测条件下,Fe 3+ 在 2 分钟内引起响应并在 5 分钟内明显淬灭(图 3c)。 BHN-Fe3O4@SiO2 (0.2 g/L) 在不同浓度 Fe 3+ 存在下的吸收光谱 (0 到 200 μM) 进行了研究,如图 3d 所示。当 Fe 3+ 逐渐加入,BHN-Fe3O4@SiO2 在 250 和 350 nm 处的吸光度逐渐增加,表明 BHN-Fe3O4@SiO2 纳米结构与 Fe 3+ 逐渐。
<图片>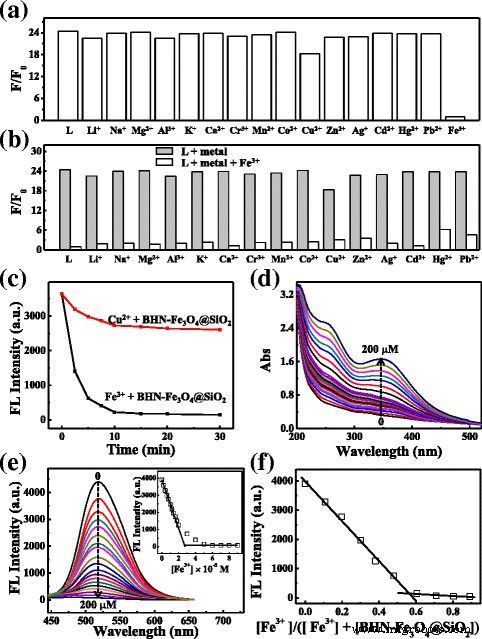
一 BHN-Fe3O4@SiO2 与各种阳离子的荧光响应。激发波长为 415 nm。添加金属离子后每 2 分钟记录一次光谱。 b Fe 3+ 的竞争 -BHN-Fe3O4@SiO2 对阳离子。添加金属离子后BHN-Fe3O4@SiO2 (0.2 g/L)的荧光发射变化(每个金属离子为5 × 10 -5 M) 在室温下在 CH3CN/H2O 1:1(HEPES 缓冲液 pH 7.36)中。 c BHN-Fe3O4@SiO2与Fe 3+ 的时间响应 和 Cu 2+ . d BHN-Fe3O4@SiO2 (0.2 g/L) 与 Fe 3+ 的紫外-可见滴定 . e BHN-Fe3O4@SiO2 (0.2 g/L) 与 Fe 3+ 的荧光滴定 .插图:不同浓度 Fe 3+ 在 518 nm 处的荧光强度 . f BHN-Fe3O4@SiO2 与 Fe 3+ 的乔布图
然后,在 CH3CN/H2O 1:1 (v /v) 用于理解 BHN-Fe3O4@SiO2 对 Fe 3+ 的结合 离子。如图 3e 所示,当 Fe 3+ 的不同浓度(0 到 100 μM)时,BHN-Fe3O4@SiO2 (0.2 g/L) 的荧光发射逐渐降低 加入 CH3CN/H2O 1:1 (v /v ) HEPES 缓冲液,表明 BHN-Fe3O4@SiO2 纳米结构与 Fe 3+ 配位 定量地形成复合物。荧光滴定实验表明缔合常数logβ 对于 Fe 3+ 与 BHN-Fe3O4@SiO2 的结合计算为 8.23。添加Fe 3+ 后观察到BHN-Fe3O4@SiO2纳米结构的荧光线性增加 在 0 到 20 μM 之间,以及 BHN-Fe3O4@SiO2 到 Fe 3+ 的检测限 被 1.25 × 10 −8 发现 M 在荧光测定下。荧光滴定和工作图结果表明 Fe 3+ 的结合率为 1:1 使用 BHN-Fe3O4@SiO2(图 3f)。阳离子竞争实验的结果如图 3b 所示,可以发现 BHN-Fe3O4@SiO2 对 Fe 3+ 的选择性和敏感性 不受其他金属离子的影响。
在此,荧光强度的显着降低可以解释如下: BHN-Fe3O4@SiO2 在 415 nm 灯下激发的荧光强度,由于 1,8-萘二甲酰亚胺在 518 nm 处显示出高荧光一个大的共轭系统。此外,结构中的给电子基团同时影响体系的荧光。当与 Fe 3+ 稳定螯合时 通过1,8-萘二甲酰亚胺四位上的O原子和N原子,金属阳离子与荧光团之间的电子或能量转移产生电子吸收效应,从而使荧光猝灭[38](图3)。 4a).
<图片>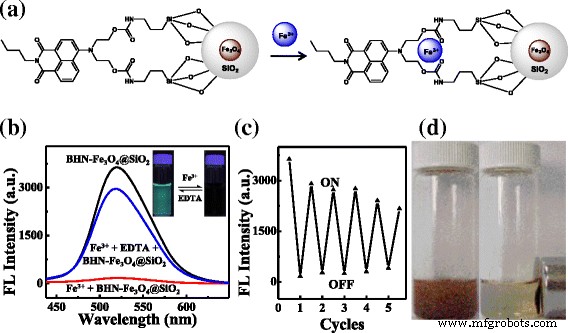
一 BHN-Fe3O4@SiO2与Fe 3+ 的示意图 . b BHN-Fe3O4@SiO2对Fe 3+ 的可逆性 .插图:BHN-Fe3O4@SiO2 与 Fe 3+ 的照片 通过处理 EDTA (2.5 × 10 −5 M) 在 415 纳米紫外光下。 c BHN-Fe3O4@SiO2 (0.2 g/L) 的荧光图,交替添加 2.5 × 10 −5 M Fe 3+ (“关”)和 EDTA(“开”)。 d BHN-Fe3O4@SiO2 (0.2 g/L) 在 CH3CN/H2O 1:1(HEPES 缓冲液 pH 7.36)中分散到外部磁体
添加Fe 3+ 的荧光猝灭 BHN-Fe3O4@SiO2 溶液完全可逆。添加EDTA时(2.5 × 10 −5 M) 到 Fe 3+ -BHN-Fe3O4@SiO2 系统,荧光强度几乎恢复到 BHN-Fe3O4@SiO2 的原始水平(图 4b)。此外,通过重复添加 Fe 3+ 来评估可重复使用性 -EDTA循环进入系统,每一步后记录BHN-Fe3O4@SiO2荧光强度的变化,相应数据如图4c所示。很明显,BHN-Fe3O4@SiO2 表现出优异的可重用性,因为只有 BHN-Fe3O4@SiO2 对 Fe 3+ 敏感性的罕见损失 重复五次 Fe 3+ 后观察到 -EDTA循环。由于其磁性,BHN-Fe3O4@SiO2 具有反向磁责任。如图 4d 所示,通过将磁铁靠近分散体放置 10 分钟后,它可以很容易地与分散体 (0.2 g/L) 分离,然后在移除磁铁时通过轻微搅拌重新分散。 BHN-Fe3O4@SiO2纳米结构的这种磁分离能力和识别特性为分离Fe 3+ 提供了一种简单有效的途径 而不是通过过滤的方法。更重要的是,在评估其可回收性时,BHN-Fe3O4@SiO2 纳米结构的反向磁责任将是一个关键因素[39]。结合其磁性,证明BHN-Fe3O4@SiO2作为一种有效的Fe 3+ 无机-有机杂化传感器在生物系统中具有相当的应用价值 .
对于生物应用,传感器应适合测量生理 pH 范围内的特定金属离子至关重要。如图 5a 所示,含/不含 Fe 3+ 的 BHN-Fe3O4@SiO2 的荧光强度 在不同的 pH 值下进行了研究。加入Fe 3+ 后,BHN-Fe3O4@SiO2的荧光强度略有降低 在酸性条件下,由于 1,8-萘二甲酰亚胺四位 N 原子的质子化导致 Fe 3+ 的配位能力较弱 .然后,Fe 3+ 的显着荧光变化 -BHN-Fe3O4@SiO2体系在pH为中性和弱碱性条件下被发现。在这里,BHN-Fe3O4@SiO2 表现出优异的 Fe 3+ pH在5.84~10.52范围内时的传感能力,表明BHN-Fe3O4@SiO2是一种有望应用于复杂环境或生物系统的探针。
<图片>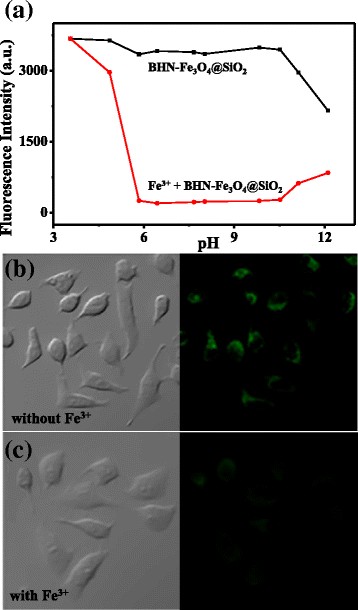
一 BHN-Fe3O4@SiO2和Fe 3+ 的荧光强度 -BHN-Fe3O4@SiO2 室温下各种 pH 值。 CH3CN/H2O 1:1, λ ex =415nm。 b 具有 BHN-Fe3O4@SiO2 的 HeLa 细胞的明场图像和荧光图像。 (c ) 含有 BHN-Fe3O4@SiO2 和 Fe 3+ 的 HeLa 细胞的明场图像和荧光图像
进一步证明BHN-Fe3O4@SiO2检测Fe 3+ 的能力 在生命系统中,我们在活的 HeLa 细胞中进行了一项实验。首先,我们研究了 BHN-Fe3O4@SiO2 和 Fe 3+ 的细胞活力 -BHN-Fe3O4@SiO2 使用 MTT 分析。 HeLa 细胞与 BHN-Fe3O4@SiO2 在 RPMI-1640 中于 37°C 孵育 0.5 小时,然后加入 Fe(ClO4)3 孵育 0.5 小时。然后观察HeLa细胞的共聚焦荧光图像,当传感器和Fe(ClO4)3的浓度达到0.2 g/L和5 × 10 -5 M. 然后,我们进行了荧光显微镜实验,以研究其在复杂生物系统中的更高层次的应用。如图 5b 所示,HeLa 细胞在 37°C 和 5% CO2 气氛中在 12 孔板上生长 24 小时,然后用 BHN-Fe3O4@SiO2(0.2 克/升)处理并孵育 0.5 小时,然后细胞显示出强烈的绿色荧光。然后,将细胞用 5 × 10 -5 M Fe(ClO4)3。 0.5 小时后,我们确实观察到荧光显着降低(图 5c)。因此,我们可以得出结论,BHN-Fe3O4@SiO2 可用于对 Fe 3+ 进行成像 在活细胞中。
结论
总之,一种新型多功能荧光探针 BHN-Fe3O4@SiO2 纳米结构 Fe 3+ 设计合成成功。探针BHN-Fe3O4@SiO2可选择性响应Fe 3+ 具有荧光猝灭和 Fe 3+ 的高效分离 与外部磁场。所构成的开关式荧光监测系统表明探头可以倒回重复使用。同时,该探针已成功应用于定量检测Fe 3+ 检测限低。此外,BHN-Fe3O4@SiO2纳米结构探针成功用于检测Fe 3+ 活HeLa细胞,显示其在生物成像检测方面的巨大潜力。
缩写
- BHN:
-
N -丁基-4-双(2-羟乙基)氨基-1,8-萘二甲酰亚胺
- EDTA:
-
乙二胺四乙酸
- FT-IR:
-
傅里叶变换红外
- IPTES:
-
3-异氰酸根合丙基-三乙氧基硅烷
- TEM:
-
透射电子显微镜
- TEOS:
-
原硅酸四乙酯
- TGA:
-
热重分析
- THF:
-
四氢呋喃
- XRD:
-
X射线粉末衍射
纳米材料
- 钼金属及其合金的应用
- 用于合成和生物医学应用的荧光纳米材料的进展和挑战
- 通过溶胶-凝胶工艺制备的纳米结构二氧化硅/金-纤维素-键合氨基-POSS 混合复合材料
- 超窄带完美吸收体及其在可见光区域中作为等离子体传感器的应用
- Au@TiO2 蛋黄-壳纳米结构的制备及其在亚甲基蓝降解和检测中的应用
- 聚(3,4-亚乙基二氧噻吩)/金/石墨烯复合材料的固态加热合成及其在安培法测定亚硝酸盐和碘酸盐中的应用
- 分子印迹核壳 CdSe@SiO2/CD 作为 4-硝基苯酚传感的比率荧光探针
- 磁性金纳米粒子标记乙酰肝素酶单克隆抗体及其在肿瘤磁共振成像中的后续应用
- 增强型近红外吸收体:两步制造结构化黑硅及其器件应用
- 荧光纳米生物质点:超声波辅助提取及其作为 Fe3+ 检测纳米探针的应用
- 可回收灵活的淀粉-银网络及其在联合传感器中的应用
- 了解混合制造的优势和挑战


