退火对溶剂热合成 Cu2SnS3 阳极纳米材料电化学性能的影响
摘要
Cu2SnS3作为高容量锡基负极的改性材料,在锂离子电池应用中具有巨大的潜力。溶剂热法简单、方便、经济、易于放大,因此被广泛用于纳米晶体的制备。在这项工作中,Cu2SnS3 纳米粒子是通过溶剂热法制备的。研究了高温退火对Cu2SnS3纳米阳极的形貌、晶体结构和电化学性能的影响。实验结果表明,与制备的样品相比,高温退火提高了 Cu2SnS3 的电化学性能,从而提高了初始库仑效率并改善了循环和倍率特性。
介绍
锂离子电池广泛应用于电动汽车和便携式电子设备,但需要进一步改进能量密度、循环寿命、功率密度、安全性和环境兼容性等参数[1,2,3,4,5,6 ,7,8,9]。能量密度是最重要的参数之一,因为它决定了电动汽车的续航里程。传统锂离子电池受限于商业石墨负极(LiC6,372 mAh g −1 )。因此,研究具有高比容量的负极以提高锂离子电池的能量密度至关重要。在这方面,Sn基负极材料因其高比容量(Li4.4Sn, ~ 993 mAh g –1 ) [10,11,12,13,14]。然而,这些材料表现出较差的导电性和大的体积膨胀(高达 300%)[15,16,17],导致低倍率和较差的循环稳定性。已经探索了各种策略来改善 Sn 基负极材料的电化学性能 [18,19,20,21]。引入惰性和非惰性元素以形成锡基复合材料,可以作为体积膨胀的缓冲基质,从而提高材料的结构和循环稳定性。常用于形成Sn基复合材料的惰性元素包括Ni、Co、Mn和Cu[22,23,24,25,26,27],非惰性元素包括Sb、Ge等[28,29,30]。电极材料的纳米化不仅可以有效抑制电池循环过程中的体积变化,释放材料的内应力,从而提高其结构稳定性,还可以增加电极的比表面积,促进电极界面的快速反应。此外,纳米化可以显着降低锂离子在活性材料中的扩散距离,从而减少电极的极化现象,提高锂离子电池的倍率性能。 Cai 和 Li 报道,多孔 SnS 纳米棒/碳杂化纳米结构表现出改善的可逆容量和循环性能 [31]。由多孔碳/碳纳米管稳定的硫化钴纳米粒子构建的3D空心CoS@PCP/CNTs复合材料表现出约1668 mAh g -1 的超高可逆容量 在 100 次循环和卓越的高倍率能力(1038、979、858 和 752 mAh g -1 在电流密度为 1、2、5 和 10 A g −1 ,分别)[32]。 Cu2SnS3 作为高容量 Sn 基负极的改性材料,通过引入惰性 Cu 形成合金,具有巨大的锂离子电池应用潜力 [17, 33,34,35]。通过简便的溶剂热法成功制备了用于钠离子电池的 Cu2SnS3(CTS)纳米结构材料。退火后的 CTS 电极表现出高初始可逆容量 447.7 mAh g -1 和良好的容量保持率 200.6 mAh g −1 在 100 mA 的电流密度下循环 50 次后 g -1 [36]。 Fu和Li使用简便的水热法制备了用于钠离子电池的Cu2SnS3/还原氧化石墨烯(CTS/RGO)复合材料。 CTS/RGO 具有 566.8 mAh g −1 的高可逆容量 并保持比容量为 339.8 mAh g −1 在 100 mA 的恒定电流密度下循环 100 次后 g -1 [37]。高温烧结硫化物已被广泛用于改善电化学性能。研究了高温退火工艺对Cu2SnS3锂离子电池电化学性能的影响。
溶剂热法简单、方便、经济、易于扩展,因此被广泛用于纳米晶体的制备。在这项工作中,本文通过溶剂热法制备了用于锂离子电池的 Cu2SnS3 纳米粒子。此外,还研究了高温退火对Cu2SnS3纳米阳极的形貌、晶体结构和电化学性能的影响。
实验部分
材料准备
CuCl2·2H2O(99.9%)、SnSO4(99.9%)、元素硫粉(99.9%)、无水乙二胺(99%)购自成都科隆化工有限公司
为了合成 Cu2SnS3 纳米颗粒,首先将 CuCl2·2H2O(0.682 g,4 mmol)和 SnSO4(0.473 g,2.2 mmol)溶解在去离子水中,磁力搅拌 20 分钟。将所得混合物装入具有25-ml Teflon容器的高压釜中,该容器预装有悬浮在无水乙二胺中的硫粉(0.290g,9mmol)溶液。将密闭的高压釜转移到烘箱中,由室温加热至200℃,保温24h,然后自然冷却至室温。所得沉淀物用去离子水洗涤数次,并通过在 6000 rpm 下离心 3 分钟以除去副产物来收集。然后,所得沉淀物在使用前在 80°C 下真空干燥 10 小时。 Cu2SnS3 纳米粒子在管式炉中在 540 °C 下退火 40 分钟,管式炉抽真空并用氮气吹扫,流速为 50–80 ml min –1 在环境压力下。
材料表征
X 射线粉末衍射 (XRD) 数据是使用带有 Cu-Kα (λ =1.5418 Å) 辐射源的 Bruker D8 ADVANCE 获得的。使用扫描电子显微镜 (SEM) (Hitachi S3400) 和透射电子显微镜 (TEM) (Tecnai G2-F30-S-TWIN, FEI) 来研究 Cu2SnS3 纳米颗粒的微观结构。使用能量色散 X 射线 (EDX) 光谱分析样品的组成。使用X射线光电子能谱仪(ESCALAB 250Xi,Thermo Scientific)获得Cu2SnS3纳米颗粒的X射线光电子能谱(XPS)。
电池组装和电化学测量
Cu2SnS3 纳米颗粒的电化学性能通过使用锂金属作为对电极的 CR2032 型纽扣电池进行测试。负极由 80wt% 的活性材料、10wt% 的超级 P 和 10wt% 的 PVDF 组成。电解质为 1 M LiPF6(EC:EMC:DEC =4:2:4,体积百分比)。 Cu2SnS3 电极被冲压成直径为 12 mm 的圆形。 Cu2SnS3活性材料的质量负载为2.65 mg/cm 2 .铸造的Cu2SnS3阳极的厚度为 ~ 30 μm,由微米确定。循环伏安法 (CV) 在 0.1 mV s -1 使用恒电位仪(VersaSTAT3F,普林斯顿应用研究)从 2.0 到 0.0 V。循环和倍率测试在室温下 0.05 至 2.0 V 的自动恒电流充放电装置(CT-4800 电池测试系统,Neware)中进行。电化学阻抗谱使用恒电位仪(VersaSTAT3F,Princeton Applied Research)在100 kHz至0.1 Hz的频率范围内进行。
结果与讨论
图 1 显示了 Cu2SnS3 纳米颗粒的 XRD 谱。两个样品在 28.61°、33.13°、47.5°、56.31°、69.42°、76.65° 和 88.44° 处的衍射峰可以归属于 (112)、(200)、(220)、(312)、( 400)、(332) 和 (424) 平面。制备和退火的 Cu2SnS3 的主要衍射峰与四方 Cu2SnS3 (JCPDS 89-4714) [38, 39, 42] 的主要衍射峰很好地匹配,并且没有检测到第二相,证实产品都是相纯的沿(112)平面优先生长。 540℃退火后,XRD图中各主要衍射峰的相对强度增加,(112)衍射峰的半峰全宽(FWHM)从0.4减小到0.35,表明退火工艺提高了材料的结晶度[40, 41]。
<图片>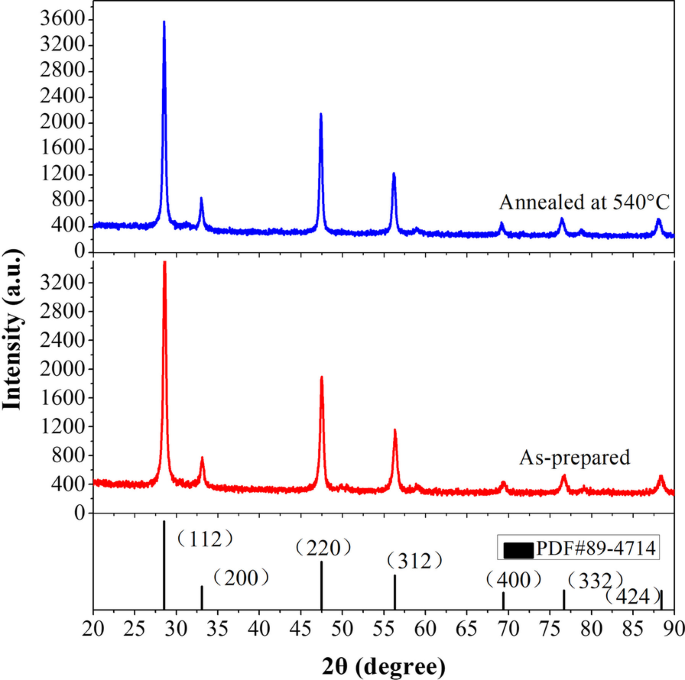
Cu2SnS3纳米颗粒的XRD谱
如图 2a、e 中的 SEM 图像所示,制备和退火的 Cu2SnS3 以球形纳米粒子的形式存在,它们聚集形成不规则的球状附聚物。由初级纳米粒子形成的微米形状的不规则球形簇是有利的,因为它们增加了阳极的压实密度,从而增加了电池的容量。为了进一步分析 Cu2SnS3 的颗粒形态和尺寸,以及详细的内部晶体结构,通过 TEM 和 HRTEM 进一步观察了 Cu2SnS3 纳米颗粒。如图 2c、g 所示,制备的和退火的 Cu2SnS3 颗粒的尺寸分别约为 25 和 41 nm,两种材料进一步聚集成 1 µm 的球形颗粒,如图 2b、f 所示。在图 2d、h 所示的 HRTEM 图像中,可以清楚地观察到晶格条纹,其中退火的 Cu2SnS3 纳米粒子(图 2h)的条纹比制备的样品的条纹更规则。这进一步证明了通过在 540°C 下退火增强了 Cu2SnS3 纳米颗粒的结晶。 Cu2SnS3 的高分辨率 TEM 的快速傅立叶变换 (FFT) 如图 2d、h 所示。材料的衍射图案清楚地显示在 FFT 中。 0.301nm的晶格间距接近Cu2SnS3的(112)面的面间距。因此,HRTEM结果与XRD结果非常吻合(图1)。
<图片>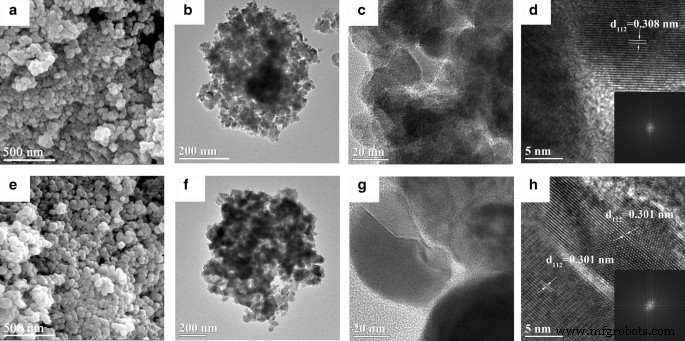
一 扫描电镜,b , c TEM 和 d 所制备的 Cu2SnS3 纳米粒子的 HRTEM 图像; e 扫描电镜,f , g TEM 和 h 退火态Cu2SnS3纳米粒子的HRTEM图
为了研究 Cu2SnS3 的分布,进行了能量色散 X 射线 (EDX) 映射。元素映射图像显示了复合材料中 Cu、Sn 和 S 元素的清晰轮廓(图 3)。结果表明,Cu、Sn 和 S 元素在 CTS 中分布均匀。 EDX 数据验证了所制备的 Cu2SnS3 的 Cu:Sn:S 元素比为 2:0.87:2.25。然而,退火后的Cu2SnS3元素比为Cu:Sn:S =2:1.006:2.89,与化学计量学基本一致。
<图片>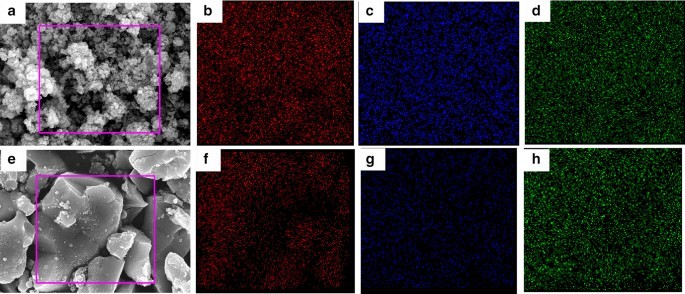
b 的 EDX 元素映射 铜,c Sn 和 d 准备好的 CTS 的 S; f 铜,g Sn 和 h 退火CTS的S
Cu2SnS3 纳米粒子的价态和组成由 XPS 进一步确定。图 4a、e 分别显示了所制备和退火的 Cu2SnS3 纳米粒子的完整 XPS 光谱。 Cu、Sn 和 S 元素,以及 C (C1s , 285.08 eV) 和 O (O1s , 533.08 eV),观察到,没有检测到其他杂质元素; C 和 O 杂质峰可能是由于环境污染 [39, 42,43,44,45,46,47]。图 4b 显示了 Cu2p 所制备的 Cu2SnS3 纳米粒子的核心级光谱。 Cu2p的结合能 3/2 和 Cu2p 1/2 分别发生在 931.9 和 951.9 eV,这与 Cu + 的值一致 文献报道 [45, 47];相比之下,Cu 2+ 未观察到 942 eV 处的峰值 [48]。 Sn3d的结合能 5/2 和 Sn3d 所制备的 Cu2SnS3 纳米粒子的 3/2 分别发生在 486.4 和 494.8 eV,对应于 Sn 4+ 文献中报道的值 [45,46,47]。图 4f 显示了 Cu2p 退火后的 Cu2SnS3 纳米粒子的核能级光谱; Cu2p的结合能 3/2 和 Cu2p 1/2 分别发生在 932.8 和 952.7 eV,这也与文献 [39, 46] 中报道的值一致。 Sn3d的结合能 5/2 和 Sn3d 退火后的 Cu2SnS3 纳米粒子的 3/2 分别发生在 486.9 和 495.3 eV(图 4g),证实了 Sn 4+ 的存在 [38, 39]。 S2p的结合能 3/2 和 S2p 制备的和退火的 Cu2SnS3 纳米晶体的 1/2 分别为 161.8 和 162.98 eV,表明 S 的存在。这些值与文献中报道的一致,这为 S 2 的存在提供了证据- [43,44,45,46,47]。因此,XPS 结果表明所制备和退火的 Cu2SnS3 纳米粒子中的 Cu、Sn 和 S 元素以 Cu + 的离子态存在 , Sn 4+ , 和 S 2− , 分别。退火工艺提高了 Cu2SnS3 颗粒的结晶度并增加了颗粒尺寸。这种现象可能会引起阳离子周围电子云的变化,从而增加Cu和Sn的结合能。
<图片>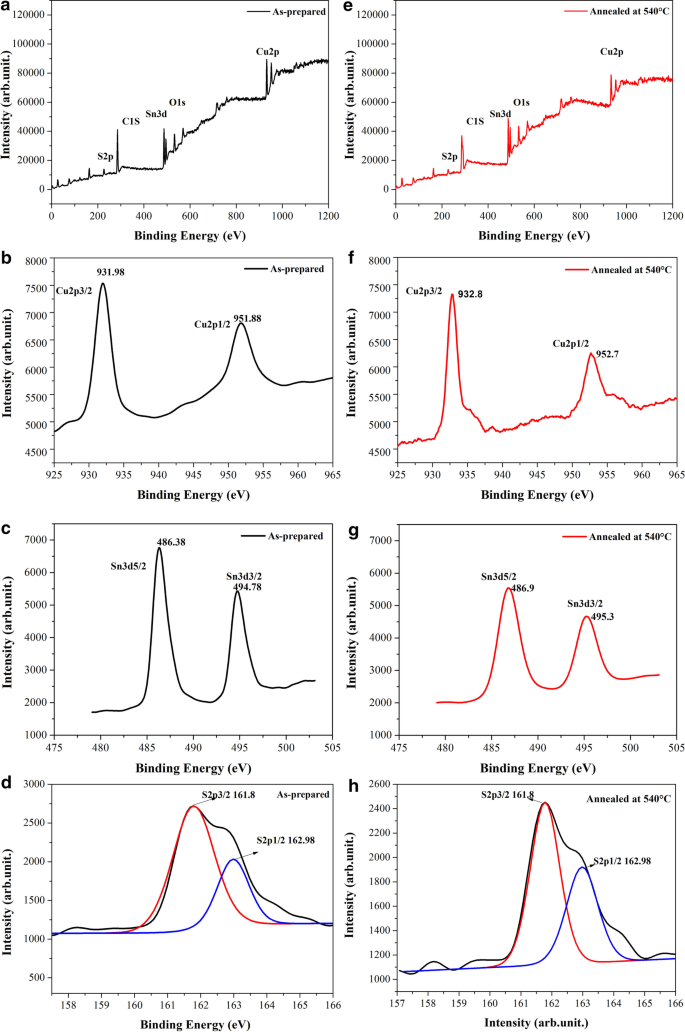
所制备的 Cu2SnS3 纳米粒子的 XPS 曲线:a 典型调查频谱,b Cu2p 核心层,c Sn3d 核心级别,以及d S2p 核心层面。退火后的 Cu2SnS3 纳米晶体的 XPS 光谱:e 典型调查频谱,f Cu2p 核心级别,g Sn3d 核心级别,以及h S2p 核心层
图 5 显示了从 2 到 0 V 以 0.1 mV s –1 的速率扫描的初始两个循环中获得的 Cu2SnS3 的 CV 图 .根据图 5a,在第一次锂嵌入过程中,所制备的 Cu2SnS3 纳米粒子在大约 1.09 处显示出较大的还原峰,即 Cu + 的价态 , Sn 2+ 变为 Cu、Sn。 1.62 V左右的大还原峰是H2O的还原峰,电流峰在第二个循环中逐渐消失。在脱锂过程中,氧化电流峰值出现在0.62 V对应式(1),Sn与Li离子形成LixSn,在第二个循环中,电流峰值基本保持不变。如图 5b 所示,在第一次锂嵌入过程中,在 540°C 下退火的 Cu2SnS3 纳米粒子在 1.1V 附近显示出一个大的还原峰,对应于公式(1)[33],其中 Cu2SnS3 被还原为 Cu 和 Sn,并且在第二个周期中,电流峰值逐渐增加到 1.59 V。低于 0.5 V 的驼峰对应于 Sn 到 Lix 的转化 Sn根据式(2)[33]。在脱锂过程中,氧化电流峰值出现在0.59和1.94 V,随着循环次数的增加,电流峰值基本保持不变。大约 0.59 V 处的阳极峰归因于 Lix Sn合金形成Sn,1.94V处的峰值对应于式(1)的逆反应[33]。不可逆容量损失由部分非晶态 Li2S 的形成不可逆地消耗 Li 引起,导致第一次和第二次循环之间的电位和峰值电流强度发生变化 [17]。相比之下,退火处理提高了Cu2SnS3纳米阳极的循环可逆性。
$${\text{Cu}}_{2} {\text{SnS}}_{3} + 6{\text{Li}}^{ + } + 6{\text{e}}^{ - } \leftrightarrow 2{\text{Cu}} + {\text{Sn}} + 3{\text{Li}}_{2} {\text{S}}$$ (1) $${\text{Sn }} + x{\text{Li}}^{ + } + x{\text{e}}^{ - } \leftrightarrow 4{\text{Li}}_{x} {\text{Sn}}\ quad \left( {0 \, \le x \le \, 4.4} \right)$$ (2) <图片>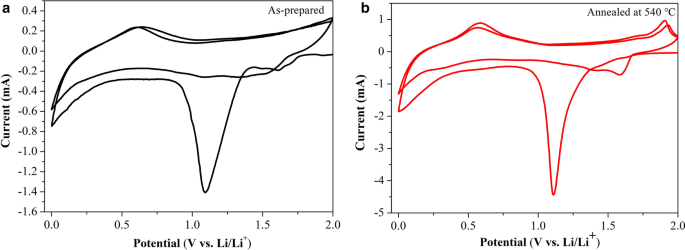
在 0 和 2 V 之间以 0.1 mV s –1 的速率扫描的初始两个循环的 CV 图 :a 准备好的和b 540℃退火
为了充分了解充放电过程,在电极上进行了 Cu2SnS3 上的非原位 XRD,如图 6 所示。 6 小时。然后在手套箱内拆开电池,用溶剂 DEC 清洗 Cu2SnS3 复合电极以去除电解质。第一次放电至 1.5 V 后,晶体结构在 1.5 V 处没有被破坏,如图 6b 所示,Cu2SnS3 复合电极的主要衍射峰与四方 Cu2SnS3 (JCPDS 89-4714) 的衍射峰匹配良好,并且没有检测到二次相。第一次放电至 0.05 V 后,图 6c,Cu2SnS3 的反射峰完全消失,Cu 峰变强,出现 Li2Sn5 峰。这种现象可以通过 CTS 分解成 Cu 和 Sn 纳米粒子,即形成 Sn 的 LixSn 来解释。充电至2 V时发生可逆过程,导致CTS相恢复,形成Cu4SnS4。
<图片>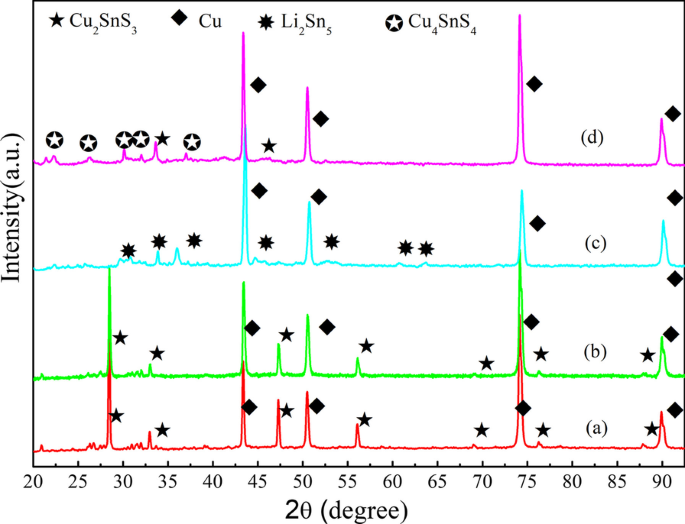
电极的非原位XRD图谱; 一 准备好的; b 首先放电至 1.5 V; c 首先放电至 0.05 V; d 第二次充电到 2 V
图 7 显示了 Cu2SnS3 电极在 OCV 下的 Nyquist 图,在 100 mA g -1 2 个循环后 (0–2 V)。在 OCV 下 Cu2SnS3 电极的奈奎斯特图中(图 7a,b),高频区域的半圆归因于电荷转移电阻 Rct,低频区域的直线斜线归因于 Li + 体 Zw 中的扩散过程 [18, 49]。退火后的 Cu2SnS3 电极的 Rct 小于制备好的电极的 Rct。在 2 个循环后的 Cu2SnS3 电极的奈奎斯特图中(图 7c,d),高频区域的半圆归因于 Li + 的电阻 通过表面膜 Rsei 扩散,中频区域的半圆分配给电荷转移电阻 Rct,低频区域的直线斜线归属于 Li + 体 Zw 中的扩散过程。实验数据由ZView软件模拟,根据等效电路得到,数值列于表1。我们可以发现,制备和退火的欧姆电阻(Rs)没有显着差异Cu2SnS3。然而,退火后的 Cu2SnS3 的 Rsei 和 Rct 值远小于制备好的 Cu2SnS3。特别是,原始样品的 Rct 在 OCV 下为 162.4Ω,并在 2 个周期后急剧增加到 206.6Ω。相比之下,退火样品的 Rct 在 OCV 下为 39.7Ω,并在 2 个循环后急剧下降至 25.9Ω。退火工艺可以抑制SEI层和电荷转移阻力,从而促进电荷转移和离子传导。因此,退火后的Cu2SnS3的电化学性能得到改善。
<图片>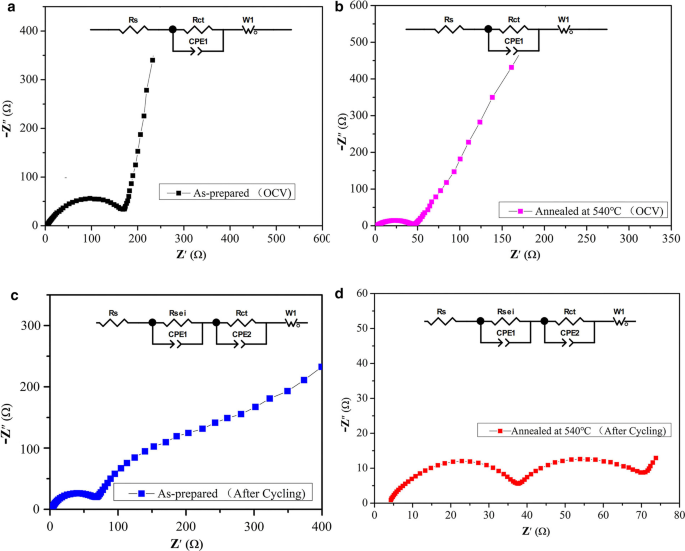
在 100 mA g -1 2 个循环后,在 OCV 下制备和退火的 Cu2SnS3 电极的 Nyquist 图 (0–2 V)
如图 8a、b 中的 SEM 图像所示,经过 5 次循环后,退火后的 Cu2SnS3 的形状没有改变,显示球形纳米粒子聚集形成不规则的球状附聚物。元素映射图像显示了复合材料中 Cu、Sn 和 S 元素的清晰轮廓(图 8d-f,h-j)。结果表明,经过5次循环后,退火后的CTS电极中Cu、Sn和S元素分布均匀。
<图片>
退火后的 Cu2SnS3 纳米粒子的 SEM 图像:a 在 OCV,b 5个循环后。 d 的 EDX 元素映射 铜,e Sn 和 f OCV 下退火 CTS 电极的 S,h 铜,i Sn 和 j 5次循环后退火CTS电极的S
在 100 mA g –1 记录了所制备和退火的 Cu2SnS3 电极的恒电流充放电曲线(图 9a、b) 在 2 到 0 V 的电位范围内(相对于 Li/Li + )。 654和809 mA的初始放电容量 g –1 分别对应于 42% 和 53% 的初始库仑效率。不可逆容量的损失可能归因于 SEI 膜和 Li2S 的形成。显然,退火处理提高了Cu2SnS3电极的放电容量和初始库仑效率。
<图片>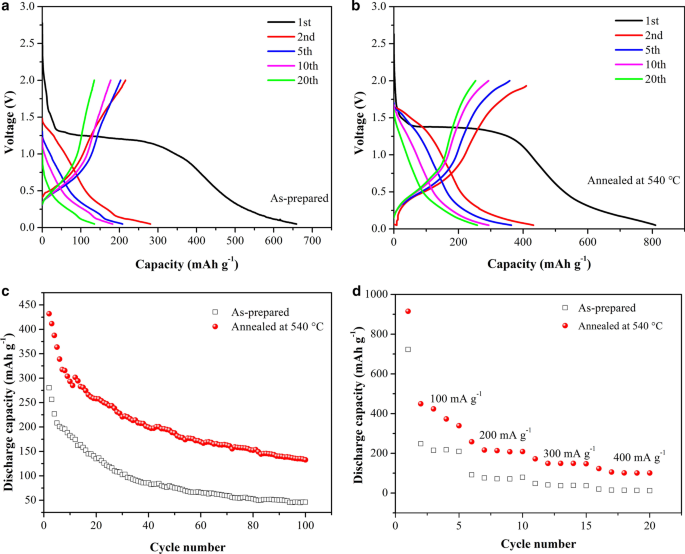
Cu2SnS3 电极的充放电曲线 (100 mA g −1 ):a 准备好的和b 在 540 °C 和 c 下退火 循环性能(100 mA g −1 ); d 不同电流密度(100 至 400 mA g -1 )下制备和退火的 Cu2SnS3 电极的倍率性能 )
制备和退火的 Cu2SnS3 电极在恒定 100 mA g –1 下循环 100 次的循环性能 如图 9c 所示。很明显,退火后的 Cu2SnS3 电极的放电比容量总体上优于制备好的电极。 50次循环后退火Cu2SnS3电极的容量为187.7 mAh g -1 , 高于所制备的电极 (75.2 mAh g −1 )。退火复合材料的容量保持率几乎等于或优于中空微球 Cu2SnS3 和 Cu2SnS3 纳米片的报道 [34, 50]。但容量保持率远低于 Cu2SnS3/RGO 复合材料(561 mAh g −1 100 次循环后)[33]。退火工艺已被证明可以提高Cu2SnS3的循环性能,但在后续研究中还需结合其他改性方法进一步提高其性能。
如图 9d 所示,所制备的 Cu2SnS3 电池的最大放电容量约为 222、78、40 和 14 mAh g –1 在 100、200、300 和 400 mA g –1 率,放电容量保持率仅为 6%。相比之下,退火后的 Cu2SnS3 电池的放电比容量分别为 396、221、153 和 106 mAh g –1 在 100、200、300 和 400 mA g –1 分别具有 26.8% 的放电容量保持率。显然,退火处理提高了 Cu2SnS3 的结晶度并导致更稳定的晶体结构。 Cu2SnS3 是多晶的,因此包含许多晶界。在充放电过程中,内部颗粒体积膨胀产生的机械应力可以通过晶界的滑动得到缓冲,从而减少材料的破裂和粉化,稳定电极结构。这有利于提高纳米Cu2SnS3负极的循环稳定性和倍率特性。
结论
Cu2SnS3 作为一种通过引入惰性 Cu 形成合金而制成的高容量 Sn 基负极的改性材料,在锂离子电池应用中具有巨大的潜力。在 540 °C 下退火会增加 Cu2SnS3 纳米颗粒的结晶度,并导致更稳定的晶体结构。高温退火处理提高了Cu2SnS3的电化学性能,与制备的样品相比,具有更高的初始库仑效率和循环和倍率特性。
数据和材料的可用性
作者声明,材料和数据可立即提供给读者,无需材料转让协议中的不当资格。本研究中生成或分析的所有数据均包含在本文中。
缩写
- PVDF:
-
聚偏二氟乙烯
- HRTEM:
-
高分辨透射电子显微镜
- EC:
-
碳酸亚乙酯
- EMC:
-
乙基甲基碳酸酯
- DEC:
-
碳酸二乙酯
- 简历:
-
循环伏安法
- XPS:
-
X射线光电子能谱
- SEM:
-
扫描电子显微镜
- EDX:
-
能量色散X射线
- OCV:
-
开路电压
- FWHM:
-
半高全宽
- XRD:
-
X射线衍射
纳米材料
- 石墨烯将纳米材料放在自己的位置
- 半导体纳米粒子
- 锂离子电池用Cr3+和F-复合掺杂LiNi0.5Mn1.5O4正极材料的合成及电化学性能
- 磁性纳米粒子组装中的相互作用
- 富勒烯衍生纳米材料及其聚合物复合材料的顺磁特性:剧烈泵出效应
- 双层厚度对 Al2O3/ZnO 纳米层压材料的形态、光学和电学特性的影响
- 不同粘合剂对锂离子电池金属氧化物阳极电化学性能的影响
- 天然和合成纳米材料的电化学、生物医学和热特性的比较研究
- 评估由食用菌根真菌 Tricholoma crassum 合成的蛋白质包覆金纳米粒子的抗菌、凋亡和癌细胞基因传递特性
- 溶胶-凝胶法合成的 Pr 掺杂钙钛矿锰酸盐 La0.67Ca0.33MnO3 纳米颗粒的微观结构、磁性和光学性能
- 纳米颗粒的尺寸和聚集/团聚对聚合物纳米复合材料的界面/相间性质和拉伸强度的影响
- C# - 属性


