结合绿原酸对硒纳米颗粒在体外抑制淀粉样蛋白 β 聚集和活性氧物种形成的增强作用
摘要
淀粉样蛋白-β (Aβ) 斑块的沉积和神经毒性活性氧 (ROS) 的形成是阿尔茨海默病 (AD) 的重要病理特征。在此,报道了一种将硒纳米颗粒独特的 Aβ 吸收特性与天然抗氧化剂绿原酸 (CGA) 相结合形成 CGA@SeNPs 的新策略。体外生物学评价表明,CGA可以清除Aβ40聚集体诱导的ROS,但不能抑制Aβ40聚集体引起的Aβ40聚集和细胞膜损伤。有趣的是,CGA@SeNPs 对 Aβ40 聚集显示出增强的抑制作用,更重要的是,保护 PC12 细胞免受 Aβ 聚集诱导的细胞死亡。相信在长期使用中,CGA@SeNPs在降低Aβ40毒性方面比CGA更有效。
背景
阿尔茨海默病 (AD) 是一种不可逆的进行性神经退行性疾病,其特征是进行性认知障碍和神经元丢失[1]。现在人们普遍认为,大脑中细胞外淀粉样斑块的积累是 AD 的常见病理特征 [2, 3]。斑块含有淀粉样蛋白-β (Aβ) 蛋白的错误折叠和聚集 [4]。虽然 Aβ 原纤维或寡聚体在 AD 发病机制中的确切作用尚不完全清楚,但越来越多的证据表明,它们中的大多数是导致神经元功能障碍和死亡的有毒物质 [5,6,7,8]。此外,Aβ 聚集体已经存在于 AD 患者的大脑中。这些聚集体将继续形成神经毒素活性氧(ROS),这将引发一系列细胞成分如 DNA、脂质和蛋白质的损伤,并导致 AD 中的氧化应激[9]。神经元的损伤通常会导致学习和记忆缺陷。因此,预计抑制β淀粉样蛋白聚集和活性氧的形成可能是预防或减轻AD病理的有希望的治疗靶点。
纳米材料具有独特的物理化学性质,如体积小、表面积大、反应活性高。最近,研究强调通过适当的表面修饰,纳米颗粒 (NPs) 可用作药物递送、成像和 AD 治疗应用的工具 [10,11,12]。通常,NPs 具有较大的表面积,这带来了很大的吸附能力。具体来说,Aβ 可以与一些 NPs 结合以延缓 Aβ 的纤维化过程。例如,Aβ 单体与多金属氧酸盐的结合会降低游离单体的浓度,并使平衡远离原纤维化 [13]。在这些纳米材料中,硒纳米粒子 (SeNPs) 显示出多种特性,使其非常适合生物医学应用,例如直接制备和稳定性。硒是一种必需的微量元素,在细胞氧化还原调节、解毒和免疫系统保护中起着重要作用[14]。因此,与无机和有机硒化合物相比,SeNPs具有更好的生物相容性和更低的毒性[15]。如今,NPs 的表面修饰促进了 NPs 和 Aβ 之间的结合亲和力,并有助于修复共轭分子的生化特性。我们之前的研究发现,通过将抗淀粉样肽 (LPFFD) 嫁接到 SeNP 表面,可以进一步增强 SeNP 的抗淀粉样蛋白能力 [12]。然而,这些研究大多没有关注纳米颗粒表面改性后的抗氧化能力。
绿原酸 (CGA) 是苹果、梨和浆果等水果中的主要多酚成分,在咖啡中含量尤为丰富 [16]。 CGA 具有许多药理特性,例如抗癌、抗炎和抗菌 [16]。特别是,CGA 具有抗氧化和神经保护活性,可用于治疗阿尔茨海默病 [17, 18]。然而,从未报道过 CGA 对 Aβ 聚集的影响。此外,CGA 的使用受到其低生物利用度和稳定性的限制,从胃肠道吸收的 CGA 只有三分之一到达血液循环[19]。多项研究报告称,由于纳米颗粒体积小,它们可以通过吸入、摄入和在整个循环中运输到许多器官直接进入血液。因此,为了解决这个问题,我们探索了 CGA 与 SeNPs (CGA@SeNPs) 的结合,以提高 CGA 的潜在治疗效果。在这种情况下,本研究的目的是研究 CGA@SeNPs 在抗 Aβ 聚集和抗氧化方面的潜在治疗功效。据我们所知,之前没有使用 CGA@SeNPs 治疗 AD 的报道。
方法/实验
材料和细胞系
Aβ40 是在 GL Biochem Ltd.(中国上海)合成的。二氧化硒 (Na2SeO3)、NaBH4、噻唑蓝四唑溴化物 (MTT)、硫黄素 T 和 2',7'-二氯二氢荧光素二乙酸酯 (DCFH-DA) 来自 Sigma(美国密苏里州圣路易斯)。 CGA 购自 Aladdin(中国上海)。 Dulbecco 改良 Eagle 培养基 (DMEM)、胎牛血清 (FBS) 和马血清购自 Gibco (Life Technologies AG, Switzerland)。 PC12 细胞(大鼠嗜铬细胞瘤,美国典型培养物保藏中心)在补充有 5% FBS 和 10% 马血清的 DMEM 培养基中在 37°C 下在 5% CO2 加湿环境中在 37°C 下培养。
CGA@SeNPs 的制备
首先,制备 25 mM CGA、0.1 M Na2SeO3 和 0.1 M NaBH4 的储备溶液。然后,将 200 μL 的 Na2SeO3 溶液与不同体积的 CGA 混合,Na2SeO3 与 CGA 的反应物浓度比为 1:1、1:2、1:4、1:6 和 1:8。之后,将 200 μL 0.1 M NaBH4 添加到混合物中并搅拌 30 分钟。溶液的颜色变为红色。通过透析去除过量的 CGA 和 Na2SeO3。我们发现Na2SeO3与CGA的最佳浓度比为1:6。
CGA@SeNPs 的表征
通过透射电子显微镜(TEM;Hitachi,H-7650)、傅立叶变换红外光谱(FT-IR;Equinox 55 IR 光谱仪)和紫外可见光谱(Carry 5000 分光光度计)对制备的 CGA@SeNP 进行表征。粒度分布由 Zetasizer Nano ZS 颗粒分析仪(Malvern Instruments Limited)测定。使用 JASCO FP6500 分光光度计 (λ 前 =350 纳米)。
H2O2 生成分析
羟基自由基,2, 29-azinobis-(3-ethylbenzothiazoline-6-sulfonic acid) (ABTS + ),并通过商业试剂盒(南京建成生物工程研究所,南京,中国)分析 CGA 和 CGA@SeNPs 的超氧阴离子清除活性。样品的还原能力测量如下:将 2 mL CGA 或 CGA@SeNPs 与 2 mL 磷酸盐缓冲液(0.2 mol/L,pH 6.6)和 2 mL K3Fe(CN)6(1%,<我>w /v ) 在 50°C 下保持 20 分钟。之后,通过加入 2.5 mL 三氯乙酸 (10%, w /v ) 并以 3000 rpm 离心 10 分钟。将 2 mL 上清液与 2 mL 蒸馏水和 1 mL FeCl3 (0.1%, w /v ) 在室温下放置 10 分钟。最后,在 700 nm 处测量吸光度。维生素c(Vc)作为抗氧化活性测定的阳性对照。
通过 DCFH-DA 分析 Aβ40 中的 H2O2 生成。 DCFH-DA 原液 (1 mM) 购自 Beyotime Institute of Biotechnology(中国上海)。在缓冲液(20 mM Tris-HCl/150 mM NaCl,pH 7.4)中制备了 4 微摩尔的辣根过氧化物酶 (HRP)。含有 35 μM Aβ40 的样品溶液(含或不含 20、40 和 60 μg/mL CGA@SeNPs/CGA)在 37°C 下孵育 3 天。将抗坏血酸 (10 μM) 添加到每个样品中并进一步孵育 1 小时。通过将 DCFH-DA(20 μL,100 μM)和 HRP(2 μL,0.04 μM)添加到样品溶液(10 μL)中来进行样品分析。激发和发射波长为488和525 nm的荧光光谱由JASCO FP6500分光荧光计测量。
硫黄素 T 荧光测量
通过使用染料硫黄素 T (ThT) 检测 Aβ40 纤维化的动力学。简而言之,35 μM Aβ40 与 20、40 和 60 μg/mL CGA@SeNPs/CGA 在 37°C 下孵育 0 至 5 天。每天取出 50 μL 溶液并加入 200 μL ThT 溶液(50 mM PBS 中的 15 μM ThT,pH 7.4)。然后,ThT的激发波长为440 nm,记录发射波长为490 nm。
TEM
通过 TEM (Hitachi, H-7650) 在存在或不存在 CGA@SeNPs/CGA 的情况下观察 Aβ40 的形态。样品的制备方法与 ThT 荧光测定法相同。孵育 3 天后,将 10 μL 样品溶液点在碳涂层铜网上 10 分钟。然后,每个网格用 1.5% (w /v ) 磷钨酸 (pH 7.4) 并使其干燥。
TEM 也证实了纳米粒子与 Aβ40 的结合。首先,将 35 μM Aβ40 孵育 3 天以形成纤维。然后,将 20 μg/mL 纳米颗粒添加到预孵育溶液中并再孵育 6 小时。之后,对该样品进行了透射电镜检查。
共振光散射测量
根据Yu等人的方法测量共振光散射(RSL)。 [20] 做了一些修改。一定量的 Aβ40 分散体用水稀释至 1 mL,而 CGA@SeNPs 的最终浓度从 0.05 到 0.45 μg/mL 不等。将混合物温育 10 分钟。通过同步扫描激发和发射单色器(Δλ =0 纳米)在 200 和 800 纳米之间。激发和发射狭缝宽度均设置为 5 nm。
细胞毒性分析
使用MTT法分析细胞活力。 PC12 细胞以每孔 5000 个细胞的密度接种在不含 FBS 的新鲜培养基中的 96 孔板上。 Aβ (35 μM) 与或不与 60 μg/mL CGA@SeNPs/CGA 共孵育 3 天。之后,用这些样品再处理细胞 72 小时。孵育后,按照 Cell Titer 96 Aqueous One Solution 细胞增殖测定 (Promega) 的手册,用每孔 10 μL MTT 处理细胞。使用商业检测试剂盒测定乳酸脱氢酶(LDH)的释放。如上处理PC12细胞。处理结束时,96孔板以1500×g离心 10 分钟。上清液中的LDH活性按照制造商的说明进行测定。
细胞内活性氧生成
通过 DCFH-DA 测定监测 CGA@SeNPs/CGA 对 Aβ40 诱导的细胞内 ROS 生成的影响。 PC12 细胞 (1 × 10 5 每个孔)以与 MTT 测定相同的方式处理。然后,将细胞用 PBS 洗涤两次,并与 DCFH-DA (10 mM) 在 37°C 下孵育 30 分钟。在荧光显微镜(放大倍数 × 200)下检测细胞内 ROS 水平,激发和发射波长分别为 488 nm 和 525 nm。为了测量细胞内 ROS 水平,细胞以相同的方式处理并通过离心收获,重新悬浮在 PBS 中。然后通过流式细胞术分析细胞。
TUNEL-DAPI 共染色分析
PC12 细胞的处理方式与 MTT 分析相同。之后,室载玻片中的细胞用 3.7% 甲醛固定,并用 0.1% Triton X-100 的 PBS 进行透化。根据制造商的方案,通过使用末端转移酶 dUTP 切口末端标记(TUNEL)测定试剂盒(KeyGen BioTECH,南京,中国)进行染色测定。图像采用荧光显微镜(放大倍数×200)拍摄。
统计数据
使用单向方差分析 (ANOVA) 和 Bonferroni 事后检验估计统计显着性。统计显着性设为P <0.05.
结果与讨论
CGA@SeNPs 的表征
在这项研究中,我们使用一种简单的方法通过用 NaBH4 还原 CGA 和 Na2SeO3 的混合物来合成 CGA@SeNP。尺寸在 30 到 150 nm 之间的纳米颗粒更有利于细胞摄取 [21]。 TEM 显示 CGA@SeNPs 具有直径约 100 nm 的球形结构(图 1a),表明 CGA@SeNPs 的尺寸适合生物应用。元素组成分析表明,在 CGA@SeNPs 的能量色散 X 射线光谱(EDX)图中可以很容易地找到 Se、C 和 O(图 1b)。 Se原子的信号为30.00%,CGA的C原子信号强(52.60%)和O原子信号(1.50%),表明我们成功制备了CGA@SeNPs。
<图片>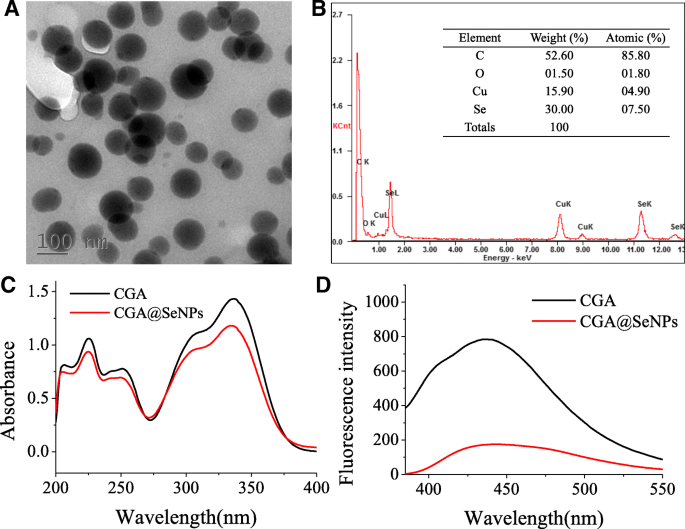
CGA@SeNPs 的表征。 一 CGA@SeNPs 的 TEM 图像。 b CGA@SeNPs 的 EDX 分析。 c CGA@SeNPs的紫外可见吸收光谱。 d CGA@SeNPs的发射光谱
CGA 的 UV-vis 吸收光谱在 334 nm 处显示出特征吸收峰(图 1c)。然而,在 CGA@SeNPs 的 UV-vis 吸收光谱中观察到轻微偏移,吸收峰变为 337 nm。 CGA和CGA@SeNPs的发射波长由荧光分光光度计检测。 CGA 的发射波长为 442.9 nm,在 CGA@SeNPs 中变为 437.5 nm(图 1d)。这些结果证实了 SeNP 表面存在 CGA。 CGA@SeNPs 的 FT-IR 光谱证明 CGA 已形成纳米复合材料的一部分。 O-H 伸缩频率位于 3353.99 cm −1 在 CGA 的 FT-IR 光谱中(附加文件 1:图 S1);然而,CGA@SeNPs 中的这个特征峰变成了 3419.00 cm -1 .这一转变证实了CGA通过-OH基团与SeNPs表面结合。
CGA@SeNPs 在生理条件下的稳定性对于评估它们未来的应用很重要。因此,在室温下监测 CGA@SeNPs 在 PBS(pH 7.4)中的大小分布 7 天。如附加文件 1:图 S2 所示,CGA@SeNPs 的尺寸保持稳定,平均尺寸约为 100 nm,并且 CGA@SeNPs 在 7 天内在 PBS 中保持良好的水分散性。 CGA@SeNPs良好的稳定性支持其在医学领域的潜在应用。
ROS 生成的抑制
沉积的 Aβ 可以激活小胶质细胞并刺激小胶质细胞产生神经毒素,如 ROS,这会进一步导致大脑中严重的神经元损伤 [22]。此外,过氧化氢 (H2O2) 等 ROS 也可以由 Aβ 聚集体产生 [23]。因此,我们研究了 CGA@SeNPs 的抗氧化活性以及 CGA@SeNPs 对 Aβ 聚集体诱导的 H2O2 形成的影响。如附加文件 1:图 S3 所示,CGA@SeNPs 以浓度依赖的方式对自由基具有很强的清除活性。当浓度达到 60 μg/mL 时,羟基自由基 ABTS + 和超氧阴离子清除活性分别达到 70.3%、95.2% 和 95.1%。显然,CGA@SeNPs 的还原能力随着浓度的增加而增加。在所有样品中,CGA@SeNPs对羟基自由基ABTS + 表现出很强的还原能力和清除能力 和超氧阴离子比 Vc 和 CGA。这些结果表明 CGA@SeNPs 显示出更高的抗氧化活性,这可能有助于清除 AD 中的活性氧。需要注意的是,CGA对SeNPs的修饰对抗氧化活性有协同作用。
通过 DCFH-DA 测定研究了 CGA@SeNPs 对 Aβ 介导的 H2O2 生成的影响 [24],这可以表明在存在或不存在 CGA@SeNPs 的情况下从 Aβ 生成 H2O2。如图 2 所示,CGA@SeNPs 和 CGA 以剂量依赖性方式降低 H2O2。更重要的是,含有CGA@SeNPs的Aβ样品比含有CGA的样品显示出更少的H2O2,表明CGA@SeNPs的高抗氧化活性在减少Aβ诱导的H2O2生成方面比CGA显示出更大的效果。
<图片>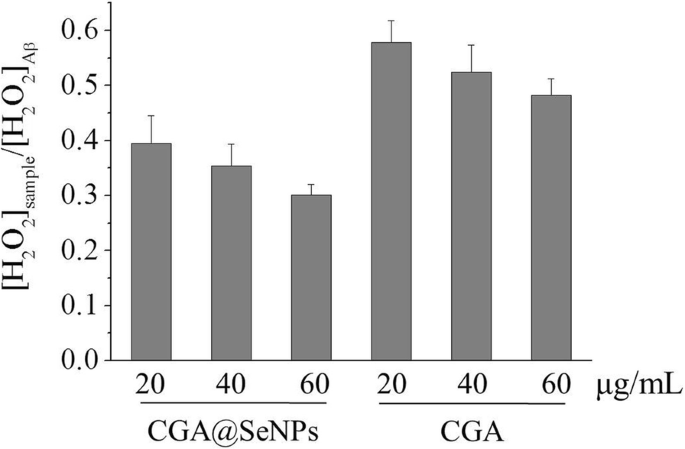
在存在或不存在纳米颗粒的情况下,Aβ40 反应生成 H2O2。 Aβ =35 μM,纳米颗粒/CGA =20、40 和 60 μg/mL
CGA@SeNPs 抑制 Aβ 聚集
尽管 CGA 的抗氧化活性是众所周知的特性,但 CGA 的抗淀粉样蛋白聚集活性仍然未知。为了验证 CGA@SeNPs 用于 AD 治疗应用的可行性,首先通过基于 ThT 的荧光测定法研究了 CGA@SeNPs 对 Aβ 聚集的抑制作用,这是一种行之有效的方法,可以在连续的条件下监测 β-折叠形成。时间 [25]。如图 3a 所示,Aβ40 自发聚集,Aβ 原纤维的荧光逐渐增加,直到孵育 3 天达到平台期。我们观察到 CGA@SeNPs 能够随着浓度的增加缓慢聚集淀粉样蛋白。 Aβ40 纤维的荧光强度大约是与 60 μg/mL CGA@SeNPs 孵育的 Aβ40 的两倍。然而,在CGA中观察到ThT荧光强度变化很小或没有变化,表明CGA仅略微抑制Aβ40聚集。
<图片>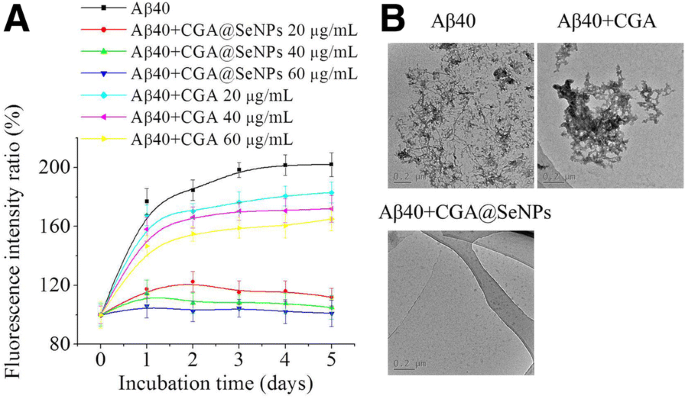
CGA@SeNPs 对 Aβ40 纤维化的抑制作用。 一 在存在或不存在纳米颗粒/CGA 的情况下,0 到 5 天 Aβ40 原纤维形成的 ThT 荧光。 Aβ40 =35 μM,纳米颗粒/CGA =20、40 和 60 μg/mL。 b Aβ40 在有或没有纳米颗粒或 CGA 的情况下孵育 3 天的形态。 Aβ40 =35 μM,纳米颗粒/CGA =60 μg/mL
在有或没有 CGA 或 CGA@SeNPs 的情况下孵育的 Aβ40 的形态变化如图 3b 所示。在 3 天内孵育的 Aβ40 形成了丰富的原纤维,而在 CGA@SeNPs (60 μg/mL) 的存在下,没有形成原纤维。正如预期的那样,CGA 没有显着抑制 Aβ 原纤维生成,而在 CGA 处理的 Aβ40 溶液中观察到大量聚集体,这与 ThT 荧光测定法一致。这些结果表明,在SeNPs上修饰CGA后,可以明显减少β-折叠的形成。
CGA@SeNPs 与 Aβ40 的结合活性
为了更好地了解 CGA@SeNPs 对 Aβ 聚集的抑制活性,我们研究了 CGA@SeNPs 对 Aβ40 的结合亲和力。首先,为了在超微结构水平上评估纳米粒子与 Aβ40 纤维的结合,将 Aβ40 纤维与 CGA@SeNPs 一起孵育。我们观察到原纤维特异性地结合在 SeNPs 的表面上,而没有任何游离的未结合的悬浮纳米颗粒(图 4a)。
<图片>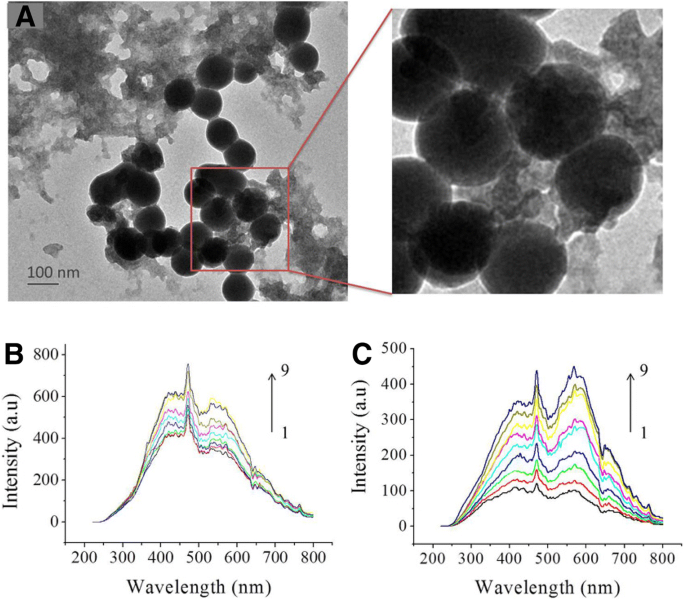
CGA@SeNPs 对 Aβ40 的亲和力。 一 CGA@SeNPs 对 Aβ40 纤维的结合能力。将 Aβ40 的执行纤维与 CGA@SeNPs 一起孵育并在 TEM 上进行检查。 Aβ40 =35 μM,CGA@SeNPs =60 μg/mL。 b Aβ40 单体的 CGA@SeNPs 的亲和力和指定。 Aβ40 单体在不同浓度 CGA@SeNPs 存在下的 RLS 光谱。 Aβ40 =600 nM,纳米颗粒浓度,1-9:0、0.05、0.1、0.15、0.2、0.25、0.3、0.35 和 0.4 μg/mL。 c CGA@SeNPs 的 RLS 光谱,纳米粒子浓度,1-9:0.05、0.1、0.15、0.2、0.25、0.3、0.35、0.4 和 0.45 μg/mL
共振光散射 (RLS) 是一种基于弹性光散射的强大光学技术,已广泛应用于研究纳米粒子在溶液中的大小、形状和分布 [26]。因此,我们接下来使用 RLS 来分析 Aβ40 单体和 CGA@SeNPs 之间的相互作用。如图 4b、c 所示,NPs 的 RLS 强度远低于与 600 nM Aβ40 单体在相同浓度下孵育的 NPs 强度。一旦 CGA@SeNPs 暴露于 Aβ 分子,Aβ 被认为通过含有氨基酸侧链的 N-供体结合在 SeNPs 的表面上,形成 Se-N 键 [27]。在 CGA@SeNPs 上形成 Aβ 分子的共轭物导致散射的大小增加,从而增强了系统的 RLS 强度(图 4b)。结合ThT测定和TEM的结果,推测大的CGA@SeNP表面与Aβ40单体之间的相互作用可能通过阻断单体之间的直接接触而导致不利于成核和原纤维生长的条件。因此,CGA@SeNPs在抑制Aβ40聚集方面比CGA发挥更大的作用。
抑制 Aβ40 神经毒性
通过 MTT 测定研究了 Aβ40 在 PC12 细胞中存在或不存在 CGA@SeNPs 的情况下的细胞毒性。图 5a 显示 Aβ40 纤维对 PC12 细胞有毒,这将细胞活力降低至 53%。在 CGA@SeNPs 的存在下,细胞的存活率增加到约 95%。然而,用 CGA 预处理细胞仅将细胞的存活率略微提高到 66%。此外,CGA@SeNPs 对 PC12 细胞无毒(附加文件 1:图 S4),表明 CGA@SeNPs 可以抑制 Aβ40 的神经毒性。
<图片>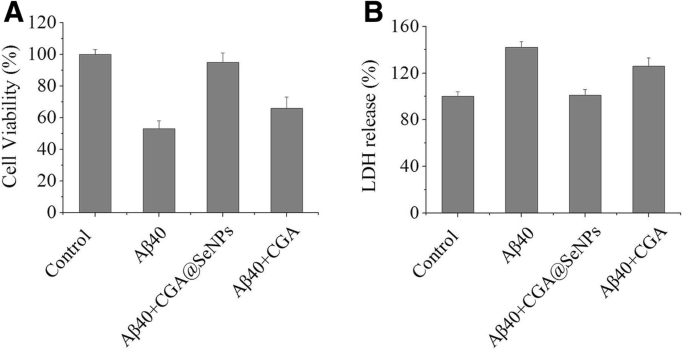
有或没有 CGA@SeNPs/CGA 孵育的 Aβ40 的神经毒性。 一 在 CGA@SeNPs 或 CGA 存在下,PC12 细胞对 Aβ40 的细胞活力通过 MTT 测定测试。 b LDH 释放到培养基中。 Aβ40 =35 μM,CGA@SeNPs/CGA =60 μg/mL
据报道,Aβ 优先固定在细胞表面并导致细胞膜损伤 [28]。因此,为了确定在存在或不存在 NPs/CGA 的情况下暴露于 Aβ40 后的细胞膜完整性,我们测量了细胞培养基中的细胞外 LDH 水平。在该测定中,高水平的 LDH 反映了细胞膜的损伤。如图 5b 所示,与对照相比,暴露于 Aβ40 后,LDH 释放增加到 142%。根据 MTT 的结果,在 CGA@SeNPs 的存在下,LDH 的释放减少到正常水平。有趣的是,我们观察到CGA并没有降低LDH浓度,表明CGA不能阻止PC12细胞受到Aβ聚集体诱导的细胞膜损伤。
预防 PC12 细胞中 Aβ40 诱导的 ROS 生成
Aβ 聚集体能够产生 ROS,这可能导致 AD 中的氧化应激 [29]。由于 CGA@SeNPs 的抗氧化和抗聚集特性,我们假设它能够减少 PC12 细胞中 Aβ40 诱导的 ROS 生成。因此,通过 DCFH-DA 测量 NPs 对 Aβ40 聚集体诱导的 ROS 生成的影响。 DCF 是一种源自非荧光 DCFH-DA 与 ROS 反应的荧光标记物,可指示 Aβ40 聚集体诱导的 ROS 的产生。如附加文件 1:图 S5 所示,相对于未处理的细胞,用 Aβ40 聚集体处理导致 ROS 含量增加 1.5 倍以上。 CGA@SeNP 处理降低了 PC12 细胞中的 DCF 荧光强度,表明 CGA@SeNPs 将 Aβ 原纤维诱导的 ROS 降低到正常水平。有趣的是,CGA 也减少了 PC12 细胞中 ROS 的产生,但不如 CGA@SeNPs 明显。
预防 PC12 细胞中 Aβ40 诱导的细胞凋亡
据报道,由 Aβ 原纤维引起的神经元细胞死亡是 AD 病理学中的一个关键事件 [30]。为了进一步研究 Aβ40 原纤维的细胞毒性,我们进行了 TUNEL-DAPI 共染色以确定 NPs 或 CGA 在 Aβ40 诱导的细胞凋亡中的作用。 DNA 片段化是细胞凋亡的标志,可以在细胞凋亡的早期阶段使用 TUNEL 检测到 [31]。如图 6 所示,TUNEL 将凋亡细胞核染成明亮的荧光绿色。 Aβ40 显着增加了 TUNEL 染色的细胞核数量,而 CGA@SeNP 处理导致 TUNEL 阳性细胞核减少,表明 CGA@SeNPs 可以保护神经元免受 Aβ40 诱导的 PC12 细胞凋亡。否则,细胞中高水平的 ROS 也会参与细胞凋亡 [32]。因此,这些结果表明 Aβ40 引起的细胞凋亡可能归因于 ROS 的产生。值得注意的是,CGA 还可以减少 Aβ40 诱导的细胞凋亡。从 MTT 和 LDH 测定来看,CGA 没有提高细胞的存活率并减少 Aβ 聚集体诱导的细胞膜损伤。结合TEM和ThT检测结果,我们发现CGA具有抗氧化特性,可以清除Aβ聚集过程中的活性氧,但不能完全抑制Aβ聚集。因此,CGA 可以减少孵育液和 PC12 细胞中 ROS 的产生,保护 ROS 诱导的细胞凋亡,但不能减少 Aβ 聚集体诱导的细胞膜损伤。细胞膜损伤会导致细胞内内容物泄漏到周围组织中,从而导致组织损伤和炎症[33]。因此,结合抑制Aβ聚集和活性氧的形成可作为一种新的治疗方法。
<图片>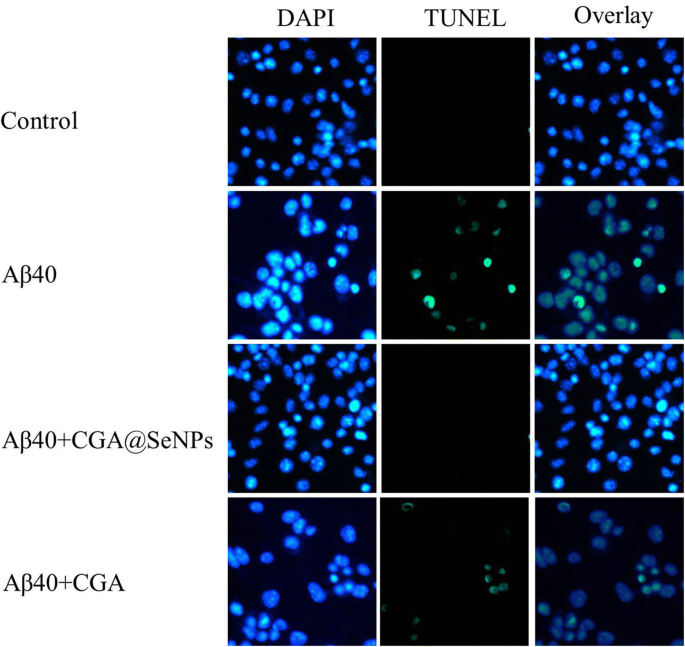
CGA@SeNPs 阻止 Aβ40 诱导的 PC12 细胞凋亡。 TUNEL-DAPI共染色法检测细胞凋亡。正常细胞核被染成蓝色,DNA片段被染成绿色。 Aβ40 =35 μM,CGA@SeNPs/CGA =60 μg/mL
结论
综上所述,CGA具有抗氧化药理作用,但对抑制Aβ纤颤没有作用。 SeNPs 上 CGA 的表面改性赋予其新的抗聚集特性。 Aβ40 可以结合在 CGA@SeNPs 的表面,这通过阻断单体之间的直接接触导致不利于成核和原纤维生长的条件。在这种情况下,CGA@SeNPs 抑制 Aβ40 聚集,清除 ROS,并保护 PC12 细胞免受 Aβ40 聚集体诱导的细胞膜破坏和 ROS 介导的细胞凋亡。然而,在CGA组中,Aβ聚集体固定在细胞表面并引起细胞膜损伤,这也导致细胞死亡。总体而言,长期使用CGA@SeNPs在降低Aβ40毒性方面比CGA更有效。
缩写
- ABTS + :
-
2, 29-Azinobis-(3-ethylbenzothiazoline-6-sulfonic acid)
- 广告:
-
阿尔茨海默病
- Aβ:
-
淀粉样蛋白-β
- CGA:
-
绿原酸
- DCFH-DA:
-
2',7'-二氯二氢荧光素二乙酸酯
- DMEM:
-
Dulbecco改良Eagle培养基
- EDX:
-
能量色散X射线光谱
- FBS:
-
胎牛血清
- FT-IR:
-
傅里叶变换红外光谱
- HRP:
-
辣根过氧化物酶
- LDH:
-
乳酸脱氢酶
- MTT:
-
噻唑蓝溴化四唑
- ROS:
-
活性氧
- RSL:
-
共振光散射测量
- SeNP:
-
硒纳米颗粒
- TEM:
-
透射电子显微镜
- ThT:
-
硫黄素T
- TUNEL:
-
末端转移酶dUTP缺口末端标记
- Vc:
-
维生素c
纳米材料
- 将活性氧种类的毒性调整到高级肿瘤治疗中
- 小型硒纳米晶体和纳米棒的简便合成和光学特性
- Sb/坡缕石 (PAL) 纳米颗粒的制备和增强催化氢化活性
- 在 Au 纳米颗粒修饰的玻碳电极上增强光电化学检测尿酸
- 纳米颗粒作为外排泵和生物膜抑制剂,恢复常规抗生素的杀菌效果
- 以叶酸受体为靶点的生物类黄酮染料木素负载壳聚糖纳米颗粒可增强对宫颈癌的抗癌作用
- Au 纳米颗粒对 HT29 和 SPEV 细胞系影响的体外研究
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- Dy2O3 和 Ca 共掺杂剂对增强稀土丰富的 RE-Fe-B 磁体矫顽力的协同作用
- 酸性胶溶剂对 TiO2 纳米颗粒锐钛矿-金红石比和光催化性能的影响
- 基于叶酸和 gH625 肽的 Fe3O4 磁性纳米颗粒功能化增强细胞内化的比较
- 辣根过氧化物酶封装的空心二氧化硅纳米球用于细胞内活性氧种类的传感


