纳米颗粒作为外排泵和生物膜抑制剂,恢复常规抗生素的杀菌效果
摘要
细菌对抗生素的耐药性这一普遍问题反映了对医生控制感染的严重威胁。细菌的进化导致各种复杂的耐药机制的发展,以中和抗生素的杀菌作用,如药物改善、靶向修饰、膜通透性降低和药物通过外排泵挤出。外排泵获得了广泛的底物特异性,以及在细菌细胞外挤出药物分子的巨大功效。外排泵功能障碍可能会恢复传统抗生素的杀菌作用。外排泵还在排除或包含负责细菌细胞生物膜形成的群体感应生物分子方面发挥重要作用。细菌细胞内外的群体感应生物分子的这种转运运动可能会因阻碍外排泵的功能而中断。金属纳米粒子代表了阻断细菌细胞外排泵的潜在候选者。纳米粒子作为外排泵抑制剂的应用不仅有助于恢复传统抗生素的杀菌作用,还有助于降低微生物的生物膜形成能力。本综述着重于金属纳米粒子与常规抗生素协同抑制外排泵的一种新颖而引人入胜的应用。
评论
与生物膜相关的慢性感染难以根除,因为它们能够抵抗抗生素和宿主免疫系统 [1]。生物膜屏障是急性感染转为慢性感染的主要原因之一[2]。根据国家卫生研究院和疾控中心的报告,大约65-80%的疾病是由生物膜诱导细菌引起的,主要是革兰氏阴性菌铜绿假单胞菌 和大肠杆菌 和革兰氏阳性菌金黄色葡萄球菌 [3]。抗生素似乎对治疗具有生物膜的感染无效,因为它们穿过生物膜壁垒和清除目标细菌细胞的能力有限[4]。此外,细菌已经进化出一种独特的外排系统来排出细菌细胞外的有毒物质和废物 [5]。外排泵是膜结合转运蛋白,具有广泛的底物特异性和巨大的药物排斥能力[6]。
所有这些与生物膜和外排泵相关的疾病都会导致多重耐药 (MDR) 细菌或广泛耐药 (EDR) 细菌的出现;因此,纳米颗粒与常规抗生素结合被提议作为根除或破坏生物膜以及治疗 MDR 或 EDR 感染的替代方法。
这些新的抗菌剂,金属纳米粒子,不仅增强了现有抗生素的抗菌活性,而且还恢复了它们的杀菌活性。抗生素和金属纳米粒子的协同应用表现出更多的潜在抗菌作用,而不是单独应用[7, 8]。纳米颗粒与抗生素作为抗生物膜或外排泵抑制剂的应用已得到充分研究和探索 [1, 9,10,11]。金属纳米粒子因其低细胞毒性(浓度依赖)、高表面积和广谱抗菌活性而被广泛用于治疗人类细胞系的感染 [12,13,14]。此外,金属纳米颗粒与抗生素的联合应用降低了它们作为药物剂量的浓度,从而降低了两种药物对人类细胞系的毒性[15]。本综述强调了纳米颗粒与抗生素作为抗生物膜和外排泵抑制剂的协同应用,对此进行了广泛的研究,以对抗由 MDR 或 EDR 病原体引起的感染。
纳米粒子作为外排泵抑制剂
已经进行了各种研究来确定纳米颗粒作为杀菌剂的作用模式。然而,关于纳米颗粒对微生物的抑制作用机制的几点仍有待解决。纳米粒子杀菌活性的可能机制之一归因于外排泵的抑制。巴诺伊等人。 2010 年提出了氧化锌纳米颗粒对 S 的 NorA 外排泵的新型外排泵抑制作用。金黄色葡萄球菌 .他们发现在 S 中存在氧化锌纳米颗粒时,环丙沙星的抑菌圈增加了 27% 和 22%。金黄色葡萄球菌 和E。大肠杆菌 ,分别[16]。之后,Padwal 等人。 2014年提出了聚丙烯酸包覆的氧化铁(磁铁矿)纳米粒子(PAA-MNP)与利福平协同使用对抗耻垢分枝杆菌的概念 强调 PAA-MNP 的外排抑制作用。他们在M中使用了PAA-MNP和利福平的融合物。耻垢 与单独使用利福平相比,这导致了四倍的生长抑制。对常见的外排泵底物溴化乙锭的实时转运研究证明,细菌细胞内抗生素的积累增加了三倍,这可以解释这一点[17]。
金属纳米粒子可以通过两种可能的机制阻止外排泵的工作。一种可能的机制是金属纳米颗粒与外排泵的活性位点直接结合,阻止抗生素向细胞外排出。金属纳米颗粒在这里可以作为外排泵结合位点的抗生素竞争性抑制剂 [18]。另一种可能的机制是通过外排动力学的中断。银纳米粒子对 MDR 外排泵 MexAM-OPrM 外排动力学的破坏作用已在 P.绿脓 [19]。可能表明金属纳米粒子可能导致质子梯度终止,随后膜电位中断或质子动力 (PMF) 丧失,导致外排泵活动必不可少的驱动力退化 [18, 20, 21]。然而,纳米粒子与外排泵直接结合的主要限制是它们的小尺寸和反应性。此外,纳米颗粒还可能与其他膜蛋白结合,而不是简单地与外排泵相互作用,因此,纳米颗粒在暴露过程中每次与外排转运蛋白结合的机会受到限制。
克里斯汀娜等人。早先在他们关于铜纳米颗粒对 NorA 外排泵的外排抑制作用的研究中已经表明,部分原因是铜纳米颗粒产生了 Cu(II) 离子。这种直接来自铜纳米颗粒的部分效应可能意味着纳米颗粒与外排泵的直接相互作用,支持第一个假设,而由于 Cu(II) 离子释放的部分影响可能表明膜电位的破坏和外排泵的工作扰动,支持第二个假设[9]。查特吉等人。还揭示了E的膜电位损失。大肠杆菌 在分别存在 3.0 和 7.5 μg/ml 铜纳米颗粒的情况下培养细菌细胞 1 小时后,细胞从 -185 到 -105 和 -75 mV [22]。纳米颗粒抑制外排作用的明确机制仍令人费解,需要进一步研究。
纳米粒子作为抗生物膜剂
生物膜对细菌有抵抗力,但如果生物膜是由耐药细菌产生的,这种抵抗就会加剧[23]。许多研究表明,金属纳米颗粒具有通过各种作用模式分解厚生物膜屏障的巨大能力 [24,25,26,27]。金属纳米粒子的穿透力始终是利用它们对抗生物膜感染的有用特征 [28,29,30]。纳米粒子和抗生素这两种不同方式的独特融合,为对抗产生 MDR 或 EDR 细菌的生物膜开辟了新途径。
Gurunathan 等人进行了一项雄辩的研究。阐明不同抗生素与银纳米颗粒的增强杀菌和抗生物膜作用。氨苄青霉素和银纳米粒子的共生使用大大增强了革兰氏阴性菌和革兰氏阳性菌的生物膜抑制作用,分别提高了 70% 和 55%,而单独使用银纳米粒子处理后的生物膜抑制作用约为 20%。类似地,银纳米颗粒和万古霉素的联合应用分别导致革兰氏阴性菌和革兰氏阳性菌的生物膜抑制率分别为 55% 和 75% [10]。这些结果表明纳米颗粒与抗生素的替代应用诱导生物膜抑制开辟了新疗法的临床可能性。
对于与抗生素协同使用的铜纳米颗粒和氧化锌纳米颗粒也观察到类似的效果。根据这项研究,与氧化锌纳米颗粒和抗生素组合相比,铜纳米颗粒和抗生素的结合在革兰氏阳性菌和革兰氏阴性菌中显示出更有效的抗生物膜活性。这种对铜纳米颗粒的抑制作用增强可能是由于纳米颗粒产生的 Cu(II) 离子的挤出。铜纳米颗粒和氧化锌纳米颗粒与特定抗生素结合在 2% 葡萄糖存在下表现出增强的抗生物膜作用,揭示了在葡萄糖存在下金属纳米颗粒和抗生素之间的键合相互作用增加 [9]。用碳水化合物包覆金属纳米粒子可能会改变纳米粒子-细胞的相互作用、细胞摄取和细胞毒性[31]。
外排系统和群体感应之间的联盟
外排泵在生物分子的细胞间信号传导中发挥重要作用,以协助生物膜形成。对抗耐药性的一种可能机制是使用外排泵抑制剂来阻断群体感应机制,最终阻碍生物膜的形成。已经进行了几项研究来证明外排泵在群体感应中的作用 [23, 32,33,34,35,36,37,38,39]。外排泵与生物膜形成之间的明确机械关系仍未完全了解。一种可行的理由可能是外排泵的作用是挤出群体感应所需的关键组件。这个功能方面已经在早期的研究中提出 [40,41,42,43,44,45,46]。通过应用外排泵抑制剂对信号分子挤出的损害可能影响群体感应或细胞间信号传导的过程[47, 48](图1)。
<图片>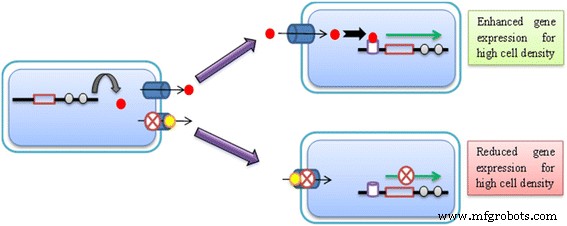
使用金属纳米粒子作为外排泵抑制剂来阻止群体感应信号分子的挤出(红色实心圆圈 )在金属纳米粒子的帮助下细菌细胞外(黄色实心圆圈 ) 阻塞外排泵(填充气缸 ) 导致信号分子与其受体的结合减少(空圆柱体 ) 和生物膜形成的障碍
另一个可行的理由可能是外排泵将有毒和废物副产品输出到细胞外的作用。生物膜中快速代谢的细胞可能依靠导电系统将细菌细胞内发生的各种生化活动产生的有害和废物副产物挤出[49]。 Kvist 等人进行的研究中也提出了这一功能方面。 2008 年 [50]。使用外排泵抑制剂来阻断这种导电系统可能会导致细菌细胞内有毒副产物的增加,最终减少生物膜的形成(图 2)。
<图片>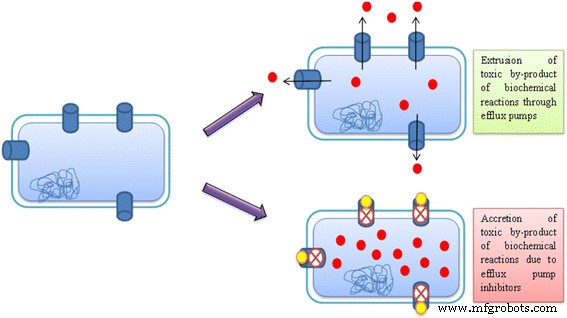
使用金属纳米粒子作为外排泵抑制剂来阻止生化反应的有毒副产物的排出(红色实心圆圈 )在金属纳米粒子的帮助下细菌细胞外(黄色实心圆圈 ) 阻塞外排泵(填充气缸 )导致生物膜形成障碍
一些研究还表明,外排泵会通过改变细胞膜特性并最终影响生物膜形成来影响细胞聚集 [47]。已经进行了大量研究来推断纳米颗粒与抗生素结合作为改进的抗菌剂和抗生物膜剂的作用。表 1 包含这些研究的摘要。
Barapatre 等人最近进行了一项研究,推断出银纳米粒子与阿米卡星、卡那霉素、土霉素和链霉素抗生素联合使用可增强协同抗菌和抗生物膜活性,以对抗革兰氏阳性菌和革兰氏阴性菌。以绿色化学为中心,通过结合两种木质素降解真菌,即黄曲霉,通过酶促还原硝酸银合成银纳米颗粒 和 Emericella nidulans .有人建议使用纳米颗粒作为探针与常规抗生素一起使用,以增强对病原微生物的抗菌和抗生物膜活性 [51]。据报道,外排泵抑制等 ATP 依赖性功能的破坏是抗生素和金属纳米颗粒协同作用的潜在机制之一 [52]。
许多报告已经成功地证明了纳米粒子可以对抗两种不同的细菌耐药机制,即 MDR 外排泵和生物膜形成,细菌通过这些机制逃避常规抗生素的作用。该综述代表了一种新的、有前景的方法,即利用金属纳米粒子与抗生素协同作为外排泵抑制剂和抗生物膜剂来对抗抗生素耐药性。
结论
在当前情况下,迫切需要一种控制耐多药感染的创新方法。外排泵具有双重作用,一是挤出抗生素,二是通过排出对群体感应很重要的生物分子来协助生物膜形成,最终导致细菌病原体的毒力。通过纳米颗粒阻断 MDR 外排泵将在两个方向上都有帮助;它阻止抗生素外流到细菌细胞外,从而增加常规抗生素的作用,同时,它阻止群体感应生物分子的外流,从而降低细菌细胞的生物膜形成能力。这种方法减少了进行新研究以研究新型外排泵抑制剂或新抗生素的需要,但鼓励使用金属纳米颗粒(用作外排泵抑制剂)与传统抗生素协同作用。它还有助于降低纳米粒子在人类细胞系中的成本、时间和细胞毒性问题,这些细胞系可以承受较低浓度的金属纳米粒子。这将是一种靶向外排泵、减少群体感应信号以抑制生物膜形成的新方法。
未来展望
细菌进化导致采用各种机制来恢复抗生素和宿主免疫系统的杀菌作用。它导致多重耐药性感染的产生,这反映出迫切需要发现对抗 MDR 或 XDR 感染的新方法。随着抗生素耐药性的出现,金属纳米粒子与常规抗生素的共生使用为对抗抗生素耐药性提供了更好的选择。纳米粒子作为外排泵抑制剂的应用在两个不同的方向上都非常重要,但最终只能达到一个结果,即对抗细菌感染。纳米粒子阻断外排泵的确切作用机制仍有待研究。 PMF 的破坏很可能是纳米颗粒抑制外排的一种可能的间接机制。这种方法的主要挑战之一与纳米颗粒的反应性有关,这可能使它们与其他膜蛋白而不是外排转运蛋白结合。这可以通过将目标纳米粒子与抗外排单克隆抗体或凝集素连接来制备目标纳米粒子来克服。这种适当的抑制将校准它们以专注于特定的区域。另一个相当大的挑战可能是毒性问题,使用这种方法是因为小尺寸纳米粒子的表面积与体积比很大,应该在最终验证之前进行优化。
纳米材料


