一种用于高灵敏度检测阿特拉津的新型磁弹性纳米生物传感器
摘要
在这里,我们首先报告了一种基于 ME 材料和金纳米粒子 (AuNPs) 的无线磁弹性 (ME) 纳米生物传感器,用于采用竞争性免疫测定法对莠去津进行高灵敏度检测。响应时变磁场,ME 材料以其共振频率纵向振动,这可能受其质量负载的影响。 ME 材料上的 AuNPs 涂层有助于其生物相容性、稳定性和灵敏度。阿特拉津抗体通过蛋白 A 定向固定在 AuNPs 包覆的 ME 材料表面,提高了纳米生物传感器的性能。原子力显微镜(AFM)分析证明阿特拉津抗体的固定化是成功的。此外,为了提高灵敏度,诱导阿特拉津-白蛋白偶联物(Atr-BSA)与阿特拉津竞争与阿特拉津抗体结合,放大信号反应。共振频移与莠去津浓度的对数成反比和线性正比,范围从 1 ng/mL 到 100 μg/mL,灵敏度为 3.43 Hz/μg mL -1 检测限为 1 ng/mL,明显低于美国环境保护署 (EPA) 制定的标准。实验结果表明,ME纳米生物传感器对阿特拉津表现出很强的特异性和稳定性。该研究为阿特拉津的快速、选择性和高灵敏度检测提供了一种新的便捷方法,对其在水质监测等环境检测领域的应用具有重要意义。
介绍
随着工农业的快速发展,越来越多的环境污染物被释放到生态环境中[1],引起了相关研究的广泛关注[2、3]。近年来,为了提高农田质量和产量,越来越多地使用除草剂,但许多除草剂可以在水和土壤中保持活性多年,造成严重的环境污染[4]。除草剂污染由于其在水或农产品中的生态污染而引起了相当大的关注[5]。在除草剂中,莠去津(2-chloro-4-ethylamino-6-isopropylamino-1, 3, 5-triazine)是世界范围内用于防治阔叶植物和禾本科杂草的最广泛的除草剂[6]。
阿特拉津虽然对一些多年生杂草有一定的抑制作用,但作为环境污染物,它具有剧毒[7],可能对人类和其他动物物种造成健康风险[8]。长期高浓度的阿特拉津摄入会损害动物或人类的健康,例如癌症、先天缺陷以及对心脏和肝脏的损害 [9, 10]。美国、欧盟和日本都将莠去津列入内分泌干扰化学品清单[11]。在美国,环境保护署 (EPA) 允许饮用水中莠去津的允许限量为 3 μg/L(终身健康咨询水平)[12]。因此,需要对低浓度莠去津进行准确定量。
已经开发了许多用于阿特拉津检测的传统分析技术,包括 LC 与质谱联用 (LC-MS) [13]、高效液相色谱 (HPLC) [14] 和气相色谱与质谱联用 (GC-MS) ) [15],但这些方法也存在成本高、需要大型仪器、选择性差、耗时等局限性[16]。
作为无线质量敏感平台,由 ME 材料制成的磁弹性 (ME) 传感器因其低成本、高灵敏度、较小尺寸和易于使用的关键优势而被广泛开发用于各种应用[17, 18]。目前,ME 传感器通常由非晶铁磁合金材料制成,例如 Metglas 2826 MB (Fe40Ni38Mo4B18) [19]。在外部施加的交变和静态磁场下,ME 材料以其共振频率纵向振动 [20],产生的磁通量密度可以由拾音线圈无线检测,无需任何直接物理连接 [21]。根据方程。 (1) [22]、基波谐振频率f 0 取决于材料长度 L , 密度 ρ , 弹性模量 E , 和泊松比 v .
$$ {f}_0=\frac{1}{2L}\sqrt{\frac{E}{\rho \left(1-{v}^2\right)}} $$ (1)一个小的附加质量负载 ∆m 沉积在质量为 M 的 ME 材料表面上 (Δm ≪ M ) 导致谐振频率的偏移 (∆f ),由等式给出。 (2) [23].
$$ \frac{\Delta f}{\Delta m}=-\frac{f_0}{2M} $$ (2)基于ME材料的上述独特性质,ME材料的共振频率随着额外质量负载的增加而降低。因此,通过传感膜的功能化,ME 材料已被开发用于物理、化学和生物分析,例如检测应力/压力 [24]、温度/湿度 [25]、二氧化碳 [26]、内毒素 [27]、鼠伤寒沙门氏菌/炭疽杆菌 孢子 [28] 和 大肠杆菌 O157:H7 [29]。然而,据我们所知,尚未将ME材料应用于阿特拉津检测。
在本研究中,我们利用其优异的性能和优势,首次提出了一种无线 ME 纳米生物传感器,以 ME 材料为基底,金纳米粒子 (AuNPs) 为涂层,在直接竞争免疫分析的基础上进行 ppb 级的莠去津检测。程序。与共价-随机抗体固定相比,共价导向策略更有利于提高纳米生物传感器的灵敏度。由于蛋白 A 是一种有趣的替代物,可以与抗体的 Fc 免疫球蛋白区域特异性结合,因此它被用于定向固定阿特拉津抗体 [30],提供最高的固定密度,以表现出更好的抗原结合效率并提高纳米生物传感器的性能[31]。阿特拉津的直接竞争性免疫分析是通过将阿特拉津抗体定向固定在 AuNPs 包覆的 ME 材料表面共价修饰的蛋白 A 上,然后阿特拉津-白蛋白偶联物 (Atr-BSA) 和阿特拉津与阿特拉津抗体的竞争反应来构建的。 Atr-BSA 被诱导放大信号响应,进而显着提高纳米生物传感器的灵敏度。对ME纳米生物传感器的效率进行了评估,证明了一种用于检测痕量莠去津的新型ME纳米生物传感器的研制成功。
材料和方法
材料
阿特拉津抗体、阿特拉津-白蛋白偶联抗原 (Atr-BSA)、阿特拉津和蛋白 A 购自 EastCoast Bio(美国缅因州)。西玛津、丙咪嗪和二氯二苯基三氯乙烷 (DDT) 购自成都华夏化学试剂有限公司。 半胱胺、1-乙基-3-(3-二甲氨基丙基)碳二亚胺盐酸盐 (EDC)、N -羟基磺基琥珀酰亚胺(NHS)、牛血清白蛋白(BSA,99%)和磷酸盐缓冲液(PBS缓冲液,pH =7.4)购自Sigma-Aldrich Corporation(美国密苏里州圣路易斯)。
ME 纳米生物传感器制造
ME 纳米传感器平台的准备
由 Metglas 合金 2826 (Fe40Ni38Mo4B18) 组成的 ME 材料带购自 Honeywell Corporation (Morristown, NJ, USA),并使用计算机控制的激光切割机切割成 5 mm × 1 mm × 0.028 mm。为了去除有机薄膜和碎屑,ME 带在丙酮和乙醇中分别超声清洗 10 分钟,然后在去离子水中冲洗,然后在氮气流中干燥(图 1a)。在 ME 带表面的两侧溅射~ 100 nm 厚的铬纳米颗粒层,以增强 AuNP 与带表面之间的附着力。随后,镀铬的 ME 带表面的两侧都溅射有 AuNPs,以提高生物相容性并保护带免受氧化和腐蚀。图 1 中的扫描电子显微镜 (SEM) 图像显示,涂覆在 ME 带上的 AuNP 呈球形。 AuNPs 和-SH 很容易形成Au-S 键。除了由于其价格低廉、无腐蚀、生物相容性和无毒 [32] 的吸引人的优势外,AuNPs 还可以为化学或生物识别元素的修饰提供极好的界面 [33, 34]。然后,将 ME 带在真空烘箱中在 200°C 下退火 2 小时,以减轻残余内应力并促进 AuNPs 层与 ME 带的粘附。然后,ME纳米传感器平台完成并准备用于阿特拉津抗体固定(图1b)。
<图片>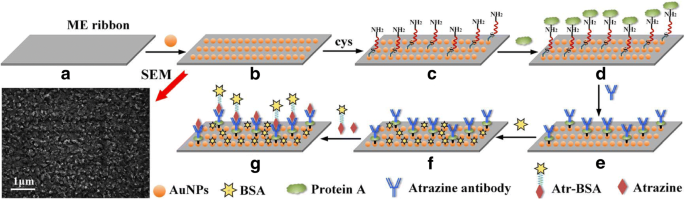
ME纳米生物传感器功能化过程的示意图:(a ) 裸露的 ME 色带; (b ) AuNPs 涂层; (c ) SAM 层; (d ) 蛋白 A 固定化; (e ) 抗体修饰; (f ) BSA 阻塞; (g ) 阿特拉津和 Atr-BSA 与抗体竞争性结合; AuNPs包覆纳米传感器表面的SEM图
阿特拉津抗体固定化
用丙酮、异丙醇、去离子水和乙醇分别超声清洗 AuNPs 涂层的纳米传感器平台 5 分钟,然后在氮气流下干燥。然后,将纳米传感器平台在室温下浸入半胱胺溶液(10 mM)中 12 小时,以获得自组装单层(SAM)(图 1c)。蛋白 A (1 mg/mL) 用 4 mg/mL EDC-4 mg/mL NHS 在室温下活化 30 分钟。之后,活化的蛋白 A 在 SAM 修饰的纳米传感器上在 37°C 下孵育 30 分钟,并用 PBS 缓冲液冲洗(图 1d)。然后将纳米传感器平台与阿特拉津抗体孵育 50 分钟,并用 PBS 缓冲液洗涤(图 1e)。为了防止非特异性吸附,将阿特拉津抗体包被的纳米传感器进一步用 0.5% BSA 处理 30 分钟,然后用 PBS 缓冲液冲洗以去除任何未结合的 BSA,并在氮气流下干燥。最后,制备了用于阿特拉津检测的ME纳米生物传感器(图1f)。
信号测量
ME 纳米生物传感器的共振频率是使用缠绕在小瓶上的拾音线圈和矢量网络分析仪(AV3620A,中国青岛市 CETC 第 41 研究所)测量的,如图 2 所示。在磁场中,与拾波线圈相连的网络分析仪工作在S11模式,为线圈提供扫频信号,它可以监测来自线圈的反射信号。此外,还应用了由条形磁铁产生的静磁场来增强共振行为。纳米生物传感器以垂直和无线方式(与测量系统没有任何电线连接)插入装有 30 μL 待测样品溶液的小瓶中。所有实验均在室温(25 ± 2°C)下在 PBS(0.1 M,pH 7.4)溶剂系统中进行。纳米生物传感器的共振频率可以通过测量S11参数来确定,每5分钟监测并记录一次。
<图片>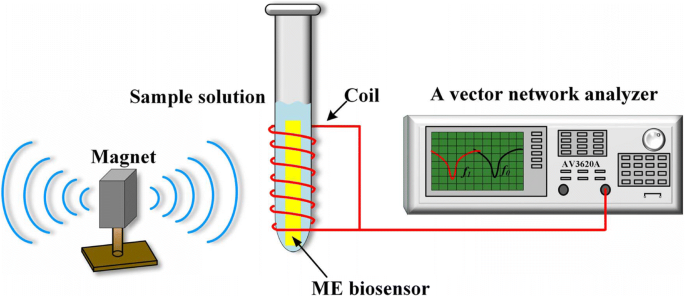
无线ME纳米生物传感器测量系统示意图
结果与讨论
纳米生物传感器表面形态的表征
进行纳米生物传感器表面的原子力显微镜(AFM,ND-100,Park System,Korea)观察以检查莠去津抗体的固定效果。 AuNPs 涂覆的纳米生物传感器和抗体修饰的纳米生物传感器表面的 AFM 图像分别显示在图 3a、b 中。很明显,增加的表面粗糙度是由共价固定的莠去津抗体引起的。对AFM横截面形貌的综合分析表明,AuNPs包覆的纳米生物传感器的高度变化为13.421 nm;然而,抗体修饰后该值增加到 28.425 nm。众所周知,抗体分子的直径约为15 nm,显然阿特拉津抗体的固定化是成功的。
<图片>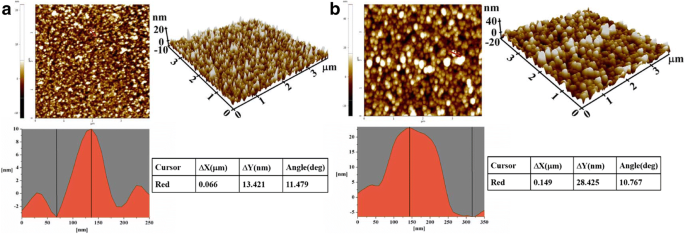
(a 的 AFM 图像 ) AuNPs 涂层和 (b ) 抗体修饰的纳米生物传感器表面
阿特拉津抗体浓度优化
抗体的固定浓度对纳米生物传感器的灵敏度有重要影响。因此,有必要评估纳米生物传感器在不同固定浓度的莠去津抗体(25 μg/mL、50 μg/mL、75 μg/mL、100 μg/mL)下的共振频率响应。从图 4 中,我们可以看到共振频移在 50 μg/mL 时达到最大值。当阿特拉津抗体的浓度上升到 75 μg/mL 时,由于空间位阻和静电排斥反应开始下降 [35]。也就是说,50 μg/mL的莠去津抗体可以达到相对饱和的固定化。因此,50 μg/mL是阿特拉津抗体的最佳固定浓度。
<图片>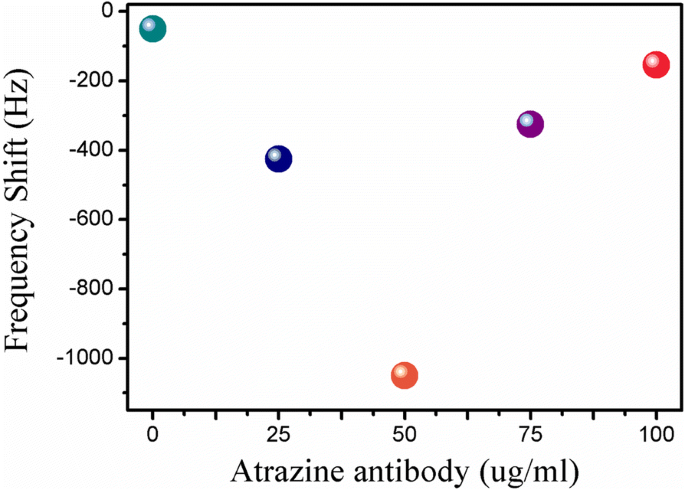
ME纳米生物传感器对不同固定浓度莠去津抗体(0 μg/mL、25 μg/mL、50 μg/mL、75 μg/mL、100 μg/mL)的频率响应
Atr–BSA 浓度优化
在免疫反应中,阿特拉津和 Atr-BSA 竞争纳米生物传感器表面上有限数量的阿特拉津抗体位点。因此,随着用于固定的莠去津抗体的最佳浓度,Atr-BSA 的工作浓度作为一个重要因素影响纳米生物传感器的灵敏度。通过确定 ME 纳米生物传感器对不同浓度(20 μg/mL、40 μg/mL、60 μg/mL、80 μg/mL)的 Atr-BSA 的共振频率响应来研究优化过程。如图 5 所示,在 40 μg/mL 时观察到最大响应。因此后续测定使用40 μg/mL Atr-BSA。
<图片>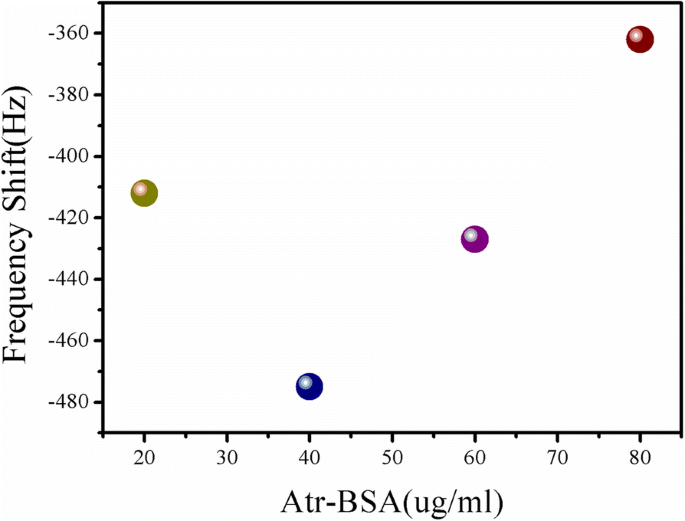
ME纳米生物传感器对不同浓度(20 μg/mL、40 μg/mL、60 μg/mL、80 μg/mL)Atr-BSA的频率响应
阿特拉津检测
图 6 描绘了在 15 μL Atr-BSA (40 μg/mL) 和 15 μL 莠去津的样品混合物中测量的 ME 纳米生物传感器的实时频率响应,不同浓度(0 ng/mL、1 ng/mL、10 ng /mL、100 ng/mL、1000 ng/mL、10 μg/mL、50 μg/mL、100 μg/mL)。如图 1g 所示,莠去津和 Atr-BSA 与固定在纳米生物传感器表面的抗体竞争性结合,这反过来导致纳米生物传感器表面的质量负载增加,从而导致共振频率随着孵育而降低时间。从图 6 可以清楚地看出,稳态响应通常在大约 50 分钟时实现。 Atr-BSA 浓度和莠去津抗体位点的数量是固定的,因此纳米生物传感器上结合的 Atr-BSA 的量与溶液中莠去津的浓度成反比。 Atr-BSA 的分子量大于莠去津。因此,纳米生物传感器的共振频率与溶液中莠去津的浓度成反比。如图 6 所示,共振频移的速率和幅度随着莠去津浓度的增加而降低,较高浓度的莠去津可以引起较小的共振频移。图 6 曲线 * 代表空白对照传感器(无莠去津抗体固定)对 Atr-BSA 的背景响应,其大约 48 Hz 远小于检测信号,表明可以忽略非特异性吸附。因此,可以通过无线ME纳米生物传感器的共振频移检测莠去津浓度,呈反比关系。
<图片>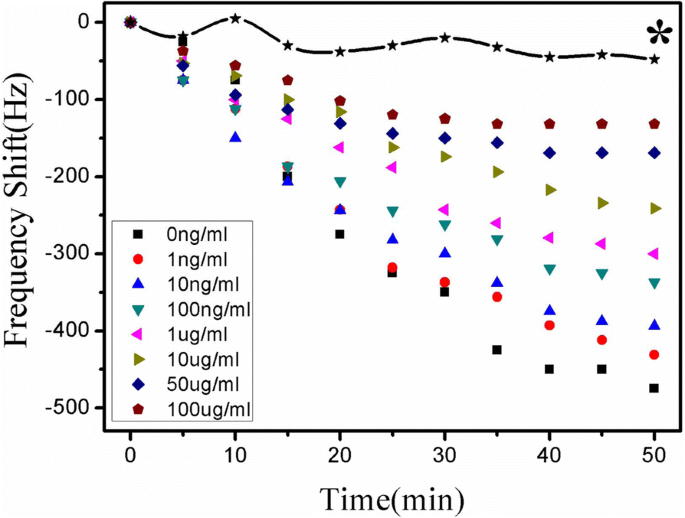
在 0 到 100 μg/mL 范围内的不同莠去津浓度下的实时频率响应。 * 对 Atr-BSA 的空白对照反应(未固定阿特拉津抗体)
在前 50 分钟内在 ME 纳米生物传感器上检测莠去津的标准校准曲线如图 7 所示。对于每个浓度,在相同条件下进行五次纳米生物传感器校准实验。发现共振频移与莠去津浓度在1 ng/mL至100 μg/mL范围内的对数值呈线性关系,可用Δf表示 =54.717 log C 阿特拉津 − 442.45 (R 2 =0.971)。灵敏度计算为 3.43 Hz/μg mL -1 .从图 7 中可以明显看出,检测限 (LOD) 为 1 ng/mL,明显低于美国 EPA 规定的莠去津 3 μg/L 的允许上限,满足现行标准。此外,检测限明显低于之前报道的方法 [36, 37]。研究表明,成功建立了一种低成本、无线、高灵敏度的纳米生物传感器,用于实时检测莠去津。
<图片>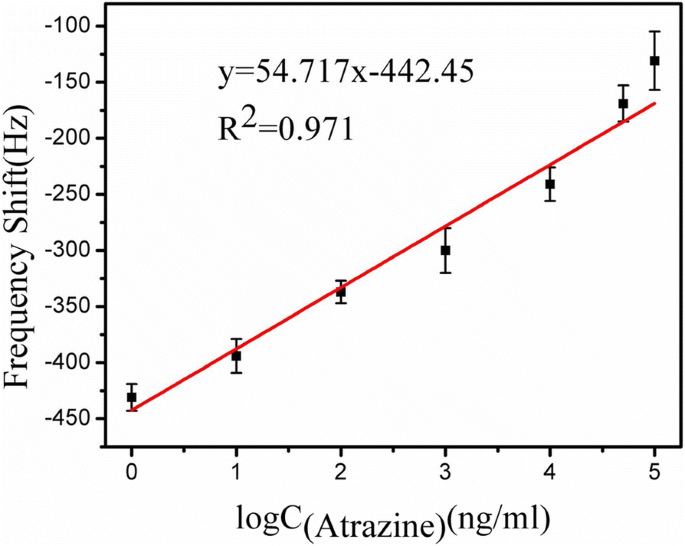
校准曲线:作为不同莠去津浓度的函数的共振频率的 50 分钟偏移
由于莠去津是小分子,因此采用直接竞争性免疫测定方法来提高 ME 纳米生物传感器的灵敏度。在直接竞争性免疫分析中,抗体在传感器表面被修饰,信号响应来自 Atr-BSA 分子的结合。相反,在间接竞争性免疫测定中,Atr-BSA 固定在传感器表面,响应来自抗体分子的结合。根据文献研究 [38] 和我们的结果,直接竞争性免疫分析对于小分子监测是可行的。间接竞争免疫测定对痕量浓度的分析物样品高度敏感 [39]。虽然间接竞争免疫测定法具有更高的灵敏度[40, 41],但它可能操作复杂且难以实施以重复可靠使用[36]。然而,直接竞争性免疫测定非常快速、使用简单且自给自足——不需要额外的试剂 [36]。因此,对于未来的发展,直接竞争免疫分析可能是最有前景的方法。
ME 纳米生物传感器特异性
ME 纳米生物传感器对莠去津的特异性通过确定纳米生物传感器对一些其他杀虫剂的反应来研究,例如 prometryn、西玛津和 DDT,如图 8 所示。从图 8 中可以明显看出,ME 纳米生物传感器对这些农药几乎没有反应由于非特异性吸收造成的干扰,对普罗米宁和西玛津的响应略大于 DDT,后者与空白溶液的响应水平相似。可能是因为扑草灭和西玛津的结构与莠去津相似,属于三嗪类农药;然而,滴滴涕是一种有机氯杀虫剂。结果表明,莠去津被有效识别并与固定在纳米生物传感器表面的抗体特异性结合。因此,ME纳米生物传感器对阿特拉津检测表现出很强的特异性。
<图片>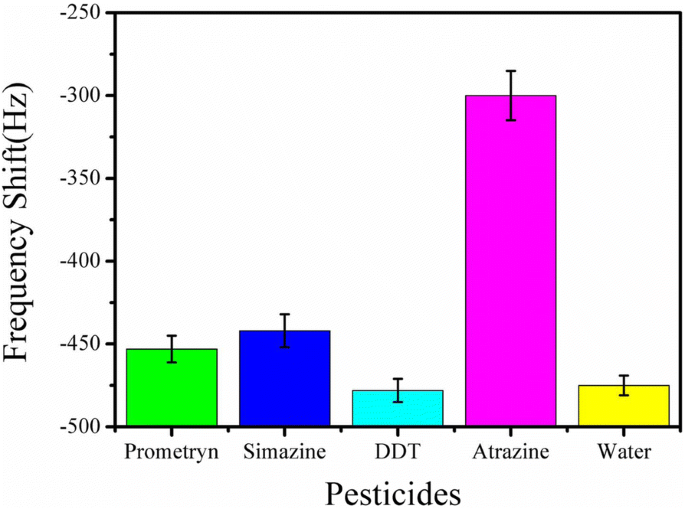
ME纳米生物传感器对浓度为100 μg/mL的其他干扰物的共振频率响应
ME 纳米生物传感器稳定性
图 9 显示了 ME 纳米生物传感器对阿特拉津检测的稳定性。制备了六个相同的 ME 纳米生物传感器并将其储存在 4°C 中,每一个都每隔一天测试 10 ng/mL 阿特拉津,直到 6 天。每个检测周期仅测试一个纳米生物传感器 50 分钟。很明显,纳米生物传感器的共振频率响应几乎保持不变,计算得出的相对标准偏差 (RSD) 为 1.8%。结果表明,ME纳米生物传感器对阿特拉津检测表现出优异的稳定性。
<图片>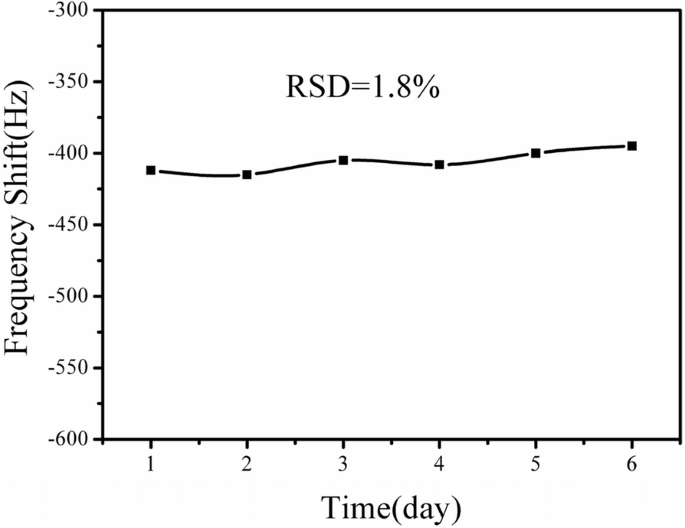
10 ng/mL阿特拉津在ME纳米生物传感器上的稳定性测量
结论
基于 ME 材料和 AuNPs 的无线 ME 纳米生物传感器已成功开发,用于采用竞争性免疫测定法实时和高灵敏度检测莠去津。通过蛋白质 A 定向固定阿特拉津抗体提高了纳米生物传感器的性能。大分子质量的 Atr-BSA 和阿特拉津与纳米生物传感器表面上的阿特拉津抗体竞争性结合,放大信号响应,进而提高灵敏度。主要由结合的 Atr-BSA 引起的共振频移与目标阿特拉津浓度成反比。此外,阿特拉津抗体和 Atr-BSA 的工作浓度分别优化为 50 μg/mL 和 40 μg/mL。在最佳条件下,ME纳米生物传感器对莠去津的线性测定范围为1 ng/mL至100 μg/mL,灵敏度为3.43 Hz/μg mL -1 1 ng/mL 的检测限足以满足立法要求,低于其他报道的方法。 AFM 图像验证了阿特拉津抗体以定向方式成功固定在纳米生物传感器表面上。实验结果表明ME纳米生物传感器对阿特拉津具有高特异性和稳定性。得益于其对检测限、简单性、一次性性和无线性质的影响,该研究不仅提出了一种高灵敏度检测阿特拉津的新方法,而且表明其在其他环境污染物检测和水质监测中具有潜在的实用性。
缩写
- 原子力显微镜:
-
原子力显微镜
- Atr–BSA:
-
阿特拉津-白蛋白结合抗原
- AuNPs:
-
金纳米粒子
- BSA:
-
牛血清白蛋白
- 滴滴涕:
-
二氯二苯基三氯乙烷
- EDC:
-
1-乙基-3-(3-二甲氨基丙基)碳二亚胺盐酸盐
- 我:
-
磁弹性
- NHS:
-
N -羟基磺基琥珀酰亚胺
- PBS:
-
磷酸盐缓冲盐水
- SAM:
-
自组装单层
- SEM:
-
扫描电子显微镜
- 美国环保署:
-
美国环保署
纳米材料
- 用于灵敏快速检测卵巢癌细胞的柔性石墨烯生物传感器的演示
- 全角度 Micro-LED 的高反射薄膜优化
- 碳纳米点作为双模式纳米传感器用于选择性检测过氧化氢
- 一种由亚克力-金纳米复合材料制成的高灵敏度电化学 DNA 生物传感器,用于确定龙鱼的性别
- 基于空心多孔氧化镍的灵敏非酶电化学葡萄糖检测
- 基于新型 Ag 掺杂介孔 α–Fe2O3 的高灵敏度乙醇化学传感器,通过改进的溶胶-凝胶工艺制备
- 一种用于超灵敏检测癌胚抗原的新型磁弹性免疫传感器
- 基于 CdSe 量子点和 g-C3N4 纳米片之间的 Förster 共振能量转移的 Hg2+ 的高选择性和灵敏检测
- 用于红外隐身应用的高度可拉伸微/纳米皱纹结构
- 使用基于智能手机的阅读器灵敏检测疾病生物标志物的等离子体 ELISA
- 检测晶体管缺陷的灵敏方法
- 空间敏感光接收器


