使用脂质纳米制剂共同递送达卡巴嗪和全反式视黄酸 (ATRA) 对恶性黑色素瘤的协同抗肿瘤功效
摘要
恶性黑色素瘤是一种高度侵袭性的皮肤癌,占死亡率的 80%,转移性黑色素瘤患者的总体中位生存期仅为 6-9 个月。通过在单个纳米载体中同时给予双重药物的联合治疗已被证明在对抗癌症方面是优雅而有效的。在此,我们采用基于达卡巴嗪 (DBZ)、FDA 批准的黑色素瘤药物和全反式维甲酸 (ATRA) 的联合疗法,这是一种有希望的脂质纳米制剂 (RD-LNF) 抗癌剂,作为恶性黑色素瘤的新治疗策略。我们已经成功地将这两种药物封装在脂质纳米制剂中,并随着时间的推移显示出有效载荷的受控释放。我们证明同时递送 DBZ 和 ATRA 可以以浓度依赖的方式有效降低细胞增殖。组合纳米颗粒显着降低了 B16F10 黑色素瘤细胞的集落形成能力。流式细胞仪分析表明,RD-LNF 诱导更大比例的细胞凋亡,并显着抑制细胞周期进程和细胞迁移。这些结果表明RD-LNF在治疗恶性黑色素瘤方面具有良好的潜力。
介绍
恶性黑色素瘤是侵袭性恶性肿瘤之一,主要发生在人类皮肤中[1]。黑色素瘤占所有皮肤癌的 4%,但它导致 80% 的皮肤癌死亡率,并在不发达国家和发展中国家日益受到关注 [2, 3]。黑色素瘤很容易转移到身体的各个部位,包括大脑、心脏和肺,使其成为恶性肿瘤的一种侵袭性形式 [4]。如果在早期确诊,手术切除是潜在的治疗选择。然而,手术干预并不能保证黑色素瘤完全康复 [5]。此外,这种恶性肿瘤的放射状生长期对大多数其他治疗方案(包括化疗和放疗)产生耐药性 [6]。具体而言,肽受体在黑色素瘤癌症的表面过度表达,使其具有诱人的前景。亚型 2 生长抑素受体 (SSTR2) 已被证明在黑色素瘤细胞中高表达 [7]。
达卡巴嗪 (DBZ) 或二甲基-三氮杂-咪唑甲酰胺 (DTIC) 是一种 DNA 烷化剂,是美国食品和药物管理局 (FDA) 批准的唯一一线化疗药物选择 [8]。 DBZ 是一种强烷化剂,通过将烷基添加到癌细胞的 DNA 或核材料中来杀死癌细胞 [9]。尽管 DBZ 具有强大的作用,但其水溶性较差,并且在血液循环中的半衰期较短(41 分钟),这削弱了其治疗黑色素瘤恶性肿瘤的疗效 [10]。此外,观察到的反应率在 10% 到 25% 之间令人失望,癌症完全康复率低于 5%,这表明单一药物治疗的局限性 [11, 12]。因此,迫切需要开发一种替代策略来提高DBZ的治疗效果。
与单个治疗剂相比,单次给药联合递送多种治疗剂被证明更有效 [13]。在单一载体系统中共同递送治疗剂将赋予协同活性、相似的药代动力学特性和更高的抗癌功效[14]。全反式视黄酸 (ATRA) 是一种很有前途的抗癌剂,可用于治疗多种癌症 [15]。 ATRA 通过与癌细胞核中的视黄酸受体结合从而抑制生长、增殖、分化和最终的细胞死亡来显示其治疗功效 [16]。与其他化疗药物不同,ATRA 不会导致任何不良反应,例如心脏毒性或骨髓发育不良。据报道,当 ATRA 与适当的化学治疗剂联合使用时,可增强抗癌功效。同样,亲脂性 ATRA 水溶性差且全身清除速度快,因此需要稳定的递送系统 [17]。
纳米颗粒递送系统已被证明可以通过将其释放到靶肿瘤组织中并通过使用增强的渗透和保留 (EPR) 效应避免体循环中的脱靶效应来提高封装疗法的治疗效果 [18, 19]。固体脂质纳米颗粒 (SLN) 被认为是许多现有载体的替代品,包括脂质体或胶束,因为它具有增强稳定性、控制药物释放、高负载效率和易于制备/放大等显着特点 [20] . SLN 作为药物递送载体的重要方面之一是具有 GRAS 状态、耐受性良好和生理脂质的脂质的安全性 [21]。药物在脂质核中的稳定掺入提高了水溶性,改善了药代动力学特征并延长了体循环中的生理稳定性[22]。
在这项研究中,我们提出了一种使用脂质纳米制剂联合递送 DBZ 和 ATRA 的有希望的策略,用于黑色素瘤恶性肿瘤的联合治疗。 DBZ 预计将加载到脂质核心中,而 ATRA 预计将成为纳米颗粒结构的一部分。我们研究了组合纳米颗粒的理化特性、细胞摄取和体外细胞毒性。此外,通过细胞凋亡分析、细胞周期分析、集落形成和细胞迁移分析进一步评估了抗癌作用。
结论
总之,我们已经成功地配制了达卡巴嗪和全反式视黄酸负载脂质纳米制剂。我们的结果清楚地表明,RD-LNF 抑制黑色素瘤细胞增殖,诱导显着的细胞凋亡,并抑制细胞周期进程和细胞迁移。未来的工作将侧重于研究临床相关动物模型中的抗癌功效,并开发针对黑色素瘤恶性肿瘤的靶向治疗。这是在黑色素瘤细胞中进行的初步研究,在不同临床相关动物模型中的广泛研究是我们研究工作的下一部分。
材料和方法
DBZ/ATRA-Loaded 脂质纳米制剂的制备
采用超声法制备载药脂质纳米粒。简而言之,将 10 mg DBZ 和 10 mg ATRA 溶解在 2 ml 氯仿溶液中,该溶液含有 50 mg Egg l-α-磷脂酰胆碱 (PC) 和 2 mg DSPE-甲基(聚乙二醇)-2000 (mPEG2000)。使用氩气暴露干燥有机溶剂20分钟。干燥的药物 + 脂质混合物加入 80 mg 三肉豆蔻苷 (Tm),并在 65 °C 下孵育 1 小时。向该油混合物中加入 5 ml 4% 泊洛沙姆溶液,并立即在 80 W 下探头超声 6 分钟。所得乳液在冰下冷却30分钟。纳米颗粒在 12000×g 下经过 Amicon Ultra 0.5 离心过滤装置(3 kDa 截断值;默克,德国) 20 分钟。用HPLC法评价滤液中游离DBZ和ATRA的含量,计算加载效率和加载能力。 Waters HPLC 系统由 Waters 1525 二元泵、Waters 2487 UV 检测器、Waters 2475 荧光检测器、1500 柱加热器和 Symmetry C18 柱组成,用于药物分析。对于 ATRA,流动相由 90/10 v/v 比率的乙腈和三氟乙酸组成,流速为 1 ml/min,并在 348 nm 处检测。对于 DBZ,使用乙腈和 0.05 M 磷酸氢二钠,比例为 30/70 v/v,其中含有 0.5% 的 TEA。流动相的pH值保持在3.7,流速为1 ml/min。
粒度和形态分析
组合纳米颗粒的粒径分布由 Malvern Zetasizer Nano ZS90 用 He-Ne 激光器(633 nm)评估。所有样品都用蒸馏水稀释,实验在 24 °C 下进行,一式三份。通过透射电子显微镜(TEM;JEOL JEM200CX 在 120 kV)评估纳米颗粒的形态。稀释后的颗粒用2%磷钨酸染色,干燥,透射电镜观察。
载药纳米制剂的体外药物释放
通过透析法评价包封药物的释放。将含有相当于 1 mg ATRA 和 1 mg DBZ 的两毫升载药纳米颗粒密封在透析膜(Spectra/Por,MWCO 3.5 kDa)中。将透析管置于 25 ml 释放缓冲液中,并在 37 °C 下保持 100 rpm 的旋转。在预定的时间间隔直到 72 小时,取出 1 ml 样品并更换为等量的新鲜缓冲液。 DBZ和ATRA的量用上述HPLC法评价。
细胞培养和细胞摄取分析
鼠皮肤黑色素瘤细胞(B16F10)购自中国细胞系资源基础设施(中国北京)。细胞在补充有 10% FBS 和 1% 抗生素混合物的 RPMI-1640 培养基中培养。每 2 天定期更换培养基,并在 90% 汇合后培养。对于细胞摄取分析,将 B16F10 细胞接种在 6 孔板中培养 24 小时。纳米颗粒负载香豆素-6 作为荧光跟踪剂。去除旧培养基并更换为含有 Coumarin-6-lipid 纳米颗粒的新鲜培养基,并以相反的顺序孵育 1-3 小时。用细胞刮刀清洗和刮除细胞。将细胞以 1200 rpm 的速度离心 5 分钟,并将细胞沉淀重悬于 1 ml 冷 PBS 中。样品采用AccuriTM C6流式细胞仪(美国BD公司)进行评估。
体外细胞毒性试验
通过MTT测定评估游离ATRA、DBZ、D-LNF和RD-LNF对B16F10细胞的细胞毒作用。单元格 (1 × 10 4 ) 接种在 96 孔板的每个孔中并孵育 24 h。这些细胞首先用不同浓度的游离 ATRA 和 DBZ 处理,并测试其对黑色素瘤细胞的抗癌作用。随后,细胞分别用固定浓度的游离 ATRA、DBZ、D-LNF 和 RD-LNF 处理,浓度分别为 25 μg/ml 和 50 μg/ml。将细胞孵育 24 小时,然后小心去除培养基并用 PBS 洗涤两次。最后,用 100 μl 5 mg/ml MTT 溶液处理细胞并孵育 4 小时。小心去除培养基并加入100 μl异丙醇并在振荡条件下温育15分钟。使用酶标仪在 570 nm 处研究溶解的甲臜晶体。未处理的细胞作为对照,根据对照的细胞活力进行计算。
细胞凋亡检测——流式细胞仪
用PE膜联蛋白V和基于7AAD的凋亡试剂盒染色后,评估游离ATRA、DBZ、D-LNF和RD-LNF在B16F10细胞中的凋亡作用。细胞接种于12孔板中,细胞密度为2×10 5 细胞/孔,孵育 24 小时。细胞用 25 μg/ml 当量的游离 ATRA、DBZ、D-LNF 和 RD-LNF 制剂处理,未处理的细胞被视为对照。处理暴露 24 小时后,按照制造商的方案对细胞进行染色。 AccuriTM C6 流式细胞仪用于 PE 和 7AAD 表达,在流式细胞仪中至少采集了 10,000 个事件。 PE阳性和7AAD阴性细胞早期凋亡; PE阳性和7AAD阳性细胞凋亡较晚。
细胞周期分析——流式细胞仪
细胞接种于12孔板中,细胞密度为2×10 5 细胞/孔,孵育 24 小时。细胞用 25 μg/ml 当量的游离 ATRA、DBZ、D-LNF 和 RD-LNF 制剂处理,未处理的细胞被视为对照。 24 小时后,洗涤并通过胰蛋白酶消化收集处理过的细胞,并在 4°C 下用 70% 乙醇固定 2 小时。然后用核糖核酸酶处理细胞以去除任何 RNA 污染。现在,将细胞在 37 °C 的培养箱中用碘化丙啶 (PI) 染色 30 分钟。 PI 染色细胞的荧光由 AccuriTM C6 流式细胞仪测定。细胞周期分为亚G1期、G1期、S期和G2/M期。
菌落形成分析
细胞接种于12孔板中,细胞密度为2×10 5 细胞/孔,孵育 24 小时。细胞用 25 μg/ml 当量的游离 ATRA、DBZ、D-LNF 和 RD-LNF 制剂处理。用细胞计数器对处理过的细胞进行胰蛋白酶消化、洗涤和计数。然后将细胞以 1500 个细胞/孔的密度接种在 6 孔板中。然后将细胞在 37°C 的环境条件下培养 12 天,直到菌落可见。细胞用 PBS 洗涤,并用甲醇与醋酸与水 (1:1:8) 固定 10 分钟,然后用 0.1% 结晶紫染色剂染色 45 分钟。然后在光学显微镜下观察染色的细胞。
细胞迁移分析
具有 8 μm 孔径的 12 孔 Transwell 室用于该测定。开始研究,5 × 10 4 细胞/孔接种在上室。上层培养基不含 FBS,而下层培养基由 10% FBS 组成。 24 h 后,将迁移到下膜表面的细胞量固定并用 0.5% 结晶紫染料染色。光镜下随机选取5个视野计数细胞数;记录并分析平均细胞数。
统计分析
除非另有说明,否则数据以平均值 ± SD 表示并一式三份进行。使用未配对的 t 比较两组 测试,而使用单向方差分析和土耳其的多重比较测试对两个以上的组进行比较。使用GraphPad Prism软件进行统计,差异p <0.05 被认为是显着的。
结果与讨论
加载 DBZ/ATRA 的脂质纳米制剂的制备和表征
黑色素瘤的治疗仍然是一个重大挑战,标准治疗方案包括化疗或放疗或手术切除仅对预后不良的实体瘤有效。 FDA已经批准了紫杉醇或其组合等药物,但未能改善对患者生存和癌症治愈的整体影响。达卡巴嗪(DBZ)是FDA批准的一线化疗药物;然而,DBZ 的物理化学特性很差,导致响应率在 10% 到 25% 之间令人失望。为了应对这些挑战,我们开发了一种在脂质纳米制剂中结合 ATRA 和 DBZ 的新型治疗策略(图 1)。我们假设两种治疗成分的组合将增强黑色素瘤恶性肿瘤的抗肿瘤功效。值得注意的是,ATRA 虽然表现出抗癌特性,但并未对全身环境造成任何不利影响 [23]。由于 DBZ 本质上是疏水的,我们设计了脂质纳米制剂,可以将疏水药物稳定地掺入脂质核心,ATRA 将作为纳米颗粒的结构组分加载。携带治疗成分的脂质纳米颗粒将有助于输送到体内较深的肿瘤。 DBZ 和 ATRA 的加载效率分别为 91.2±1.25% 和 95.8±1.14%。 DBZ 和 ATRA 在 RD-LNF 中的负载能力分别为 7.07 ± 0.65% w/w 和 7.48 ± 1.05% w/w。观察到 D-LNF 的粒径为 121.5 ± 1.65 nm,多分散指数 (PDI) 为 0.134,zeta 电位为 -23.5 ± 0.85 mV。 RD-LNF 的粒径为 138.2 ± 1.28 nm,PDI 为 0.159,zeta 电位为 - 25.4 ± 0.58 mV。整体粒径的增加主要归因于 ATRA 的结构载荷;然而,由于 EPR 效应,RD-LNF 的最终大小小于 150 nm,允许优先积累恶性黑色素瘤肿瘤。此外,亲水性 PEG 的存在将防止颗粒聚集并减少其被网状内皮系统 (RES) 的吸收,从而提高其在体内的全身性能。 – 25 mV 左右的表面电荷将赋予出色的储存稳定性。通过透射电子显微镜 (TEM) 研究颗粒形态(图 2)。如图所示,D-LNF 和 RD-LNF 都是完美的球形,并且均匀分布在铜网格中。 D-LNF 和 RD-LNF 之间的大小差异与 DLS 观察一致。没有颗粒碎片、小颗粒和聚集,表明配方过程成功。
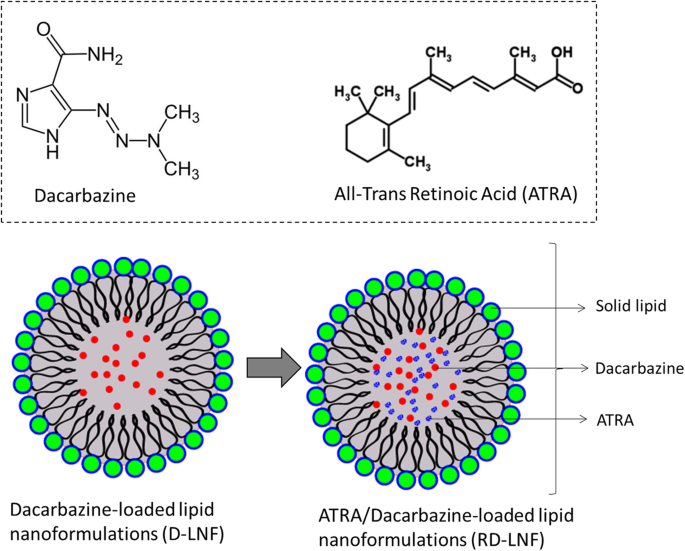
达卡巴嗪 (DBZ) 和全反式视黄酸 (ATRA) 的结构。介绍了加载 DBZ/ATRA 的脂质纳米制剂的示意图。采用超声法制备脂质纳米制剂。 DBZ 和 ATRA 都是疏水性分子,分子量小于 300 g/mol。疏水性分子有望集中在表面活性剂稳定的纳米粒子的核内

使用透射电子显微镜对 D-LNF 和 RD-LNF 进行形态学分析。呈现描绘准确形态的代表性图像
D-LNF 和 RD-LNF 的稳定性分析和体外药物释放
RD-LNF 在 pH 7.4 (PBS) 和血清 (10% FBS) 条件下均表现出优异的稳定性(图 3a)。在整个研究期间,两种条件下的粒径均未显示出任何显着增加,表明纳米颗粒的稳定性。药物及时释放的能力决定了载药纳米颗粒系统的有效性。我们已经在磷酸盐缓冲盐水(PBS,pH 7.4)中进行了 DBZ 和 ATRA 从 D-LNF 和 RD-LNF 的释放动力学。如图 3b 所示,从两个纳米颗粒系统中的任一个中都没有观察到药物的突释或分阶段释放,表明纳米颗粒的核心中而不是纳米颗粒表面中的稳定负载。从 D-LNF 和 RD-LNF 中观察到 DBZ 的释放没有显着差异,表明 ATRA 的存在不会减慢或改变药物释放模式。 DBZ 从 RD-LNF 释放药物的轻微延迟可能是由于脂质结构中的 ATRA 导致的路径长度增加。有趣的是,在 RD-LNF 载波系统中,ATRA 的释放速度明显慢于 DBZ。 24 小时后开始出现显着差异,直到 72 小时,这主要归因于 ATRA 的极端疏水性和结构成分的一部分。总体而言,缺乏治疗成分的突释和控释将有利于黑色素瘤的治疗。
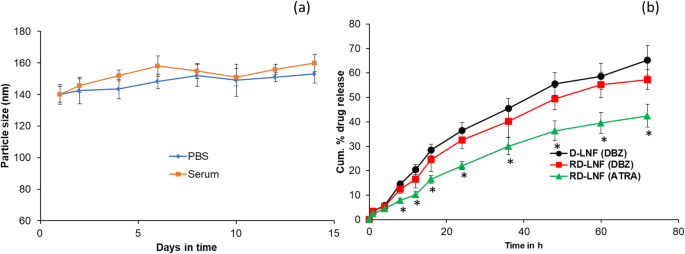
一 RD-LNF 在 pH 7.4 和血清 (10% FBS) 条件下的稳定性分析。 b D-LNF 中 DBZ 的体外药物释放; DBZ 和 ATRA 从 RD-LNF 的体外药物释放。释放研究在磷酸盐缓冲盐水 (pH 7.4) 中进行了 72 小时的研究。结果表示为平均值 ± 标准偏差 (n =4)
体外细胞摄取
纳米颗粒的更高或增强的细胞摄取决定了癌细胞的治疗功效。我们已经在 B16F10 癌细胞中进行了 RD-LNF 的细胞摄取,香豆素-6 被用作荧光跟踪剂。如图 4 所示,纳米颗粒孵育 1 小时后观察到纳米颗粒的显着内化,并且吸收持续增加直到 3 小时。脂质纳米制剂的显着吸收与基于脂质的载体系统的更高细胞吸收一致。据推测,基于被动扩散和内吞作用的机制可能是导致更高细胞摄取的原因。内吞后的纳米颗粒将到达溶酶体,在溶酶体中释放出包封的药物并表现出各自的药理作用。
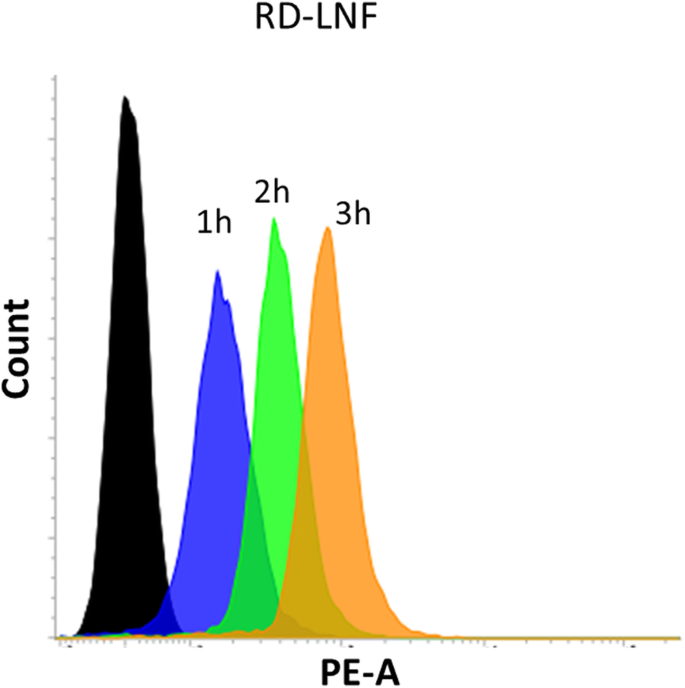
B16F10 黑色素瘤细胞的体外细胞摄取分析。癌细胞用 RD-LNF 处理,孵育时间从 1 小时到 3 小时不等,并使用流式细胞仪分析细胞摄取。 Coumarin-6用作荧光追踪剂
体外细胞毒性试验
在用各自的制剂处理后对 B16F10 细胞进行 MTT 测定以评估单个治疗剂的抗癌效果(图 5a)。首先,评估单个游离 DBZ 和 ATRA 的细胞毒性。 DBZ 在黑色素瘤癌细胞中表现出浓度依赖性细胞毒作用,而 ATRA 在 B16F10 细胞中表现出显着更高的细胞毒作用。在 100 μg/ml 时,DBZ 表现出约 45% 的细胞活力,而 ATRA 的细胞活力约为 22%,表明 ATRA 具有出色的治疗效果。为了证明 DBZ 和 ATRA 的共同递送可能抑制癌症进展,将 DBZ+ATRA 负载的脂质纳米制剂 (RD-LNF) 处理黑色素瘤细胞。含有单一实体药物的负载 DBZ 的脂质纳米制剂 (D-LNF) 用作参考组,以突出 ATRA 的协同功效(图 5b)。正如预期的那样,在 25 μg/ml 的固定浓度下,与 DBZ 相比,ATRA 显示出略低的细胞活力,而基于纳米颗粒的 D-LNF 没有改善 DBZ 的抗癌作用,并且仍然远未有效。正如预期的那样,与 D-LNF 相比,RD-LNF 显示出显着更低的细胞活力和更高的抗癌作用,表明双组分对黑色素瘤癌细胞死亡具有明显的协同治疗作用。与任何其他治疗组相比,RD-LNF 显示出显着更高的抗癌效果。可以预期 DBZ 的缓慢和持续释放以及 ATRA 从纳米载体系统的缓慢释放可能有助于协同治疗效果。在这项研究中,达卡巴嗪 (DBZ) 是主要的化疗药物,ATRA 被用作脂质纳米颗粒的结构成分,因此没有为 R-LNF 创建一个单独的组。我们研究了裸 ATRA 和 DBZ 在癌细胞中的抗癌作用。此外,许多已发表的报告证明了ATRA的抗癌作用;因此,我们使用ATRA作为结构成分,也可以协同提高胶囊化疗法的抗癌功效。
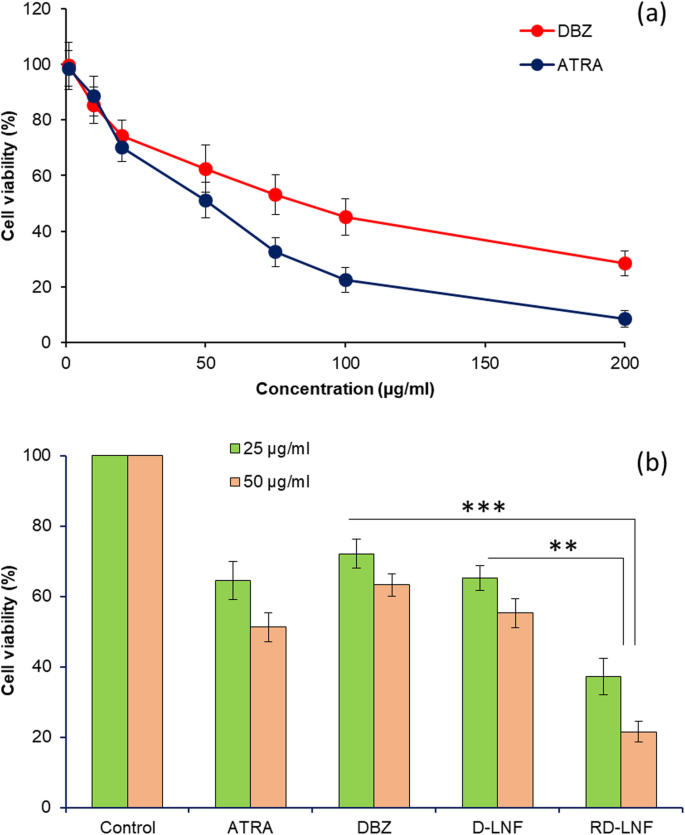
一 以浓度依赖性方式对游离 DBZ 和 ATRA 进行体外细胞毒性测定。 b 25 μg/ml和50 μg/ml固定浓度下游离ATRA、DBZ、D-LNF和RD-LNF的体外细胞毒性
菌落形成分析
进行集落形成试验以评估黑色素瘤细胞的肿瘤发生潜力。如图所示,游离 DBZ 和 ATRA 在抑制集落形成方面的作用有限,同样,D-LNF 在控制集落形成方面无效(图 6)。正如预期的那样,与单个游离药物或单个载药纳米颗粒相比,DBZ + ATRA 的组合显着增强了集落形成的抑制作用。菌落制剂试验进一步重申了RD-LNF优于游离药物的抗癌功效。
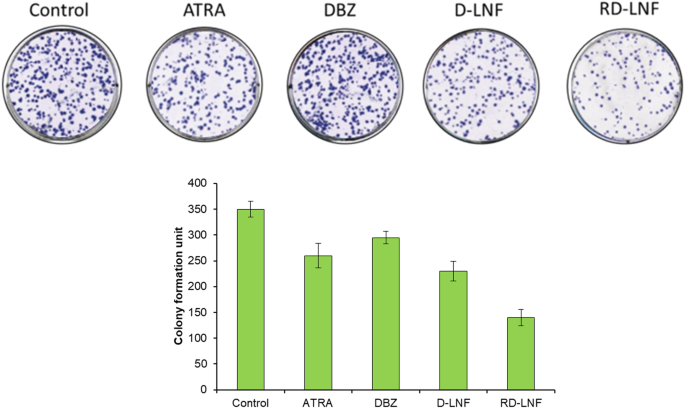
游离 ATRA、DBZ、D-LNF 和 RD-LNF 对集落形成的影响。 B16F10细胞用各制剂处理,结晶紫染色后拍摄集落形成
体外细胞凋亡测定和细胞周期分析
在用膜联蛋白 V-FITC/PI 混合物染色细胞后,使用流式细胞仪研究用 D-LNF 和 RD-LNF 处理后 B16F10 细胞的凋亡诱导(图 7a)。如图所示,ATRA 和 DBZ 仅导致癌细胞凋亡的 10-12%,并且大部分细胞保持完整。在 D-LNF 处理后观察到早期凋亡细胞的轻微增加可能表明递送载体的作用。重要的是,RD-LNF 诱导了更大比例的细胞凋亡,其中晚期细胞凋亡和早期细胞凋亡的细胞比例更大,表明组合纳米颗粒具有优异的抗癌功效。 RD-LNF 显示晚期凋亡细胞增加 21.5%,早期凋亡细胞增加 18.3%,活细胞比例分别从 95% 降至 52%,表明 DBZ + ATRA 的组合有助于癌细胞的凋亡,并能抑制 B16F10 黑色素瘤细胞的增殖抑制。通过细胞周期分析进一步证实了制剂的细胞凋亡作用。如图所示,与单个游离药物相比,DBZ 和 ATRA 在亚 G0 群体中表现出轻微增加,而 D-LNF 显示出相对较高的亚 G0 群体(图 7b)。值得注意的是,对于 RD-LNF 处理的黑素瘤细胞,观察到亚 G0 群体的显着增加,表明癌细胞明显凋亡。众所周知,DBZ 可以增加 p21、caspase-3 和裂解 PARP 的表达水平,从而通过稳定 p53 促进细胞凋亡。 p53 的诱导将抑制细胞周期进程 [24, 25]。 DBZ+ATRA的联合应用有望增强癌细胞的凋亡机制,阻止癌细胞的细胞周期进程,并表现出抗癌功效。
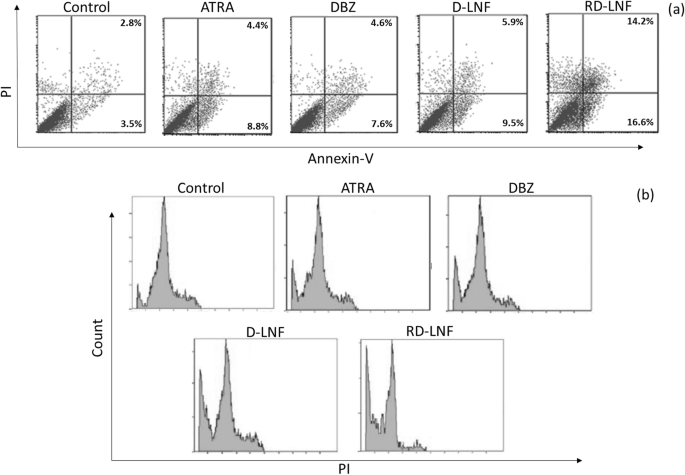
一 用游离 ATRA、DBZ、D-LNF 和 RD-LNF 处理后 B16F10 细胞凋亡的图示。未处理的细胞被认为是合适的对照。使用流式细胞仪分析细胞凋亡。 b B16F10细胞用各制剂处理后的细胞周期分析图
复合纳米粒子对细胞迁移的影响
通过transwell膜分析细胞迁移并通过结晶紫染色观察迁移细胞(图8)。 24小时后,对照细胞几乎实现了癌细胞的完全迁移。 ATRA 似乎比 DBZ 处理的细胞更好地抑制细胞迁移。 D-LNF 对细胞迁移也表现出显着的抑制作用;然而,在 RD-LNF 处理的 B10F16 黑色素瘤细胞中观察到最显着的细胞迁移效果。正如所见,与未处理的对照细胞相比,观察到细胞迁移的多样性下降。这些结果清楚地表明,RD-LNF可能会降低异常恶性细胞增殖并有效抑制细胞迁移。
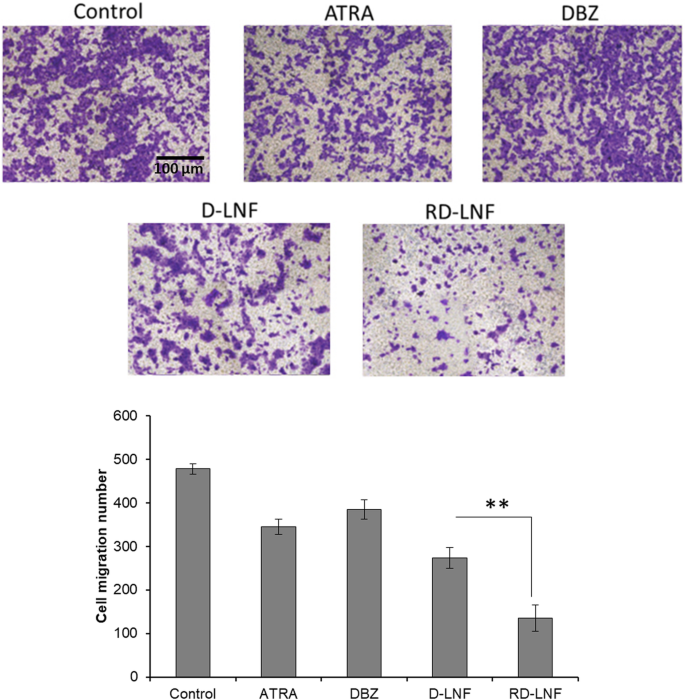
游离ATRA、DBZ、D-LNF和RD-LNF处理后B16F10细胞迁移实验的代表性显微照片及其定量
数据和材料的可用性
不适用
缩写
- DBZ:
-
达卡巴嗪
- ATRA:
-
全反式视黄酸
- D-LNF:
-
负载DBZ的脂质纳米制剂
- RD-LNF:
-
ATRA/DBZ负载脂质纳米制剂
- SLN:
-
固体脂质纳米粒
纳米材料
- 使用 Fiix CMMS 的 7 个 CMMS 提示和技巧
- 用于灵敏快速检测卵巢癌细胞的柔性石墨烯生物传感器的演示
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 通过聚乙二醇化脂质体改善蟾蜍灵的抗肿瘤功效和药代动力学
- 生物相容性 5-氨基乙酰丙酸/金纳米颗粒负载的 Ethosomal 囊泡用于肥厚性疤痕的体外透皮协同光动力/光热疗法
- 基于叶酸和 gH625 肽的 Fe3O4 磁性纳米颗粒功能化增强细胞内化的比较
- 自噬抑制剂 (LY294002) 和 5-氟尿嘧啶 (5-FU) 基于组合的纳米脂质体,可增强对食管鳞状细胞癌的疗效
- 使用冻干单相溶液法制备甘草次酸脂质体:预配制、优化和体外评估
- 基于铂和镍锯齿状纳米线的用于检测咖啡酸的超稳定电化学传感器
- 肿瘤靶向和生物相容性 MoSe2 纳米点@白蛋白纳米球作为协同光热放射治疗的双模态治疗剂
- 使用工业梯子和平台的5个技巧
- 使用重型设备进行拆除和解构的指南


