用于近红外光声成像的可调谐纵横比金纳米棒的种子介导合成
摘要
已通过改进的种子介导的合成方法合成了长宽比可调的金纳米棒。抗坏血酸被用作形状控制器以诱导各向异性生长,这使得合成的金纳米棒的纵横比在 8.5 到 15.6 之间。这些纳米棒具有可调谐的纵向表面等离子体共振吸收带,覆盖了广泛的近红外 (NIR) 范围,从 ~ 680 到 1100 nm。当用硫醇-聚乙二醇(SH-PEG)修饰时,合成的金纳米棒表现出优异的生物相容性和稳定性,预示着其作为光声造影剂的近红外应用的巨大潜力。由于它们在 NIR 中的可调节吸光度,合成的 Au 纳米棒可以在光声成像中提供更强的对比度(是不使用造影剂的对照组的 3.1 倍)和更高的信噪比值(SNR;是对照组的 5.6 倍),体外和体内实验。我们在这里展示的工作不仅添加了一些新型的基于金的光声造影剂,而且还描述了一种覆盖整个生物近红外窗口的造影剂制备的可能性。
背景
一维 (1D) 纳米结构,例如纳米线、纳米棒、纳米管和纳米带,特别有趣,因为它们不仅是纳米器件的新型基本构建块,而且还具有高几何纵横比,可为特殊应用产生各向异性特征 [1, 2,3,4,5,6]。在这些一维纳米结构中,新型金属纳米棒 (NRs) 因其形状相关的表面等离子体共振 (SPR) 带 [7, 8]、易于合成 [9,10,11]、良好的生物相容性和容易修改 [12,13,14]。例如,叶等人。报道了一种小于 100 nm 的 Au 纳米棒 (AuNR) 壳内结构,在 600-900 nm 处表现出很强的纵向吸光度,并且对光诱导疗法具有良好的适用性 [8]。王等人。通过将带有DNA的功能化AuNR定位在设计的DNA捕获链排列的“X”图案的折纸上,成功构建了具有定制手性的各向异性AuNR螺旋超结构[12]。
此外,AuNRs 合成和纯化的改进通过调整长度和纵横比 [15,16,17] 来轻松调整纵向 SPR 带,用于特定应用,如光声成像 (PAI) 和光诱导疗法 [18,19,20,21,22,23],这需要 Au NRs 的纵向 SPR 落在生物组织的光学透明窗口中(首先在 700-950 nm,其次在 1000-1350 nm)[8 , 18]。例如,Huang 及其同事合成了纵横比为 2.4 到 5.6 的金 NR,显示出有效的癌细胞诊断和选择性光热治疗 [19]。小丑等人。开发了长宽比约为 3.5 的金 NRs 和二氧化硅涂层金 NRs,其显示出用于卵巢癌检测和间充质干细胞成像的高 PAI 信号 [20, 21]。 Yang 及其同事报道了用于双磁共振 PAI 和靶向光热疗法的磁性金纳米棒/PNIPAAmMA [23]。尽管已经开发了许多基于 Au NR 的造影剂,但大尺寸可调纵横比 AuNR 的简便、可扩展合成及其依赖于吸收行为的 PAI 性能仍然存在挑战。
在此,通过使用改良的种子介导生长方法在抗坏血酸的帮助下合成了纵横比为 8.5 到 15.6 的 AuNR。 AuNRs 被证明具有高生物相容性,并通过 SH-PEG 修饰进一步降低了它们的细胞毒性。得益于它们在 NIR 区域的大且可调的吸光度,合成的 AuNR 可以在体外和体内实验中在 PAI 中提供更强的对比度和更高的信噪比 (SNR) 值。这种构建可调纵横比金NRs的简便方法可用于在第一近红外窗口中制造任何波长下的造影剂。
实验
金纳米棒的合成
可调长宽比 AuNRs 是通过改良的种子介导合成方法合成的 [16, 17]。在典型的程序中,体积为 10.3 mL 0.025 M HAuCl4(国药集团化学试剂有限公司,≥ 99.9%)和 3.644 g 十六烷基三甲基溴化铵 (CTAB) 表面活性剂(天津光复精细化工研究所,≥0% 99. ) 首先添加到烧杯中。然后,加入去离子水(18 MΩ)使 HAuCl4 的浓度为 2.5 × 10 -3 M 和 0.1 M 的 CTAB。将上述溶液的 10 mL、4.5 mL、4.5 mL 和 45 mL 分别转移到标记为 A、B、C 和 D 的四个烧瓶中。然后,体积为 350 μL ,将 0.01 M 冰冷的 NaBH4(国药集团化学试剂有限公司,≥ 98.0%)加入烧瓶 A 中并搅拌 3 分钟。将烧瓶 A 的 0.4 mL 溶液和 25 μL 0.1 M L(+)-抗坏血酸 (AA)(天津申泰化工有限公司,≥ 99.7%)转移到烧瓶 B 中,再搅拌 3 分钟。然后,将烧瓶 B 的 0.4 mL 溶液和 25 µL 0.1 M AA 加入烧瓶 C 中,再次搅拌 3 分钟。最后,将烧瓶 C 的 4 mL 溶液和 250 µL 0.1 M AA 加入烧瓶 D 中,搅拌 5 秒,然后在 28°C 水浴中静置 12 小时。小心去除顶部溶液,将沉淀物离心并用蒸馏水洗涤数次以确保完全去除过量的 CTAB。因此,最终产品被签署为Au典型纳米棒(AuTR)。
重复上述过程,只需改变AA的用量,就可以开发出纵横比为8.5到15.6的Au NRs。具体如下:金棒1的AA用量为(35μL、35μL、350μL),金棒2为(30μL、30μL、300μL),金棒2为(20μL、20μL、200μL) Au 棒 3,以及 Au 棒 4 的(15 μL、15 μL、150 μL)。
AuNRs 的表面改性
首先,将 10 mg SH-PEG(南京鹏盛生物科技有限公司)溶解在 1 mL 去离子水中并超声处理 10 分钟。然后,将溶液用 50 mL 0.1 M NaBH4 溶液在超声处理下再处理 15 分钟,以减少可能的二聚化 SH-PEG (PEG-S-S-PEG)。其次,将净化后的 Au NR 分散到 10 mL 去离子水中并与上述 SH-PEG 溶液(10 mL)混合,搅拌 5 分钟,然后静置 5 小时。最后,将样品离心并用去离子水洗涤以备进一步应用。
表征方法
通过扫描电子显微镜(SEM;JEOL JSM-7001F)和透射电子显微镜(TEM;JEOL 2100F,200 kV)鉴定合成的 AuNR 的形态和结构。通过分光光度计(Shimadzu,3100 UV-vis-NIR)测量各种AuNR的UV-vis吸光度。光声信号由单元旋转扫描光声检测系统记录,该系统包含激光装置(Surelite I-20,Continuum),光学参量振荡器(OPO)(Surelite OPO Plus),非聚焦超声换能器(PMUT)(V310- SU, Olympus, 5 Hz), 电机步进转台及其电机控制箱(MC)(M600,北京卓力仪器有限公司),前置放大器(5077PR,Olympus),PCI4732数据采集(DAQ)卡等
细胞活力实验
所有生物实验程序均经太原理工大学 IACUC 委员会批准。并按照批准的指南进行实验。
Hela 细胞在美国典型培养物保藏中心 (ATCC) 推荐的标准细胞培养基中在 37°C 和 5% CO2 气氛中培养。接种到 96 孔板中的细胞与不同浓度的 AuNR 和 AuNR-PEG 孵育 24 小时。相对细胞活力通过标准甲基噻唑基四唑鎓(MTT)测定法测定并在光学显微镜下成像。
体外和体内 PAI
将两克琼脂粉(Gene Company Ltd.)溶解在 100 mL 去离子水中并通过玻璃棒在烧杯中充分混合。将混浊液体在微波炉(美的集团股份有限公司)中加热至沸腾。然后取出液体,在 60°C 水浴中搅拌 20 分钟,直至液体变稠。然后,将粘性材料倒入直径为 4.5 厘米的圆柱形模具中,冷却并固化。最后将凝固的琼脂作为生物组织的模型,因为它们对近红外激光有近似吸收。
在体模表面植入直径为0.9mm的玻璃毛细管以模拟血管,具体实验中可用新鲜牛血或混合不同浓度AuNR-PEG的血液来实现。将体模置于水下,用 680 nm 或 800 nm 激光照射,功率密度为 11 mJ/cm 2 .
用异氟醚暂时麻醉小鼠,然后腹腔注射 0.04 mL/10 g 10 wt% 水合氯醛,使小鼠彻底麻醉。轻轻剃掉小鼠头部的毛发并平滑涂抹超声偶联剂(Boline Healthcare Ltd.)。将激光波长调整为 800 nm,并将小鼠置于水下。然后,对小鼠的脑血管进行前后成像,并将造影剂(1 nM,0.1 mL/10 g)静脉内(I.V)注射到小鼠体内。将激光更改为 680 nm,并重复上述实验。注意:更换对比剂后,静脉注射至少需要24小时后才能让残留物完全代谢。
结果和讨论
AuTR 的典型形态和结构已通过 TEM 系统地讨论过(图 1)。如图 1a 所示,合成的 AuTR(AA 的剂量为 25 μL)形状均匀,直径为 22 ± 1.5 nm,长度为 290 ± 13 nm,纵横比约为 13.2。图 1b 显示了一些代表性 AuTR 的高倍放大 TEM 图像。单个纳米棒末端区域的高分辨率 TEM (HRTEM) 图像(图 1b 中的“1”矩形区域)如图 1c 所示。其结果表明,垂直于纳米棒长轴的晶格条纹可以用 1.44 埃的 d 间距辨别,对应于 (110) 晶格平面。根据选区电子衍射 (SAED) 图案和 HRTEM 图像 [16, 17] 的分析,纳米棒沿 [110] 方向生长,这由 Au 的立方结构决定。图 1d 中 AuTR 的 UV-vis 吸收光谱显示出两个吸收峰,特征峰位于 520 nm 左右,纵向峰位于 900 nm 左右。 HS-PEG(红线)功能化后,吸收带峰强度略有下降(约5%),但峰位无明显偏移。
<图片>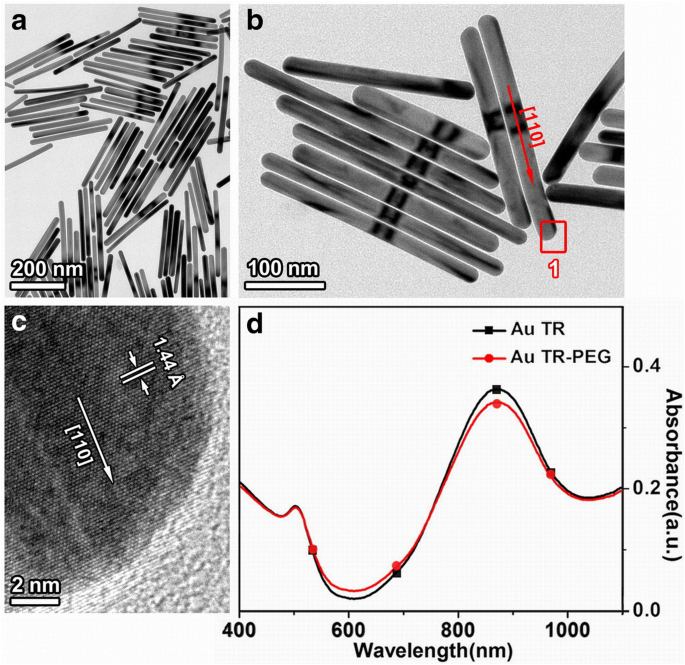
在 25 μL 0.1 M AA (AuTR) 下合成的 Au 纳米棒的典型形态和结构:a 明场 TEM 图像。 b 单个杆的放大 TEM 图像。 c 来自面板 b 的矩形区域“1”中单个杆的 HRTEM 图像 . d AuTR和AuTR-PEG的紫外-可见吸收光谱
众所周知,单体浓度和晶体生长速率的动力学控制是控制颗粒尺寸以及从各向异性生长开始的材料形状的关键因素 [24, 25]。因此,在这项工作中,进行了浓度依赖实验来探索 AA 对 Au NRs 各向异性生长的影响。当 AA 的用量为 35 μL (0.1 M) 时,合成的 AuNRs 的纵横比约为 8.5 ± 0.6(图 2a,随机选择了约 50 个单独的 AuNRs 用于纵横比的数理统计)。将 AA 的剂量从 35 μL 减少到 15 μL,AuNR 的纵横比从 8.5 增加到 15.6(图 2a-d)。一般常用AA作还原剂还原淡黄色Au 3+ 到 Au + 并且不能诱导Au 0 的形成 纳米粒子 [26, 27]。然而,在我们的实验中,合成的 AuNRs 的纵横比随 AA 的浓度而变化。在我们的实验中,人们怀疑 AA 不仅充当还原剂,而且还起到封端剂的作用,以协助调节 AuNRs 的各向异性生长 [28,29,30]。随着反应体系中AA浓度的降低,Au + 离子必然会加速它们的释放并诱导沿 Au 纳米棒纵轴的快速生长(图 2e)。图 2f 显示了所有样品的 UV-vis 吸收光谱。随着纵横比从 8.5 增加到 15.6,AuNRs 的强纵向 SPR 吸收带从~ 680 红移到 1100 nm,覆盖了广泛的 NIR 范围(图 2f),表明它们在生物医学应用方面的巨大潜力 [31, 32 ].
<图片>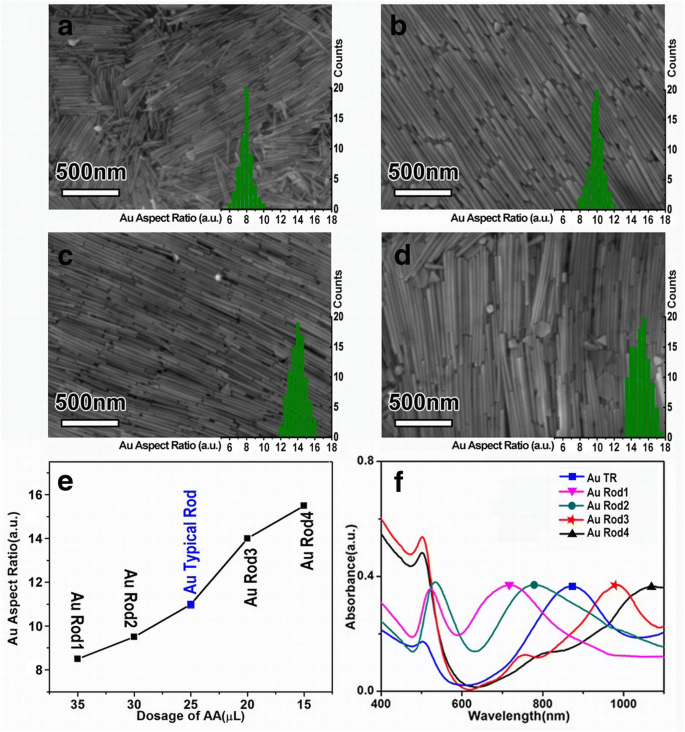
不同AA剂量下AuNRs的形态和纵横比统计:a–d SEM 和直方图,a 杆1,b Rod2,c Rod3 和 d 杆 4。 e AA用量与纵横比对应的折线图。 f 不同AuNRs的紫外-可见吸收光谱
AuNRs 的体外光声特性如图 3 所示。用 HS-PEG 功能化的 AuNRs 的光声 (PA) 振幅是在 0.25 到 1.0 nM 的一系列光学组分浓度下确定的(图 3a),其中表现出良好的线性关系。 AuTR 在 800 纳米激光和 680 纳米金棒 1 辐射的 PA 信号中提供了很大的增强。当激光波长调整不当(例如 680 nm 的 AuTR 和 800 nm 的 Au rod1)时,PA 信号的强度会急剧减弱。图 3b 显示了充满新鲜牛血或混合 1 nM AuTR 和 Au 棒1 的血液平衡的玻璃毛细血管的 PA 图像。其结果表明b3(800 nm处的AuTR)和b7(680 nm处的Au rod1)具有更好的成像效果。显然,适当的造影剂可以在 PAI 中提供更强的吸收,从而提高 PA 图像的分辨率。图 3c、d 显示了纯血与混合 AuTR 和棒 1 的血液之间光声信号的定量比较。结果表明,混合AuTR的血液在800 nm处的光声信号幅度比纯新鲜牛血高2.3倍,Au rod1组在680 nm处的光声信号幅度高2.1倍。大的增强出现在它们的纵向吸收峰的位置。换言之,AuNRs 的吸收行为决定了它们的 PAI 性能。
<图片>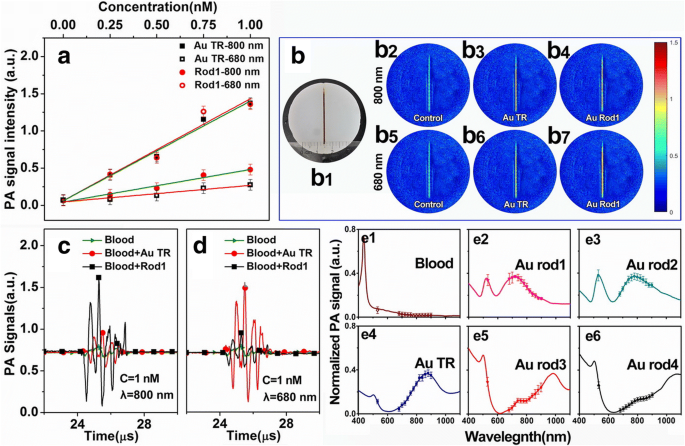
AuTR和AuNRs的体外光声特性:a AuTR和Au rod1分别被800-和680-nm激光照射的浓度依赖性光声信号强度,b 玻璃毛细管的 PAI 与 800 和 680 纳米激光照射的 1 nM AuTR 或 Au 棒1 混合实现血液平衡,c , d 纯血与混合 1 nM AuTR 或 Au 棒 1 的血液平衡在 800 和 680 nm 激光照射下的光声信号幅度比较,e1 –e6 5种合成AuNRs与新鲜牛血的多波长光声信号幅值(数据点)吸收光谱(实线)对比
五种 AuNRs 和血液的光声和光谱如图 3e1-e6 所示。多波长光声信号光谱是通过收集不同波长(680-900 nm)激光的光声信号振幅获得的,1 nm 水溶液在玻璃毛细管中完成。显然,这些图表明光声信号光谱和 AuNRs 的光谱之间有很好的一致性。这些结果清楚地表明在合适波长的激光下将 AuNRs 应用于 PAI 的可行性,并定量地给出了 AuNRs 在 680 到 900 nm 不同波长下的光声效应。
为了检查 AuNR 对主动靶向的生物毒性,将 Hela 细胞与浓度为 0.25-1.0 nM 的 AuTR 一起孵育。进行标准 MTT 测定以确定细胞的活力(图 4a)。其结果证实,与 24 小时内的其他组相比,AuTR-PEG 的组合诱导最大的细胞存活率(1 nM 时为 95.3%)。这表明 AuNR-PEG 具有低细胞毒性和良好的生物相容性 [33, 34],可能是一种很有前途的光声造影剂。虽然纯 AuTR 没有明显的毒性(1 nM 时细胞活力可以达到 71.2%),但在 0.75 和 1.0 nM 浓度下出现细胞死亡(图 4b),表明低浓度的 AuTR 更适合光声成像,而高浓度会导致细胞死亡 [35, 36]。因此,考虑到AuNRs的光声增强效果和生物毒性,选择1 nM的浓度作为体内PAI的合适条件。
<图片>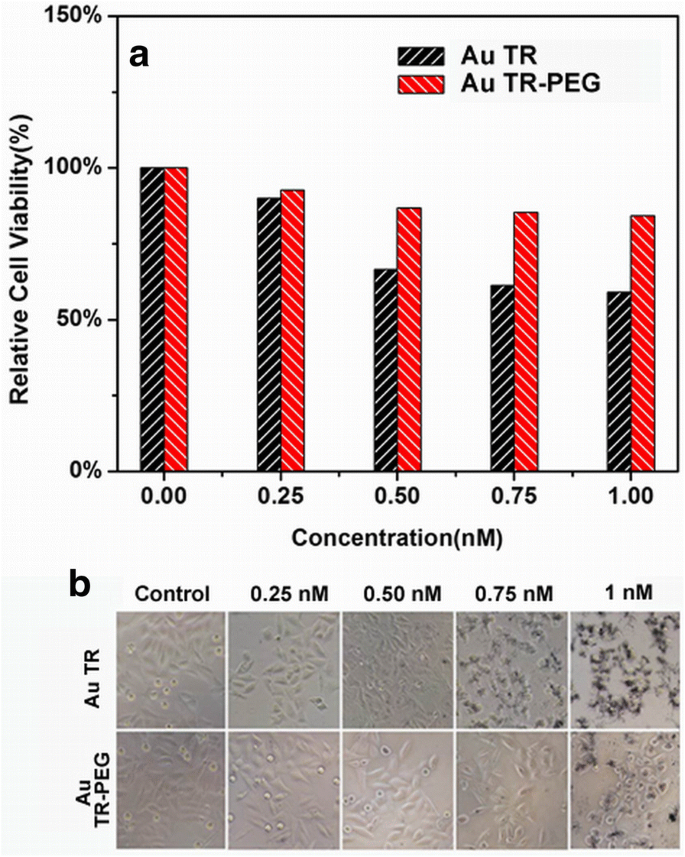
Hela 细胞在 24 小时内与不同浓度的 AuTR 一起孵育后的相对活力,其中有和没有 PEG 修饰:a 相对细胞活力和b的直方图 Hela细胞光学显微图像
与其他传统光学成像方法相比,光声成像是一种非侵入性成像方式,可提供更高的体内成像深度和空间分辨率 [37,38,39,40]。我们发现具有高 NIR 吸光度的 AuNR-PEG 可用作光声成像中的一种很好的对比剂(图 5)。图 5a 显示了被选为体内 PAI 标本的小鼠脑血管的照片。图 5b1–b6 分别显示了在 800 和 680 nm 波长激光下,含有和不含 AuNR-PEG 添加剂的样本的小鼠脑血管的光声图像。结果表明,AuNR-PEG注射前,对照组PA图像中只有大致的主要脑血管形状(图5b1,b4),部分分支血管混入背景中,难以区分,无论使用哪种波长的激光。注射造影剂(AuTR-PEG和Au rod1-PEG)后,PA图像质量得到很大提高,部分消失的大脑(对照组)细小分支血管清晰地出现,尤其是图像800 nm 处捕获的 AuTR-PEG 和 680 nm 处捕获的 Au rod1-PEG。
<图片>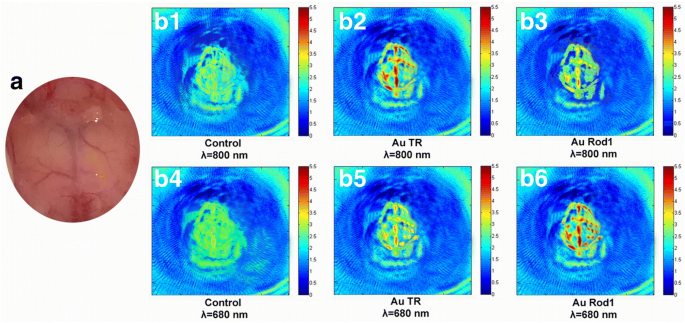
小鼠脑血管的照片和 PA 图像:a 小鼠脑血管照片,b 800和680nm波长激光照射AuTR或Au rod1静脉注射前后小鼠脑血管PA图像图
还从对比度和信噪比 (SNR) 方面对图 5b1-b6 的光声图像进行了定量分析(表 1)。从小鼠脑血管的同一位置随机选取的十个点计算每个像素对应的整幅图像的平均对比度。对照组图像的平均对比度在图 5b1 中为 1.113,在图 5b4 中为 1.076。注入AuNR-PEG后,所有图像的质量都有不同程度的提高。 AuTR/800 nm组主动脉清晰可见(图5b2),平均对比度可达3.451,是对照组的3.1倍。在与 Au rod1/800 nm 组(图 5b3)的平行比较中,平均对比度仅为 1.514,是对照组的 1.36 倍。然而,当激光波长变为680 nm时,AuTR的对比度仅为1.925,远低于Au rod1的对比度(3.692,是对照组的3.6倍)。 AuTR 组图片的 SNR 在 800 nm 处比对照组优化了 5.6 倍,Au rod1 组在 680 nm 处也增强了 5.7 倍。这些结果与体外基本一致,即图像质量的大幅提升可归因于各自较大的纵向吸收峰。
结论
在抗坏血酸的帮助下,通过改良的种子介导合成方法合成了长宽比可调的金纳米棒,范围从 8.5 到 15.6。这些金纳米棒可以提供 680 到 1100 nm 的可调吸收峰,覆盖第一个生物 NIR 窗口。当用 SH-PEG 修饰时,合成的 AuNRs 表现出优异的生物相容性和稳定性,预示着它们作为光声造影剂的近红外应用的巨大潜力。体外和体内实验都证实,合成的可调纵横比 AuNR 在合适波长的激光下可以在 PAI 中提供更强的对比度和更高的 SNR 值。该工作为在第一近红外窗口中任意波长下可控合成造影剂提供了一种可能的方法,用于脑出血和血栓等疾病的可视化。
缩写
- 一维:
-
一维
- AA:
-
l(+)-抗坏血酸
- AuNR:
-
金纳米棒
- AuTR:
-
Au典型纳米棒
- CTAB:
-
十六烷基三甲基溴化铵
- DNA:
-
脱氧核糖核酸
- MTT:
-
甲基噻唑基四唑
- 近红外:
-
近红外
- NR:
-
纳米棒
- OPO:
-
光参量振荡器
- PA:
-
光声
- PAI:
-
光声成像
- SAED:
-
选区电子衍射
- SEM:
-
扫描电镜
- SH-PEG:
-
硫醇聚乙二醇
- 信噪比:
-
信噪比
- SPR:
-
表面等离子体共振
- TEM:
-
透射电子显微镜
纳米材料
- 用于化学传感器的金纳米粒子
- 用于 NIR-II 光热疗法的 BSA 涂层金纳米棒
- 用于合成和生物医学应用的荧光纳米材料的进展和挑战
- 小型硒纳米晶体和纳米棒的简便合成和光学特性
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 合成单分散二元 FePt-Fe3O4 纳米粒子的后处理方法
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- 聚(3,4-亚乙基二氧噻吩)/金/石墨烯复合材料的固态加热合成及其在安培法测定亚硝酸盐和碘酸盐中的应用
- 桔梗皂苷(桔梗)用于金和银纳米颗粒的绿色合成
- 磁性金纳米粒子标记乙酰肝素酶单克隆抗体及其在肿瘤磁共振成像中的后续应用
- 用于新型隐球菌诊断和光热治疗的抗体偶联二氧化硅修饰金纳米棒:体外实验
- 生长用于形状选择性细胞摄取的金纳米结构


