用于高效结肠癌基因治疗的基于阳离子胶束的 siRNA 递送
摘要
基于小干扰 RNA (siRNA) 的基因治疗为癌症治疗提供了一种替代策略。基因治疗过程中的关键组成部分之一是传递系统。作为一种新型的非病毒基因载体,通过用阳离子 DOTAP 脂质修饰 mPEG-PCL 胶束制备的 DMP 已制备并成功应用于基于质粒 DNA 的结肠癌基因治疗研究。然而,它在 siRNA 传递中的潜力是未知的。本研究优化了DMP的制备工艺,并在小鼠结肠癌模型上研究了DMP/siMcl1和DMP/siBcl-xl复合物的抗癌作用。我们的研究结果表明,DMP 阳离子胶束传递的 siRNA 在体外可以有效抑制 C26 结肠癌细胞的生长。 同时,DMP/siMcl1和DMP/siBcl-xl复合物的瘤内给药明显抑制体内皮下肿瘤模型。这些结果表明DMP/siRNA复合物是癌症基因治疗的潜在候选者。
介绍
癌症是一个主要的全球公共卫生问题。结肠癌是一种常见的恶性肿瘤,每年在全球范围内折磨着超过一百万人[1]。基因治疗已被用作治疗实体瘤和血液肿瘤的方法[2, 3]。癌症基因治疗的关键取决于安全有效的基因传递系统[4, 5]。非病毒载体,包括阳离子脂质、脂质纳米乳剂、固体脂质纳米粒和聚合物载体,由于其在基因传递方面的潜在优势,比病毒载体更受关注:易于制备,引起较少的免疫反应,具有较低的毒性,以及更好的生物相容性 [6, 7]。纳米技术为非病毒载体的研究提供了一种新的手段,具有生物相容性、生物降解性、安全性和靶向能力等优点[2, 8]。其中,大量具有高正电荷的纳米颗粒载体可以通过电荷效应与阴离子核酸药物结合,在基因治疗中显示出广阔而光明的应用前景[9, 10]。
作为一种聚合物共聚物,具有生物降解性和生物相容性,PEG/PCL 共聚物在药物递送系统中显示出有前景的应用 [11,12,13]。基于 MPEG-PCL 胶束,我们使用两亲性 DOTAP 一步修改 MPEG-PCL 共聚物,形成阳离子自组装 DOTAP 和 MPEG-PCL 混合胶束 (DMP) [14,15,16,17]。这些胶束在化学药物和基因药物的递送中显示出良好的稳定性和安全性。例如,DMP 已被用于传递 survivinT34A 自杀基因和姜黄素用于结肠癌治疗 [14, 18]。然而,以往的研究仅限于质粒DNA的传递,目前还没有将DMP胶束传递给其他形式的基因治疗的报道,这限制了DMP胶束在基因治疗中的应用。
除了质粒DNA的治疗基因外,基于siRNA的基因干扰也是基因治疗的重要组成部分。作为基因药物的重要成员,siRNA是双链RNA的小分子。 siRNA 抗癌药物利用内源性 RNAi 机制来沉默癌基因的表达。由于具有提高稳定性和沉默功效等显着优势,siRNA 有潜力发展为癌症治疗应用 [19]。与大分子量的质粒DNA相比,siRNA具有更高的转染效率,特别适用于基因治疗中的特定基因打靶点。因此,它可能是基因治疗的不错选择。目前,多种基于非病毒载体的siRNA治疗药物已经在临床试验中进行了测试,如基于环糊精阳离子聚合物纳米颗粒的CALAA-01和基于脂质的ALN-TTR02[2]。然而,仍然需要基于siRNA的基因治疗来开发新的siRNA靶向点,寻找安全、有效、高特异性的siRNA递送载体。
在本研究中,我们尝试使用 DMP 胶束传递 siRNA 来研究 DMP 胶束传递 siRNA 的效率和安全性。我们使用 Bcl-xl siRNA 和 Mcl1 siRNA 作为治疗靶点,探索它们在体外和体内治疗结肠癌的抗肿瘤作用。 Bcl-xl 基因和 Mcl1 基因是抗凋亡基因 Bcl-2 家族的成员,在抑制细胞凋亡中发挥着至关重要的作用 [20, 21]。我们猜测合成 DMP 胶束可以有效和安全地传递 Bcl-xl siRNA 和 Mcl1 siRNA。 Bcl-xl siRNA和Mcl1 siRNA可以抑制Bcl-xl基因和Mcl1基因的表达,诱导C26细胞凋亡,进而达到抑制C26细胞生长的治疗效果。
材料和方法
材料
N-[1-(2,3-二油酰氧基)丙基]-N, N, N-三甲基甲基硫酸铵 (DOTAP) 购自 Avanti Polar Lipids (Alabaster, AL, USA)。根据我们之前的报道[22],合成了设计分子量为 4000 的 MPEG-PCL 双嵌段共聚物。 MPEG-PCL 共聚物的 Mn 为 4050。 Dulbecco 改良的 Eagle 培养基 (DMEM) 和 3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑 (MTT) 购自 Sigma-Aldrich (USA) ),无需进一步纯化即可使用。二氯甲烷等有机溶剂购自成都科朗化工有限公司(中国成都)。 C26(鼠结肠腺癌)细胞和 293 T(HEK 293 T/17)细胞购自美国典型培养物保藏中心(Manassas, VA, USA)。细胞在含10%胎牛血清的DMEM培养基中培养,37 °C、5% CO2加湿空气培养。
DMP 胶束的制备
为了选择更好的 DMP 制备工艺,在三种有机溶剂中制备 DMP 胶束,每种溶剂具有三种不同剂量的 DOTAP。溶剂方面,选择二氯甲烷、氯仿和乙酸乙酯进行研究,DOTAP的剂量包括5 mg、10 mg和20 mg。 DOTAP和MPEG-PCL共溶解在有机溶剂中,然后用真空泵蒸发,形成干膜。随后将干燥的薄膜在蒸馏水中再水化。最后将制备的DMP胶束保存在4 °C。
DMP 胶束的表征
DMP 胶束的粒径和 zeta 电位由 Zeta 粒度仪 Nano ZS (Malvern Instruments, Worcestershire, UK) 测定,并在测量过程中保持在 25 °C。所有结果都是三个运行的平均值。定性评价 DMP 胶束的稳定性。用肉眼检查 DMP 胶束的聚集体。沉淀的存在表明DMP胶束不稳定,而均匀透明的溶液表明稳定性。
凝胶阻滞
DMP 递送的 Scramble siRNA(DMP/Scramble siRNA)与 2 μL 上样缓冲液混合,上样至 1% 琼脂糖凝胶,140 V 电泳 10 min。 0.2 μg Scramble siRNA 与1、2、3、4、5 和6 μg DMP 胶束组合。凝胶用金观察器染色,紫外灯下可见Scramble siRNA对应的条带。
DMP 胶束的细胞毒性
MTT法评价DMP胶束对293 T细胞和C26细胞的细胞毒性。简而言之,293T细胞和C26细胞以1.2×10 3 的密度铺板 细胞每孔在 100 μL 含 10% FBS(胎牛血清)的 DMEM 培养基中,在 96 孔板中培养 24 h。然后将细胞暴露于一系列不同浓度的 DMP 胶束或 PEI25K 72 小时。使用MTT测定法测量细胞的活力。结果是六次测试运行的平均值。
体外转染
转染前24小时,将C26细胞以5×10 4 的密度接种于24孔板中 每孔含有 10% FBS(胎牛血清)的 0.5 mL DMEM 培养基。转染时,每孔培养基更换为0.5 mL培养基,分别含有0%、10%、20%和30% FBS,以及DMP-delivered FAM(Carboxyfluorescein)siRNA(DMP/FAM siRNA)和PEI-将在无血清培养基中含有 1 μg siRNA 的递送的 FAM siRNA(PEI/FAM siRNA)移入每孔中,DMP/FAM siRNA 和 PEI25K/FAM siRNA 的质量比为 30:1 和 2:1。 24小时后,显微镜下观察转移细胞,流式细胞仪(Epics Elite ESP,美国)测定荧光素酶活性
体内 基因沉默
siRNA靶向小鼠Bcl-xl、Mcl1-1、Scramble siRNA和FAM标记的阴性对照siRNA均以未保护、脱盐、退火形式购自GenePharma Co., Ltd(中国上海)。
为了确定 Bcl-xl mRNA 的水平,使用 TRIzol™ 试剂(Thermo Fisher Scientific,美国)从 C26 细胞中提取总 RNA,并使用 SuperScript II 逆转录酶测定法(Invitrogen)合成单个 cDNA。使用 SYBR GreenER 定量 PCR SuperMix Universal 试剂盒(Invitrogen)进行实时定量 PCR。 PCR引物由TSINGKE Biological Technology (Chengdu, P. R. China)合成。
防扩散研究
MTT法评价DMP/siBcl-xl和DMP/siMcl1对C26细胞的抗增殖能力。简而言之,C26 细胞以 1.2 × 10 3 的密度接种 细胞每孔在 100 μL 含有 10% FBS 的 DMEM 中,在 96 孔板中生长 24 小时。然后将细胞暴露于一系列不同浓度的 DMP/siBcl-xl 和 DMP/siMcl1 72 小时。使用MTT方法测量细胞活力。结果是六次测试运行的平均值。
克隆形成研究
C26细胞以10 3 的密度接种于6孔板 在含有 10% FBS 的 2 mL DMEM 培养基中每孔加入细胞数。二十四小时后,然后将细胞暴露于一系列不同浓度的 DMP 胶束或 DMP/Scramble siRNA 和 DMP/siBcl-xl 和 DMP/siMcl1。当细胞长到肉眼可见的克隆时,终止培养,然后进行漂洗、固定和染色。直接计数克隆数,计算抑制率。
体外 细胞凋亡研究
通过膜联蛋白 V-异硫氰酸荧光素 (FITC) 和碘化丙啶染色观察细胞凋亡。简而言之,将 C26 细胞接种到六孔板中并暴露于一系列 DMP 胶束、DMP/Scramble siRNA、DMP/siBcl-xl 和 DMP/siMcl1 72 小时。然后对细胞进行Annexin V-FITC和碘化丙啶染色。
体内肿瘤异种移植研究
6-8 周龄的BALB/c小鼠接种5×10 6 右侧的 C26 细胞。自肿瘤体积达到100 mm 3 后,每隔一天瘤内注射相当于10 μg siRNA的DMP/siRNA复合物,共进行5个治疗。 .接受等量生理盐水或DMP的小鼠作为对照组。每2 天测量肿瘤大小并监测动物体重,直至处死所有动物。肿瘤体积计算为(1/2×长×宽[2])。
组织学分析
切除的组织在4%中性福尔马林缓冲液中固定24 小时以上,石蜡包埋。组织切片(3-5 μm)用苏木精和伊红染色。该分析按照制造商的方案进行,并用荧光显微镜(× 400)检查样品。
市售的 TUNEL 试剂盒 (Promega, Madison, WI) 用于分析 C26 小鼠黑色素瘤异种移植肿瘤组织的凋亡效应。该分析是按照制造商的协议进行的。
统计分析
数据表示为平均值±SD。使用SPSS软件通过单因素方差分析(ANOVA)进行统计分析。对于所有结果,P ≤ 0.05 被认为具有统计学意义。
结果
准备过程研究
为了获得有效的转染效率和低细胞毒性,我们研究了不同的 DMP 胶束制备工艺,如表 1 所示。 在我们的研究中,在溶剂方面,乙酸乙酯制备的 DMP 胶束非常不稳定,DMP 胶束的稳定时间不超过10 分钟。二氯甲烷和氯仿制备的DMP胶束均具有优异的稳定性,可在96 小时内保持稳定,但氯仿制备的DMP为20mg剂量的DOTAP。更重要的是,它们还具有合适的尺寸、zeta 电位和 PDI。然而,通过比较初始转染效率,二氯甲烷制备的DMP胶束的转染效率高于氯仿制备的DMP胶束。因此我们选择二氯甲烷来制备DMP胶束。
三种剂量的 DOTAP 制备的 DMP 胶束在大小、zeta 电位和 PDI 方面没有明显差异,但用 20 mg 剂量的 DOTAP 制备的 DMP 胶束在三种剂量的 DOTAP 中转染效率最高。通过以上比较,我们选择了基于DOTAP和MPEG-PCL的制备工艺(图1a),制备出稳定性优异、转染效率高的DMP胶束。 DMP胶束的制备流程见图1b。
<图片>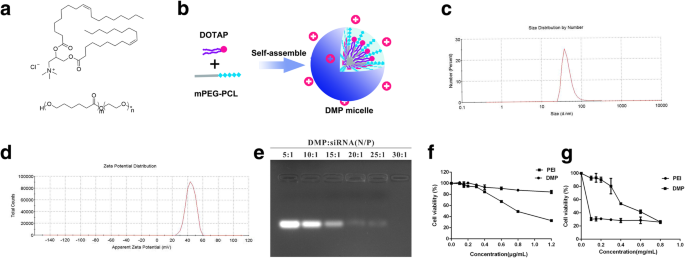
一 DOTAP 和 MPEG-PCL 的分子结构。 b DMP胶束的制备方案。 c DMP 胶束的尺寸分布谱。 d DMP 胶束的 zeta 电位谱。 e siRNA延迟测定。 f DMP 胶束对 293T 细胞的细胞毒性。 g DMP胶束对C26细胞的细胞毒性
DMP 胶束的表征
如图 1c 所示,粒径分布谱表明 DMP 胶束是纳米级的(PDI =0.315),平均粒径为 144.8 nm,表明它的粒径分布非常窄。 DMP 的 zeta 电位谱如图 1d 所示,zeta 电位为 46.4 mV。定性评价了DMP胶束的稳定性。
为了评估 DMP 与 siRNA 的结合能力,进行了凝胶延迟测定,结果如图 1e 所示。当DMP与siRNA的质量比≥ 30时,实现了Scramble siRNA的完全阻滞。阴离子Scramble siRNA通过静电作用吸附在DMP表面,形成DMP/siRNA复合物。
通过MTT方法评估DMP胶束对C26细胞和293T细胞的细胞毒性。如图1f和g所示,PEI25K对293T细胞显示出高毒性,IC50为0.83 μg/mL。然而,DMP 胶束的毒性要小得多,DMP 的 IC50 为 3.7 μg/mL。 DMP 胶束对 C26 细胞的 IC50 为 0.497 mg/mL。然而,PEI25K 表现出巨大的毒性,IC50 <0.1 μg。因此,DMP胶束比PEI25K具有更低的细胞毒性,可用于将siRNA安全地传递给C26细胞。
体外 转染
进一步进行生物物理表征,我们将 DMP 胶束的转染效率与 PEI25K(“黄金标准”转染剂)的转染效率进行了比较体外 .如图2所示,在含有0%、10%、20%和30% FBS转染的培养基中,DMP胶束的转染效率分别为85.47±1.01%、81.57±2.04%、75.29±1.20%和±71.64 1.59%,PEI 的转染效率为 86.38 ± 2.92%。血清组与非血清组的转染效率差异不大。血清组和非血清组转染效率与PEI转染效率相似。此外,图 2a 中的图片展示了对基于 FAM 的报告基因的 DMP 胶束转染能力的直接观察。从图中可以看出,PEI组的细胞室形态与DMP组相比发生了变化,证明PEI具有较高的细胞毒性,而DMP胶束具有较低的细胞毒性。
<图片>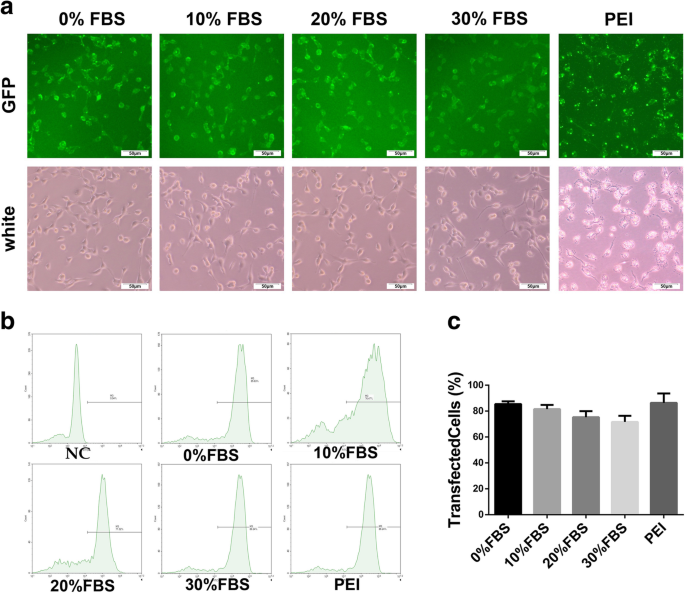
DMP胶束的转染效率。 一 转染 C26 细胞的图片 (b , c ) DMP胶束在含有0%、10%、20%和30% FBS和PEI25K的培养基中的转染效率,流式细胞仪计数
抗癌活性体外
在基因治疗过程中,siRNA起着至关重要的作用。因此,我们设计了一个 Bcl-xl 靶向 siRNA 和一个 Mcl1 靶向 siRNA 来研究它们的抗癌活性。为了评估 Bcl-xl siRNA 和 Mcl1 siRNA 的干扰能力,我们通过 qPCR 确认了 Bcl-xl siRNA 和 Mcl1 siRNA 的干扰能力。根据我们的结果(图 3),DMP/siMcl1 组的 mRNA 水平低于对照组(图 3a)。并且 DMP/siBcl-xl 组的 mRNA 水平低于对照组(图 3b)。已充分证明DMP/siBcl-xl和DMP/siMCL1可有效降低相关mRNA水平。
<图片>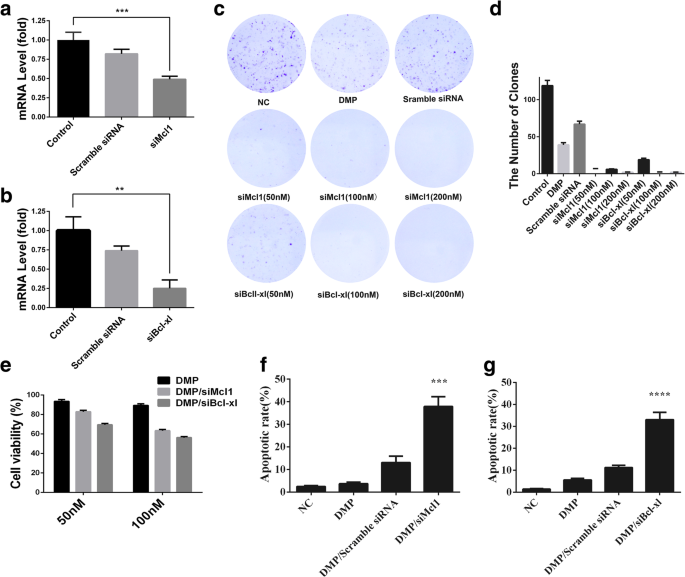
一 DMP/siMcl1明显降低了Bcl-xl的mRNA水平。 b DMP/siBcl-xl明显降低了Mcl1的mRNA水平。 c 用不同浓度的 DMP/siBcl-xl 或 DMP/siMcl1 处理后克隆形成的图片。 d 用不同浓度siRNA的DMP/siBcl-xl处理后的克隆数。 e DMP/siBcl-xl 和 DMP/siMcl1 在 50-nM 和 100-nM siRNA 浓度下对 C26 细胞的体外抗癌能力。 f 不同浓度siMcl1的DMP/siMcl1处理后克隆形成的抑制率。 g 不同浓度siBcl-xl的DMP/siBcl-xl处理对克隆形成的抑制率
此外,使用DMP胶束将siRNA递送至C26细胞以研究DMP/siBcl-xl和DMP/siMcl1可抑制C26细胞的生长。 C26细胞的活力通过MTT法测定。结果显示DMP/siBcl-xl(50 nM和100 nM)的细胞存活率分别为69.6%±3.3%和56.3%±1.9%,DMP/siMcl1(50 nM和100 nM)的细胞存活率分别为82.8 %±3.1% 和 56.3%±3.2%(图 3e)。
为了进一步研究 DMP/siBcl-xl 和 DMP/siMcl1 的抗癌活性,进行了克隆形成试验。很明显,图3c和d中,与对照组相比,DMP/siBcl-xl和DMP/siMcl1(50 nM和100 nM)中的克隆数较少。这些结果表明DMP/siBcl-xl和DMP/siMcl1对C26细胞有明显的抗增殖作用。因此,结合MTT检测结果,结果表明DMP/siBcl-xl和DMP/siMcl1均能抑制C26细胞的增殖,对C26细胞具有显着的抗癌活性。
为了确定 DMP/siBcl-xl 和 DMP/siMcl1 诱导的 DMP 胶束增殖能力和细胞活力的丧失是否与诱导细胞凋亡有关,通过流式细胞术评估了凋亡细胞的数量。如图 3f 所示,DMP/siMcl1 组的细胞凋亡率为 37.9%±4.7%,高于对照组和 DMP 组和 DMP/Scramble siRNA 组。如图3g所示,DMP/siBcl-xl组的细胞凋亡率为33.0%±3.8%,也高于其他对照组。这些凋亡数据表明DMP/siMcl1和DMP/siBcl-xl具有很强的诱导凋亡能力。细胞凋亡检测结果与MTT结果和前面描述的克隆形成结果一致,表明诱导细胞凋亡是抑制C26细胞增殖和活力的可能机制。
DMP/siRNA 复合物抑制 C26 肿瘤生长体内
还利用 C26 异种移植动物模型来测试 DMP/siRNA 复合物的体内抗肿瘤功效。各组C26异种移植肿瘤的肿瘤生长曲线和图像如图4a和b所示。根据我们的结果,与对照组相比,瘤内注射 DMP/siMcl1 和 DMP/siBcl-xl 导致异种移植肿瘤生长的显着抑制。每组肿瘤的重量如图4b所示。与 NS 治疗组 (0.85 ± 0.09 g) 和 DMP 组 (0.76 ± 0.11 g) 相比,DMP/siMcl1 复合物导致肿瘤重量显着降低 (0.34 ± 0.06 g, P <0.01),同时,DMP/siBcl-xl 复合物导致肿瘤重量的统计学显着降低 (0.42 ± 0.08 g, P <0.01)。这些结果表明瘤内注射DMP/siRNA复合物可以有效抑制C26结肠癌模型皮下移植瘤的生长。通过 HE 分析检查 DMP/siRNA 复合物对其他器官的体内副作用。如图4所示,心脏、肝脏、脾脏、肺脏、肾脏均未见明显病理改变。
<图片>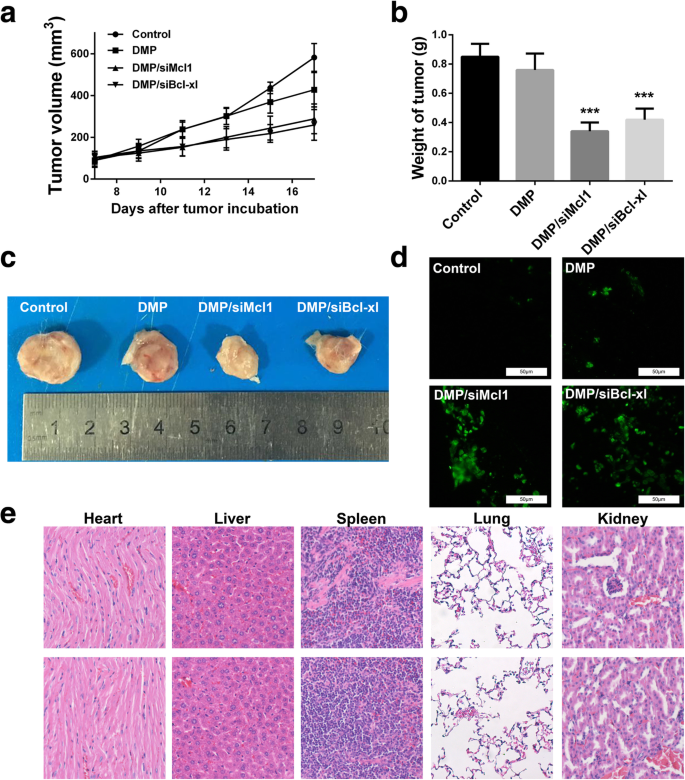
DMP/siRNA 对 C26 小鼠异种移植模型的抗癌作用和安全性。 一 肿瘤发展曲线,按肿瘤体积计算。 b 每组肿瘤的平均重量。与其他治疗组相比,DMP/siMcl1组和DMP/siBcl-xl组的肿瘤重量有统计学意义的降低(***P , 0.001)。 c C26 结肠癌肿瘤的代表性图像。 d TUNEL 法检测肿瘤组织中的细胞凋亡。 e 两种模型中每个治疗组的主要器官的 HE 分析。心、肝、脾、肺、肾未见明显病理改变
讨论
在本研究中,制备了阳离子自组装 DOTAP 和 MPEG-PCL 混合胶束以提供 Bcl-xl siRNA 和 Mcl1 siRNA,用于治疗 C26 结肠癌。这些 DMP 胶束具有优异的稳定性,能够有效地结合 Bcl-xl siRNA 和 Mcl1 siRNA 并将其传递给 C26 细胞。更重要的是,DMP胶束前所未有地传递siRNA(Bcl-xl siRNA和Mcl1 siRNA),可以有效诱导C26细胞凋亡,从而在体外和体内抑制C26细胞的生长,安全性高。综上所述,我们的研究表明,DMP 是一种潜在的 siRNA 基因传递载体。
有报道称,阳离子脂质DOTAP已被广泛应用于siRNA的递送,但其产生强正电荷引发溶血且具有高细胞毒性。基于DOTAP阳离子脂质体转染效率高,但其正电荷会产生毒性,原因可能是带正电荷的DMP季铵盐头部暴露在脂质体磷脂双层表面。然而,基于 DOTAP 脂质的 DMP 胶束具有高转染率和低细胞毒性。我们推测在胶束自组装过程中,DOTAP嵌入在聚合物纳米粒子内部,其中季铵盐头部没有完全暴露在表面。因此,部分正电荷被掩盖了;同时,我们的结果也表明,与PEI25K的转染效率相比,DMP胶束的转染效率并不低。说明被覆盖后DOTAP的正电荷仍有部分暴露,显示出适当的电位,证明该电位水平足以结合和传输siRNA。此外,我们的结果表明,基于 MPEG-PCL 的 DMP 胶束是一种有效且安全的基因传递载体,它针对 DOTAP 的细胞毒性进行了优化,并保留了 DOTAP 的基因传递能力。并且有类似的研究报道了DOTAP与其他材料结合后的细胞毒性降低[23]。最近,与 lipofectamine 相比,由 DOTAP 和 SWNT 组成的新型载体在 siRNA 递送中具有更低的细胞毒性 [8]。通过使用双乳液溶剂蒸发 (DESE) 方法制备 DOTAP-PLGA 胶束的 LPN 产生纳米级载体 [24,25,26]。这些研究与我们的研究中描述的非常吻合,在一定程度上使我们的猜想更有说服力。
基因转移载体的传递效率受血清的影响很大。血清中的血清蛋白可以中和纳米载体/siRNA复合物表面的正电荷,这是受负电荷细胞表面静电效应的影响[27,28,29]。
在我们的研究中,当我们研究 DMP 胶束的转染效率时,我们设置了一系列含有 0%、10%、20% 和 30% FBS 的 DMEM 培养基用于转染,研究血清对加载的转染效率的影响。 FAM siRNA 纳米粒子。我们的结果表明 FBS 的存在对转染效率几乎没有影响。在本文中,我们使用MPEG-PCL来覆盖DOTAP,将DOTAP嵌入MP内部,部分部分以适当的比例留在表面。基于这种结构,我们推测DOTAP的正电荷由于MPEG-PCL的覆盖而部分隐藏,降低了暴露于血清蛋白的水平,从而避免了血清对转染的影响。这意味着除了修饰后阳离子载体表面电荷降低外,血清转染的存在对阳离子聚合物载体的效率影响不大。由于DMP胶束体外在血清环境中表现出优异的转染能力,表明该血清对DMP介导的siRNA体外细胞实验几乎没有影响。
结论
在这项研究中,制备的 DMP 胶束具有递送 siRNA 的能力。并且使用DMP胶束将Bcl-xl siRNA和Mcl1 siRNA递送到C26细胞中用于体外抗癌活性研究。我们研究了DMP胶束的制备工艺,选择了一种优良的制备工艺,制备了尺寸窄、zeta电位好、稳定性好的DMP胶束。此外,制备的DMP胶束在体外转染实验中不受血清存在的影响。更重要的是,DMP/siBcl-xl和DMP/siMcl1可以抑制Bcl-xl基因和Mcl1基因的表达,诱导C26细胞凋亡,进而达到抑制C26细胞生长的治疗效果。 DMP/siRNA复合物瘤内注射可有效抑制C26结肠癌模型皮下移植瘤的生长。心、肝、脾、肺、肾未见明显病理改变。相信DMP胶束可以作为一种有效的载体来传递siRNA治疗结肠癌。
缩写
- DOTAP:
-
N-[1-(2, 3-二油酰氧基)丙基]-N, N, N-三甲基甲基硫酸铵
- mPEG-PCL:
-
甲氧基聚(乙二醇)聚(己内酯)
- MTT:
-
3-(4, 5-dimethythiazol-2-yl)-2,5-二苯基溴化四唑
- siRNA:
-
小干扰RNA
纳米材料
- 用于增强药物递送的纳米纤维和细丝
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 用于 NIR-II 光热疗法的 BSA 涂层金纳米棒
- 环境响应金属-有机框架作为肿瘤治疗的给药系统
- 用于癌症应用的基于细胞的药物递送
- DNA 四面体递送增强多柔比星诱导的 HT-29 结肠癌细胞凋亡
- 用于索拉非尼递送的基于核苷脂质的纳米载体
- 掺杂 Sb2O3 纳米晶体:一种用于有机降解的高效可见光催化剂
- 纳米粒子相关疗法的新途径
- Carbon Dots @ Platinum Porphyrin Composite 作为用于有效光动力癌症治疗的治疗诊断纳米剂
- 环境兼容的生物共轭金纳米粒子作为炎症诱导的癌症成像的有效造影剂
- 远程状态监测和远程服务:服务团队高效服务交付的关键


