撤回文章:聚乙二醇包覆的钴铁氧体纳米球和纳米颗粒的毒性比较研究
摘要
我们对聚乙二醇 (PEG) 涂层的铁氧体钴纳米粒子和纳米球的毒性进行了比较研究。纳米粒子采用水热法制备,纳米球采用溶剂热法制备。纳米材料的表面被成功地用聚乙二醇改性。为了研究制备的样品的形貌,采用了 X 射线衍射 (XRD)、傅里叶变换红外 (FTIR) 光谱、拉曼光谱、热重分析 (TGA) 和电子显微镜技术。结构分析证实了多晶钴铁氧体纳米粒子的形成,其直径分别在 20-25 nm 范围内和纳米球在 80-100 nm 范围内。昆明SPF小鼠(雌性,6-8 周龄)被用来研究钴铁氧体纳米颗粒和纳米球在小鼠不同器官中的毒性。进行生物分布研究、生化指标、组织病理学评估、炎症因子、氧化和抗氧化水平以及细胞毒性测试,以评估铁酸钴纳米颗粒和纳米球对小鼠的毒性。结果表明,铁氧体钴纳米球比纳米颗粒毒性更大,并且姜黄素被证明是一种良好的治疗剂,可以治疗由PEG包覆的铁氧体钴纳米材料引起的小鼠毒性。
介绍
近年来,磁性纳米材料在基础研究和技术应用方面都受到了极大的关注。这些应用包括但不限于药物输送载体 [1,2,3]、磁共振成像 (MRI) [4,5,6]、热疗 [7,8,9]、生物传感器 [10]、细胞分离 [11]、蛋白质分离 [11、12]、基因磁转染 [13、14、15],以及环境污染和修复 [16、17]。钴铁氧体作为硬磁材料,被用作 MRI 的造影剂、靶向药物输送和热疗中的加热介质 [18,19,20,21,22,23]。铁氧体钴虽然用于生物医学应用,但由于在溶液中释放出大量钴而具有高毒性、在溶液中聚集以及使用表面活性剂时表面可及性差等限制条件。因此,通过使用某些生物相容、无毒、水稳定和分散的材料进行表面改性,克服了这个问题 [24,25,26,27,28]。此外,钴铁氧体的制造简单且具有成本效益,可为任何特定应用定制成分、形状和尺寸。纳米铁氧体钴的合成技术多种多样,包括机械化学[29]、声化学[30]、共沉淀[31、32]、微乳液[33]等[34,35,36,37] ,38]。类似地,采用其他技术,包括单步环保方法,以姜黄素为模板制备定制的荧光铜纳米团簇 [39]。大多数这些技术的主要缺点是所制备材料的低结晶度,这反过来会导致磁特性的显着劣化。在这方面,水热[40]和溶剂热[41]技术是合成形貌和结晶度可控的钴铁氧体的最有效和最有效的技术。
在文献中,各种纳米材料,如银纳米粒子 (Ag NPs) 已被报道用于抗菌治疗和相关的传染病,以及它们被用作药物输送和治疗不同疾病的纳米载体 [42]。在另一篇评论文章中,据报道高铁酸盐可用于去除废水中的各种化学和生物物种 [43]。在铁酸钴纳米材料的生物医学应用中,主要问题是铁酸钴在器官中的积累,导致体内毒性,需要紧急从器官中清除收集到的纳米材料,并需要修复铁酸钴引起的损伤。一些研究人员对抗炎药物进行了研究,发现这些药物可以降低纳米材料引起的毒性[44, 45]。姜黄素具有抗氧化、抗突变、抗肿瘤和致癌等特性,可作为铁酸钴纳米材料诱导毒性的治愈剂[46,47,48]。通过直接与TNF结合,具有在体外和体内用作TNF阻滞剂的能力[49]。
这项工作的目的是在实验室中以可控的形态制造聚乙二醇 (PEG) 涂层的铁氧体钴纳米颗粒和纳米球。将不同剂量的纳米材料静脉注射到小鼠体内,并进行血液分析、生物分布、HE 染色和细胞活力研究,以评估这些纳米材料的毒性。比较了铁氧体钴纳米颗粒和纳米球的毒性,并以姜黄素为治疗剂治疗铁氧体钴纳米球对小鼠的毒性。结果表明,钴铁氧体纳米球比纳米颗粒的毒性更大,因为它们的表面积增大,这使得它们比纳米颗粒更具毒性和反应性。据我们所知,这是我们之前没有进行的此类详细研究。
材料和方法
纳米材料的制备
为了制备 PEG 包覆的铁氧体钴纳米粒子,我们采用了水热技术 [40, 47]。为此,分别在 25 mL 去离子 (DI) 水中制备氯化钴 (0.2 M) 和硝酸铁 (0.4 M) 溶液,然后将这些溶液与 25 mL 聚乙二醇水溶液 (2.5 mM) 和分别为氢氧化钠 (3 M)。然后将混合物搅拌 20 分钟并倒入不锈钢 (SS) 高压釜中,将其在 180°C 下加热 6 小时。该过程完成后,将混合物冷却至室温,然后使用去离子水和乙醇将溶液洗涤 2-3 次,以去除混合物中任何不需要的杂质。混合物在烘箱中约80°C干燥过夜,然后研磨成细粉,得到所需的钴铁氧体纳米颗粒。
为制备 PEG 包覆的铁氧体钴纳米球,使用溶剂热技术。为此,将六水氯化钴溶解在 40 mL 乙二醇 (2.5 mM) 中,然后加入 1.35 g 六水氯化铁和 1 g 聚乙二醇 (PEG)。然后将混合物搅拌约 30 分钟,然后密封在衬有聚四氟乙烯的 SS 高压釜中。然后将高压釜在 200°C 下加热 8 h,反应完成后,将其冷却至室温。将混合物用去离子水和乙醇洗涤,然后在烘箱中在 80°C 下干燥过夜。最后,将混合物研磨成细粉,得到直径在 80-100 nm 范围内的 PEG 包覆的铁氧体钴纳米球。按照参考文献中使用的方法通过 X 射线衍射 (XRD) 研究制备的纳米材料的形态。 [50],参考文献中使用的扫描和透射电子显微镜(SEM 和 TEM)。 [50, 51],室温傅里叶变换红外 (FTIR) 光谱测定铁氧体钴中的官能团,类似于参考文献。 [51]、拉曼光谱和热重 (TGA) 分析,如参考文献中所用。 [52].
纳米材料的放射性标记
用 99m 对PEG包覆的铁氧体钴纳米颗粒和纳米球进行放射性标记 Tc 使用氯化亚锡作为还原剂 [53,54,55]。为此,新鲜的 99m 通过将 TcO4 发生器洗脱液(50 μL,活性约为 4 mCi)添加到 30 μL SnCl2 悬浮液(1 mg/mL,在 0.5 N HCl 中)来制备。在 NaHCO3 溶液 (1 M) 的帮助下,将悬浮液的 pH 值调整为 8-10。将含有约 0.4%wt 铁氧体钴的纳米颗粒和纳米球溶液(各 40 μL)与氯化亚锡(50 μg)、抗坏血酸(10 mg/mL)和 99m 的悬浮液混合 氧化钛。然后将混合物在 80 °C 下以 10,000 rpm 搅拌 25 分钟。为了准确测量,由于 99m 的短寿命,放射性计数在24 h内记录 Tc (~ 6 h)。离心后倒出上清液,鉴定剩余物质为 99m Tc-PEG-钴铁氧体纳米颗粒和纳米球。采用纸色谱法测定标记化合物的放射性产率,超过65%,反映了纳米材料在小鼠体内的真实生物分布。
纳米材料的生物分布
如图1所示,昆明SPF小鼠(雌性,6-8 周龄,体重18-20 g)来自中国兰州大学医学实验室中心。所有小鼠都被关在笼子里,温度控制系统保持在 21-22 °C,灯从 08:00 到 20:00 h 打开。小鼠可以免费获得食物和自来水,并按照美国国家医学研究学会制定的实验动物护理协议和美国国立卫生研究院的指导方针进行处理。将小鼠随机分为几组,每组5只,然后静脉注射 99m 纳米颗粒和纳米球的 Tc-PEG-钴铁氧体溶液,分别在 1 h、6 h、16 h 和 24 h 后被杀死。立即解剖心、肺、肝、脾和肾组织,用箔纸包裹,称重,然后测定 99m 的放射性 使用伽马计数器检测器测量每个组织中的 Tc。纳米材料在小鼠不同器官中的生物分布以每克湿组织的注射剂量百分比(即% ID/g)表示。
<图片>
实验模型示意图
苏木精和曙红染色
对于苏木精和伊红 (HE) 染色,将石蜡切片放入二甲苯中进行脱蜡,该过程重复两次,每次约 10 分钟。通过将载玻片转移到浓度分别为 100%、95% 和 70% 乙醇的不同乙醇溶液中 2 分钟来进行样品的水合。室温下自来水冲洗玻片约2 min,完成后,将细胞核在60℃苏木精染色液中染色10 s,然后在室温下1 min,然后放置玻片在流动的自来水下在室温下放置约 5 分钟。将样品在伊红 Y 工作液中染色 2 分钟,然后先将样品浸入 95% 乙醇中脱水,然后在 100% 乙醇中各浸 2 分钟。通过在曙红染色溶液中浸渍15 秒,将细胞质染色7 秒。去除后,细胞质用无水乙醇洗涤脱水2次,每次1 min。然后用二甲苯使组织透明 15 秒,检查细胞质,然后使用中性树胶密封拍照。使用Olympus Microphot-CX41显微镜结合数码相机对组织进行显微检查。
生化指标和炎症因子
暴露组小鼠静脉注射PEG包覆铁氧体钴纳米颗粒和纳米球250μg,对照组小鼠用0.9%生理盐水处理,24 h后处死小鼠。从小鼠身上采集血液并离心约10 分钟以获得血清。血清TB、ALT、AST、BUN、CREA和Cys-C的含量采用酶联免疫吸附试验(ELISA)和蛋白质印迹法测定。与肝脏相关的酶 IL-6、IL-8 和 TNF-α 在坏死诱导的炎症反应中起关键作用。当器官对炎症作出反应时,通常会出现高水平的这些表达。
MTT 细胞活力测定
通过 MTT(一种用于评估细胞代谢活动的比色法)测定 PEG 包覆的铁氧体钴纳米颗粒和纳米球的细胞毒性潜力。购自中国上海的人上皮细胞 L-132 和人单核细胞 THP-1 暴露于不同浓度的纳米颗粒,范围为 30-125 μg/mL,纳米球的范围为 50-250 μg/mL,光密度为使用微孔板分光光度计系统(UNICO WFZ UV-2000,上海,中国)在 590 nm 处测量不同的测定。选择 L-132 细胞是因为吸入是暴露纳米材料的主要途径,并且使用 THP-1 细胞是因为它们具有清除异物的作用。在每个测定中,未处理的细胞被评估为阴性对照。在细胞中观察到酶活性的抑制,将其与未处理的(阴性对照)细胞进行比较,数值以阴性对照的比率的形式导出,并与纳米颗粒和纳米球的浓度作图。
统计分析
每个数据点报告为一式三份进行的实验的平均值(±sem)。通过方差分析评价差异的显着性,并借助Origin和Microsoft Excel软件绘制统计图表。
结果与讨论
结构分析
制备的纳米材料的结构分析(XRD、FTIR、拉曼和 TGA)如图 2 所示。图 2a 中的 XRD 结果代表纳米级的涂覆和未涂覆的铁酸钴,这证实了铁酸钴的制备成功。 XRD 数据中所有观察到的峰的位置和相对强度证实了钴铁氧体的结晶性质。没有观察到额外的峰,这表明制备的钴铁氧体的纯度。钴铁氧体的平均微晶尺寸是通过使用 Scherrer 方程 [56] 确定的,发现其为 ~ 24 nm。进行傅里叶变换红外 (FTIR) 光谱以研究铁酸钴中的阳离子分布(镍、钴和铁)。图 2b 显示了在室温下收集的 FTIR 数据。理论上,钴铁氧体有两个强吸收带(ʋ1 和 ʋ2),以及少数出现在 400–600 cm −1 范围内的吸收带 .所有这些峰都清楚地显示在我们的数据中,如图 2b 所示。在 FTIR 数据中,ʋ1 对应于金属在四面体位置的固有伸缩振动,而 ʋ2 对应于金属离子在八面体位置的伸缩振动 [57,58,59]。 FTIR 峰出现在 3421 cm −1 对应于聚乙二醇 (PEG),表明它成功地键合在钴铁氧体表面。在室温下收集的钴铁氧体的拉曼分析如图 2c 所示,这表明数据中可以看到 5 个不同的峰。峰值出现在 700 cm −1 以下 是主要特征峰(A 1g 模式)的钴铁氧体对应于氧离子沿四面体位置的 Fe-O 键的拉伸 [60],而数据中出现的其他峰也属于铁氧体钴。这证实了在我们的实验中成功制造了 PEG-钴铁氧体。图 2d 显示了在 50-380 °C 温度范围内收集的样品的 TGA 结果,这表明钴铁氧体在不同温度下重量减轻。 TGA分析也表明PEG的热稳定性较低,而PEG-钴铁氧体的热稳定性较高。
<图片>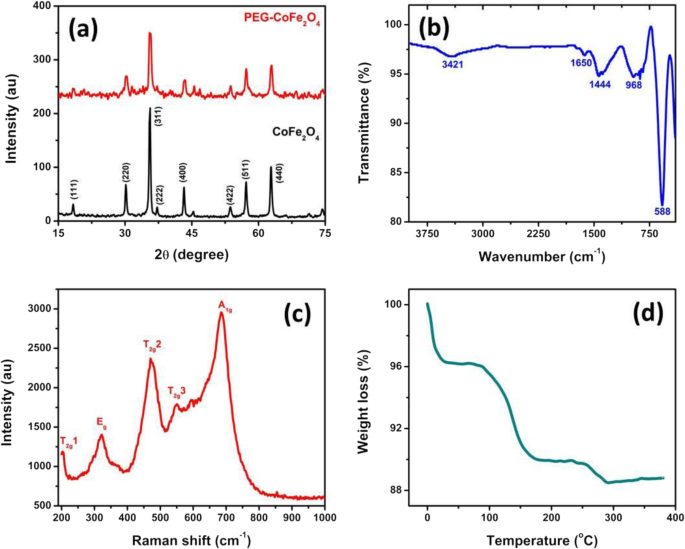
一 钴铁氧体的XRD结果。 b 在 500–4000 cm -1 范围内使用的傅里叶变换红外 (FTIR) 光谱 . c 190-1000 cm −1 采集样品的室温拉曼光谱 频率范围。 d 在 50–400 °C 温度范围内收集的 PEG 包覆的 CoFe2O4 的热重分析 (TGA)
样品的电子显微镜分析如图 3 所示。图 3(a) 和 (b) 分别表示 PEG 包覆的铁氧体钴纳米粒子和纳米球的 SEM 图像,而图 3(c) 和 (d) 表示分别对纳米球和纳米粒子进行 TEM 分析。这些结果表明纳米颗粒的平均尺寸约为 25 nm,纳米球的平均尺寸为 80-100 nm。从纳米球的 TEM 图像可以看出,纳米球由大量具有大表面积的较小纳米粒子组成,从而使它们具有介孔性,这对于纳米材料作为载药载体的医学应用非常理想。所有这些结构分析都证实了纯相PEG包覆的铁氧体钴纳米颗粒和纳米球的成功形成。
<图片>
钴铁氧体纳米粒子 (a ) 和纳米球 (b )。 PEG 包覆的铁氧体钴纳米粒子的 TEM 图像 (c ) 和纳米球 (d ),以不同分辨率收集
生物分布研究
定量地,不同时间间隔(1、6、16和24 h)后,PE包覆的铁氧体钴纳米粒子和纳米球在血液、心脏、肝脏、脾脏、肺脏和肾脏中的生物分布如图4所示。在静脉注射 99m 后24 h内评估血液和其他器官中铁酸钴的存在 Tc-PEG-钴铁氧体溶液(纳米颗粒和纳米球)。对于图 4(a) 所示的纳米球,在暴露 1 小时后发现铁酸钴的血液滞留率为 6.5 ± 0.33% ID/g,然后在接下来的时间间隔内逐渐降低(即, 6、16 和 24 h)。可见纳米球主要分布于心、肝、脾、肺、肾;然而,它们中的大部分主要积聚在脾脏中。此外,发现纳米球在各器官中的生物分布在第一小时后最高,然后逐渐下降,6 小时后仍低于 30%。在钴铁氧体纳米粒子的情况下,纳米粒子在暴露 1 h 后的血液滞留率约为 2.8±0.14% ID/g,表明放射性物质从人体血池中的清除速度相对较快,然后随着时间的推移而减少如图4(b)所示。纳米颗粒分布在心脏、肝脏、脾脏、肺和肾脏中,在脾脏和肝脏中浓度最大。从图中可以看出,纳米颗粒在血液和其他器官中的生物分布在第一小时后最高,然后在6 小时后逐渐下降,最终在24 小时后达到最低值。如果我们比较纳米球和纳米颗粒的生物分布结果,可以看出,与纳米颗粒相比,PEG 包覆的铁氧体钴纳米球在小鼠血液和其他器官中的积累/存在更多。与纳米颗粒相比,这可能与纳米球的大表面积和高孔隙率有关,这是确定纳米材料与生物系统相互作用的关键因素之一。在纳米粒子的情况下,它们的非介孔性质和低比表面积使它们在相同条件下的反应性低于纳米球。这些特征可能降低了 PEG 包覆的铁氧体钴纳米粒子在小鼠血液和其他器官中的长期抵抗力。此外,纳米球与生物分子形成复合物,导致自由基种类增加,氧化应激水平增加,损伤细胞DNA,脂质过氧化导致氧化应激。
<图片>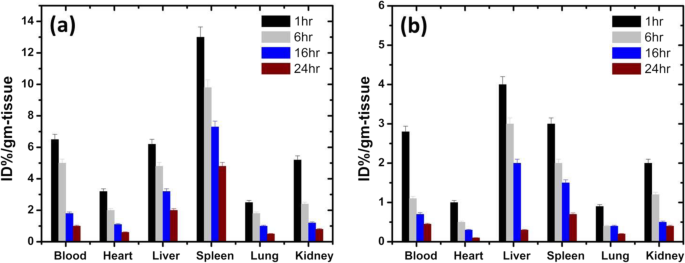
不同时间间隔(1、6、16、24 h)暴露于纳米球后PEG-CoFe2O4在血液、心脏、肝脏、脾脏、肺和肾脏中的生物分布(a ) 和纳米粒子 (b )
生化指数
为了研究 PEG-钴铁氧体纳米颗粒和纳米球对小鼠的毒性作用,测量了生化指标,结果如图 5 所示。测量了包括 ALT、AST、BUN、CREA、TB 和 Cys-C 在内的各种参数对照组和暴露组小鼠。采用SPSS软件进行数据提取,*P <0.05 代表测量期间的显着变化。在纳米球和纳米颗粒中,与对照组小鼠相比,所有生化指标都显示出显着变化(*P <0.05)。在钴铁氧体纳米球暴露组的情况下,ALT、AST和BUN的水平表现出显着差异(*P <0.05) 与对照组小鼠相比,而在纳米颗粒暴露组的情况下,只有 Cys-C 与对照组小鼠相比表现出显着差异 (*P <0.05)。可以看出,在纳米球的情况下,主要负责肾功能生物标志物的TB和Cys-C显着降低。这表明与纳米颗粒相比,暴露于 PEG-钴铁氧体纳米球对肾脏的影响更大。 AST 作为肝脏的生物标志物,受纳米颗粒和纳米球暴露的影响更大。这表明接触铁酸钴会对肝功能产生不利影响。从所有这些结果可以看出,与铁氧体钴纳米颗粒相比,PEG-铁氧体钴纳米球在小鼠体内造成的损伤更大。
<图片>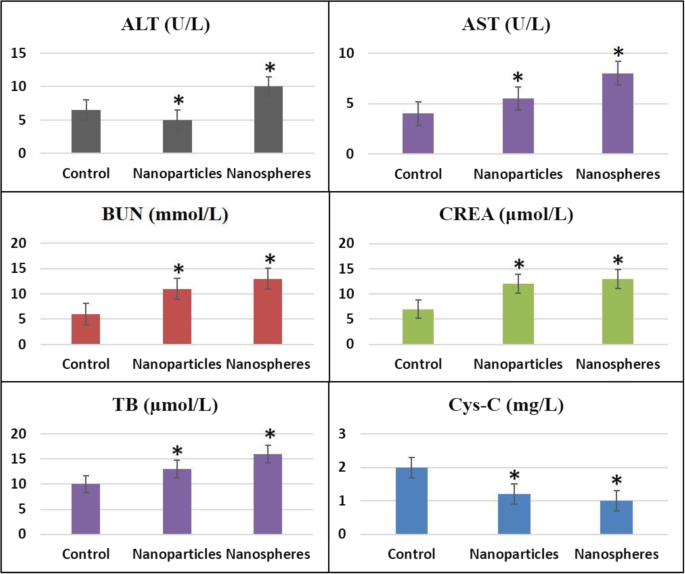
对照组、纳米颗粒和纳米球暴露组小鼠血清生化指标。数据代表一式三份进行的两次独立实验的平均值±标准差。 *P <0.01
组织病理学研究
我们已经展示了对照组、纳米颗粒、纳米球和治疗组小鼠的组织病理学分析,如图 6 所示。如果我们将纳米球和纳米颗粒暴露组与对照组小鼠的结果进行比较,可以看出 PEG-钴铁氧体纳米球是与纳米颗粒暴露组相比,在小鼠的不同器官(肝、脾、肾和肺)中产生更多的损伤。在肾脏中,与纳米颗粒暴露和对照组小鼠相比,在摄入纳米球的情况下,肾小球充血发生并伴有轻度水肿和间质炎症细胞。还可以看出,纳米颗粒比纳米球显示出更少的炎症。在纳米颗粒暴露的情况下,发现肺部受到的影响相对较小,而在纳米球的情况下,发现肺泡壁增厚并观察到轻度纤维化。此外,纳米球暴露组的肝细胞出现肿胀和水肿,而纳米颗粒暴露组小鼠的炎症相对较少。
<图片>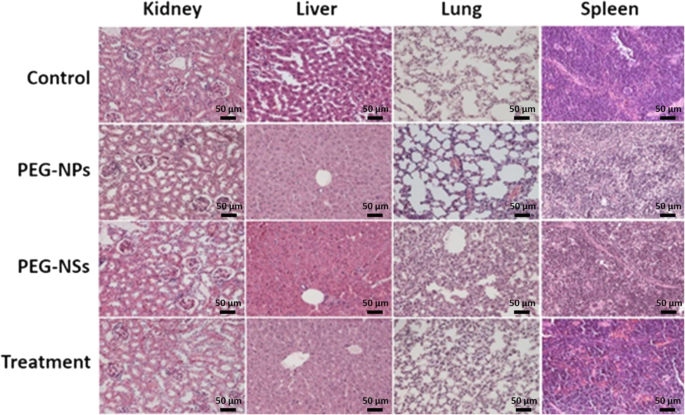
不同组(对照组、纳米颗粒、纳米球和治疗组)组织的组织切片
炎症因子和氧化/抗氧化水平
测量IL-6、IL-8、TNF-α、MDA和T-AOC的表达水平,结果如图7所示。图7a代表IL-6、IL-8、和 β-肌动蛋白用于对照组、纳米颗粒和纳米球暴露组。对照、纳米颗粒和纳米球暴露组的 IL-6 和 IL-8 的相对蛋白质水平如图 7b 所示,而 TNF-α、MDA 和 T-AOC 的含量如图 7c-所示。 e 带 *P <0.05 暴露组与对照组± sem。结果显示钴铁氧体纳米球暴露组小鼠的IL-6、IL-8、TNF-α和MDA水平高于纳米颗粒组,且均高于对照组小鼠。在 T-AOC 的情况下,纳米球的水平低于纳米颗粒暴露和对照组小鼠的水平。所有这些结果表明,纳米颗粒和纳米球正在引起小鼠的炎症,尤其是肝脏。然而,纳米球比纳米颗粒对器官的影响更大。众所周知,纳米材料在体内会产生氧自由基(ROS),导致抗氧化剂的一系列质的减少,导致生物组织氧化损伤,对细胞生物产生不利影响[61, 62]。此外,当暴露于纳米颗粒的小鼠与暴露于纳米球的小鼠的 IL-6、IL-8、TNF-α、MDA 和 T-AOC 水平进行比较时,发现铁酸钴纳米球导致更多的炎症与纳米粒子暴露组小鼠相比。
<图片>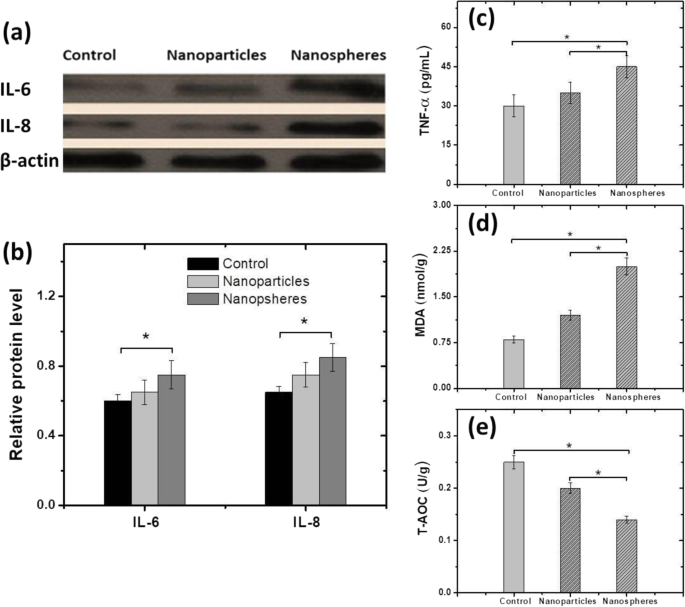
IL-6、IL-8、TNF-α、MDA 和 T-AOC 的表达。 一 对照、纳米颗粒和纳米球暴露组中 IL-6、IL-8 和 β-肌动蛋白的蛋白质印迹条带。 b IL-6 和 IL-8 的相对表达水平。 c TNF-α的含量。 d MDA 级别。 e 对照组和暴露组(纳米颗粒和纳米球)的 T-AOC 含量统计图表。 (*P <0.05 暴露组 vs 对照组± sem)
细胞毒性评估
对不同浓度的 PEG 包覆的铁氧体钴纳米球和纳米粒子进行了细胞毒性研究,结果如图 8 所示。L-132 细胞的存活百分比如图 8(a) 所示,而图 8 (b) 代表 THP-1 细胞的存活百分比。可以看出,对于高于 100 μg/mL 的浓度,在两种细胞中观察到的细胞活力都有显着变化,并且可以看出,在 PEG 纳米球的情况下,结果更加明显。这证实了钴铁氧体纳米球与纳米颗粒相比产生了更多的损伤。此外,细胞活力随着纳米颗粒和纳米球浓度的增加而降低,这表明两种形式的 PEG 包覆的铁氧体钴在小鼠中随着浓度的增加而产生更多的毒性。由于两种不同的细胞靶标(L-132 和 THP-1),根据细胞死亡机制,人们可以预期细胞反应不会完全相同 [63]。即使对于相似大小的颗粒,解释细胞靶标特异性的可能原因可能归因于吞噬作用的功能,其特征在于单核细胞(THP-1 细胞),而不是肺上皮细胞 [64]。众所周知,单个纳米球是由大量的小纳米粒子组成的。因此,与纳米颗粒相比,它具有较大的表面积,因此与纳米颗粒相比,它具有更高的反应性和更多的与生物系统(组织)相互作用的机会。此外,由于纳米球的尺寸较大,一旦进入器官,它们就不容易通过血液或尿液循环被分泌出来。因此,与纳米颗粒相比,它们在体内(器官)停留的时间相对较长,进而对组织产生不利影响。此外,纳米球导致巨噬细胞功能降低,纳米球自身的吞噬作用降低,巨噬细胞迁移率降低和细胞骨架功能障碍。
<图片>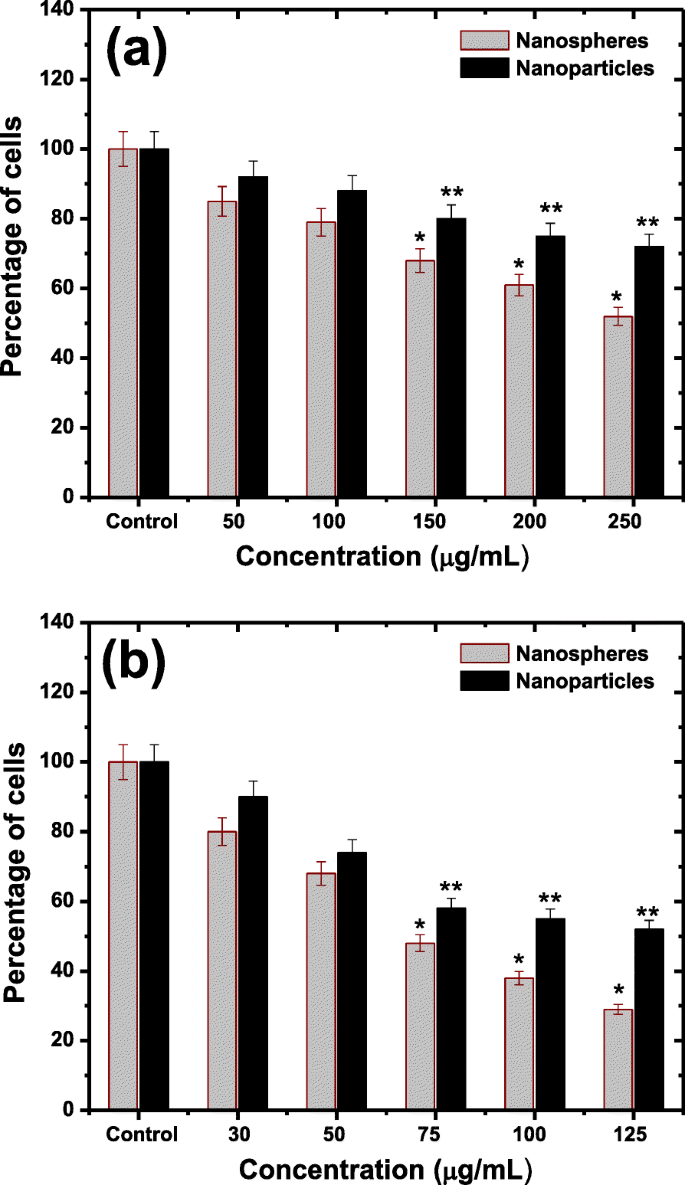
PEG 包覆的铁酸钴纳米颗粒和纳米球在 L-132 细胞中的细胞毒性 (a ) 和 THP-1 细胞 (b )。 *P <0.01 和 **P 与未处理的对照相比,两种细胞 <0.05。数据代表一式三份进行的两次独立实验的平均值±标准差
姜黄素对毒性的影响
对纳米球暴露组和姜黄素处理组小鼠血清生化指标进行了研究,结果与对照组小鼠进行了比较,见图9。发现处理组小鼠的各项指标均显示出显着改善。 the administration of curcumin when compared their values with nanosphere exposure and control group mice. In the figure, it is seen that the expression levels of ALT, AST, BUN, CREA, CYS-C, and TB were approached towards the normal values after the administration of curcumin. This can be attributed to the fact that curcumin has strong antioxidant characteristics which reduces the oxidative stress produced as a result of the toxicity induced by cobalt ferrite [47]. It has also been reported that TNF-α and IL-1 play important role in the induction of hepatic necrosis and curcumin reduces the effect of toxicity by inhibiting the secretion of TNF-α and IL-1 by macrophages [48], similar to the work reported earlier in Ref. [65].
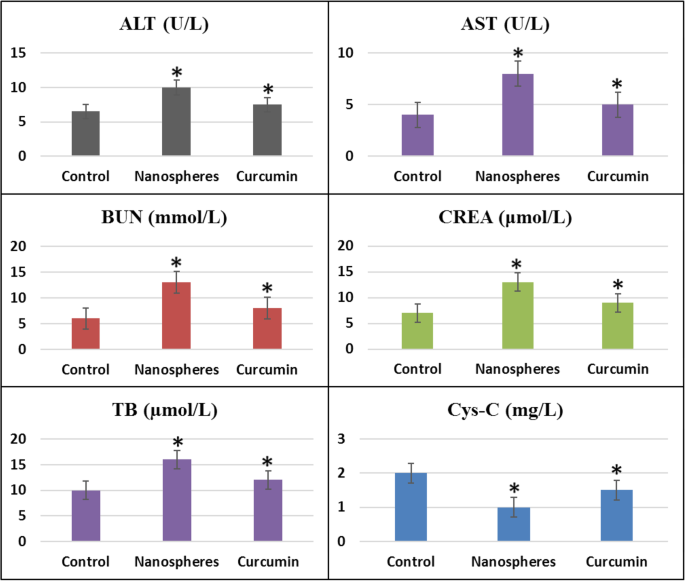
Biochemical indexes in blood serum of the control, nanosphere exposure, and treatment group mice (*P <0.05 compared with untreated controls)
Conclusion
In this work, we successfully fabricated PEG-coated cobalt ferrite nanoparticles and nanospheres via hydrothermal and solvothermal methods, respectively. From structural analyses, it was found that the prepared nanomaterials are highly pure, crystalline, and biocompatible in nature resulting from the successful attachment of PEG. It was found that both nanospheres and nanoparticles of cobalt ferrite are toxic to biological systems. Furthermore, it was shown that nanospheres of cobalt ferrite are more toxic than the nanoparticles due to their large surface area and more reactivity with biological tissues. Positive changes were monitored in biochemical indexes after the administration of curcumin which is a natural chemical possessing no side effects, thus confirming it can be used as the healing agent for the toxicity induced by cobalt ferrite nanospheres.
更改历史
缩写
- PEG:
-
Polyethylene glycol
- XRD:
-
X射线衍射
- FTIR:
-
傅里叶变换红外光谱
- TGA:
-
热重分析
- SPF:
-
Specific pathogens free
- MRI:
-
磁共振成像
- TNF:
-
Tumor necrosis factor
- HE:
-
Hematoxylin–eosin
- SS:
-
Stainless steel
- DI:
-
Deionized
- SEM:
-
扫描电镜
- TEM:
-
透射电子显微镜
- TB:
-
Total bilirubin
- ALT:
-
Alanine aminotransferase
- AST:
-
Aspartate transferase
- BUN:
-
Blood urea nitrogen
- CREA:
-
Creatinine
- Cys-C:
-
Cystatin C
- DNA:
-
Deoxyribonucleic acid
- MDA:
-
Malondialdehyde assay
- ROS:
-
Oxygen free radicals
- T-AOC:
-
Total antioxidant capacity
纳米材料
- 什么是钴合金以及钴合金的特性是什么?
- 负载 ICA 的 mPEG-ICA 纳米颗粒的制备及其在治疗 LPS 诱导的 H9c2 细胞损伤中的应用
- 硼烯稳定性和STM图像的第一性原理研究
- Au 纳米颗粒对 HT29 和 SPEV 细胞系影响的体外研究
- 二氧化钛纳米颗粒对小鼠的潜在肝脏、大脑和胚胎毒性
- 基于苯基三甲氧基硅烷改性氧化铝纳米颗粒的 Al2O3:SiOC 纳米复合材料的形成和发光特性
- Au@TiO2 蛋黄-壳纳米结构的制备及其在亚甲基蓝降解和检测中的应用
- TiO2-水纳米流体在螺旋槽管中的流动和传热特性的实验研究
- Pt/Nd:SrTiO3结中多级电阻开关记忆和记忆状态相关光电压的研究
- 碳纳米纤维和活性炭作为水性电解质中对称超级电容器的研究:一项比较研究
- 铜纳米粒子合成和稳定方面的环保能力:催化、抗菌、细胞毒性和抗氧化活性
- 新研究:COVID-19 对未来工作和自动化的影响


