具有抗血栓形成和增强内皮细胞亲和力的硫酸软骨素/聚己内酯/明胶电纺纳米纤维作为血管组织工程的潜在支架
摘要
静电纺聚合物纳米纤维在血管组织工程中备受关注。然而,传统的纳米纤维材料具有内皮化缓慢和血栓形成的缺陷,在促进血管组织修复和再生方面效果不佳。在此,通过静电纺丝技术开发了包含不同量硫酸软骨素(CS)的仿生明胶(Gt)/聚己内酯(PCL)复合纳米纤维,以研究它们对抗血栓形成和内皮细胞亲和力的影响。 PG 纳米纤维中不同的 CS 浓度会影响纤维形态和直径。 CS/Gt/PCL 纳米纤维具有合适的孔隙率(~ 80%)和 PBS 溶液吸收(高达 650%)。在 Gt/PCL 纳米纤维中引入 CS 极大地增强了它们的抗凝特性,延长了它们的凝固时间,并促进了细胞反应。特别是,10% CS/Gt/PCL 纳米纤维显示出良好的细胞附着、伸长和增殖。因此,含有一定量CS的Gt/PCL纳米纤维可作为血管修复和再生领域有前景的组织工程支架材料。
介绍
纳米纤维材料作为组织修复和再生中的仿生支架,由于其独特的(生物)物理化学特征,包括其细胞外基质(ECM)样超细纤维结构、优异的机械性能、大的比表面积和具有互连性的高孔隙率 [1, 2]。已经证明,纳米纤维结构在介导细胞反应中起着关键作用,例如细胞粘附、形态(例如,扩散、排列、伸长等)、排列、迁移、增殖、表型和通过接触引导的分化 [3] ,4,5]。虽然许多纳米制造策略(例如纳米切削、模板合成、相分离等)已经提供了一种制造纳米纤维材料的可用技术,但静电纺丝是从不同材料(金属、陶瓷、聚合物)制造纳米纤维的最有效方法之一。 、复合材料等)的工业规模[6,7,8]。
除了(生物)物理信号外,选择合适的生物材料可以显着影响细胞活性以及组织修复和再生 [9]。应考虑一些关键特征,例如生物相容性、生物可吸收性、机械性能和生物功能 [9, 10]。与天然/天然和合成/合成复合材料相比,由天然和合成聚合物组成的复合纳米纤维材料由于结合了天然聚合物优异的生物学特性和合成聚合物的机械强度而受到更多关注[9]。其中,明胶(Gt)/聚己内酯(PCL)组合是最具代表性的天然-合成混合体系之一,广泛应用于血管组织工程[11,12,13,14]。然而,Gt/PCL复合纳米纤维仍存在一些局限性,如内皮化缓慢和血栓形成。最近,硫酸软骨素 (CS) 是一种含有糖胺聚糖和半乳糖胺的硫酸化多糖,已被证明对内皮细胞 (EC) 具有高粘附性,与蛋白质和血小板的相互作用较弱,以及对带负电荷的血液成分具有静电排斥作用 [15] ,16,17]。此外,CS可以抑制细胞凋亡并促进血管伤口的愈合[18, 19]。因此,结合CS的Gt/PCL(PG)电纺纳米纤维将成为血管修复和再生的生物指导性组织工程支架的理想候选者。
在目前的工作中,通过一步静电纺丝开发了含有不同 CS 比例的仿生 PG 复合纳米纤维。通过不同的表征技术检测了 CS/PG 复合纳米纤维的形态、化学特征孔隙率和降解。评价了PG/CS复合纳米纤维的抗凝剂。此外,这些具有不同 CS 比例的复合纳米纤维接种人主动脉内皮细胞 (HAECs) 以研究它们对细胞反应的影响。
材料和方法
材料
CS(牛气管,A 型,纯度:95%)由上海麦克林生化科技有限公司(中国)提供。 PCL 购自 Aladdin Biochemical Polytron Technologies Inc.(中国)。 Gt(牛皮肤,B 型)购自 Sigma-Aldrich Biochemical Technology Co., Ltd.(中国)。活化部分凝血活酶时间(APTT)试剂盒购自雷根生物技术有限公司(中国)。乙酸(纯度:99.5%)购自国药集团化学试剂有限公司(中国)。人主动脉内皮细胞(HAEC)来自青岛大学(中国)附属医院。培养基 Dulbecco's Modified Eagle 培养基/营养混合物 F-12 (DMEM/F-12)、胎牛血清 (FBS)、0.25% 胰蛋白酶-EDTA 购自 Biological Industries(以色列)。除非另有说明,所有试剂均购自Sigma Aldrich(中国)。实验用水均为去离子水。
纳米纤维的电纺
PCL (10% w/v) 在机械搅拌下在室温下溶解在乙酸中 4 小时。 Gt (10% w/v) 溶解在 90% 乙酸中,持续搅拌 2 小时。将不同浓度的 CS 加入 Gt 溶液中,并在室温下轻轻搅拌 1 小时,以获得相对于总聚合物浓度含有 5、10 和 15 重量%的 CS 的均质溶液。然后,通过将上述两种溶液以 50/50 (w/w) 的重量比在搅拌下混合 2 小时来制备 PG 溶液,命名为 5%CS@PG、10%CS@PG 和 15%CS@PG .
对制备的均质溶液进行静电纺丝工艺,配备带有 21 G 针头的 1 mL 注射器和铝箔覆盖的收集器。在这项研究中,收集器板和针尖之间的距离固定在 18 厘米左右,电压设置为 23 kV,聚合物溶液以 1 mL/h 的速率泵出。所有溶液在室温和小心控制的湿度(<40%)下在静电纺丝仪器(Technology,Tk602TH,China)中静电纺丝。在进行任何进一步的实验之前,将样品放入真空干燥箱中至少 72 小时以去除任何残留的溶剂。
扫描电子显微镜 (SEM) 和透射电子显微镜 (TEM)
CS@PG 纳米纤维支架的形态通过 SEM(VEGAS,TESCAN,捷克)在室温下 20 kV 的加速电压下进行研究。纳米纤维的直径 (n =100) 使用图像分析软件 (Image J) 从 SEM 图像进一步测量。
TEM观察和能量色散X射线光谱(EDS)分析使用JEOL JEM-2100 plus(日本)进行。
傅立叶变换红外光谱 (FTIR)
FTIR 由 Nicolet iN10 FTIR 光谱仪(Thermo Fisher Scientific,Waltham,MA,USA)进行,以评估 CS、PG 纳米纤维和 CS@PG 纳米纤维的特征官能团。以透射模式记录样品的光谱,波长范围为 4000-500 cm -1 分辨率为 2 cm −1 .
磷酸盐缓冲盐水 (PBS) 溶液的孔隙率和吸收
纳米纤维的孔隙率使用液体置换法进行。首先称取纳米纤维的干重为W1。然后,将四组纳米纤维在 25°C 下浸入乙醇中 2 小时并称重为 W2。用滤纸除去样品表面的乙醇,然后记下样品的重量为W3。纳米纤维的孔隙率由下式计算:
$${\text{孔隙度}}\left( \% \right) =\left( {W_{3} - W_{1} } \right)/\left( {W_{3} - W_{2} } \right) \times 100$$对于PBS溶液吸收测试,将获得的纳米纤维在干燥状态下称重并记录为Wd。然后,将纳米纤维在 25°C 的 PBS 中浸泡 24 小时,去除样品表面多余的液体后,将湿态的重量记录为 Ww。溶胀率可由下式测量:
$${\text{PBS}}\;{\text{吸收}}\left( \% \right) =\left( {W_{{\text{W}}} - W_{{\text{d} }} } \right)/W_{{\text{d}}} \times 100$$上述实验中的所有值均表示为平均值 ± SD (n =3).
体外降解行为
为了确定获得的纳米纤维对溶菌酶的抗性,在预定的时间(1、4、7、10 和 14 天)测量了样品的降解性。纳米纤维的初始重量记录为 Wi。然后,将样品浸入含有溶菌酶 (500 μg/mL) 的 PBS 溶液 (pH 7.4) 中,并在 37°C 下体外孵育。以预定的降解间隔取出每组样品,用去离子水洗涤,冷冻干燥,得到最终重量(W F)。溶菌酶溶液每周更换 3 次。纳米纤维支架的剩余质量(%)按以下公式计算:
$${\text{质量}}\;{\text{剩余}}\left( \% \right) =\left( {1 - \frac{{w_{i} - w_{f} }}{{ w_{i} }}} \right) \times 100\%$$为了评估样品在 7 天后的降解行为,通过扫描电镜观察纳米纤维的形貌。
血液相容性分析
凝血时间
活化部分凝血活酶时间 (APTT) 用于通过在盖玻片上与电纺纳米纤维孵育后测试贫血小板血浆 (PPP) 的凝血时间来评估内在和共同凝血途径的活性。为此,收集抗凝血(约 10 mL)并以 3000 rpm 离心 20 分钟以获得贫血小板血浆 (PPP)。每个样品在 37°C 下与 200 μL PPP 孵育 10 分钟,并按照制造商的说明使用 APTT 试剂盒进行分析 (n =3).
溶血测试
通过测量暴露于电纺纳米纤维的稀释全血中红细胞释放到溶液相中的血红蛋白浓度来评估溶血率。将盖玻片上的样品单独放入 24 孔板中,并在 37°C 下浸入 2 mL PBS 中 30 分钟。阴性对照组仅含 2 mL PBS,而阳性对照组则由 2 mL 去离子水组成,目的是诱导红细胞最大裂解 (n =3 对于每个测试组)。然后,每孔加入40 μL上述抗凝新鲜全血,37°C孵育60分钟,然后将悬浮液移入离心管中,100× g离心 5 分钟。使用酶标仪(SynergyH1/H1M,BioTek,China)测量上清液在 570 nm 处的吸光度。
血栓形成性
将电纺样品与富含血小板的血浆 (PRP) 孵育后,在体外评估了血栓形成潜力。通过离心(1500 rpm,20 分钟)制备 PRP,弃去上半部分血浆。然后,将盖玻片上的纳米纤维在 100 μL PRP 中在 37°C 下孵育 2 小时,并用 PBS 轻轻冲洗 3 次用于后续实验。为了评估与 PRP 孵育后的血小板活性,将电纺纳米纤维保存在补充有 10% FBS 的 DMEM 中 2 小时和 24 小时,然后使用 CCK-8 检测试剂盒测量纳米纤维上的血小板活力。将 CCK-8 (20 μL) 添加到 24 孔板中的 200 μL 无血清 DMEM 培养基中并孵育 1 小时。最后,通过酶标仪在 450 nm 波长下测量悬浮液。
细胞培养和细胞活力
在补充有 FBS(10%,v/v)和链霉素/青霉素(1%,v/v)的 DMEM 中,在 37°C 和 5% CO2 的气氛中培养人主动脉内皮细胞 (HAEC)。培养基每周更换3次。细胞一般用0.05%胰蛋白酶/EDTA分离3 min,1000 rpm离心,悬浮于新鲜培养基中进行细胞传代或细胞接种。
在细胞接种之前,将 24 孔板中的所有纳米纤维材料在紫外线照射下消毒 1 小时,然后浸入 75% 乙醇 (v/v, %) 中 1 小时。然后,将纳米纤维用 PBS 溶液冲洗四次,并在 CO2 培养箱中的 DMEM 中浸泡 12 小时。细胞接种密度为1 × 10 4 纳米纤维上每孔一个细胞,培养基每天更换。共培养 24 h 后,用 PBS 溶液洗涤细胞 3 次,然后用 Calcein-AM/PI 双染试剂盒(YEASEN Biochemical Technology Co., Ltd, Shanghai, China)染色。 PI染色死细胞,Calcein-AM染色活细胞。
纳米纤维上的细胞形态
为了观察纳米纤维上的细胞粘附,通过荧光显微镜(Nikon A1 MP,日本)在共培养 24 小时后观察细胞的形态。首先,细胞在室温下用 4% 多聚甲醛固定 30 分钟。然后,使用 0.5% Triton X-100 溶液 5 分钟以渗透细胞膜。最后,4'6-二脒基-2-苯基吲哚(DAPI)用于染色细胞核,罗丹明-鬼笔环肽用于染色 F-肌动蛋白。使用Image J进一步进行定量分析(细胞密度、单细胞面积、细胞伸长率)。
细胞增殖
使用 CCK-8 检测试剂盒进行复合纳米纤维的细胞增殖活性。 HAECs以8 × 10 3 的密度接种在纳米纤维上 细胞/孔。每两天更换一次培养基。共培养 1、4、7 天后,用 PBS 溶液洗涤细胞以去除非贴壁细胞。然后,将 20 μL CCK-8 和完全培养基以 1:10 的体积比加入到 24 孔板中,在培养箱中培养 1 小时。 Elisa Reader 在 450 nm 处测试吸光度。
DAPI和罗丹明-鬼笔环肽细胞染色,荧光显微镜直接观察与不同纳米纤维共培养2天和6天后细胞计数的变化。
统计分析
实验中的所有样品均一式三份处理。所有数据均表示为平均值 ± 标准偏差 (SD)。通过单向分析方差 (ANOVA) 确定样本的统计分析,以比较差异与 p 指定的显着性 <0.05.
结果与讨论
CS@PG 纳米纤维的制备和表征
图 1 显示了 CS@PG 纳米纤维支架的静电纺丝过程示意图以及抗凝和细胞相容性的体外评估。为了开发用于促进内皮细胞增殖的工程血管组织支架,将不同比例的 CS(5、10 和 15 wt%)加入 PG(10%,v/v)溶液中,通过静电纺丝工艺制造复合纳米纤维。
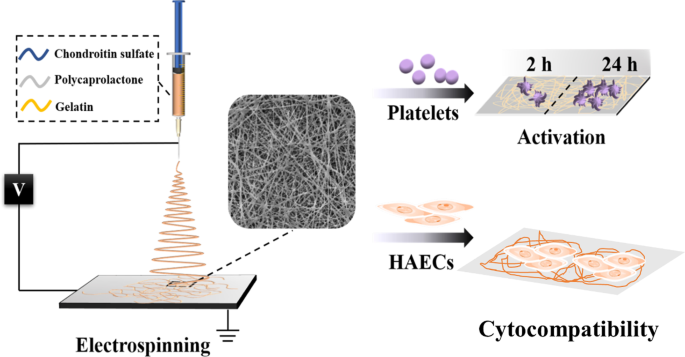
纳米纤维制备示意图及体外评价
进行SEM以观察CS@PG电纺纳米纤维的结构。如图 2 所示,PG、5%CS@PG、10%CS@PG、15%CS@PG 纳米纤维的 SEM 图像显示出致密的纤维结构,通过静电纺丝技术包含连续、光滑和纳米级的纤维. PG 纳米纤维(图 2a)通过静电纺丝过程在纳米纤维上显示出许多不规则的珠子,平均直径为 406.01 ± 146.28 nm。可以解释为 10% w/v 的电纺溶液表现出低粘度,导致形成含有珠的不均匀纳米纤维 [20]。随着聚合物溶液中 CS 的量从 5% 增加到 10% wt.,由于溶液粘度增加,可以获得没有任何珠子的均匀纳米纤维(图 2b,c)。相应地,5%CS@PG 和 10%CS@PG 的平均直径较小,分别为 382.35 ± 152.99 nm 和 300.29 ± 100.85 nm。这一结果主要是因为 CS 含量的增加相应地提高了静电纺丝溶液的电导率 [20]。然而,当聚合物浓度高达 15% 时,聚合物溶液的粘度太高,无法在电场中拉伸。在与前几组相同的 1 mL/h 流速下,我们观察到在施加 23 kV 电压下,出现针尖阻塞现象,无法观察到泰勒锥。因此,电纺溶液的流速和施加的电压分别调整为 0.9 mL/h 和 20 kV。成功制备出平均直径为 266.92 ± 105.43 nm 的 15% CS@PG 纳米纤维。
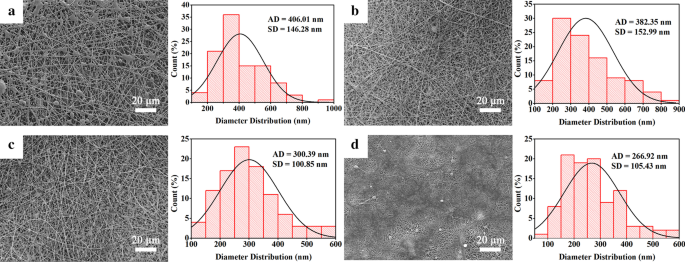
不同CS比例下CS@PG电纺支架的SEM图像和直径分布。 一 PG,b 5%CS@PG,c 10%CS@PG,d 15%CS@PG
如图 3a 所示,发现 CS 均匀分布在 5%CS@PG 和 10%CS@PG 纳米纤维中。然而,在 15% CS@PG 纤维中检测到 CS 聚集。如图 3b 所示,进行 EDX 元素分析以检测制备纤维的硫含量。正如预期的那样,随着所得纤维中 CS 浓度的增加,硫含量增加。

TEM 图像 (a )和不同CS比例下CS@PG电纺支架的EDX元素分析,即PG、5%CS@PG、10%CS@PG和15%CS@PG
FTIR 光谱分析
进行FTIR光谱分析以确定制备的纳米纤维支架的化学基团的特征吸收峰。将PG和CS的FTIR光谱作为对照组与CS@PG纳米纤维组进行比较。在 PG 光谱中,出现在 3300 cm −1 处的强吸收带 和 2935 厘米 −1 可分别归因于–NH2 和–OH 伸缩振动以及CH2 不对称伸缩。在1652 cm -1 出现了几个特征吸收峰 (酰胺 I)用于 C=O 伸缩振动,1542 cm −1 (酰胺 II)用于 N–H 弯曲振动,1441 cm -1 用于 CH2 拉伸和 1267 cm −1 (酰胺 III)用于 C-N 伸缩振动 [21, 22]。 CS光谱在1245 cm -1 处表现出特征吸收带 , 表示带负电荷的 SO4 2− 中的 S=O 伸缩振动 [23, 24]。
如图 4 所示,5%CS@PG、10%CS@PG 和 15%CS@PG 纳米纤维的 FTIR 光谱同时显示出 PCL、Gt 和 CS 的特征峰。与PG组的光谱相比,CS@PG组在1245 cm -1 处显示出CS的特征带 ,并且 CS 带的强度因纳米纤维中 CS 的存在而增加。这一发现证实了CS@PG电纺纳米纤维中存在不同含量的CS。
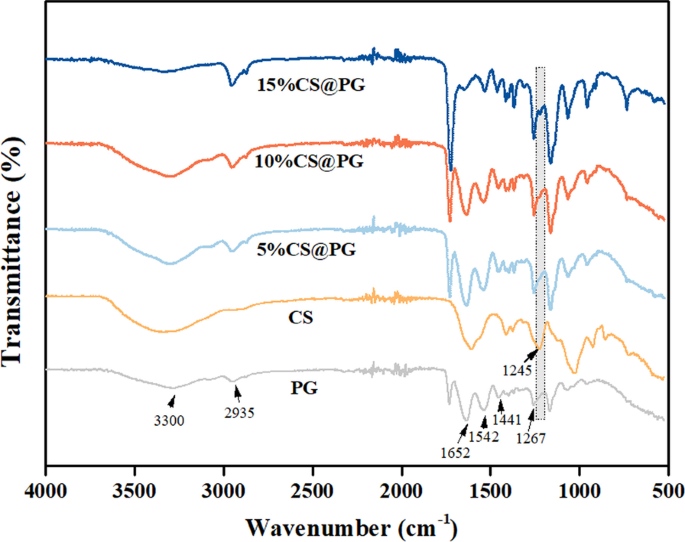
CS@PG电纺支架的FT-IR光谱
纳米纤维的孔隙率、膨胀率和降解性
纤维的高孔隙率表明该材料具有极好的互连性,有利于氧气和营养物质扩散到孔隙中,促进细胞浸润[25, 26]。图 5a 显示了纳米纤维薄膜的孔隙率。所获得的含有不同 CS 比例的纳米纤维的孔隙率大约高达 80%。通过电纺纳米纤维获得的高多孔结构可以模拟天然 ECM,从而为细胞提供有利的 3D 微环境 [27]。据报道,孔隙率高达80%的组织工程支架有利于营养物质和代谢物的运输。
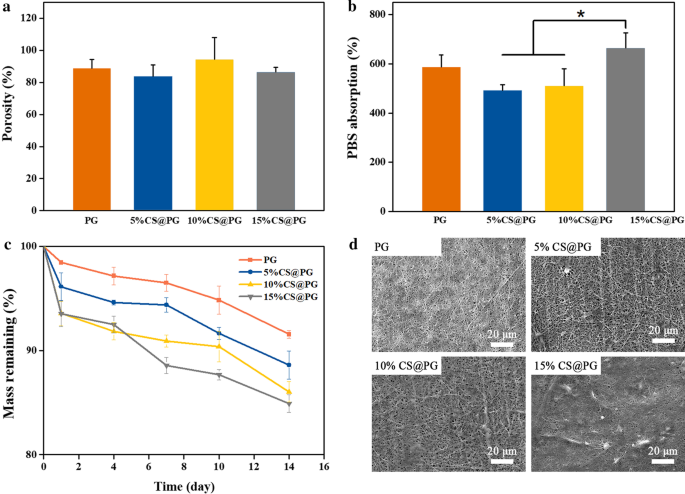
一 制备的纳米纤维的孔隙率。 b 制备的纳米纤维的 PBS 吸收。 c 在 PBS 溶液中降解长达 14 天后,CS@PG 纳米纤维的大量残留。 d 37°C PBS 溶液中纳米纤维膜的 SEM 显微照片
比较 CS@PG 纳米纤维支架的 PBS 吸收率,以评估 CS 对薄膜 PBS 吸收的影响。如图 5b 所示,PG 支架的 PBS 吸收率为 586.34 ± 49.44%,5%CS@PG 和 10%CS@PG 纳米纤维分别为 492.86 ± 21.99% 和 510.04 9.5 %,分别为 510.04 ± 49.44% 15%CS@PG基团的PBS吸收率(665.07 ± 59.81%)显着高于5%CS@PG和10%CS@PG。该结果表明复合纳米纤维中CS含量的增加可以提高薄膜的PBS吸收性能,这可能是由于含有亲水基团(羧基和羟基)的CS分子具有高亲水性[28]。
体外降解实验数据如图5c所示,发现随着CS比例的增加,CS@PG纳米纤维支架的降解率也增加。这可能归因于 SO4 2− 的存在 组 [29]。如图 5c 所示,大多数支架的降解率在 7 天后开始增加,第 14 天的降解结果分别为 PG 8.45%、11.39%、13.97% 和 15.10%,5% CS@PG,10分别为 %CS@PG 和 15%CS@PG 纳米纤维支架。纳米纤维支架的 SEM 图像(图 5d)在浸入 PBS 溶液中 7 天后显示出轻微的膨胀。 SEM图像表明,所开发的纳米纤维足够稳定,可在长达7天的时间内避免严重降解和膨胀,从而影响体内或体外细胞反应。
血液相容性评价
APTT 是一种通过内在凝血机制检测血液或血浆的简单可靠的方法。测试 APTT 以测量电纺纳米纤维对可能的凝血延迟的影响。 APTT 检测的凝血时间显示,对照 PG 与 5%CS@PG 和 10%CS@PG 纳米纤维之间的凝血时间在统计学上显着减少。相比之下,在 15% CS@PG 纳米纤维与 PPP 孵育后发现 APTT 延长,表明其抗凝特性得到改善。如图 6a 所示,凝血的影响取决于纳米纤维样品的直径。与 5%CS@PG 纳米纤维相互作用后发现 APTT 凝固时间最短,与电纺 10%CS@PG 相互作用后 APTT 最高,与溶血程度相似。随着CS比的增加,凝固时间延长。
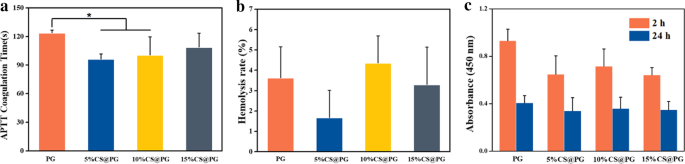
一 CS@PG 纳米纤维的 APTT。 b 样品的溶血率。 c 纳米纤维上的血小板代谢活性。 n =3, *p <0.05
根据ASTM F756-00 (2000),生物材料的溶血率要求为 <5% [30]。本研究中的溶血程度是使用从红细胞中释放的血红蛋白的比色测定法进行的,可以通过以下公式计算:溶血 (%) =(ODsam − ODneg)/(ODpos − ODneg) × 100%。如图 6b 所示,所有样品均未溶血且未导致任何明显溶血(溶血率小于 5%)。
血小板活力实验的数据如图 6c 所示。 2 小时后,附着的血小板的代谢活性最高,在 PRP 与纳米纤维,尤其是 PG 纳米纤维相互作用后达到最大值。有趣的是,24 小时后,所有样品的血小板活性都降低了。这一结果可能是由于纳米纤维结构对血小板的快速激活,与与光滑表面接触时稳定和长期的血小板激活相比,导致生长因子的快速消耗和释放 [31]。血小板的正常寿命约为 8-10 天,随着血小板开始活化,寿命会缩短。
活/死细胞染色
CS 对纳米纤维细胞相容性的影响通过细胞活力、粘附形态和 HAEC 评估在纳米纤维上的增殖 6 天来探索。使用Calcein-AM/PI双染试剂盒、DAPI染色和CCK-8检测试剂盒对贴壁细胞进行评估。
图 7a-e 显示了附着在不同纳米纤维上的活的和死的 HAEC 的荧光图像。 Calcein-AM(绿色)和 PI(红色)分别用于染色活细胞和死细胞。可以观察到活细胞粘附在 CS@PG 复合纳米纤维上,表明含有不同比例 CS 的纳米纤维对 HAEC 没有毒性。通过图像 J 对纳米纤维上的活/死细胞数进行了进一步的定量分析(图 7f)。与PG纳米纤维上的活细胞和死细胞比例相比,其他三组含有不同CS比例的PG,尤其是10%CS@PG和15%CS@PG组的活细胞比例较大,且比例有所增加随着 CS 浓度的增加。该结果表明纳米纤维中CS的存在有利于维持细胞活力[32]。
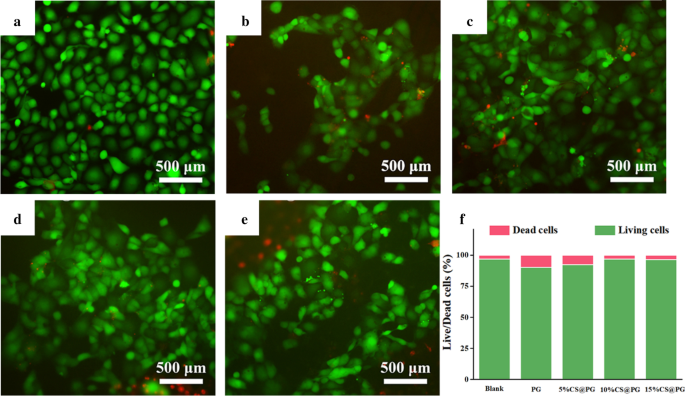
HAEC 在 CS@PG 支架上的细胞活力。 一 组织培养板 (TCP),b PG,c 5%CS@PG,d 10%CS@PG,e 15%CS@PG,f 不同纳米纤维支架的活/死细胞数百分比,n =3
纳米纤维上的细胞粘附行为
具有良好生物相容性的纳米纤维支架被认为是生成血管的首要条件。具有良好生物降解性的PCL和具有优异生物相容性的天然Gt被广泛应用于不同结构的组织工程中,包括水凝胶、电纺纳米纤维和三维支架[21,33,34]。通过荧光显微镜观察复合纳米纤维上 HAEC 的形态以及 24 小时的细胞-材料相互作用。细胞密度 10%CS@PG 和 15%CS@PG 比 PG 和 5%CS@PG 具有统计学意义,表明添加更高水平的 CS 促进细胞粘附。如图 8c 所示,5%CS@PG 和 15%CS@PG 的单细胞面积大于其他纳米纤维组。然而,10%CS@PG 的细胞伸长率显着高于 PG、5%CS@PG 和 15%CS@PG(图 8d)。这一结果可以解释为添加 10% 浓度的 CS 可以促进 HAEC 的传播。发现HAECs在复合纳米纤维上可以很好地粘附、扩散和生长,尤其是10%CS@PG和15%CS@PG。因此,这两种纳米纤维材料可作为临床应用中安全且有前景的血管候选材料。
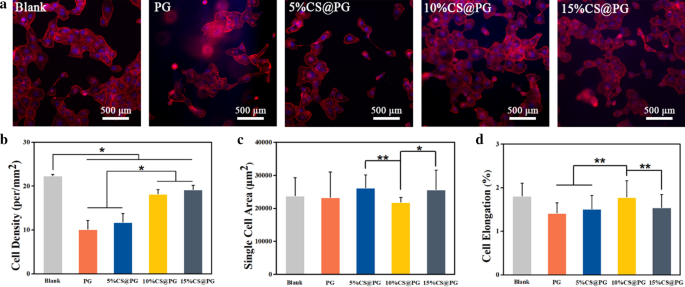
一 CS@PG 支架上 HAEC 的细胞粘附形态(DAPI:细胞核;若丹明-鬼笔环肽:细胞骨架)。 b 细胞密度。 c 单细胞区域,d 不同组纳米纤维的细胞伸长率
细胞增殖
通过荧光显微镜和 CCK-8 测试在体外研究了 CS@PG 纳米纤维上的细胞生长和活力(图 9a-c)。选择电纺PG支架作为阳性对照。不同纳米纤维膜的 CCK-8 测定结果显示在图 9c 中。在细胞培养的第 2、4、6 天,所有组的细胞数量都随着培养时间的增加而增加。第 6 天,10%CS@PG 纳米纤维的 OD 值明显高于 PG 支架。 5%CS@PG、10%CS@PG和15%CS@PG的细胞增殖比较表明,随着复合纳米纤维中CS的存在在一定范围内,细胞增殖率增加。然而,细胞增殖能力也受到纳米纤维材料表面形态的影响。由于15%CS@PG纳米纤维在静电纺丝聚合物溶液中的CS比例较高而表现出较强的粘度,可能会影响细胞增殖。
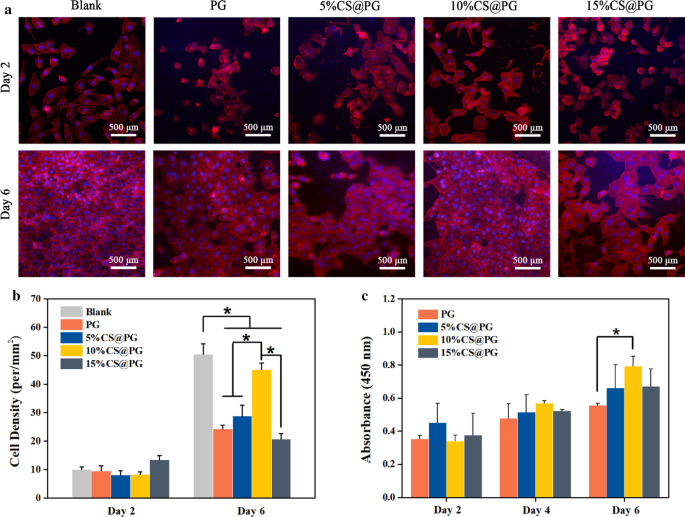
一 HAEC 在通过细胞染色检测的纳米纤维上增殖 2、6 天,b 在第 2 天、第 6 天、n 时纳米纤维支架上的细胞密度 =3, *p <0.05, c 在 PG 和 CS@PG 纳米纤维上培养 HAECs 后第 2、4、6 天的 CCK-8 检测
结论
总之,使用静电纺丝技术成功制备了仿生 CS@PG 复合纳米纤维。通过改变 PG 纳米纤维中的 CS 浓度,可以获得改变的纤维形态和直径。 CS@PG 纳米纤维具有适当的孔隙率(~ 80%)和 PBS 溶液吸收(高达 650%)。 CS 在 PG 纳米纤维中的加入显着改善了它们的抗凝特性,延长了它们的凝固时间,并增强了细胞反应。特别是,10% CS@PG 纳米纤维表现出良好的细胞粘附、伸长和增殖。因此,掺入一定量CS的PG复合纳米纤维可抑制抗血栓形成并增强内皮细胞反应,可作为一种有前景的血管修复和再生组织工程支架。
数据和材料的可用性
本研究中生成或分析的所有数据均包含在本文中。
纳米材料
- 用于增强药物递送的纳米纤维和细丝
- 三态电致变色器件的浸涂工艺工程和性能优化
- 用贵金属纳米粒子装饰的电纺聚合物纳米纤维用于化学传感
- 加载白藜芦醇的白蛋白纳米颗粒具有延长血液循环和改善生物相容性的高效靶向胰腺肿瘤治疗
- 增强新型阳极 PdAu/VGCNF 催化剂在甘油燃料电池中的电氧化性能
- 用 6-巯基嘌呤和神经元穿透肽修饰的金纳米颗粒促进 SH-SY5Y 细胞生长
- 基于叶酸和 gH625 肽的 Fe3O4 磁性纳米颗粒功能化增强细胞内化的比较
- 开发用于潜在伤口愈合应用的电纺壳聚糖-聚氧化乙烯/纤维蛋白原生物复合材料
- 基于紫杉醇的靶向脂质纳米颗粒的抗增殖和细胞凋亡触发潜力,通过转铁蛋白受体增强细胞内化——白血病细胞研究
- 通过快速硒化方法增强 Sb2S3 平面异质结太阳能电池的光伏特性
- Mg 掺杂对用于增强光催化评估和抗菌分析的 ZnO 纳米颗粒的影响
- 自噬抑制剂 (LY294002) 和 5-氟尿嘧啶 (5-FU) 基于组合的纳米脂质体,可增强对食管鳞状细胞癌的疗效


