恢复的 microRNA-326-5p 通过抑制脑缺血/再灌注损伤中的 STAT3 抑制神经元凋亡并减轻线粒体损伤
摘要
研究已经极大地探索了 microRNAs (miRNAs) 在脑缺血/再灌注损伤 (CI/RI) 中的作用。但 miR-326-5p 在 CI/RI 中的具体机制仍不清楚。因此,本研究旨在揭示 miR-326-5p/信号转导器和转录激活因子 3(STAT3)轴在 CI/RI 中的机制。建立了两种模型(原代大鼠皮层神经元的氧气和葡萄糖剥夺 [OGD] 和 Sprague-Dawley 大鼠的大脑中动脉闭塞 [MCAO])分别在体外和体内模拟 CI/RI。使用 OGD 处理的神经元和 MCAO 大鼠进行功能丧失和获得的测定。随后,检测了OGD处理神经元的活力、凋亡、氧化应激和线粒体膜电位,以及MCAO大鼠脑组织的病理变化、凋亡和线粒体膜电位。检测到 OGD 处理的神经元和 MCAO 大鼠脑组织中的 Mitofusin-2 (Mfn2)、miR-326-5p 和 STAT3 表达。 Mfn2 和 miR-326-5p 降低,而 OGD 处理的 MCAO 大鼠神经元和脑组织中 STAT3 升高。 miR-326-5p 靶向并负调控 STAT3 表达。恢复 miR-326-5p 或减少 STAT3 可增强细胞活力、抑制细胞凋亡和氧化应激、增加线粒体膜电位并增加 OGD 处理的神经元中 Mfn2 的表达。上调miR-326-5p或下调STAT3可缓解MCAO大鼠脑组织病理改变、抑制细胞凋亡、升高线粒体膜电位和Mfn2表达。本研究阐明了上调miR-326-5p或下调STAT3通过提高Mfn2表达来预防CI/RI。
介绍
脑缺血/再灌注损伤(CI/RI)是继缺血性卒中后继发的一种脑损伤[1]。脑 I/R 最典型的特征是再灌注后的初始短暂性脑缺血 [2]。 CI/RI 激活神经元凋亡并导致海马和皮质损伤 [3]。目前,最常见的临床应用是溶栓治疗 CI/RI [4]。然而,再灌注会增加活性氧 (ROS) 的产生,导致细胞内 DNA 损伤、氧化应激相关损伤、蛋白质氧化和脂质过氧化,从而进一步恶化血脑屏障和水肿 [5]。因此,寻找新的有针对性的选项的紧迫性是 CI/RI 的首要任务。
MicroRNA (miRNA) 被广泛认为在 CI/RI 中具有潜在和预后作用 [6, 7]。例如,一篇文章证明 miR-202-5p 可减轻缺血性损伤大脑中动脉闭塞 (MCAO) 模型大鼠的神经元损伤和神经功能缺损,以及氧和葡萄糖剥夺 (OGD) 诱导的细胞损伤 [8] .此外,还发现 miR-98 的上调可改善 I/R 中风小鼠的神经学结果 [9],而 miR-451 的过表达可减轻 CI/RI 小鼠的缺血性脑细胞凋亡 [10]。具体而言,miR-326-5p 对内皮祖细胞具有促血管生成能力,可改善急性心肌梗死后的心脏功能 [11]。然而,在 CI/RI 中以 miR-326-5p 为中心的研究仍处于起步阶段。信号转导和转录激活因子 (STAT) 是由 CI/RI 激活的独特蛋白质家族 [12]。在生物信息学网站上,STAT3 被预测为 miR-326-5p 的靶点;因此,我们研究了 miR-326-5p 介导的 STAT3 在 CI/RI 中的作用。 STAT3 通过释放促炎介质使缺血性神经炎症过程和继发性脑损伤恶化 [13, 14]。具体而言,Janus 激活激酶 2(JAK2)/STAT3 通路在阻断 CI/RI 诱导的细胞凋亡中发挥功能作用 [15]。 Mitofusin-2 (Mfn2) 是一种线粒体融合因子,可以防止心脑血管 I/RI [16] 并改善缺血性脑损伤中缺氧诱导的神经元凋亡 [17]。也有报道称Mfn2对CI/RI有保护作用[18]。
总之,较少深入的研究发现了 miR-326-5p 和 STAT3 在 CI/RI 中的联合作用。鉴于此,本研究假设miR-326-5p通过靶向STAT3减弱CI/RI。
材料和方法
道德声明
实验经扬州大学附属医院动物护理与使用委员会批准;扬州大学,在《扬州大学附属医院实验大鼠饲养与使用指南》下开展;扬州大学。
实验动物
来自扬州大学(中国扬州)比较医学中心的雄性成年 Sprague-Dawley 大鼠(6-8 周龄,250 ± 30 g)被饲养在特定的无病原体环境中,可以自由获取食物和水, (24 ± 1)°C,(50 ± 5)% 湿度和 12 小时光/暗循环。
细胞分离与识别
将大鼠斩首安乐死,将大脑切成1 mm 3 配置细胞悬液,将其与0.4%台盼蓝溶液按9:1混合(台盼蓝终浓度为0.04%),用血细胞计数器计算细胞密度和存活率。细胞(1 × 10 6 细胞/mL)以5 × 10 6 接种于用L-聚赖氨酸(0.1mg/mL)预包被的细胞培养瓶中 每瓶细胞。当细胞贴壁时,将其与更新的培养基(NeurobasalA + B27 + L-谷氨酰胺)一起培养并连续培养6-7天,每2-3天换液一次。
细胞鉴定:利用大鼠皮质神经元制备神经元载玻片,与原代兔抗大鼠巢蛋白(NES)多克隆抗体(1:200),以及异硫氰酸荧光素(FITC)标记的山羊抗兔免疫球蛋白孵育G(1:50,均来自 Cell Signaling Technology,Beverly,MA,USA)。之后,用抗荧光猝灭剂密封细胞并通过荧光显微镜观察。
OGD模型建立
神经元在不含葡萄糖的厄尔氏溶液中培养,并暴露于 95% N2 和 5% CO2 的混合气体中。正压通气30分钟后,形成细胞培养的缺氧环境(体外OGD模拟缺血)。孵育 90 分钟后,除去不含葡萄糖的厄尔溶液后,将细胞与维持细胞培养基一起孵育。细胞被常规培养用于后续实验(体外氧-葡萄糖再灌注的再灌注模拟)。常氧条件下的正常培养基作为对照。
神经元被分为对照组; OGD组、阴性对照(NC)组(OGD处理的神经元转染乱序寡核苷酸)、miR-326-5p agomir组(OGD处理的神经元转染miR-326-5p agomir)、sh-STAT3组(经OGD处理的神经元转染STAT3 shRNA)和miR-326-5p agomir + 过表达(oe)-STAT3组(经OGD处理的神经元转染miR-326-5p agomir和pcDNA-STAT3载体)。寡核苷酸和载体均由GenePharma(中国上海)提供。
使用 lipofectamine 2000 (Invitrogen; Thermo Fisher Scientific),将杂乱寡核苷酸、miR-326-5p agomir、STAT3 shRNA 或 miR-326-5p agomir 和 pcDNA-STAT3 转染到原代大鼠神经元中,并通过逆转录定量检测转染效果48小时后聚合酶链反应(RT-qPCR)或蛋白质印迹。
3-(4, 5-Dimethylthiazol-2-yl)-2, 5-Diphenyltetrazolium Bromide (MTT) 检测
使神经元悬浮于 1 × 10 6 细胞/mL,分别培养 0、24 和 48 小时。在无菌环境中,将神经元在 10% MTT 溶液中孵育 2-4 小时,并加入 150 μL 福曼赞溶解溶液(二甲基亚砜)直至晶体充分溶解。光密度(OD)值在酶标仪上于 570 nm 处测量。
流式细胞术凋亡检测
神经元用 0.25% 胰蛋白酶分离,以 2000 rpm 离心并重悬于 PBS 中。然后,将神经元以 2000 rpm 离心,用结合缓冲液重悬沉淀,依次与 5 μL Annexin V-FITC 和 5 μL 碘化丙啶 (PI) 孵育。流式细胞仪检测细胞凋亡率。
JC-1 线粒体膜电位检测
6孔板细胞用PBS漂洗,加入1 mL细胞培养基和1 mL JC-1染色工作液(50 μL JC-1、8 mL超纯水和2 mL JC-1染色缓冲液)(SolarbioScience ,北京,中国)并孵育 15 分钟。 1 × JC-1染色缓冲液由4 mL蒸馏水和1 mL JC-1染色缓冲液构成。孵育后,细胞被胰蛋白酶消化,重新悬浮在 JC-1 缓冲液中,并在流式细胞仪上进行测试。计算绿色荧光的相对比例。
氧化应激检测
通过 2,7-二氯荧光素二乙酸酯 (DCF-DA) 检测试剂盒 (Abcam) 测量细胞内 ROS 水平。简而言之,神经元用 0.25% 胰蛋白酶分离,重新悬浮并与 10 μm DCF-DA 孵育 30 分钟。之后,通过荧光光谱法(BD Biosciences)测量激发/发射光为495 nm/529 nm的DCF荧光。
使用商业化验试剂盒(Beyotime Biotechnology Co.,Shanghai,China)通过化学比色法检测细胞内丙二醛(MDA)、谷胱甘肽(GSH)含量和超氧化物歧化酶(SOD)活性。 OD值由酶标仪测定。
大鼠模型建立
大鼠腹腔注射戊巴比妥钠(50 μg/kg)麻醉。在颈部做中线切口,结扎外颈动脉,用动脉夹阻塞颈总动脉。将一根 3-0 硅酮涂层尼龙单丝缝线小心地插入颈内动脉直至耐光。短暂脑缺血90分钟后,撤线,再灌注24小时。假手术组除缝线不进入颈内动脉外接受相同处理。术中采用恒温床将直肠温度维持在37 ± 0.5℃[19]。
将大鼠分为6组(n =6),在建立MCAO模型前向侧脑室注射质粒或miR,包括sham组、MCAO组(模型大鼠)、NC组(模型大鼠侧脑室注射5 μL 乱序寡核苷酸 [100 μM])、miR-326-5p agomir 组(模型大鼠侧脑室注射 5 μL miR-326-5p agomir [100 μM])、sh-STAT3 组(模型大鼠侧脑室注射 5 μL STAT3 干扰载体 [100 μM])和 miR-326-5p agomir + oe-STAT3 组(模型大鼠侧脑室注射 5 μL miR-326-5p agomir [100 μM] 和 5 μL STAT3 过表达载体 [100 μM]) [20, 21]。
标本集
对大鼠进行麻醉安乐死,心脏灌注,并获得整个大脑。将脑损伤组织切成1 × 1 × 1 mm 3 用于石蜡切片制备、RT-qPCR、蛋白质印迹分析和线粒体膜电位检测的组织块。
检测大脑皮层线粒体膜电位
分离SD大鼠大脑皮层并切成1 mm 3 .将组织块置于 300 目尼龙网上并加入 PBS。然后将细胞悬液1000r/min离心,加入70%乙醇,再次1000r/min离心。之后,将样品重悬于 1 mL PBS 中,悬浮液(1 × 10 6 细胞(100 μL)与罗丹明 123 染料溶液(10 μL,5 μg/mL)反应,并在流式细胞仪上于 488 nm 处分析。
HE 染色
大鼠脑组织在4%多聚甲醛中浸泡24 h,制备石蜡切片,切成4 μm,铺在40 ℃水中,60 ℃烘烤。石蜡切片常规脱蜡水化,HE染色液染色。 HE染色后,受损神经元表现为细胞核收缩、细胞水肿、空泡化和细胞核变暗。使用光学显微镜(日本尼康)获得图像,存活神经元数(mm 2 )的缺血皮层计数。
TUNEL 染色
石蜡切片用100%、95%、80%和70%酒精脱蜡脱水。然后,将切片浸入 4% 多聚甲醛中,然后与 0.1% Triton X-100 柠檬酸钠缓冲液孵育 20 分钟,然后将 TUNEL 反应混合物孵育 1-1.5 小时。接下来,切片用过氧化物酶溶液和二氨基联苯胺(DAB)显色,苏木精复染,梯度酒精脱水,透化,中性树胶密封。在光学显微镜下观察切片以计数TUNEL阳性细胞。细胞核内棕黄色颗粒定义为TUNEL阳性细胞(凋亡细胞)。
免疫组织化学
切片经脱蜡、水化、柠檬酸抗原回收,3% H2O2封闭内源性过氧化氢酶。每个切片加入山羊血清(50 μL),与一抗(50 μL)孵育,并与二抗(50 μL)和辣根过氧化物酶标记的链霉亲和素(50 μL)反应。切片经DAB显色,苏木精复染,梯度酒精脱水,二甲苯透化,中性树胶封孔。显微镜下观察切片(缺血脑组织细胞质或细胞核呈黄色或棕黄色颗粒)。测量OD值并取平均值。
RT-qPCR
从组织和细胞中提取总 RNA 由 Trizol (Invitrogen) 进行。使用 SYBR Green PCR Mix(Applied Biosystems,CA,USA)和 QuantStudio TM 6Flex 实时 PCR 系统(Applied Biosystems)通过 qPCR 分析 mRNA 表达。特异的茎环逆转录引物和正向/反向引物(BioTNT,上海,中国)被设计用来分析 miRNA 水平。表 1 列出了所有引物。 2 −△△CT 方法计算miRNA或mRNA水平。
Western Blot 分析
蛋白质样品通过 10% 十二烷基硫酸钠聚丙烯酰胺凝胶电泳分离并电印迹到聚偏二氟乙烯 (PVDF) 膜上。之后,PVDF 膜用含 5% 脱脂奶粉的 Tris 盐水封闭,用一抗探测,用二抗重新探测 2 h。然后,用含有 Nitroblue 四唑氯化物和 5-Bromo-4-Chloro-3-Indolyl Phosphate 的碱性磷酸酶缓冲液分析蛋白质条带,并通过 ImageJ 软件(NIH,Bethesda,MD,USA)定量。主要抗体为 STAT3 (1:1000)、Mfn2(1:1000,Abcam,MA,美国)和 3-磷酸甘油醛脱氢酶 (GAPDH)(1:1000,Cell Signaling Technology,Beverly,MA,USA)。
双荧光素酶报告基因检测
将含有 miR-326-5p 野生型(WT)或突变型(Mut)结合位点的 STAT3 3'UTR 克隆到 pmirGLO 载体(Promega,WI,USA)中,命名为 STAT3-WT 和 STAT3-Mut。细胞以2 × 10 4 接种于24孔板 细胞/孔,并用 100 ng STAT3-WT 或 STAT3-Mut 荧光素酶载体和 50 nM miR-326-5p agomir 或 it agomir NC 在 70% 汇合处共转染。使用双荧光素酶报告基因检测系统(Promega Corporation,WI,USA)测量荧光素酶活性。
统计分析
SPSS 21.0 (IBM, NY, USA) 统计软件用于数据分析。数据表示为平均值 ± 标准偏差(SD)。通过Student's t-test分析两组之间的差异,而通过单向方差分析(ANOVA)分析多重比较,然后是Tukey的事后检验。 P 代表两侧检验,P <0.05 被认为具有统计学意义。
结果
上调 miR-326-5p 或下调 STAT3 减弱 OGD 处理的皮质神经元的凋亡
培养一周,大鼠皮层神经元分化成熟。镜下神经元呈较大的神经元体,细胞质较透明,细胞核大,密度低,折射率强。神经元体呈圆锥形或圆形,树突交错排列并粘附在壁上(图1a、b)。 NES是大脑神经元的特异性化学标志物,可通过免疫荧光法定位具有高特异性的神经元。发现神经元与NES特异性结合并显示绿色荧光(图1c)。
<图片>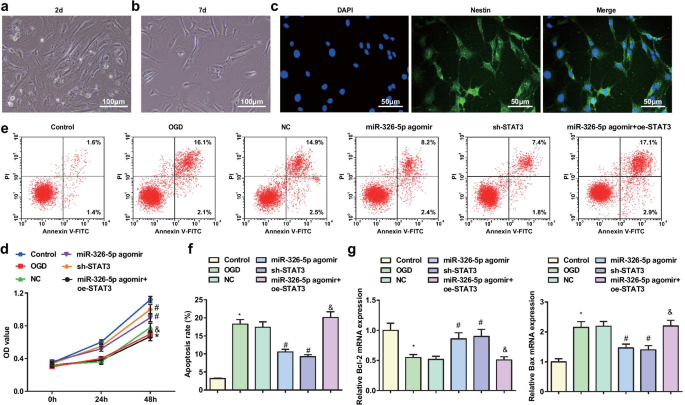
miR-326-5p 的上调或 STAT3 的下调减弱了 OGD 处理的皮质神经元的凋亡。 一 具有二维贴壁培养的脑神经元(比例尺:100 μm); b 7 天贴壁培养的脑神经元(比例尺:100 μm); c NES 免疫荧光法染色的 7 天贴壁培养的脑神经元(比例尺:50 μm); d MTT 法测定 OGD 处理的皮层神经元的活力; e 流式细胞术检测OGD处理的皮层神经元凋亡; f OGD处理的皮质神经元的凋亡率; g OGD 处理的皮质神经元中 Bcl-2 和 Bax mRNA 的表达; *P 与对照组相比<0.05; #P 与NC组相比<0.05; &P <0.05与miR-326-5p agomir组相比
MTT测定用于检测皮质神经元活力(图1d)。结果表明,与对照组和miR-326-5p agomir组相比,OGD组和miR-326-5p agomir + oe-STAT3组大鼠皮质神经元活力受损,但在miR-326-5p中增强agomir 组和 sh-STAT3 组与 NC 组(所有 P <0.05).
通过流式细胞术测定大鼠皮质神经元凋亡,而通过 RT-qPCR 测定 Bcl-2 和 Bax mRNA 表达(图 1e-g)。结果说明与对照组和miR-326-5p agomir组相比,OGD组和miR-326-5p agomir + oe-STAT3组细胞凋亡率增加,Bcl-2表达降低,Bax表达增加(所有P <0.05)。与NC组相比,miR-326-5p agomir组和sh-STAT3组细胞凋亡率降低,Bcl-2水平升高,Bax水平受到抑制(均P <0.05).
上调 miR-326-5p 或下调 STAT3 可增加 OGD 损伤后皮质神经元的 Mfn2 和线粒体膜电位水平
通过蛋白质印迹分析检测 OGD 处理的皮质神经元中的 Mfn2 表达(图 2a,b)。与对照组和miR-326-5p agomir组相比,OGD组和miR-326-5p agomir + oe-STAT3组Mfn2蛋白表达降低,而miR-326-5p agomir组和sh组Mfn2蛋白表达升高-STAT3 组与 NC 组(所有 P <0.05).
<图片>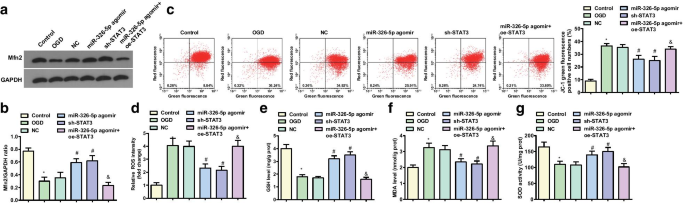
miR-326-5p 的上调或 STAT3 的下调会增加 OGD 处理的皮质神经元中的 Mfn2 和线粒体膜电位水平。 一 , b OGD 处理的皮质神经元中的 Mfn2 蛋白表达; c OGD 处理的皮质神经元线粒体膜电位水平的 JC-1 流式细胞术; d 上调 miR-326-5p 或下调 STAT3 后 OGD 处理的皮质神经元中的 ROS 含量; e 上调 miR-326-5p 或下调 STAT3 后,OGD 处理的皮质神经元中的 GSH 活性; f 上调miR-326-5p或下调STAT3后OGD处理的皮质神经元中MDA含量; g 上调 miR-326-5p 或下调 STAT3 后神经元中的 SOD 活性; *P 与对照组相比<0.05; #P 与NC组相比<0.05; &P <0.05与miR-326-5p agomir组相比
JC-1检测线粒体膜电位发现(图2c、d)相对于对照组和miR-326-5p agomir组,OGD组和miR-326-5p agomir组线粒体膜电位水平降低+ oe-STAT3组(所有P <0.05)。相对于NC组,miR-326-5p agomir组和sh-STAT3组线粒体膜电位水平升高(均P <0.05).
测定OGD处理的皮质神经元的ROS和MDA含量以及GSH和SOD活性,结果表明与对照组和miR-326-5p agomir组相比,OGD组和miR-326-5p agomir + oe -STAT3 组 ROS 和 MDA 含量增加,GSH 和 SOD 活性受损(所有 P <0.05)。与NC组相比,miR-326-5p agomir组和sh-STAT3组ROS和MDA含量降低,GSH和SOD活性增强(均P <0.05)(图2e-g)。
上调 miR-326-5p 或下调 STAT3 阻碍皮层神经元的病理损伤并抑制 CI/RI 大鼠的细胞凋亡
HE染色观察脑组织病理损伤(图3a、b),可见sham组神经元结构正常,排列整齐,胞质淡红色,细胞核蓝色,核仁清晰。在MCAO组、NC组和miR-326-5p agomir + oe-STAT3组中,观察到神经元排列紊乱,染色较深,核膜破裂,细胞结构消失,核固缩,深染色的细胞核和大量裂解。 miR-326-5p agomir组和sh-STAT3组神经元肿胀减轻,神经元排列有序,坏死细胞减少,与MCAO组和NC组相比状态更好。 <图片>
上调 miR-326-5p 或下调 STAT3 可阻止皮层神经元的病理损伤并抑制 CI/RI 大鼠的细胞凋亡。 一 HE染色观察MCAO大鼠脑组织病理损伤(比例尺:50 μm); b 上调miR-326-5p或下调STAT3后MCAO大鼠脑组织完整神经元数量; c TUNEL染色检测MCAO大鼠脑组织神经元凋亡(比例尺:50 μm); d 上调miR-326-5p或下调STAT3后MCAO大鼠脑组织TUNEL阳性率; e 上调miR-326-5p或下调STAT3后MCAO大鼠脑组织中Bcl-2和Bax mRNA的表达; *P <0.05 与假手术组比较; #P 与NC组相比<0.05; &P <0.05与miR-326-5p agomir组相比
TUNEL染色用于检测脑组织中的Bcl-2和Bax mRNA表达的神经元凋亡和RT-qPCR。结果显示(图3c-e)与假手术组和miR-326-5p agomir组相比,MCAO组TUNEL阳性率增加,Bcl-2 mRNA表达降低,Bax mRNA表达增加, miR-326-5p agomir + oe-STAT3组(所有P <0.05)。 miR-326-5p agomir和sh-STAT3组TUNEL阳性率和Bax mRNA表达低于NC组,Bcl-2 mRNA表达高于NC组(均P <0.05).
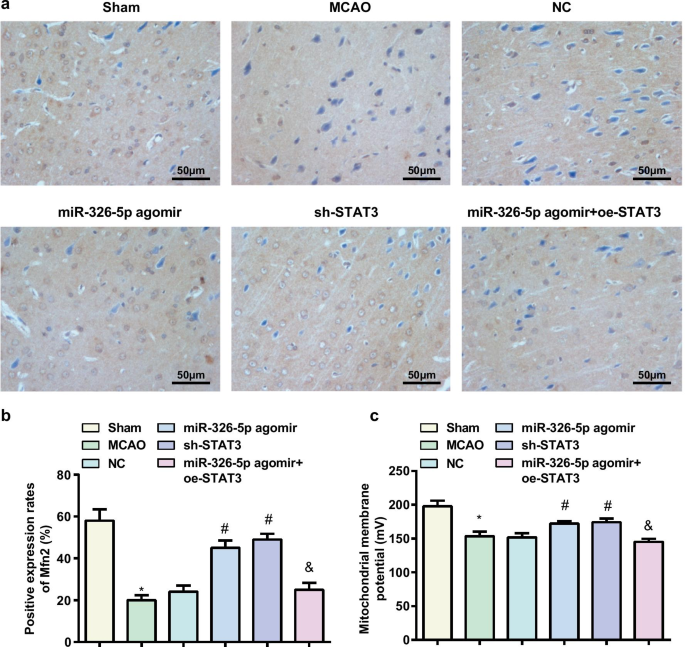
采用免疫组化法检测大鼠脑组织中Mfn2蛋白表达,结果显示(图4a、b)在sham组和miR-326-5p agomir组与MCAO组和MCAO组检测到较低的Mfn2蛋白表达。 miR-326-5p agomir + oe-STAT3组,而在miR-326-5p agomir组和sh-STAT3组而不是NC组测量到更高的Mfn2蛋白表达(所有P <0.05).
上调 miR-326-5p 或下调 STAT3 会增加 CI/RI 大鼠脑组织中的线粒体膜电位水平。 一 免疫组化法检测大鼠脑组织中 Mfn2 的表达(比例尺:50 μm); b 上调miR-326-5p或下调STAT3后MCAO大鼠脑组织中Mfn2阳性细胞数; c 上调miR-326-5p或下调STAT3后MCAO大鼠脑组织神经元线粒体跨膜电位; *P <0.05 与假手术组比较; #P 与NC组相比<0.05; &P <0.05与miR-326-5p agomir组相比
线粒体膜电位水平检测发现(图4c)与sham组和miR-326-5p agomir组相比,MCAO组和miR-326-5p agomir + oe-STAT3线粒体膜电位水平降低组,而在 miR-326-5p agomir 组和 sh-STAT3 组与 NC 组相比增加(所有 P <0.05).
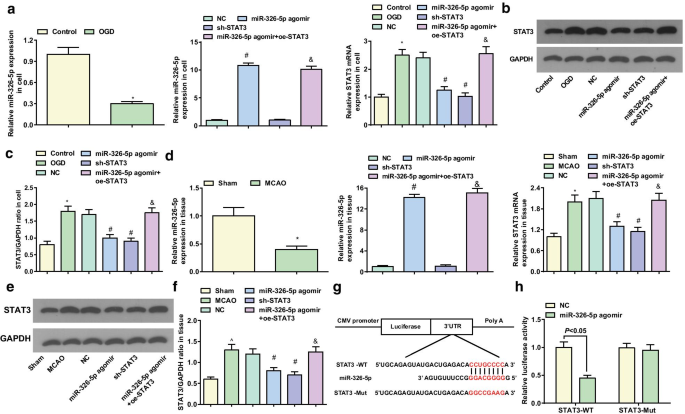
通过RT-qPCR和蛋白质印迹分析检测皮质神经元和脑组织中miR-326-5p和STAT3的表达。在体外皮层神经元中,与对照组相比,OGD 组中 miR-326-5p 表达降低和 STAT3 表达增加(均P <0.05)。与NC组相比,miR-326-5p agomir组miR-326-5p表达升高,STAT3表达降低(均P <0.05); STAT3 表达降低 (P <0.05) 在 sh-STAT3 组中。与miR-326-5p agomir组相比,miR-326-5p agomir + oe-STAT3组中STAT3表达上调(P <0.05)(图5a-c)。
miR-326-5p 靶向 STAT3。 一 miR-326-5p 和 STAT3 mRNA 在体外 OGD 处理的皮质神经元中的表达; b , c 体外 OGD 处理的皮质神经元中 STAT3 蛋白的表达; d MCAO大鼠脑组织中miR-326-5p和STAT3 mRNA的表达; e , f MCAO大鼠脑组织中STAT3蛋白表达; g 通过生物信息学软件预测miR-326-5p与STAT3的结合位点; h 双荧光素酶报告基因检测验证miR-326-5p与STAT3的靶向关系;在图a –c , *P 与对照组相比<0.05; #P 与NC组相比<0.05; &P <0.05 与 miR-326-5p agomir 组相比。在图d –f , *P <0.05 与假手术组比较; #P 与NC组相比<0.05; &P <0.05与miR-326-5p agomir组相比
在体内脑组织中,与假手术组相比,MCAO 组出现较低的 miR-326-5p 和较高的 STAT3(均P <0.05)。相对于 NC 组,miR-326-5p 表达升高而 STAT3 表达在 miR-326-5p agomir 组中降低(均P <0.05)。 sh-STAT3 组中 STAT3 表达降低 (P <0.05)。与miR-326-5p agomir组相比,miR-326-5p agomir + oe-STAT3组中STAT3表达升高(P <0.05)(图5d-f)。
DIANA 和 miRDB 软件发现了 STAT3 3'UTR 上潜在的 miR-326-5p 靶向位点(图 5g)。构建包含WT miR-326-5p结合位点和Mut结合位点的STAT3 3'UTR并将其插入到pmirGLO质粒中。通过荧光素酶报告基因测定进一步验证了 miR-326-5p 与 STAT3 3'UTR 的结合。荧光素酶报告基因检测显示 miR-326-5p agomir 降低 STAT3-WT 的相对荧光素酶活性,但不降低 STAT3-Mut(图 5h),暗示 STAT3 是 miR-326-5p 的直接靶基因。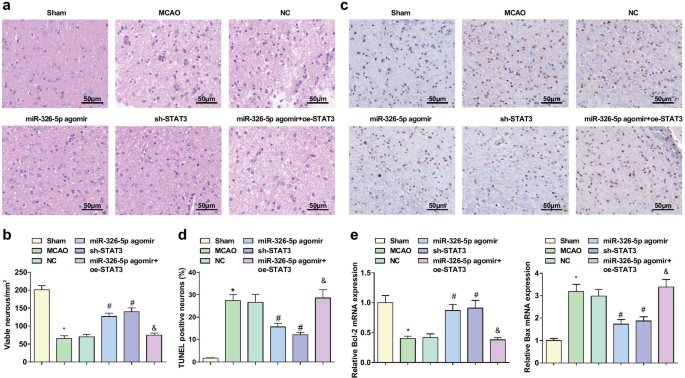
上调 miR-326-5p 或下调 STAT3 可增加 CI/RI 大鼠脑组织线粒体膜电位水平
miR-326-5p 目标 STAT3
讨论
CI/RI 是脑血管死亡的主要原因 [22]。表明 miRNA 参与 CI/RI [23]。然而,对 miR-326-5p 相关机制的全面了解在 CI/RI 中仍然不足。因此,本研究旨在揭示 miR-326-5p 在 CI/RI 中的具体作用,重点是 miR-326-5p 和 STAT3 的联合倒数。富有成效的研究表明,miR-326-5p 的上调通过抑制 STAT3 减弱 CI/RI 并提高 Mfn2 的表达。
开始时,确定 miR-326-5p 表达在体内和体外在 CI/RI 中降低。随后,我们安排了一系列检测,发现上调 miR-326-5p 可增强神经元活力和线粒体功能,提高 Mfn2 表达并抑制氧化应激和细胞凋亡。 Furthermore, in vivo experiments in rats further verified the functional roles of restored miR-326-5p in CI/RI. As a matter of fact, high miR-326 is proved to correlate with long overall survival of patients with glioblastoma, the common type of brain tumor [24]. Also, miR-326 expression has been further evidenced to reduce in Parkinson's disease and miR-326 could suppress apoptosis of dopaminergic neurons and reduce inflammatory response [25]. Except for that, the reduction in miR-326-5p is manifested in endothelial progenitor cells in the course of myocardial infarction, and introduction of endothelial progenitor cells overexpressing could promote cardiac function recovery [11]. There has been a study illustrating that up-regulation of miR-326 improves the behavioral function, enhances neuronal viability and depresses neuronal apoptosis in mice with Alzheimer's disease [26]. Furthermore, it is documented that up-regulation of miR-326 by miR-326 mimic could suppress inducible nitric oxide synthase in dopaminergic neurons in Parkinson's disease [27].
In this study, we found that STAT3 was a target gene of miR-326-5p. Supported by an advanced study, it is indicated that STAT3 expression is negatively regulated by miR-326 in human endometrial carcinoma stem cells [28]. In the present study, we measured that STAT3 expression was enhanced in CI/RI. Currently, it has been found that I/R injury and OGD would induce STAT3 expression to increase [29]. Intriguingly, STAT3 mRNA expression trends to an increment in I/R animals [30]. Additionally, STAT3 protein expression is reported to up-regulate in CI/RI [31]. Next, our study revealed that down-regulating STAT3 had the therapeutic effects on CI/RI rats and OGD-treated neurons. As supported by a study, it is concluded that miR-31 induction discourages oxidative stress by inactivation of JAK/STAT3 pathway in ischemic stroke [32]. Also, inhibition of JAK2/STAT3 pathway is beneficial to oxidative stress impairment in CI/RI [31]. Furthermore, knockdown of JAK/STAT3 pathway is identified to enhance cell viability, and reduce oxidative stress and neuron apoptosis in ischemic brain injury [33]. Lately, inhibited JAK/STAT3 signaling pathway is witnessed to relieve myocardial infarction in myocardial I/R injury [34]. As demonstrated, depleted STAT3 undermines neuronal apoptosis in rats with white matter injury [35]. Moreover, the suppression of neuronal apoptosis, and alleviation of cerebral infarct size are attributed to JAK2/STAT3 inhibition in rats with CI/RI [36].
Finally, we focused on the effects of miR-326-5p and STAT3 on Mfn2 expression and discovered that the reduced level Mfn2 in rats with CI/RI and OGD-treated neurons could be elevated by either restoring miR-326-5p or silencing STAT3. As implicated by a previous study, it is documented that Mfn2 is decreased in the lately phase of reperfusion and poorly expressed of Mfn2 exacerbates CI/RI via restrained autophagosome formation and autophagosome and lysosome fusion [18]. Additionally, Mfn2 is implied to reduce even disappear in I/R injury in old hepatocytes [37]. However, few researches have discussed the regulatory mechanism of miR-326-5p and STAT3 for Mfn2.
Conclusion
In general, this study has elucidated the mechanisms that elevated miR-326-5p inhibits neuronal apoptosis, attenuates pathological damage of neurons and increases the expression of Mfn2 via STAT3 downregulation in CI/RI. The study may update the potential mechanism of miR-326-5p and STAT3 in CI/RI. However, more studies are still needed for further development of the molecular mechanism in CI/RI.
数据和材料的可用性
不适用。
缩写
- miRNAs:
-
MicroRNAs
- STAT3:
-
Signal transducer and activator of transcription-3
- OGD:
-
Oxygen and glucose deprivation
- MCAO:
-
Middle cerebral artery occlusion
- ROS:
-
活性氧
- STAT:
-
Signal transducers and transcriptional activator
- Mfn2:
-
Mitofusin-2
- FITC:
-
Fluorescein isothiocyanate
- NES:
-
Nestin
- NC:
-
阴性对照
- Oe:
-
过度表达
- RT-qPCR:
-
逆转录定量聚合酶链反应
- OD:
-
光密度
- PI:
-
碘化丙啶
- MDA:
-
Malondialchehyche
- GSH:
-
Glutathione
- SOD:
-
超氧化物歧化酶
- DAB:
-
Diaminobenzidine
- PVDF:
-
聚偏二氟乙烯
- WT:
-
Wild-type
- Mut:
-
Mutant
- 标准差:
-
标准差
- ANOVA:
-
单因素方差分析
纳米材料
- 火灾危害与预防
- microRNA-342-5p 的下调或 Wnt3a 的上调抑制血管生成并维持动脉粥样硬化小鼠的动脉粥样硬化斑块稳定性
- 负载 ICA 的 mPEG-ICA 纳米颗粒的制备及其在治疗 LPS 诱导的 H9c2 细胞损伤中的应用
- 通过溶胶-凝胶工艺制备的纳米结构二氧化硅/金-纤维素-键合氨基-POSS 混合复合材料
- 通过聚乙二醇化脂质体改善蟾蜍灵的抗肿瘤功效和药代动力学
- 通过蒸发诱导自组装和增强的气敏特性简便合成虫孔状介孔氧化锡
- 通过尺寸、修饰、缺陷和掺杂设计和调整石墨烯功函数:第一性原理理论研究
- 用于氧化还原刺激触发释放的新型双线粒体和 CD44 受体靶向纳米颗粒
- 通过海藻酸钠电解质-磺化氧化石墨烯生物膜增强质子电导率和降低甲醇渗透率
- 利用柠檬汁通过水热反应制备的荧光碳量子点的材料和光学特性
- 溶胶-凝胶法合成的 Pr 掺杂钙钛矿锰酸盐 La0.67Ca0.33MnO3 纳米颗粒的微观结构、磁性和光学性能
- 通过生长掺杂方法实现双发射和颜色可调的 Mn 掺杂 InP/ZnS 量子点


