Mg 掺杂对用于增强光催化评估和抗菌分析的 ZnO 纳米颗粒的影响
摘要
在这项研究中,一种简便的共沉淀方法用于合成纯的和 Mg 掺杂的 ZnO 纳米粒子 (NPs)。研究了合成纳米粒子 (NPs) 的结构、形态、化学成分以及光学和抗菌活性,其与纯和 Mg 掺杂的 ZnO 浓度(0-7.5 摩尔(M)%)有关。 X 射线衍射图证实了 ZnO 的结晶六方纤锌矿相的存在。扫描电子显微镜 (SEM) 图像显示,纯的和掺杂 Mg 的 ZnO NP 处于纳米级状态,六方晶体形态约为 30-110 nm。样品的光学特性表明带隙能量 (E g) 随着 Mg 2+ 的增加,从 3.36 eV 降低到 3.04 eV 掺杂浓度。当 Mg 浓度从 2.5 到 7.5 M 变化时,ZnO 的光吸收光谱发生红移。光致发光 (PL) 光谱在 400 nm 附近显示出紫外发射峰。使用 Mg 2+ 在 430 到 600 nm 之间增强可见光发射 掺杂通过占据Zn 2+ 来指示ZnO中的缺陷密度 含 Mg 2+ 的空位 离子。光催化研究表明,7.5% Mg 掺杂的 ZnO NPs 在 UV-Vis 照射下表现出对罗丹明 B (RhB) 染料的最大降解 (78%)。使用革兰氏阳性菌和革兰氏阴性菌进行抗菌研究。结果表明,在ZnO基体中掺杂Mg离子增强了对各类细菌的抗菌活性,并且随着ZnO纳米颗粒中Mg离子浓度的不断增加,其抗菌性能得到提高。
背景
纳米颗粒表现出新的特性,这取决于它们的大小、形状和形态,使它们能够与植物、动物和微生物相互作用 [1]。在一些有机材料或植物提取物的存在下,直接从金属或金属盐合成具有商业重要性的纳米颗粒。藤蔓和许多其他植物散发出一种有机物质,可能是一种多糖和一些树脂,有助于植物垂直攀爬或穿过不定根,以产生微量元素的纳米颗粒,以便它们被吸收 [2]。纳米级无机化合物由于其高表面积体积比和独特的化学和物理特性,在非常低的浓度下已显示出显着的抗菌活性 [3]。此外,这些颗粒在高温高压下也更加稳定[4]。其中一些被认为是无毒的,甚至含有对人体至关重要的矿物质元素 [5]。据报道,抗菌性最强的无机材料是金属纳米粒子和金属氧化物纳米粒子,如银、金、铜、氧化钛和氧化锌[6, 7]。锌是人体系统必不可少的微量元素,没有它,许多酶如碳酸酐酶、羧肽酶和乙醇脱氢酶就会失去活性,而另外两种元素镉和汞属于同一组元素,具有相同的电子构型,有毒[8]。对于纳米颗粒的生物合成,使用植物的不同部分,因为它们含有代谢物,例如生物碱、黄酮类化合物、酚类、萜类化合物、醇类、糖类和蛋白质,它们作为还原剂产生纳米颗粒。它们还充当封端剂和稳定剂。它们用于医学、农业和许多其他领域以及技术。因此,注意力集中在所有植物物种上,它们的叶子、花朵或根部具有香气或颜色以合成纳米颗粒,因为它们都含有将金属离子还原为金属纳米颗粒的化学物质 [9]。最近,纳米粒子因其独特的机械、光学、磁性、电学和其他特性而开始引起人们的兴趣 [10]。这些新兴特性使它们成为用于电子、医学和其他领域的有希望的候选者。据观察,纳米材料与其传统形式相比具有更大的表面积与体积比 [11]。这就是纳米材料表现出更大化学反应性的原因。基本上在纳米尺度上,量子效应更加明显,以确定它们的最终特性,从而导致新的光学、磁性和电学行为。在各种金属氧化物半导体纳米结构中,ZnO 纳米结构因其低成本、高化学稳定性和大规模生产而引起了相当大的兴趣[12]。 ZnO 研究仅占当前纳米研究的合理部分;然而,所有因素都认为它是重要的材料之一,它将无限制地扩展纳米技术的一部分。 ZnO 是有史以来最普遍的外用药物之一。它用于大多数防晒霜中,并发现其用于缓解疼痛和瘙痒的多种治疗方法 [13]。将看到光催化的功能,主要是在氧化锌和掺杂氧化锌上;光催化剂表面可能发生大量潜在的化学、光化学和电化学反应 [14]。氧化锌在环境污染物的降解和总矿化方面赢得了很多关注[15]。与某些半导体金属氧化物相比,ZnO 的最佳观点是能够吸引广泛的太阳能光范围和更多的光量子。 ZnO由于其新颖的特性而成为绿色生态管理结构的主要材料和有潜力的候选材料[16]。
基本上有两个因素,即表面积和表面缺陷,是决定半导体金属氧化物光催化活性的最重要的变量。由于其高表面活性、结晶性、形态特征和质地; ZnO 纳米颗粒被认为是降解有机污染物最有利的催化剂[17]。最近的文献报道,Mg 掺杂的 ZnO 纳米结构可以表现出优异的器件应用性能 [18]。用 ZnO 掺杂 II 族元素的研究表明,掺杂剂可以改变带隙能量 (E g) 随着紫外-可见发光强度的增加[19]。
预计将 Mg 掺杂到 ZnO 中会改变 ZnO 的吸收、物理和化学性质 [20]。金属离子掺杂的 ZnO 纳米结构由于其光学性能的增强而成为降解各种污染物最有前途的催化剂 [21]。由细菌引起的不同类型的传染病对全世界的公共卫生构成严重威胁。为了增强氧化锌的抗菌活性,需要通过掺杂金属或非金属来改变不同类型的理化性质,如粒径、结晶度指数和光学性质[22]。
通过在 ZnO 表面引入更多缺陷,可以增强光吸附性能。基本上微量的掺杂剂足以充当半导体晶格内的施主或受主,这将在更大程度上显着改变半导体的性质。尺寸量化使导带电子和价带空穴之间的能隙发生变化,从而导致掺杂金属氧化物纳米结构的光学性质发生变化[23]。较早的文献报道,氧化锌纳米粒子可以抵抗细菌,并且具有屏蔽紫外线辐射的能力[24]。氧化锌纳米颗粒具有破坏大肠杆菌革兰氏阴性细胞膜结构的能力 [25, 26]。据报道,带正电荷的纳米粒子可以通过静电引力与革兰氏阴性细胞膜结合 [27]。用不同金属离子掺杂的 ZnO NPs 与 E 进行了评估。大肠杆菌 , 和金黄色葡萄球菌 表明抗菌活性随着微晶尺寸的增加而增加 [28]。研究人员已经采用各种物理和化学技术来合成纯和掺杂的 ZnO 纳米粒子,如蒸汽传输过程 [29]、喷雾热解 [30]、热分解 [31]、电化学法 [32]、溶胶-凝胶法 [33]、水解 [34]、化学沉淀 [35] 和水热法 [36],以调整其形态和尺寸。在所有这些方法中,共沉淀法相对简单且成本低廉。此外,它可以在室温下获得高产率,用于合成纯和掺杂的 ZnO NPs [37]。
在这里,我们通过使用简单的化学共沉淀方法研究了具有不同浓度 Mg 掺杂剂的 ZnO 纳米颗粒的制备和表征。 Mg 2+ 的影响 ZnO 晶格内的离子浓度已在结构、形态、光学和光催化研究方面进行了评估。此外,Mg 2+ 的影响 研究了离子对(革兰氏阳性和革兰氏阴性)S 的抗菌活性。金黄色葡萄球菌 ,E。大肠杆菌 , 和 Proteus 文化。
方法
所有分析级试剂均购自 Sigma-Aldrich,无需进一步纯化即可直接使用。流程图(图 1)描述了纯和 Mg 掺杂的 ZnO NPs 的制备方法。在该方法中,将 1 M 氢氧化钠 (NaOH) 溶液添加到 1 M 氯化锌 (ZnCl2) 溶液中。最终溶液在持续搅拌下保持 6 小时。氢氧化钠的碱性溶液有助于过渡金属氢氧化物的沉淀。它加速了还原过程,从而导致 ZnO 和 Mg 掺杂的 ZnO 纳米粒子的形成。此外,氢氧化钠将 ZnCl2 转化为 Zn(OH)2,加热后生成 ZnO 纳米颗粒。沉淀后,取出烧杯并给予足够的时间来沉淀最终产品。过滤所得产物并用去离子水和丙酮洗涤数次。最后,样品在 100°C 下干燥 5 小时,然后通过在玛瑙研钵中研磨转化为细粉。将由此获得的粉末在 300°C 下煅烧 4 小时以产生纳米尺寸的 ZnO 颗粒。
<图片>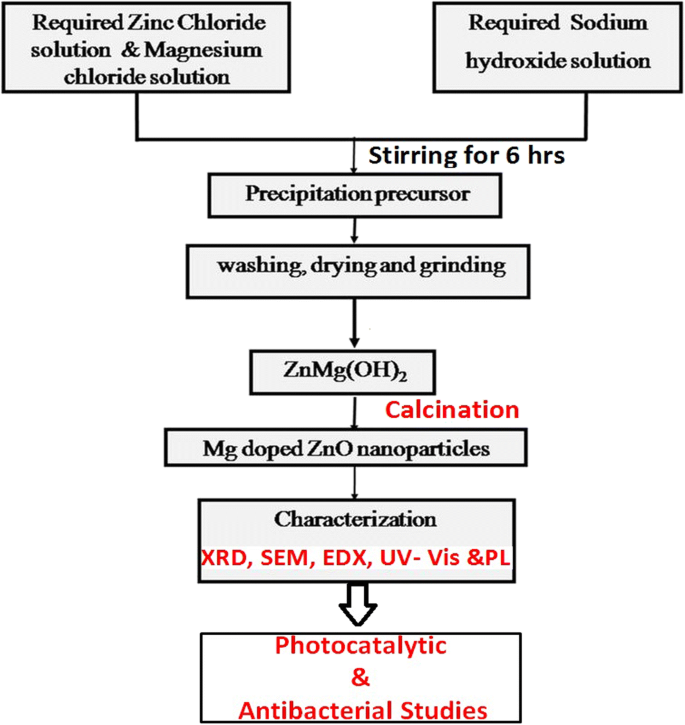
Mg掺杂ZnO纳米颗粒的合成流程图
为了合成 Mg 掺杂的 ZnO,ZnCl2 和 MgCl2 的摩尔比被测量为 Zn1 − x 镁 x O(其中 x =0.025、0.050 和 0.075) 并重复相同的程序。合成纯和 Mg 掺杂的 ZnO 的化学方程式显示在方程式中。 (1–4)
$$ {\mathrm{ZnCl}}_2+2\mathrm{NaOH}\to \mathrm{Zn}{\left(\mathrm{OH}\right)}_2+2\mathrm{NaCl}\left(\mathrm {aq}\right) $$ (1) $$ \mathrm{Zn}{\left(\mathrm{OH}\right)}_2\to \mathrm{Sintering}\to \mathrm{Mg}\hbox{- } \mathrm{掺杂}\ \mathrm{ZnO}+{\mathrm{H}}_2\mathrm{O} $$ (2) $$ {\mathrm{MgCl}}_2+{\mathrm{ZnCl}}_2+ 2\mathrm{NaOH}\to\mathrm{ZnMg}{\left(\mathrm{OH}\right)}_2+2\mathrm{NaCl}\left(\mathrm{aq}\right) $$ (3) $$ \mathrm{ZnMg}{\left(\mathrm{OH}\right)}_2\to \mathrm{Sintering}\to \mathrm{Mg}\hbox{-} \mathrm{掺杂}\ \mathrm{ZnO }+{\mathrm{H}}_2\mathrm{O} $$ (4)在电化学系列中,Mg比Zn更具反应性,因此发生还原以占据Zn晶格。
特征化
样品的晶体结构通过 X 射线衍射 (XRD) Bruker D8 高级 X 射线衍射仪) 与 Cukα 辐射 (λ =1.54 Å) 和表面形态特征通过场发射扫描电子显微镜 (FESEM, ZEISS) 进行研究。使用日立 U-3900H 的双光束紫外-可见分光光度计在 200-1200 nm 范围内记录样品的光吸收光谱。光致发光 (PL) 发射研究通过光谱仪 (JOB HR800 IN Yoon Horbe) 使用波长为 325 nm 的 He-Cd 激光源进行。采用琼脂圆盘扩散技术测试合成样品对不同微生物的抗菌活性。
光催化活性的测量
实验在容量为 150 毫升的光催化石英反应器中进行。反应堆有水循环设施以确保恒温。通过使用 125 W (311 nm) 中压汞弧灯 (SAIC, INDIA) 进行 UV 照射。在自然 pH (6.2) 下,将 150 毫升所需初始浓度 (20 ppm) 的 RhB 染料溶液与固定量的 ZnO NP (50 毫克/升) 混合。将溶液置于紫外线照射下并进行磁力搅拌。以不同的时间间隔从光反应器中取出样品并离心。使用紫外-可见分光光度计分析上清液的最大吸收(554nm)。使用 RhB 染料溶液对 Mg 掺杂剂(2.5%、5% 和 7.5%)-ZnO NPs 采用了类似的程序。催化剂表面降解RhB的百分比由下式计算:
$$ \mathrm{Percentage}\ \mathrm{of}\ \mathrm{degradation}=\left({C}_0-{C}_t\right)/{C}_0\times 100\% $$ (5)其中 C 0 代表吸收的初始时间,C t 表示不同时间间隔(0、30、60、90 和 120 分钟)后的吸收。
抗菌研究
E。大肠杆菌 (革兰氏阴性),S。金黄色葡萄球菌 (革兰氏阳性)和变形杆菌 (革兰氏阴性菌株)在使用前在肉汤培养基上保持在 4°C。制备营养琼脂培养基并在 121°C 下灭菌 15 分钟。将 25 毫升营养琼脂倒入无菌培养皿中并使其凝固。在每个培养皿中涂抹 0.2 毫升不同的细菌种类(大肠杆菌 ,S。金黄色葡萄球菌 , 和 Proteus )。制备一个圆盘,借助无菌环放入平板中,每盘制作两个圆盘,制成含细菌培养物的凝固琼脂。
结果与讨论
结构研究
图 2 说明了纯和 Mg 掺杂的 ZnO 样品的 X 射线衍射 (XRD) 图案。在图中,在 31.8°、34.5°、36.3°、47.5°、56.7°、62.9° 和 68° 处看到七个主要峰,它们可以归因于来自(100)、(002)、(101)、 (102)、(110)、(103) 和 (112) 平面分别用于晶格常数 a =b =3.24 Å 和 c =5.2066 Å [38]。 XRD 图清楚地反映了纯 ZnO 纳米颗粒 (JCPDS:36-1451) [39] 的六方纤锌矿相晶体结构的存在。同样从衍射图中可以看出,没有观察到进一步的二次相,Mg 掺杂剂进入 ZnO 晶格,并且在 Mg 掺杂的 ZnO NPs 的 XRD 图中没有观察到显着变化。还注意到 XRD 峰的强度随着 Mg 掺杂浓度的增加而降低(如图 2a-d 所示),这证实了由于晶格畸变导致的结晶度的细长损失。由于 Mg 离子掺杂在 ZnO 的周期性晶格内,因此产生了少量应变。这导致晶格的交换,连续导致晶体规则性的改变。然而,非常谨慎的推论表明,在 Mg 掺杂到 ZnO 基质中时观察到的峰值位置向较低的角度值移动。特别是位于(101)面35°.84处的峰,随着掺杂浓度的增加,它确实向较低的值移动,这可以归因于Zn 2+ 的置换 Mg 2+ 离子 离子 [40]。文献中充分报道了由于掺杂剂材料的掺入,主体材料的晶格特性发生了变化。这是由于它们在原子半径上的差异而发生的。此外,掺杂离子可以替代主晶格中的锌离子(镁离子)[41]。因此,ZnO NPs 的基本结构没有改变,它们保留了其原始的纤锌矿结构。这表明大部分 Mg 2+ 离子作为取代离子进入晶格以取代 Zn 2+ 离子并且不进入空隙空间。由于取代Mg 2+ 的离子半径 (R 镁 2+ =0.057 nm 为 0.57 Å) 小于 Zn 2+ (R 锌 2+ =0.06 nm 为 0.60 Å) [42],观察到由于 Mg 2+ ,该位移对应于少量晶格应变 进入氧化锌环境。
<图片>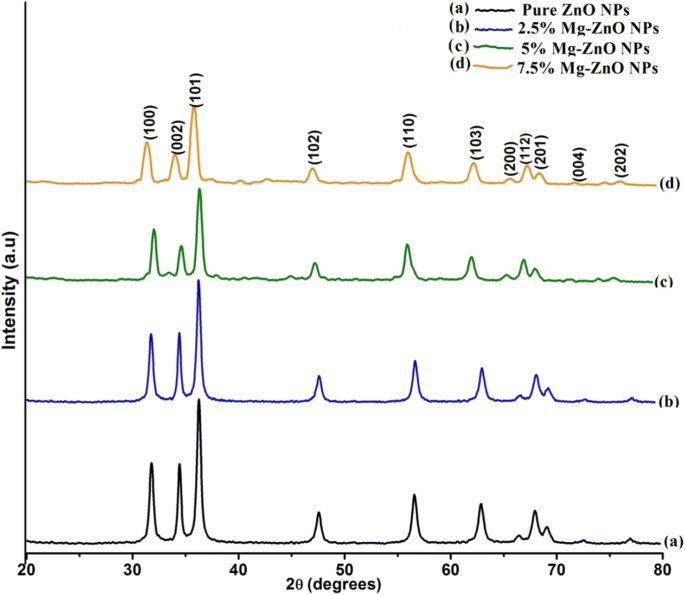
纯纳米颗粒和 Mg-ZnO 纳米颗粒的 XRD 图。 一 纯氧化锌纳米颗粒。 b 2.5% Mg-ZnO 纳米颗粒。 c 5% Mg-ZnO 纳米颗粒。 d 7.5% Mg-ZnO纳米颗粒
平均晶粒尺寸采用谢乐公式[43]计算。
$$ d=\frac{0.89\lambda }{\beta \cos \theta } $$ (6)其中 λ 是辐射的波长 (1.54056 Å),β 是半峰全宽,θ 是衍射角。从计算值可以看出,平均晶粒尺寸随着 Mg 掺杂浓度的增加而增加(表 1)。
掺杂对晶格参数的影响
微晶尺寸、晶格参数、原子堆积率 (APF)、晶格应变和体积显示了纯和掺杂 ZnO NPs 的物理特性 [44]。对于纤锌矿相,晶格参数通过使用方程计算。 (7-9) 其中,a =b,c为晶格参数,d hkl 是对应于其米勒指数(hkl)的面间距。
$$ \frac{1}{d_{hkl}}=\frac{\left({h}^2+{k}^2\right)}{a^2}+\frac{l^2}{c ^2} $$ (7) $$ a=\frac{\lambda }{\sqrt{3\sin {\theta}_{100}}} $$ (8) $$ c=\frac{\lambda } {\sin {\theta}_{002}} $$ (9) $$ D=\frac{1}{APF} $$计算得到的晶格参数列于表 1。从表 1 中可以看出,其晶格参数值随着 Mg 2+ 发生变化 离子替代物 Zn 2+ 晶格中的离子。随着掺杂浓度的增加,掺入的掺杂剂原子占据了置换晶格位置。从表 1 还观察到,微晶尺寸 (D) 与原子堆积率 (APF) 成反比,如方程式 1 所示。 (10).
使用方程计算应变诱导。 (10).
$$ \varepsilon ={\beta}_{hkl}\cos \theta /4 $$ (10)此外,注意到由于 Mg 2+ 其晶格应变降低 ZnO 基质中掺杂的离子(表 1),这会导致晶体结构的局部变形。这一点很明显,并且在文献中也较早地注意到它们的原子半径和掺杂浓度的差异[45]。
场发射扫描电子显微镜 (FESEM) 和 EDS 分析
图 3a-d 说明了不同 Mg 摩尔浓度下 Mg 掺杂的 ZnO NPs 的形态。从 FESEM 图像中,观察到大多数晶粒落在纳米尺度范围内。还注意到颗粒在它们的表面上聚集。颗粒在表面的聚集可能源于合成纳米颗粒的高表面能 [46]。有趣的是,对于 5 M % 和 7.5 M % 的掺杂浓度,观察到一些六边形晶体形状和分布良好的纳米结构晶粒,表明较高掺杂的 Mg 对 ZnO 基体表面的影响。随着 ZnO 基质内 Mg 离子浓度的增加,最终颗粒的晶粒尺寸从 30 nm 增加到 110 nm。图3c、d与XRD分析得到的微晶尺寸一致。
<图片>
纯和 Mg 掺杂的 ZnO NPs 的 FESEM 照片。 一 纯氧化锌纳米颗粒。 b 2.5% Mg-ZnO 纳米颗粒。 c 5% Mg-ZnO 纳米颗粒。 d 7.5% Mg-ZnO纳米颗粒
图 4a-d 显示了使用 EDS 进行的纯和 Mg 掺杂的 ZnO 纳米颗粒的化学成分分析。从获得的 EDS 光谱中,观察到各种元素如 Zn、Mg 和 O 的存在。图 4c、d 清楚地显示了随着 Mg 注入 ZnO 环境,Mg 的强度略有增加。 Mg离子的掺入对结构和光学性质有显着影响。从EDS光谱也可以得出结论,合成样品中没有其他外来元素存在。
<图片>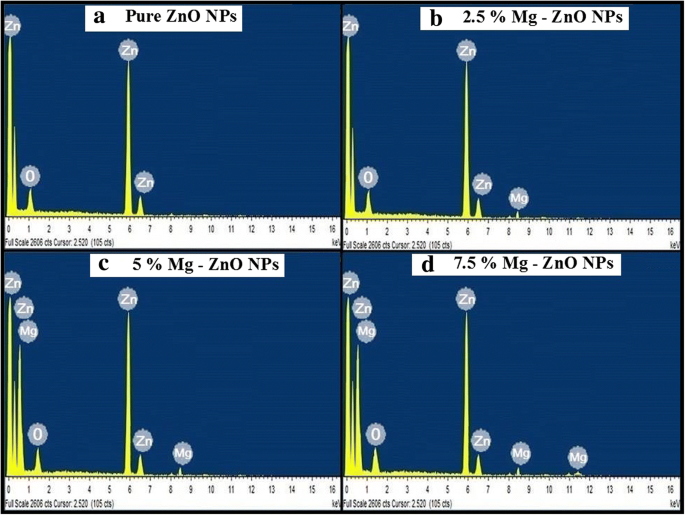
能量色散 X 射线 (EDS) 光谱。 一 纯氧化锌纳米颗粒。 b 2.5% Mg-ZnO 纳米颗粒。 c 5% Mg-ZnO 纳米颗粒。 d 7.5% Mg-ZnO NPs
光学研究
图 5a 说明了纯的和掺杂 Mg 的 ZnO NP 的 UV-Vis 吸收光谱作为波长的函数,范围为 200 至 1200 nm。从图中可以看出,吸收峰随着掺杂浓度的增加而增加。吸光度的增加可能是由于各种因素造成的,如粒径、缺氧和晶粒结构缺陷 [47]。对于 Mg 掺杂的 ZnO 纳米粒子,在低于 380 nm 的波长处发现强吸光度,而在可见光区域中观察到非常低的吸光度,如图 5a 所示。这是由于处于较低能态的分子被激发到较高能级对入射光子能量的吸收更大。
<图片>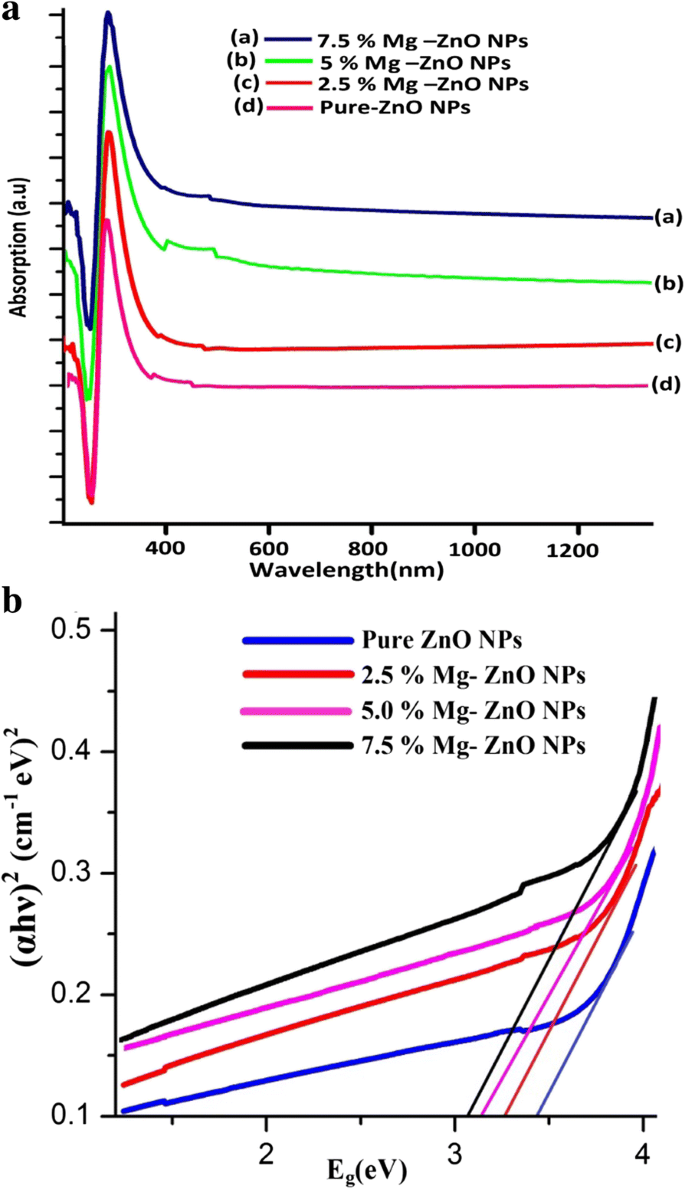
一 光吸收和b 带隙能量 (E g) 对于纯的和掺杂 Mg 的 ZnO NPs
观察到随着 Mg 含量从 2.5% 变为 7.5 M%,Mg 掺杂的 ZnO NPs 的吸收边向更长的波长移动(红移)。这可能是由于 Mg 掺杂到 ZnO 导致样品中存在少量晶格应变。预计这种红移行为会降低其带隙 (E g) 价值。光学带隙 (E g) 由以下关系式 (11) 的 Tauc-plot 确定。
$$ \alpha =\frac{A{\left( h\nu -{E}_{\mathrm{g}}\right)}^{1/2}}{hv} $$ (11)其中 α 是吸收系数,h 是普朗克常数,ν 是光辐射的频率,E g 是带隙能量,其中“n ”取½值表示允许的直接转换[48]。 (αhν) 2 的图 与 (hν) 的对比是针对纯和 Mg 掺杂的 ZnO NP 进行的。带隙能量 (E g) 从图的线性部分外推到 x -轴。
从图 5b 可以看出,带隙能量 (E g) 对于纯 ZnO NPs 约为 3.36 eV,并且随着 Mg 掺杂剂的增加而降低(3.36 到 3.04 eV)。由于强量子限制和表面积与体积比的增强,带隙减小 [49]。红移增强和带隙能量降低 (E g) 确认存在 Mg 2+ Zn 2+ ZnO晶格位点。
光致发光研究
图 6 说明了纯镁和 Mg 2+ 的光致发光光谱 波长为 325 nm 的掺杂 ZnO NP。在可见光谱区域观察到 400 nm 附近的相对稳定的 UV 发射带和 450 至 620 nm 的宽带。强紫外线发射归因于激子的辐射复合(激子发射)[50]。 450 至 620 nm 宽可见光发射带的起源是由于表面阴离子空位 [51]。这可能是由于表面束缚电子通过预先存在的陷阱空穴隧穿 [52]。还观察到在 390 和 525 nm 处观察到的发射带的强度随着 Mg 含量(7.5%)的更高掺杂而降低。 ZnO NPs 内部较高的掺杂百分比阻止了光生电子和空穴的复合。此外,Mg (7.5%) 离子在 ZnO 晶格内部产生额外的活性缺陷位点,导致通过这些活性缺陷位点进一步吸收可见光 [53]。
<图片>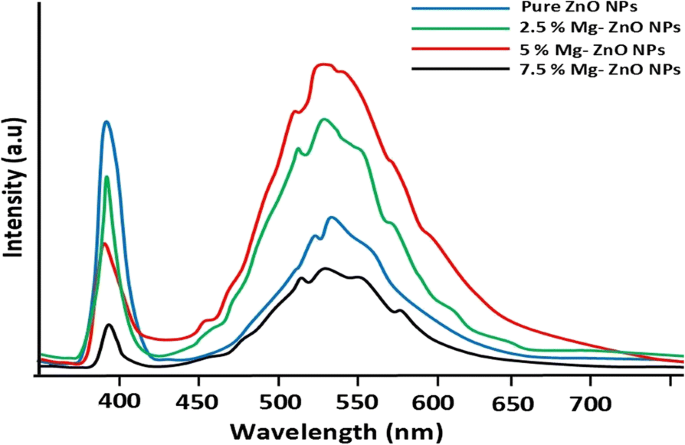
纯纳米粒子和Mg-ZnO纳米粒子的光致发光光谱
光催化研究
在不同的时间间隔(0-120 分钟)下研究了纯和 Mg 掺杂的 ZnO 与罗丹明 B (Rh B) 染料溶液的光催化降解研究。记录了不同时间间隔(0-120 分钟)RhB 染料溶液的光吸收光谱,如图 7 所示。观察到,随着时间的推移,峰高降低,表明罗丹明 B 降解更大ZnO 的光催化活性。 120 分钟后,使用纯 ZnO 降解的染料数量可忽略不计,而 7.5% Mg 掺杂的样品显示出更高的降解效率。这是由于在 ZnO 基体中掺杂 Mg 造成的缺陷和氧空位的存在[54]。图 8 显示了纯和 Mg 掺杂的 ZnO NP 的降解百分比。据观察,与其他掺杂浓度相比,7.5% Mg 掺杂的 ZnO 表现出的最大降解为 78%(表 2)。还应注意,较高的 Mg(10% 或更高)掺杂浓度到 ZnO 中会降低光催化活性。由于物理缺陷以及阳离子氧化态的增加,这是可以理解的。这种现象在较早的文献中观察到,该文献描述了在掺杂过程中产生的过量阳离子将作为空穴和电子的俘获点。随后,这将刺激光生带电物质的重组。这逐渐阻碍了•OH(羟基)和O•2 −的生成 (氧)超氧自由基。这种现象会降低光催化活性。 Lee 等人 也报道了类似的结果。 [55] 和 Yousefi 等人。 [56]。此外,在我们的共沉淀技术中,对于较高的 Mg 掺杂浓度到 ZnO 中,热力学溶解度较小。 Javed Iqbal等[57]也报道了类似的结果。
<图片>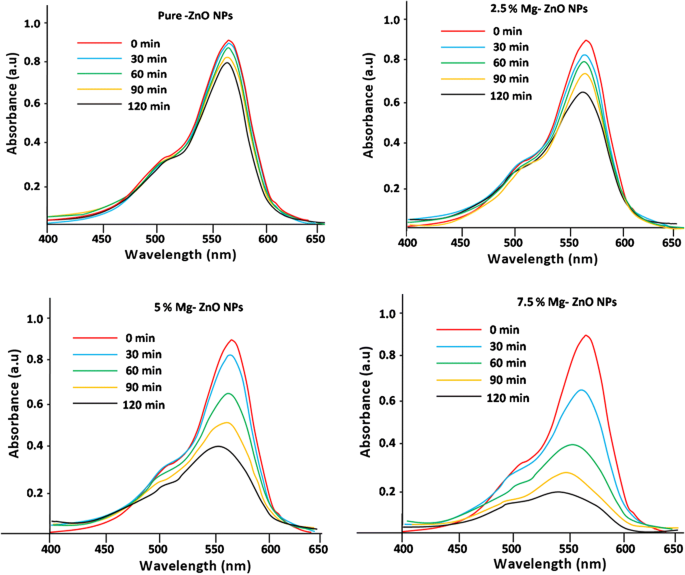
罗丹明 B 染料水溶液从 (0-120 min) 降解的吸收光谱衰减
<图片>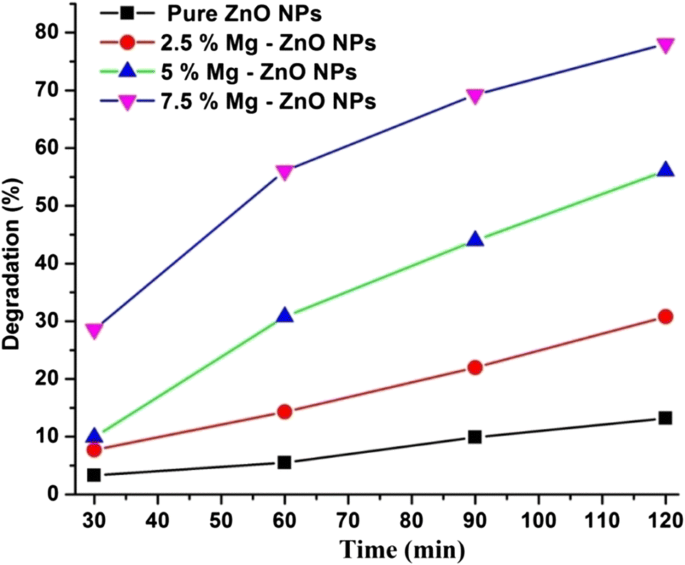
纯和IZ-NPs光降解罗丹明B
似乎Mg掺杂的ZnO NPs的作用类似于电子汇,因此可以显着增强光生电子-空穴对的分离并抑制它们的复合,从而提高光催化活性[58]。
可以通过绘制浓度比 ln(C/Co) 与辐照时间“t”的线性曲线来观察反应动力学 ”。从图表(图 9a)中可以明显看出,ZnO 基质中 2.5% 到 7.5% 的 Mg 离子的存在实际上激活了光催化过程。从图 9b 可以看出,RhB 降解速率常数 k 为 1.09 × 10 - 3 , 2.76 × 10 − 3 , 5.72 × 10 − 3 , 和 1.26 × 10 − 2 对于纯 ZnO NPs,分别为 2.5% Mg-ZnO NPs、2.5% Mg-ZnO NPs 和 2.5% Mg-ZnO NPs。其中,7.5% Mg-ZnO NPs 表现出最高的降解速率常数(k)值,与纯 ZnO NPs 相比有相当显着的增加(表 2)。该光催化实验结果清楚地表明,Mg离子掺杂到一定限度可以有效提高ZnO光催化剂的光催化活性。
<图片>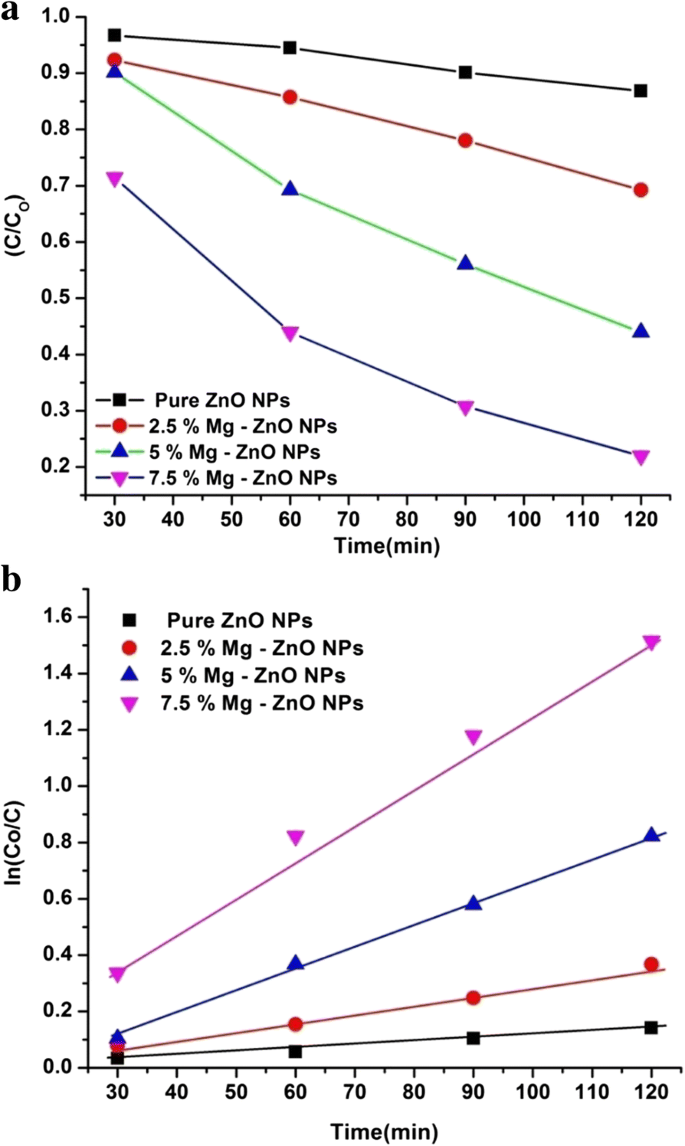
(a ) 纯纳米颗粒和 Mg-ZnO 纳米颗粒的 RhB 相对浓度随时间的变化 (b ) RhB染料降解纯纳米粒子和Mg-ZnO纳米粒子的反应动力学
Mg 掺杂的 ZnO NPs 光催化活性增强的原因是由于表面氧空位的存在而增大了表面积 [59]。半导体材料的光催化机理是通过形成电子-空穴对(e − , h + ) 以及随后的分离以及电子和空穴的复合 [60]。纯 ZnO 的光催化活性归因于由大量缺陷位点(如氧空位和间隙锌原子)引起的供体态,以及由锌空位和间隙氧原子引起的受体态 [61]。 But for Mg-doped ZnO NPs for the degradation of RhB under UV-Visible irradiation, initially electron–hole pairs are created and then the species such as •OH and •O − 2 are formed as shown in the equation.
$$ ZnO+ h\nu \to ZnO\left({e}_{CB}+{h}_{VB}\right) $$ (12)The photo-induced electrons are easily trapped by electronic acceptors like adsorbed (O2), in order to produce a superoxide radical anion (O• − 2 ) Eq. (13)
$$ {e}_{CB}+{O}_2\to {O}_2^{\bullet -} $$ (13)Further, the photo-induced holes are easily trapped by negative OH − ions to errand the production of hydroxyl radical species (OH•) Eq. (14)
$$ {OH}^{-}+{h}^{+}\to {OH}^{\bullet } $$ (14)Thus produced OH − radical and superoxide radical anion will carry out the total photocatalytic reaction. However, •OH radical is a particularly strong oxidant which can cause fractional or complete mineralization of organic molecules. The high oxidative potential of the hole in the valence band causes the oxidation of organic compounds to form some reactive intermediates [62] as shown by Eq. (15–16).
$$ {O}_2^{\bullet -}+\mathrm{RhB}\ \mathrm{degradation}\ \mathrm{products}+{CO}_2+{H}_2O $$ (15) $$ {OH}^{\bullet }+\mathrm{RhB}\ \mathrm{degradation}\ \mathrm{products}+{CO}_2+{H}_2O $$ (16)Thus, it is necessary to prevent the recombination of electron–hole pairs to have better photocatalytic activity of semiconductor based NPs. Controlled doping of Mg over the ZnO NPs up to a certain limit can enhance the photocatalytic activities. All the Mg-doped ZnO NPs show a significant enhancement of the photo-degradation of RhB dye compared with the pure ZnO NPs. In this research, 7.5% Mg-doped ZnO NPs show better photocatalytic properties after 120 min compared with pure ZnO sample. This might be due to the change in their particle size and band gap effects [63].
Antibacterial Studies
The zone of inhibition by using Mg-doped ZnO NPs for E.大肠杆菌 (Gram-negative), S.金黄色葡萄球菌 (Gram-positive bacteria), and Proteus (Gram-negative strains) is displayed by Fig. 10. It was carried out using disc diffusion method to observe their ability as a potential antimicrobial agent. The prepared NPs were highly reactive due to their high surface to volume ratio. From Fig. 10, it is clear that the Mg 2+ -doped ZnO NPs inhibit the growth of both Gram-negative and Gram-positive bacteria. It was observed that the zone of inhibition is proportional with the amount of Mg doping in ZnO NPs. The results obtained to show the effect of Mg doping in ZnO NPs are illustrated in Table 3. This might be attributed to the reduction in their band gap values. Due to reduction in the band gap, there is a possibility of exciton generation. Overall, this enhances the photocatalyst activities for improved bactericidal activity of Mg-doped ZnO NPs [64]. Furthermore, due to the various surface-interface characteristics may have different chemical-physical, adsorption-desorption abilities in the direction towards bacteria, make sure in different antibacterial performances [65].

Zones of Inhibition of ZnO and Mg-doped ZnO NPs against the given bacteria
The interaction between the NPs and the cell wall of bacteria was changed due to doping of Mg. The growth of S.金黄色葡萄球菌 and the other two bacteria was more commendably affected by Mg 2+ -doped ZnO nanostructures compared with pure ZnO NPs. From Table 3, it is noted that Gram-negative and Gram-positive have different inhibition zones. This difference in the antibacterial activity of Mg-doped ZnO nanostructures against Gram-negative and Gram-positive bacterial strains may be due to the difference in cell wall structure of those respective bacteria. It was also reported earlier that various bacterial strains had considerably different infectivity and tolerance levels towards the different agents including antibiotics [66]. Also differences in the antibacterial activity might be due to different particle dissolution.
Basically, the antibacterial efficiency of pure and Mg-doped ZnO NPs is mainly dependent on the increased levels of reactive oxygen species (ROS), mostly hydroxyl radicals (OH) and singlet oxygen [67]. This is mainly due to the enlarged surface area which causes increase in oxygen vacancies as well as the diffusion capacity of the reactant molecules inside the NPs [68]. The reactive oxygen group contains superoxide radical and hydrogen peroxide. Both of them can damage the DNA and cellular protein leading to cell death [69]. Moreover, the presence or addition of the nanostructures on the surface or cytoplasm of the bacteria can cause the disruption of cellular function as well as disorganization of the cell membranes [70]. The doping of Mg with ZnO may lead to the variation in grain size, morphology, and solubility of Zn 2+ ions. All these factors combined together have a robust impact on the antibacterial activity of ZnO [71, 72]. The results have revealed that Mg-doped ZnO nanostructures will be a promising candidate to be used for potential drug delivery systems to cure some significant infections in the near future.
Conclusions
To conclude, pure and Mg-doped ZnO structures were successfully synthesized by co-precipitation method. The XRD patterns revealed the wurtzite structure for all the nanosamples and no impurity phase was noted. The maximum crystallite size obtained from XRD was less than 100 nm. FE-SEM studies confirmed that the crystallite size increased with increase in Mg content. The UV-Visible results revealed that absorption underwent a redshift with Mg into ZnO as compared to pure ZnO exhibiting strong quantum confinement effects. Optical band gap energy was found to decrease from 3.36 to 3.04 eV with Mg doping, resulting in the increment in their crystallite size as a result of Mg doping. PL results confirmed the enhanced visible emissions with Mg-doped ZnO leading to the increase in delocalization of electron-hole pairs. Photocatalytic measurements revealed the increase in Mg doping in the ZnO nanoparticles that caused higher photocatalytic activity. The antibacterial activities of the synthesized nanosamples were tested against E.大肠杆菌 (Gram-negative), S.金黄色葡萄球菌 (Gram-positive bacteria), and Proteus (Gram-negative strains).
纳米材料
- 用于增强药物递送的纳米纤维和细丝
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 氧化铜纳米颗粒对大肠杆菌的生物合成、表征和抗菌潜力评估
- Sb/坡缕石 (PAL) 纳米颗粒的制备和增强催化氢化活性
- 铝硅酸盐矿物的替代掺杂和优异的水分解性能
- Au 纳米颗粒对 HT29 和 SPEV 细胞系影响的体外研究
- 水热合成 In2O3 纳米颗粒混合孪晶六边形圆盘 ZnO 异质结构以提高光催化活性和稳定性
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- Ag 纳米颗粒/BiV1-xMoxO4 与增强的光催化活性的协同效应
- 弹性刚度和表面附着力对纳米粒子弹跳的影响
- 基于叶酸和 gH625 肽的 Fe3O4 磁性纳米颗粒功能化增强细胞内化的比较
- 用 Au 纳米粒子定制的二氧化硅硅藻壳可以对用于生物、安全和环境应用的分子进行灵敏分析


