斑马鱼:一种用于纳米技术介导的神经特异性药物递送的有前景的实时模型系统
摘要
向大脑输送药物一直是研究界和医生面临的挑战。血脑屏障 (BBB) 是将药物输送到大脑和中枢神经系统特定部位的主要障碍。它在生理上由复杂的毛细血管网络组成,以保护大脑免受任何侵入性物质或外来颗粒的侵害。因此,对于成功的治疗干预,绝对需要了解 BBB。最近的研究表明,斑马鱼作为一种评估血脑屏障通透性的模型强势出现,血脑屏障在斑马鱼和哺乳动物之间的结构和功能上高度保守。斑马鱼模型系统具有诸多优点,包括易于维护、繁殖力强、胚胎和幼虫透明。因此,它有可能被开发为一种模型,用于分析和阐明 BBB 对具有神经特异性的新型渗透技术的渗透性。纳米技术现在已成为工业和研究界将药物输送到大脑的重点领域。纳米粒子正在以更高的效率和准确性开发,以克服 BBB 并将神经特异性药物输送到大脑。斑马鱼是评估纳米颗粒生物相容性和毒性的优秀模型系统。因此,斑马鱼模型对于神经特异性药物递送新技术和脑疾病潜在疗法的发现或开发是必不可少的。
介绍
药物递送是指将化合物转移到体内以达到治疗目的的方法。这些化合物在性质上主要是药物,并且针对特定疾病状况在体内针对特定细胞群。药物递送一词包含两个主要概念:剂量形式和给药途径 [1]。适当的药物递送通过调节以下各项来确保有效的药物活性:药物释放、细胞吸收和系统内的正确分布 [2]。一些常见的给药途径包括肠内(胃肠道)、肠胃外(通过注射)、吸入(嗅觉介导)、透皮(通过真皮)、局部(通过皮肤)和口服途径(通过食道)[3]。提供药物在治疗领域至关重要且具有重要意义。所选择的方法必须最有效,对系统的毒性也最低 [4]。当有问题的器官是大脑时,问题就变得更大了。几十年来,研究人员一直在努力向大脑输送药物 [5, 6]。无数的技术和想法已被用于开发一种有效的技术 [7, 8]。然而,成功似乎并不太近。这场斗争中最大的障碍是穿越血脑屏障 (BBB) 的能力。 BBB 是一种生理屏障,可保护我们的大脑免受从血液转移到大脑的化合物的影响 [9]。屏障的自然构成只允许血流中非常小的分子进入大脑 [10]。小分子量 <400 Da 的分子和脂溶性分子具有穿透大脑的能力 [11]。神经特异性药物必须满足这些参数才能有效地通过 BBB 进行药物递送。目前,大多数针对大脑开发的药物都未能成功穿越 BBB [9, 12, 13]。中枢神经系统疾病是影响生命各个阶段的许多人的一些最普遍的疾病。然而,这些疾病仍然是治疗最少的疾病 [14]。由于现有药物靶向大脑的成功率极低,因此迫切需要新型神经特异性药物递送技术。除了 BBB 的渗透性受限外,还需要考虑大脑的复杂性和现有药物递送技术引起的副作用 [15]。缺乏有效递送神经特异性药物的绝对方法阻碍了该领域的有效药物开发。研究界已经探索了各种途径来向大脑提供安全和有针对性的药物。正在探索将大分子转化为纳米颗粒以确保最大效率 [16]。
纳米技术对脑药物输送研究的巨大影响越来越引起科学界的兴趣 [17]。随着纳米技术的发展,纳米毒理学领域也在同步扩张。纳米粒子的毒性评估在分析纳米粒子对单个物种和整个环境的影响方面起着关键作用 [18]。近年来,斑马鱼被用作毒性研究的原型 [19]。斑马鱼已被广泛用于实验生物学研究,现在正在发展成为研究纳米毒性的强大模型系统 [20]。在纳米毒性的模型系统方面,斑马鱼提供了几个优势。作为实验动物使用非常经济且易于维护。它具有高繁殖率,使它们易于获得,并有助于以更简单的方式了解脊椎动物的生理学 [21]。然而,使用斑马鱼作为模型系统也有其局限性。首先,斑马鱼的神经系统可能不像人类那样复杂和发达;啮齿类和鼠类的神经系统相对发达,可用于研究复杂的人脑疾病;然而,它们与人类并不相同 [22]。其次,斑马鱼缺乏人类的一些器官系统,如肺、前列腺和乳腺;此外,无法研究由斑马鱼中不存在的基因引起的疾病 [23]。然而,斑马鱼与人类基因组有 70% 的基因组相似性,与人类致病基因有 84% 的同源性,这使得它非常适合模拟人类疾病病理[24]。以前曾假设成年斑马鱼没有肝脏巨噬细胞。库普弗细胞被认为仅在早期胚胎阶段短暂存在,而在发育后期则不存在或稀疏 [25,26,27]。然而,最近的工作表明库普弗细胞的造血起源及其在成年斑马鱼肝脏中的持久性,使斑马鱼也擅长研究库普弗细胞 [28, 29]。此外,更高的脊椎动物模型有望比斑马鱼更准确地模拟复杂的人类病理。最近,一场关于依赖动物模型可用数据及其对人类的推断的争论已经开始 [30]。这表明任何动物模型在应用于临床研究时都有其自身的局限性 [30, 31]。
本综述讨论了使用斑马鱼作为模型系统专门针对大脑的纳米技术介导的药物递送的最新研究。它总结了 BBB 的障碍和各种纳米药物优化、它们的毒性评估以及使用斑马鱼胚胎和成鱼治疗神经退行性疾病的影响。最后,该综述强调了用于神经特异性药物递送的斑马鱼模型的优缺点,并揭示了它对未来转化研究的巨大影响。
血脑屏障:神经特异性药物输送的主要障碍
BBB 确保物质进入大脑受到限制,因此充当有助于维持正常大脑稳态的扩散屏障 [32]。几个细胞参与组成 BBB 的复合结构 [33]。周细胞、星形胶质细胞和神经元构成细胞成分,而内皮细胞、紧密连接和基底膜共同构成 BBB [34]。大脑内皮细胞缺乏开窗确保小分子不会通过其表面扩散。由于内皮间连接如紧密连接、粘附连接和间隙连接的存在,连接内皮细胞 [35],即使是水溶性物质也无法进入大脑。这些内皮细胞又被周细胞、星形胶质细胞和基底膜包围,它们完成了 BBB 的结构 [36]。粘附连接和紧密连接调节内皮细胞层的渗透性。间隙连接由连接蛋白分子组成,它们控制内皮细胞之间的通讯 [37]。分子可以通过两种途径穿过 BBB:细胞旁途径或跨细胞途径 [38]。在细胞旁通路中,离子和分子通过使用浓度梯度在细胞之间被动扩散而通过 BBB [39]。跨细胞途径利用各种机制,如转胞吞作用或受体介导的转运,使分子通过细胞 [40]。几个参数影响 BBB 的渗透性。分子量、表面电荷、表面活性、分子溶解度和分子相对大小影响血脑屏障通透性[41]。
血脑屏障:现代给药技术
健康大脑中的血脑屏障 (BBB) 主要作为扩散屏障来保护正常大脑功能。它可以防止大多数化合物从血液转移到大脑。严格的 BBB 只允许非常小的分子进入大脑;然而,观察到它在疾病条件下被破坏。
为什么纳米粒子是神经特异性药物递送的当前选择
在分子水平上工程和合成材料的技术被称为纳米技术。美国国家纳米技术研究所将纳米技术定义为至少存在于一个维度且尺寸范围在 1 到 100 纳米之间的任何材料(图 1)。过去十年见证了纳米技术领域及其在生物医学领域的应用的繁荣。据信,基于纳米技术的药物输送已经激起了整个生物技术和制药行业,并在未来几年给该领域带来了深刻的变化 [42,43,44,45,46,47]。纳米技术的应用在靶向药物递送方面具有多项优势。这些包括将 (a) 水溶性较低的药物输送到其各自的目标部位的能力,(b) 两种或多种类型的药物以实现组合治疗,(c) 在特定作用部位靶向输送,(d) 转运药物穿过严密的屏障,即血脑屏障,(e) 更好地理解和分析药物活动的可视化机会 [48] 和 (f) 在药物活动模式下实现完美疗效的实时跟踪设施 [44]。因此,纳米技术在神经特异性治疗方面具有巨大的潜力。
<图片>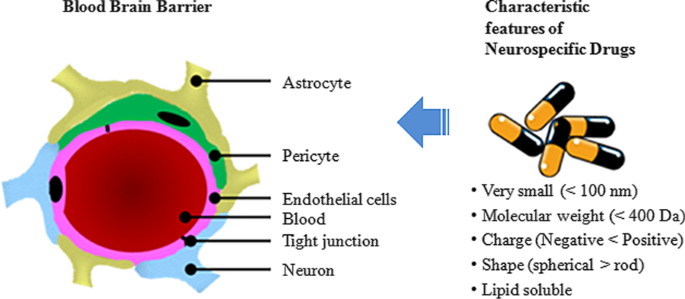
神经特异性药物的特征。 BBB 通常由星形胶质细胞、周细胞和神经元包围的内皮细胞中的紧密连接组成。神经特异性分子应该具有特定的特性才能穿过血脑屏障 (BBB)。优选特征是:直径小于100nm的极小尺寸,低分子量优选小于400Da,应带正电荷,球形和脂溶性
斑马鱼作为神经特异性药物递送模型
Danio rerio (斑马鱼)是一种用于探索发育研究和退行性疾病研究的证明脊椎动物模型 [49,50,51,52]。它可以为广泛的分析建模,从基础和毒理学分析到临床前研究 [53,54,55]。在斑马鱼提供的几个优点中,其具有成本效益的维护、简单的外壳要求和大的离合器尺寸的简单测试非常适合高通量测试[56]。高繁殖力是一个显着特征,进一步强调了该模型系统的使用 [24, 57]。斑马鱼的器官系统与高等脊椎动物的器官系统高度保守[58]。
斑马鱼胚胎具有外部发育并且完全透明,因此可以进行广泛的视觉研究。因此,它们是使用破坏正常生长、发育和细胞周期的试剂进行筛选分析的绝佳工具 [59]。它们展示了从外包到关键结构的最终开发的全面开发模式 [60, 61]。斑马鱼现在被广泛用于神经精神病学研究和各种研究,以分析纳米颗粒介导的药物递送中的发育毒性。通过简单的光学显微镜观察,斑马鱼接触金纳米粒子会破坏正常的眼睛发育和色素沉着 [62, 63]。对斑马鱼施用金纳米粒子会导致基因毒性效应和其基因组构成的严重改变 [64]。二氧化硅 NPs 的剂量和时间依赖性毒性是通过分析其对心血管系统 [65, 66] 和死亡率 [67] 的影响来确定的。还发现壳聚糖纳米粒与普通壳聚糖相比具有更高的相容性[68]。
用于临床干预的纳米颗粒必须可生物降解且无毒,这一点绝对至关重要。纳米粒子在靶向药物递送和转化研究领域具有巨大潜力。纳米粒子的使用已应用于越来越多的领域,包括体内应用。纳米颗粒使用的这种广泛增加暗示了这些纳米载体过度暴露于人类的潜在危险。纳米粒子的毒性研究是纳米技术不可或缺的一部分。必须在细胞和分子水平上对纳米颗粒相互作用进行研究,以分析其毒性,然后才能临床使用。表 1 总结了使用斑马鱼进行脑靶向药物递送的各种纳米载体的神经毒性研究。纳米粒子毒性包括对毒性、渗透性、死亡率、致畸性、免疫反应和基因组毒性的分析。
斑马鱼被广泛用作评估纳米颗粒毒性和生物相容性的模型系统 [111,112,113],它作为研究神经毒性和纳米颗粒高通量筛选的模型具有巨大潜力 [114,115,116,117]。除斑马鱼外,没有任何模型如此适合进行此类分析。该模型系统可用于研究、分析和管理纳米材料毒性引起的风险。所获得的信息将有助于在处理纳米技术相关产品时制定具体的指导方针、制定保护措施和质量控制 [118, 119]。
使用斑马鱼胚胎对纳米粒子介导的药物递送的见解
为了使用纳米粒子靶向大脑,对其在体内的影响的先验知识是必不可少的。斑马鱼模型最适合此目的。最近的研究使用纳米粒子进行,以获得对斑马鱼幼虫孵化的重要见解。使用二氧化钛纳米粒子以剂量依赖性方式诱导幼虫早期孵化[120]。陈等人。表明二氧化钛纳米粒子对幼虫游泳行为有影响,影响速度和活动水平[121]。另一方面,Ong 等人。报道了暴露于纳米颗粒后幼虫孵化和胚胎死亡的完全抑制。他们进一步补充说,胚胎死亡的原因是纳米粒子与胚胎的物理相互作用,而不是纳米粒子物理化学特性的影响[122]。当斑马鱼幼虫暴露于 TiO2 纳米颗粒时,也观察到它们的甲状腺内分泌系统被破坏 [123]。铅的积累被认为是造成这种不利影响的原因。据报道,TiO2 纳米颗粒也能显着激活 BDNF、C-fos 和 C-jun 的表达水平。相反,还发现它对 p38、NGF 和 CRE 等基因具有抑制作用,导致斑马鱼的脑损伤 [124]。 TiO2 纳米颗粒也被证明对鱼的繁殖能力有不利影响,导致释放的卵数量减少 9.5% [125]。沃格特等人。进一步报告了在受精后 24-48 小时将小分子 BCI 添加到斑马鱼胚胎时的化学毒性 [126]。阿里和莱格勒等人。即使在低剂量下,也显示出壬基酚纳米颗粒诱导的胚胎畸形[127]。乌森科等人。使用斑马鱼胚胎评估了碳富勒烯 [C60、C70 和 C60(OH)24] 诱导的毒性 [128],而 Daroczi 等人。列举了相同纳米材料对电离辐射的保护潜力 [129]。还通过评估其毒性报告了 C60 富勒烯衍生物树状富勒烯纳米颗粒 (DF-1) 在斑马鱼胚胎中的神经保护作用 [129]。向鱼胚胎施用二氧化硅纳米粒子会导致死亡率增加 [67],而纳米氧化锌会增加死亡率并导致皮肤溃疡和孵化延迟 [82]。 Brun 等人首先报道了水性纳米颗粒暴露对调节免疫系统的基因的影响。 [130]。这项研究强调了分子反应作为生物毒性指标的重要性。斑马鱼胚胎植入癌细胞并接受聚合物体纳米颗粒的实时成像,以了解纳米颗粒的毒性和治疗策略[131]。
有趣的是,使用不同发育阶段的斑马鱼胚胎进行的生物成像揭示了胆酸钠聚集的银纳米粒子的毒性作用 [132, 133]。这项研究非常重要 [134],因为它表明银纳米粒子产生的毒性会影响鱼的鳃和薄片的发育。这种抑制作用主要是由银离子在鳃中的相互作用引起的,它们阻断了 Na + /K + ATPase 的活性 [135, 136]。此外,据报道,Cu 纳米颗粒对鱼鳃的生长也有类似的抑制作用 [76]。在幼虫中使用铜纳米粒子会导致畸形和孵化延迟 [69, 76]。金纳米粒子的应用对幼虫没有毒性作用[69],而银纳米粒子影响发育[137]。由锌、镁、铁、铜和镍制成的纳米颗粒对成虫没有毒性,但在幼虫中观察到孵化延迟 [78, 79, 81, 82, 138]。有机化合物富勒烯的纳米颗粒也被证明在浓度低于 200 毫克/升时对幼虫无毒[139]。此外,还表明,与通常的壳聚糖颗粒相比,壳聚糖纳米颗粒更有效且无毒[68]。
据报道,像二氧化钛这样的金属氧化物纳米粒子会导致斑马鱼幼虫的一些发育畸形 [120],而一些报道称它是完全无毒的 [140, 141]。这里的关键参数是剂量和暴露时间。更高剂量的 TiO2 NPs 证明对幼虫是致命的,因为 NP 在鳃、心脏、肝脏和大脑中积累 [141, 142]。基因毒性效应也是鱼类接触高剂量二氧化钛的结果 [143]。长期暴露于较低浓度 (<4 mg/L) 的 TiO2 NP 会导致较低的毒性和较高的死亡率 [142]。另一个需要考虑的纳米粒子的重要特征是纳米粒子的形状和其表面的蛋白质。 ZnO NPs 的颗粒柱状六方晶体影响斑马鱼细胞周期 [144],而与球形 NPs 相比,叶形且涂有聚合物的 ZnO NPs 显示出更高的生物相容性 [122]。此外,已经表明纳米棒比球体和立方体纳米颗粒毒性更大 [145]。铁纳米颗粒导致幼虫严重畸形 [146] 和成虫发生基因毒性作用 [134],而镍、钴和铝纳米颗粒等金属纳米颗粒被证明是相对惰性的 [82, 147]。
考虑到当今世界塑料造成的日益严重的破坏,皮特等人。显示了它对斑马鱼的影响。他们观察到发育中的斑马鱼对水生生态系统中可用的纳米塑料非常敏感。这些纳米颗粒可以穿透绒毛膜并对它们的生理和行为反应产生严重影响 [148]。这项研究继续阐明塑料对水下世界造成的滋扰,进而影响人类文明。研究表明,具有高表面积/体积比的非常小的纳米粒子非常有能力从环境中吸收污染物。聚苯乙烯纳米塑料珠在化妆品中的使用已经过研究,因为它们的发育毒性和对斑马鱼胚胎的影响 [149]。另一项关于小于 20 nm 的聚苯乙烯纳米塑料的研究表明,它会在胚胎的大脑中积累 [150]。
对成年斑马鱼的纳米粒子研究揭示的见解
已经对纳米粒子对成年斑马鱼的影响进行了相对广泛的研究。它是有关在脊椎动物中使用纳米粒子的宝贵信息来源。 Truong 等人评估了 122 dpf 胚胎因暴露于金纳米粒子而引起的行为异常 [151]。还通过将纳米颗粒给药于斑马鱼来实现向皮肤的药物递送。研究人员已经表明,Ag-BSA 纳米粒子通过内吞作用进入皮肤,在那里它们积聚并导致皮肤异常 [63]。通过纳米颗粒输送药物也已被用于诱导斑马鱼的压力状况,作为药物发现的潜在模型 [152]。一些纳米颗粒已被证明会诱发鱼的哮喘、细胞凋亡和增强的免疫反应,从而使它们有可能用于免疫毒理学研究 [153,154,155,156]。斑马鱼模型已被广泛研究用于药物诱导的心脏毒性 [157, 158]。斑马鱼的心脏表现出一些与人类心脏相似的功能特征,包括药物反应 [159,160,161,162]。斑马鱼心脏在 22 hpf 时首先发育,而整个心血管系统在 48 hpf 时准备就绪 [163]。斑马鱼胚胎已被可视化以研究药物对心率、节律性、收缩性和循环的影响。已经使用斑马鱼进行了几种视觉检测,以帮助详细说明心脏健康。 QT 间期是大多数心脏药物所基于的参数之一。 QT 间期是心脏电周期中 Q 波和 T 波之间的时间间隔。已经使用斑马鱼评估了许多药物对 QT 间期(心室动作电位持续时间)的影响 [164,165,166]。其中一项研究报告称,导致人体 QT 间期延长的药物实际上会导致心动过缓并阻断耳室传导 [160]。斑马鱼肝脏在 48 hpf 时形成并在 72 hpf 时完全发挥作用;该模型系统广泛用于研究基于肝脏的药物递送。该领域的研究表明,斑马鱼对肝毒性的反应与高等脊椎动物相似[167]。斑马鱼已被用于表征细胞色素 P450、CYP3A 和 CYP3A65 的直向同源物 [168, 169]。已进行进一步评估以详细说明药物对 CYP3A4、CYP2D6 和 CYP3A65 的影响 [170]。在斑马鱼创伤性脑损伤模型中研究了橙皮素纳米制剂的神经保护作用[171]。
斑马鱼为神经特异性药物递送提供完整的病理学研究模型
将药物输送到大脑时,可能会发生多种不良反应。斑马鱼模型提供了详细研究这些的优势,因此提供了一种合适的向大脑输送药物的技术[172]。致畸性:通过观察透明斑马鱼胚胎,可以轻松评估任何类型的异常致畸生长或发育 [59]。在畸胎瘤形成过程中可以观察到的关键扰动是眼睛的色素沉着 [67]、死亡率 [65]、心血管系统的变化 [68] 和对孵化的影响 [115]。免疫毒性:研究了斑马鱼对药物或纳米颗粒的免疫反应。这导致中性粒细胞和巨噬细胞的积累 [173]。据报道,金纳米颗粒的使用会破坏炎症免疫反应 [174],而另一方面,银纳米颗粒已被证明会诱导炎症反应 [175]。基因毒性:可以通过实时 PCR [143] 和其他彗星试验 [134] 观察 DNA 水平上发生的变化。最近对碳基 NP 的研究最近引起了越来越多的关注 [176],主要是因为它们的低毒性 [177]。碳纳米粒子在斑马鱼中以各种形式使用,包括富勒烯 [128]、碳纳米粒子、碳纳米管 (CNT) [178]、石墨烯量子点 [179] 和碳量子点(C 点)[180]。自 1985 年发现碳的同素异形体(如富勒烯)以来,它们也被用作 NP。它们已广泛用于药物递送应用 [181, 182]。对斑马鱼的研究表明,富勒烯 NPs 的毒性取决于其表面的电荷。与带负电的富勒烯相比,带正电的富勒烯毒性更大 [128]。研究表明,水溶性富勒烯具有通过充当自由基清除剂来防止细胞死亡的能力 [129, 183]。最近的研究是在斑马鱼中进行的,纳米洋葱是多壳富勒烯结构。它们在斑马鱼幼虫中表现出低毒性和良好的生物相容性 [184]。碳纳米管 (CNT) 具有独特的物理化学特性,因此对研究人员来说,它们是一种有吸引力的药物输送方式 [176, 185, 186]。碳纳米管的效率取决于它们的长度和它们的壁的性质,无论是单壁还是多壁。报告表明,单壁或多壁原始碳纳米管对斑马鱼幼虫的生长和发育影响最小[187]。碳纳米管长度的变化可能会导致分子水平的变化,碳纳米管越长,细胞毒性越大[188]。成年斑马鱼在暴露于多壁碳纳米管时表现出毒性,包括炎症性鳃 [189] 以及碳纳米管在大脑和性腺中的积累 [105、190]。另一种形式的碳基纳米颗粒是量子点 (QD) 和石墨烯量子点 (GQD)。 QDs 的典型特征是直径小于 10 nm [191] 的准球形碳结构,GQDs 的典型特征是小于 30 nm [192, 193]。 QD 的另一个特点包括其独特的光稳定性,使其能够与荧光团结合,从而开辟了一系列生物成像的可能性 [194]。量子点的毒性最小,因为它们主要由惰性碳分子组成 [195]。因此,荧光发光和低毒性的结合使其成为一种非常有吸引力的药物递送工具[195,196,197]。
专注于向大脑输送药物的纳米粒子
有了纳米粒子对斑马鱼生理学作用的背景知识,研究人员现在正尝试使用表 2 的斑马鱼模型通过纳米技术将药物输送到大脑。已经报道了聚合物纳米粒子在其表面与苯基硼酸标签缀合,这有助于使用斑马鱼幼虫检测神经递质多巴胺的荧光[91]。这一发现为多巴胺相关疾病的治疗诊断铺平了道路。然而,最近的一份报告详细说明了金纳米颗粒与受到加标沉积物影响的斑马鱼中的离子金相比的毒性 [64]。他们报告说,纳米颗粒改变了斑马鱼大脑中的神经传递,因为它对乙酰胆碱酯酶活性有影响。在一项有趣的工作中,Sivaji 等人。 [198] 旨在通过功能化聚 N 递送多奈哌齐,这是一种成熟的阿尔茨海默病药物 -异丙基丙烯酰胺纳米凝胶 PNIPAM 纳米凝胶到大脑。他们报告说该凝胶可以克服 BBB,并且还使用斑马鱼模型显示出持续的药物释放。因此,这项研究推动了神经特异性纳米凝胶的开发,用于将药物靶向递送至大脑。同一小组进一步报道了用聚山梨醇酯 80 和聚乙二醇功能化的胶体金纳米颗粒的合成,具有克服血脑屏障用于治疗目的的能力 [199]。在这项研究中,他们合成并验证了一种生物相容性纳米载体,具有穿越血脑屏障并有效递送神经特异性药物的能力。
神经特异性纳米粒子的转化方法:斑马鱼到人类
迄今为止,已经使用多种模式生物来研究人类疾病。 While chimpanzees and monkeys have a high degree of similarity with humans, mice and rats have been used extensively over the past few decades. Research using zebrafish models to study various human diseases is now on the increase [31]. Various state-of-the-art technologies have been analysed and evaluated using the zebrafish model. In this context, nanodiamonds (ND) which refer to a newer class of nanoparticles belonging to the carbon family are being explored in the latest techniques for drug delivery across the BBB [200, 201]. They possess outstanding optical properties, malleability of surface structures and mechanical properties which are pertinent for targeted drug delivery. The zebrafish has proved to be an apt model system to study the fluorescent nanodiamonds (FND) in detail. Chang et al. have studied the photostability and non-toxicity of FNDs by single particle tracking using zebrafish yolk cells [202]. Further, evaluation of ND to facilitate their application as nanolabels has been performed using laser confocal microscopy and real-time fluorescence tagging in zebrafish [203]. Zebrafish model can hence be explored to assess the potential of NDs as nanolabelling systems to deliver neurospecific drugs. The use of zebrafish is validated by its high genetic and systems similarity with that of humans. Regenerative ability of zebrafish is also a very interesting aspect of its physiology which has made it an important model organism to study neurodegenerative diseases. Recent studies have identified pivotal insights into brain drug delivery mechanism using zebrafish models of neurodegenerative diseases. Recent research conducted regarding drug delivery in the brain using the zebrafish model has revealed pivotal insights about the dynamics of this mechanism. The only drawback withholding accelerated research in this arena is the lack of established protocols to validate the studies. However, it is only a matter of time when such protocols are developed through ongoing research in this field. A great deal of scope still exists for further research on the following focus areas.
-
Admixture of nanoparticles along with two or more drugs to provide better holistic treatment
-
Analysis of fullerenes, nano-onions and nanodiamonds in neurodegenerative diseases
-
Understanding the biocompatibility of the newer nanoparticles and their brain-penetrating ability.
All the above-mentioned focus areas can be easily assessed using zebrafish model systems. The zebrafish model, therefore, holds great promise for development and evaluation of novel techniques for targeted drug delivery within the brain for translational analysis (Fig. 2). This could open up exciting new vistas for medical intervention to develop therapeutic strategies to treat neurodegenerative diseases.
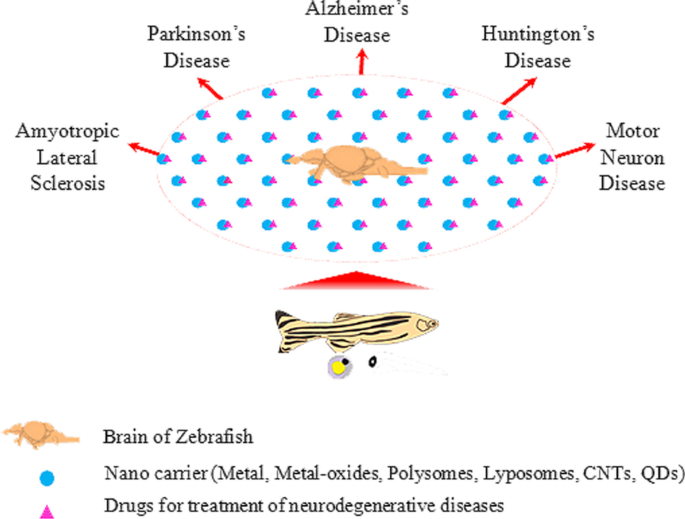
Schematic representation of zebrafish model for delivering drugs encapsulated in nanoparticles to the brain. This method ensures efficient delivery of drugs across the blood–brain barrier (BBB). Several nanoparticles possess the potential to treat a variety of neurodegenerative diseases like Alzheimer’s disease (AD), Parkinson’s disease (PD), Huntington’s disease (HD), amyotrophic lateral sclerosis (ALS) and motor neuron diseases (MND)
Future Research Directions
The last decade witnessed a surge in the use of nanotechnology for brain drug delivery unfolding several exciting new strategies in this arena [16, 17, 204, 205]. However, problems like toxicity, immunogenicity and efficient drug delivery still persist and have restrained the research community from achieving their ultimate goal [206,207,208,209]. Future research prospects for neurospecific drug delivery therefore involve overcoming the existing challenges in this field. Research on nanomaterial toxicity and side effects should be extensive, accurate and always preceed the in vivo implementation of any new nanocarrier formulation. Proper comprehensive analysis of the nano-bio-interactions is absolutely essential for developing strategies for neurospecific drug delivery [210]. Newer imaging techniques should be adopted to broaden the understanding of bio distribution and pharmacokinetics of the delivered drug. Complete knowledge on the bio availability and clearance of the drug is indispensable for achieving the translation from bench side to bed side. Zebrafish, long considered as a “gold standard” for studying several developmental and metabolic diseases, is highly prospective for studies on nanodrug delivery. The transparent embryonic development with the ability to facilitate large-scale drug screening in a vertebrate model among other innumerable key attributes of the zebrafish holds promise for overcoming these roadblocks. The use of this robust model system therefore has immense potential for further research in nanotherapeutics to achieve safe and successful neurospecific drug delivery.
Conclusion
The BBB poses as the main obstacle in delivering drugs to the brain. The physiological function of the BBB is to protect the brain from foreign substances and in doing so it acts as a hurdle even for therapeutic purpose. The current need of the hour is a strategy in drug delivery which is able to overcome the BBB. Only then can effective treatments for brain specific diseases be possible. Recent focus on nanotechnology-based approaches for drug delivery across the BBB seems to have promising prospects for the field of neurospecific drug delivery in the future. Research towards this end is ongoing using a variety of nanoparticles like liposomes, dendrimers, micelles and carbon nanotubes as nanocarriers and nanogels. The zebrafish model is a favourite when it comes to nanotechnology-based toxicity studies and neurospecific drug delivery. Further research on nanotechnology using this model is needed for newer insights which can lead to possible breakthroughs in discovery in neurospecific drug delivery.
数据和材料的可用性
Not applicable.
缩写
- BBB:
-
Blood–brain barrier
- NPs:
-
Nanoparticles
- Au:
-
Gold
- Ag:
-
Silver
- Cu:
-
Copper
- Cd:
-
Cadmium
- CuO:
-
Copper oxide
- MgO:
-
Magnesium oxide
- NiO:
-
Nickel oxide
- ZnO:
-
Zinc oxide
- MPs:
-
Microplastics
- MOFs:
-
Metal organic frameworks
- CNTs:
-
Carbon nanotubes
- TiO2 :
-
Titanium dioxide
- QDs:
-
Quantum dots
- PCR:
-
Polymerase chain reaction
- GQDs:
-
Graphene quantum dots
- PNIPAM:
-
Poly N -isopropyl acrylamide
- NDs:
-
Nanodiamonds
- FND:
-
Fluorescent nanodiamonds
- AD:
-
Disease
- PD:
-
Parkinson’s disease
- HD:
-
Huntington’s disease
- ALS:
-
Amyotrophic lateral sclerosis
- MND:
-
Motor neuron diseases
纳米材料


