PPy 包覆的 MnO2 混合微材料的制备及其作为锂离子电池阳极的改进循环性能
摘要
MnO2@PPy核壳微材料是通过吡咯在MnO2表面的化学聚合制备的。聚吡咯 (PPy) 在 MnO2 表面形成均匀的有机壳。 PPy壳的厚度可以通过吡咯的用量来调整。 SEM、FT-IR、X 射线光电子能谱 (XPS)、热重分析 (TGA) 和 XRD 的分析用于确认 PPy 壳的形成。恒电流电池循环和电化学阻抗谱 (EIS) 用于评估作为锂离子电池负极的电化学性能。结果表明,MnO2@PPy核壳微材料形成后,作为锂离子电池负极的循环性能得到提高。 50 微升 PPy 包覆的 caddice-clew 状 MnO2 具有最佳循环性能,620 mAh g −1 300 次循环后的放电比容量。作为比较,裸 MnO2 材料的放电比容量降至 200 mAh g −1 以下 10 个周期后。 MnO2@PPy 样品的储锂循环稳定性的提高归因于核壳杂化结构,可以缓冲锂离子反复嵌入和脱嵌引起的 MnO2 结构膨胀和收缩,并可以防止 MnO2 粉化。该实验为缓解过渡金属氧化物材料作为(锂离子电池)LIBs负极材料的容量衰减问题提供了有效途径。
背景
由于 3d 过渡金属氧化物(MO;其中 M 是 Fe、Co、Ni 和 Cu)被 Tarascon 等人提议用作锂离子电池的高理论容量负极。 [1],在制备具有各种形态的微/纳米金属氧化物和研究它们作为锂离子电池负极的电化学性能方面做出了许多努力[2,3,4,5,6]。例如,朱的研究小组通过无表面活性剂的溶剂热法制备了单分散的 Fe3O4 和 γ-Fe2O3 微球 [3]。它们具有 1307 和 1453 mAh g −1 的高初始放电容量 , 分别。 110 次循环后,放电容量保持在 450 mAh g -1 对于 Fe3O4 和 697 mAh g −1 γ-Fe2O3。吴红景等。已经通过简单的逐壳自组装水热处理制备了均匀的多壳尤其是五重壳的 NiO 空心球。这项研究的价值为多壳空心结构的合成方法做出了重大贡献。但是 NiO 空心球的储锂性能不是很好 [4]。 MnO2 具有约 1230 mAh g −1 的高理论重量锂存储容量;因此,人们对锂离子电池MnO2负极的设计、合成和应用进行了大量研究[7,8,9,10]。例如,Chen 的研究小组已经制成了具有中空微球形状和纳米立方形状的 γ-MnO2 [11]。 20 次循环后,纳米立方体和微球体的放电容量分别为 656.5 和 602.1 mAh g -1 .此外,从2000年至今,他们对锂离子电池用MnO2材料进行了大量研究[12, 13]。我们还研究了 MnO2 负极在锂离子电池中的应用,但裸 MnO2 材料的放电比容量下降得如此之快,低于 200 mAh g −1 10 次循环后 [14]。
尽管过渡金属氧化物材料具有较大的理论比容量,但包括 MnO2 负极在内的所有这些材料通常都受到容量快速衰减的困扰。循环稳定性差的原因如下:(1)过渡金属氧化物材料的电子电导率通常较低,电子或离子在扩散过程中存在困难,导致电极反应不可逆,容量衰减快。 (2) 在充放电循环后,过渡金属氧化物受到巨大的机械应力并粉化,导致活性颗粒与集电器之间的电接触损失。没有电接触的过渡金属氧化物颗粒不能再参与充放电循环,导致容量衰减[15, 16]。
壳涂层是提高循环稳定性的有效策略。在这种结构中,壳层在一定程度上可以缓冲锂离子反复嵌入和脱嵌引起的金属氧化物材料的结构膨胀和收缩。目前,碳涂层、有机导电聚合物涂层、石墨烯杂化和其他无机化合物涂层已被使用[17, 18]。例如,尹等人。制备聚吡咯(PPy)包覆的CuO纳米复合材料。核壳样品具有760 mAh g -1 的高可逆容量 这比裸露的 CuO 样品要好得多 [19]。李等人。制备了石墨烯包裹的 MnO2 纳米带。可逆比放电容量达到890 mAh g −1 在 0.1 A g −1 180 次循环后。因此,在MnO2材料上制备PPy壳涂层以提高其作为锂离子电池负极的循环稳定性是必要和紧迫的[20]。
在目前的工作中,为了提高作为锂离子电池负极的 MnO2 材料的循环性能,通过化学聚合制备了聚吡咯(一种有机导电聚合物)涂层。结果,在形成MnO2@PPy核壳微材料后,循环性能得到改善。该实验为缓解过渡金属氧化物材料作为(锂离子电池)LIBs负极材料的容量衰减问题提供了有效途径。
方法
样品准备
所有试剂均为分析纯,购自上海化学公司。吡咯在使用前通过减压蒸馏纯化,并储存在 0-5°C 下,并避免暴露在光线下以防止残留聚合。其他试剂无需进一步纯化即可使用。
使用 Yu 等人描述的类似方法制备 MnO2 微材料。 [14, 21] 作为一些修改。为了制备类似 caddice-clew 的 MnO2 微材料,在剧烈搅拌下将 1.70 g MnSO4·H2O 溶解在 15 mL 蒸馏水中。当溶液澄清时,在连续搅拌下将含有 2.72 g K2S2O8 的 20 mL 水溶液加入上述溶液中。然后,将所得透明溶液转移到总体积的 80% 容量的衬有聚四氟乙烯的不锈钢高压釜 (50 mL) 中。将高压釜密封并在 110°C 下保持 6 小时。反应完成后,让高压釜自然冷却至室温。过滤黑色固体沉淀物,用蒸馏水洗涤数次以除去杂质,然后在空气中在 80°C 下干燥 3 小时。收集获得的caddice-clew状MnO2微材料用于制备PPy包覆的MnO2材料。类似方法制备海胆状MnO2微材料;在 35 mL 蒸馏水中加入 1.70 g MnSO4·H2O 和 2.72 g K2S2O8 后,再加入 2 mL H2SO4。
以苯磺酸钠(BSNa)为表面活性剂,FeCl3为氧化剂,通过吡咯在MnO2表面化学聚合制备MnO2@PPy杂化微材料。单体吡咯与BSNa的摩尔比为3:1。首先,将 0.2 g MnO2 分散到一个装有 50 mL 0.01 mol L -1 的烧杯中 BSNa 水溶液并搅拌 0.5 小时。在搅拌下将混合物放入冰/水浴(0-5°C)中。然后,将一定量的吡咯加入混合物中。搅拌0.5小时后,向水溶液中滴加少量FeCl3溶液,开始聚合过程。颜色从浅黑色到深黑色的渐变表明PPy的形成。将混合物在 0-5°C 下搅拌 12 小时以形成 MnO2@PPy 核壳微材料。 PPy 的厚度由吡咯的用量控制。最后,将得到的复合物过滤,用水和乙醇洗涤,然后在 60°C 下真空干燥 4 h。
样本特征
在扫描电子显微镜(QUANTA-200 America FEI Company)上进行SEM图像和能量色散光谱(EDS)的形态研究。产品的晶体结构用 XRD 测定,在 Rigaku D/max-2200/PC 上用 Cu 靶以 7°/min 的扫描速率记录,2θ 范围从 10° 到 70°。用 KBr 码垛的 MnO2@PPy 混合微材料的傅里叶变换红外 (FT-IR) 光谱在 Nicolet IS10 光谱仪上进行。热重分析 (TGA) 还用于确定 MnO2@PPy 杂化微材料在空气中以 10°C/min 从 25°C 到 800°C 的重量损失(MELER/1600H 热重分析仪)。 X 射线光电子能谱 (XPS) 测量记录在 Ulvac-PHI、PHI5000 Versaprobe-II X 射线光电子能谱仪上,使用 Al Kα X 射线作为激发源。 XPS 分析中获得的结合能针对 284.8 eV 的 C1s 峰进行校准。
细胞组装和电化学研究
通过使用 CR2025 硬币型测试电池组装在干燥的充满氩气的手套箱中,测量合成产品的电化学储锂性能。为了制造工作电极,浆液由 60 重量%的活性材料、10 重量%的乙炔黑和 30 重量%的聚偏二氟乙烯 (PVDF) 溶解在 N 中组成 -甲基吡咯烷酮浇铸在铜箔上,在 80°C 下真空干燥 5 小时。锂片用作反电极和参比电极,而 Celgard 2320 膜用作隔板。电解质是 1 M LiPF6 在碳酸亚乙酯 (EC)-1,2-碳酸二甲酯 (DMC) 中的溶液(体积比为 1:1)。恒流充放电实验由兰德电气测试系统 CT2001A(武汉兰德电子有限公司)在 0.2 C 的电流密度下在 0.01 和 3.00 V(相对于 Li/Li + )。在计算 MnO2@PPy 核壳微材料的比容量时,包括了 PPy 的质量。电化学阻抗谱 (EIS) 测量在电化学工作站 (CHI604D, Chenhua, Shanghai) 上进行,频率范围为 0.1 Hz 至 100 KHz,施加的交流信号幅度为 5 mV。
结果与讨论
样本的形态特征
通过SEM测量表征了纯PPy样品、海胆状MnO2样品和不同吡咯聚合量的MnO2@PPy杂化微材料的形貌。如图 1 所示,纯 PPy 样品具有直径约 800 nm 的球体形状,并且倾向于聚集在一起形成层状岩石。海胆状 MnO2 样品如图 1a 所示。 MnO2 微材料是一种直径约 3 μm 的均匀海胆状形状,它由几个均匀长度约 1 μm 的直线和径向生长的纳米棒组成。 MnO2@PPy 杂化微材料的形貌演变如图 1b-e 所示。当吡咯的量较少时,PPy首先成核,然后嵌入MnO2样品的针状纳米棒的间隙中。图 1b 中的针状纳米棒明显比图 1a 中的更宽。当吡咯量增加到 20 μL 时,纳米棒结构仍然存在但不明显。随着吡咯量增加到 30 μL,MnO2 微材料的针状纳米棒结构完全消失,变成球形。当吡咯量进一步增加时(图 1e),PPy 壳变得非常厚。方案 1 说明了 MnO2@PPy 杂化微材料的可能形成过程。在第一阶段,由单体吡咯通过 FeCl3 氧化生成一个微小的 PPy 晶核。然后,晶核沉积在“海胆”表面的刺之间的缝隙中。随着PPy的不断聚合,荆棘之间的空隙逐渐被填满。最后,整个“海胆”都均匀地涂上了PPy。附加文件1中MnO2@PPy杂化微材料的低倍SEM图像证实PPy壳在MnO2@PPy样品上均匀形成。
<图片>
PPy 涂层的海胆状 MnO2 样品的 SEM 图像。左上角是纯 PPy,a 类似海胆的 MnO2 样品,b 10 μL,c 20 μL,d 30 μL 和 e 50 μL 吡咯涂层的海胆状 MnO2 样品。比例尺为 1 μm
<图片>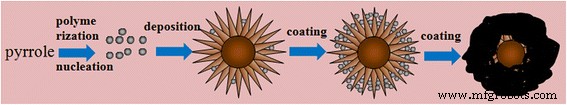
MnO2@PPy材料形成机理示意图
在这项工作中,caddice-clew 状 MnO2 微材料也使用类似的方法由 PPy 包覆。 SEM 形态显示在附加文件 1:支持信息 1. 类似 caddice-clew 的 MnO2 微材料呈纳米线形状并聚集成 2–4 μm 直径的球体,看起来像一个 caddice-clew。当吡咯的量较小时,PPy 首先形成小颗粒并粘附在 MnO2 样品的表面。随着吡咯用量的增加,PPy逐渐完全覆盖了caddice-clew状的MnO2,形成了岩石状的大块状结构。
通过能量色散 X 射线 (EDX) 光谱分析(如表 1 所示)进一步验证了 PPy 的均匀涂层。在纯 MnO2 样品上未检测到碳和氮信号。由于 PPy 壳的形成,在 PPy 和 MnO2@PPy 样品上检测到大量的碳和氮信号。随着吡咯用量的增加,碳和氮的含量也增加。 Caddice-clew-like MnO2@PPy样品的EDX数据见附加文件1:支持信息4。
样品的 FT-IR 分析
通过FT-IR光谱进一步表征合成的PPy和MnO2@PPy样品的结构特征和组成(如图2所示)。对于所有 MnO2@PPy 样品和 PPy 样品,在 1550、1448、1283 和 1130 cm -1 处的谱带 是 PPy 环的特征峰。其中,峰值在 1550 cm -1 是由于 C-C 和 C=C 拉伸,峰值在 1448 cm -1 来自PPy的C-N拉伸。约 1130 cm −1 处的峰值 是由于属于 BSNa 的 S=O 伸缩振动峰,表明磺酸根离子掺杂到吡咯环中。 I1550 和 I1448 的比率通常归因于 PPy 的共轭和掺杂程度 [22]。 I1550/I1448 越高,PPy 的共轭和掺杂程度越高。即如果I1550/I1448高,PPy的导电性应该更好。 1550、917 和 778 cm −1 处的波段 30 μL PPy 包覆的类似海胆的 MnO2 样品比 50 μL PPy 包覆的 Caddice-Cew 状 MnO2 样品弱。因此,PPy 包覆的caddice-clew-like MnO2 样品的电导率应该更好,50 μL PPy 包覆的caddice-clew-like MnO2 样品应该具有更好的储锂性能。 1040 和 778 cm −1 处的波段 是 Cβ-H 吸收带 C-H 变形的面内和面外振动。在光谱中没有观察到 Cα-H 吸收带,这表明吡咯环主要由 PPy 中的 α-α 连接。 1657 cm −1 处的吸收带 是由于产品中存在水分子。因此,FT-IR结果证明在MnO2@PPy样品上形成了PPy壳。
<图片>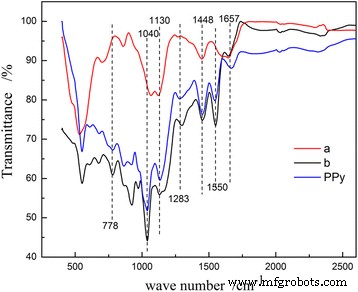
(a) 30 μL PPy 包覆的海胆状 MnO2 样品和 (b) 50 μL PPy 包覆的caddice-clew 状 MnO2 样品和纯 PPy 的 FT-IR 光谱
XPS 结果
通常,核壳结构应通过 TEM 验证。然而,这里的纯 MnO2 样品太厚而无法获得良好的 TEM 图像。因此,为了验证核壳结构,我们进行了 XPS 测试和 EDS 测试,以验证表面和整个样品中的不同成分。为清楚起见,图 3 中仅显示了 30 μL PPy 涂层海胆状 MnO2 样品和 50 μL PPy 涂层 caddice-clew 样 MnO2 样品的光谱。其他在附加文件 1:支持信息 5 中。最终结果列于表 2。O1s、N1s、C1s 和 Mn(2p1/2、2p3/2)的主要结合能 (BE) 分别确定为 531.2、398.9、284.8 和 651.4 和 640.3 eV。 973 和 901.6 以及 848.9 eV 处的峰是 O KLL 峰(来自氧原子的俄歇峰)和 Mn LMM 峰(来自 Mn 原子的俄歇峰)。 XPS 检测到少量 Fe 或 Cl,如图 3 所示。这里,Fe 或 Cl 信号的出现是由于在制备 PPy 壳时使用 FeCl3 作为聚合氧化剂。从表 2 中可以看出,EDS 分析和 XPS 分析的差异是明显的。在XPS分析中,O、N、C的含量要高得多; Mn含量较低。 XPS 的最大分析深度约为 5-10 纳米。强烈的 O、N 和 C 峰证实 MnO2 样品被 PPy 有机薄膜覆盖(如 SEM 段落中所述)。
<图片>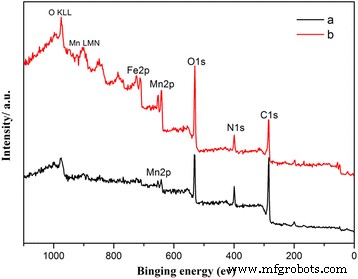
(a) 30 μL PPy 包覆的海胆状 MnO2 样品和 (b) 50 μL PPy 包覆的caddice-clew 状 MnO2 样品的 XPS 光谱
TGA 结果
为了证明合成的 MnO2@PPy 样品上的 PPy 壳,在空气中进行了裸 MnO2 样品、裸 PPy 和 MnO2@PPy 样品的 TGA。图 4 是 TGA 结果。从图 4 中可以看出,裸露的 PPy 粉末显示出两个失重区域。在 60-260°C 的温度范围内,第一次重量损失约 12% 可归因于物理吸附水的解吸和表面吸附溶剂的去除,如先前文献 [19、23、24] 中所述。而在 260-600°C 范围内,第二次重量损失约 88% 归因于 PPy 的氧化。结果,裸露的 PPy 粉末在 600 °C 时会被彻底烧掉。 TGA 测试后,裸海胆状 MnO2 样品和 Caddice-clew 状 MnO2 样品在 800°C 时保持 88.7wt.% 和 91.6%。重量损失最大的是在 60-300°C 的温度范围内,因此可以归因于去除了表面吸收的溶剂,尽管两个样品看起来都非常干燥。对于 30 μL PPy 包覆的海胆状 MnO2 样品,60-260°C 范围内的重量损失为 10%,0-800°C 范围内的整体重量损失为 32.3%。 PPy 氧化前后的重量变化可以直接转化为 MnO2@PPy 样品中 PPy 的量[25]。使用这种方法,30 μL PPy 包覆的海胆状 MnO2 样品中的 PPy 含量约为 22%。该值接近于 PPy 的理论量。对于 50 μL PPy 包覆的 caddice-clew 状 MnO2 样品,在 0-800°C 范围内的整体重量损失为 43.9%,而在 60-260°C 范围内的重量损失为 14%。因此,在 50 μL PPy 包覆的 caddice-clew 状 MnO2 样品中,PPy 的实际含量约为 30%,这与理论值非常接近。因此,结果证实了MnO2颗粒被PPy有机薄膜覆盖。
<图片>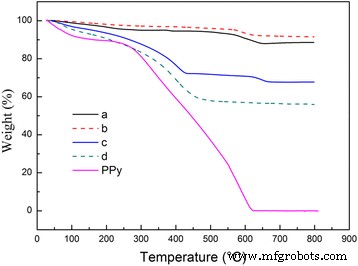
PPy 和 MnO2 样品的 TGA 曲线。 (a ) 类似海胆的 MnO2 样品,(b ) 类似 caddice-clew 的 MnO2 样品,(c ) 30 μL PPy 涂层的海胆状 MnO2 样品,和 (d ) 50 μL PPy 包覆的caddice-clew-like MnO2 样品
样品的 XRD 表征
通过 XRD 检查 MnO2@PPy 样品的晶体结构(图 5)。如图所示,PPy 是一种无定形结构。当被 PPy 包覆时,类似海胆的 MnO2@PPy 样品保留了 α-MnO2 结构。衍射峰出现在 2θ =12.7°、18.1°、28.8°、37.5°、42.1°、49.9°、56.2°和 60.3°,与 (110)、(200)、(310)、 α-MnO2 标准数据的 (211)、(301)、(411)、(600) 和 (521) 晶面(JCPDS 卡 PDF 文件编号 44-0141)。随着PPy量的增加,由于非晶PPy的形成,XRD峰的强度逐渐降低。如PPy包覆的caddice-clew-like MnO2样品所示,75和100uL样品在15°到30°有明显的非晶峰。当被PPy包覆时,类似caddice-clew的MnO2@PPy样品也保留了α-MnO2结构。随着 PPy 用量的增加,材料明显从结晶转变为非晶。这些结果进一步证明PPy有机薄膜已成功包覆在MnO2颗粒上。
<图片>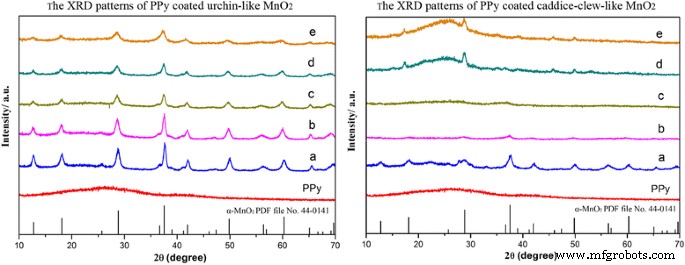
PPy 包覆的 MnO2 样品的 XRD 谱。左边是 (a ) 海胆状 MnO2 样品和 (b ) 10 μL,(c ) 20 μL,(d ) 30 μL,和 (e ) 50 μL PPy 涂层。右边是 (a ) 类似 caddice-clew 的 MnO2 样品和 (b ) 30 μL,(c) 50 μL,(d ) 75 μL(e ) 和 100 μL PPy 涂层
电化学性能
研究了这些 MnO2@PPy 样品作为锂离子电池负极材料的电化学性能。图 6a、b 显示了由裸 MnO2 样品和 MnO2@PPy 样品在 0.2 C 倍率下在 0.01-3.00 V(vs. Li/李 + )。为清楚起见,仅显示了裸露的 MnO2 样品和具有最佳充放电性能的 MnO2@PPy。可以看出,MnO2@PPy 样品的充放电曲线与裸 MnO2 相似,这表明有机 PPy 壳包覆的杂化产品不会改变 MnO2 LIBs 负极的电化学性质。然而,PPy包覆的MnO2样品的储锂性能得到了很大的提高。裸海胆状 MnO2 样品和 PPy 包覆的海胆状 MnO2 样品均具有高初始放电比容量,约为 1200–1400 mAh g -1 ,而理论放电比容量为 1232 mAh g −1 .额外的放电比容量可能是由于 SEI 层的形成 [14]。 10 次循环后,裸海胆状 MnO2 样品的放电比容量降至 200 mAh g −1 以下 .作为对比,PPy 包覆的类似海胆的 MnO2 样品的放电比容量保持在约 500 mAh g -1 即使经过 300 次循环。 caddice-clew-like MnO2 和 PPy 包覆的 caddice-clew-like MnO2 非常相似。 10 次循环后,裸卡迪丝线状 MnO2 的放电比容量降至 200 mAh g −1 以下 . PPy 涂层的caddice-clew-like MnO2 样品保持在500-600 mAh g -1 300 次循环后。
<图片>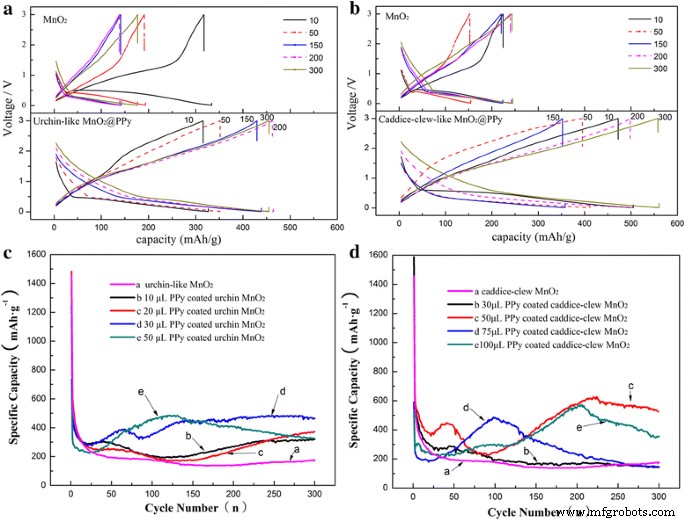
一 , b 30 μL PPy 包覆的 MnO2 样品和 50 μL PPy 包覆的 caddice-clew 状 MnO2 样品的选定循环的充放电曲线。 c , d MnO2样品和PPy包覆的MnO2样品的循环性能
为了评估它们的锂储存循环稳定性,对具有不同吡咯涂层的 MnO2@PPy 样品进行了 300 次循环的放电/充电测量。 PPy的厚度由吡咯的量控制。如图 6c、d 所示,当吡咯的量较小时(例如 30 uL 的类似 caddice-clew 的 MnO2 和 10 uL 的类似海胆的 MnO2),这种混合 MnO2@PPy 样品的锂存储容量改善不明显。这表明 PPy 薄膜太薄,无法防止 MnO2 材料粉化。然而,当吡咯量增加时,杂化 MnO2@PPy 样品的放电比容量显着提高。对于caddice-clew-like MnO2,当吡咯量增加到50 uL时,混合MnO2@PPy样品的放电比容量最大为620 mAh g -1 300 次循环后。对于类似海胆的 MnO2,当使用 30 uL 吡咯时出现最大的放电比容量。第 300 次循环的放电比容量为 480 mAh g −1 .此外,从图 6c、d 可以看出,所有混合 MnO2@PPy 样品都具有改进的循环稳定性。混合 MnO2@PPy 样品改善的锂储存循环稳定性可归因于金属氧化物/导电聚合物核壳混合产品的独特结构。在这种结构中,柔性的PPy壳可以有效地缓冲由于锂离子的反复嵌入和脱离而引起的MnO2的结构膨胀和收缩。此外,PPy 壳可以防止 MnO2 粉化,以及保护 MnO2 材料和集电器(铜箔)之间的电接触损失。而裸 MnO2 的低容量和快速容量衰减可归因于重复充放电过程中由于大的体积膨胀/收缩导致 MnO2 的颗粒间接触或 MnO2 与铜箔集电器的接触粉化和丧失。因此,本次PPy涂层实验为缓解所有过渡金属氧化物材料作为LIBs负极材料的容量衰减问题提供了有效途径。
MnO2@PPy 样品的倍率性能如图 7 所示。为了测试倍率性能,在 0.01-3.0 V 的电压范围内进行充电/放电循环,放电率为 0.2C → 0.5C → 1.0C → 2.0C → 5.0C → 2.0 C → 1.0 C → 0.5C → 0.2C。图 7a 是 5.0 到 0.2 C 阶段的倍率能力。如图所示,所有 MnO2 样品在 5.0 到 0.2 C 阶段的放电比容量与 0.2 到 5 C 阶段的放电比容量非常相似,这证明MnO2 样品具有较高的可逆性。然而,所有 MnO2 样品的放电比容量都低于 1 C 倍率。在低倍率(0.2、0.5 和 1 C)下可以看出混合 MnO2@PPy 样品在倍率性能方面的优势。 5 C 放电后,PPy 包覆的caddice-clew-like MnO2 样品的放电容量为508 mAh g -1 在 0.2 C 时,获得的放电容量要小得多,仅为 160 mAh g −1 在 0.2 C 的裸卡迪斯线状 MnO2 样品中。因此,PPy 涂层的caddice-clew-like MnO2 样品具有改进的倍率性能。 PPy包覆的海胆状MnO2样品的情况非常相似;尽管如此,放电容量略低于PPy包覆的caddice-clew-like MnO2样品。
<图片>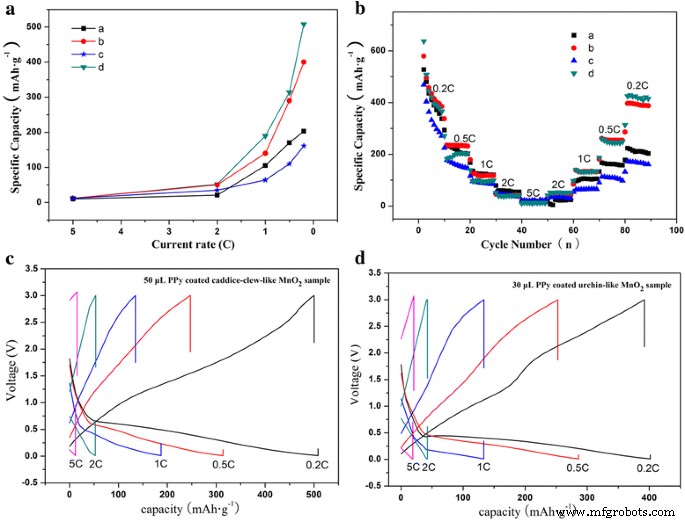
一 速率能力,b 评价性能,以及 c , d MnO2@PPy 样品的充放电曲线。 (a , b ) Urchin 样 MnO2 样品和 30 μL PPy 涂层样品。 (c , d ) Caddice-clew-like MnO2 样品和 50 μL PPy 涂层样品
如倍率性能所示,类海胆的 MnO2 微材料比 Caddice-clew 类 MnO2 微材料具有相对较高的放电比容量,这与之前的报道一致 [14]。然而,在PPy涂层后,类似caddice-clew的MnO2@PPy样品具有更好的储锂循环稳定性。在这里,PPy 的共轭度可能是原因之一。 FT-IR 分析表明,caddice-clew-like MnO2@PPy 样品的 PPy 共轭度较高。因此,caddice-clew-like MnO2@PPy 样品应该具有更好的导电性和更好的电化学性能。为了证实这一点,进行了EIS测试。
图 8 显示了锂电池在开路电压下第五次循环后的 EIS 结果。如图 8a 所示,caddice-clew-like MnO2 的阻抗谱明显由高频到中频区域的两个扁圆半圆和低频区域的一条斜线组成。但是,其他三个样本的两个半圆不容易区分。在 Z 处截取 高频区域的实轴对应于欧姆电解质电阻(R s)。高频中的第一个半圆归因于锂离子迁移阻力(R sf)通过SEI电影。高频到中频的第二个半圆归因于电荷转移电阻(R ct)。低频区的斜线代表 Warburg 阻抗 (W s),这与活性材料中的锂离子扩散有关。 The semicircular parts of both the hybrid MnO2@PPy samples are much smaller than that of the uncoated MnO2 sample. This indicates that the conductivities of the hybrid MnO2@PPy samples are better and the charge transfer resistance of Li ion decreases after PPy coating. The semicircle resistance of caddice-clew-like MnO2@PPy sample is only 77 Ω. The semicircle resistance of urchin-like MnO2@PPy sample is only 95 Ω. Here, after PPy coating, the lower resistance of caddice-clew-like MnO2 micromaterial can explain the better lithium-storage cyclic stability.
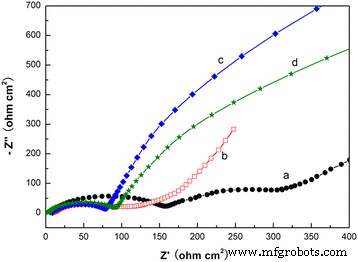
Nyquist plot of Li/MnO2 cells at open-circuit voltage. (a ) caddice-clew-like MnO2 sample. (b ) Urchin-like MnO2 sample. (c ) 50 μL PPy-coated caddice-clew-like MnO2 sample. (d ) 30 μL PPy-coated urchin-like MnO2 sample
Conclusions
In summary, MnO2@PPy core-shell micromaterials are successfully prepared by chemical polymerization of pyrrole on the MnO2 surface. The thickness of the PPy shell can be adjusted by the usage of pyrrole. After formation of MnO2@PPy core-shell micromaterials, the cyclic performances as an anode for lithium-ion batteries are improved. Fifty microliters of PPy-coated caddice-clew-like MnO2 has the best cyclic performances and has 620 mAh g −1 discharge specific capacities after 300 cycles. As a comparison, the discharge specific capacity of bare MnO2 materials falls below 200 mAh g −1 after 10 cycles. The improved lithium-storage cyclic stability of the MnO2@PPy samples can attribute to the core-shell hybrid structure. In this structure, the flexible PPy shell can effectively buffer the structural expansion and contraction of MnO2 caused by the repeated embedding and disengagement of Li ions and can prevent the pulverization of MnO2. Therefore, this experiment of PPy coating provides us an effective way to mitigate the problem of capacity fading of the transition metal oxide materials as anode materials for LIBs.
纳米材料
- 用于改进诊断和治疗应用的多功能金纳米粒子:综述
- LiNi0.8Co0.15Al0.05O2/碳纳米管的机械复合材料具有增强的锂离子电池电化学性能
- 锂离子电池用Cr3+和F-复合掺杂LiNi0.5Mn1.5O4正极材料的合成及电化学性能
- 少层二硫化钼/乙炔黑复合材料作为锂离子电池的高效阳极材料
- 中空结构LiNb3O8光催化剂的制备和光催化性能
- 不同粘合剂对锂离子电池金属氧化物阳极电化学性能的影响
- 通过镁-热还原制备的嵌入式硅/石墨烯复合材料作为锂离子电池的阳极材料
- Co3O4 纳米线的环境友好和简便合成及其与石墨烯在锂离子电池中的有前景的应用
- 通过脉冲激光沉积制备用于锂离子电池的纳米晶 Fe2O3 薄膜阳极
- 分层多孔 Silicalite-1 封装的 Ag NP 的制备及其对 4-硝基苯酚还原的催化性能
- 通过氧向内扩散将污泥 Si 转化为纳米 Si/SiOx 结构作为锂离子电池高性能负极的前驱体
- CuGeO3 纳米线作为高级钠离子电池负极材料的合成和研究


