用于生物医学应用的球形共轭金-鸟蛤壳衍生的碳酸钙纳米颗粒的制造、表征和细胞毒性
摘要
纳米材料在科学中的发展带来了纳米技术、生物医学和工程领域的日益增长。本研究旨在制备和表征用于生物医学应用的共轭金-鸟蛤壳衍生的碳酸钙纳米粒子 (Au-CSCaCO3NPs)。所采用的合成技术使用金纳米颗粒柠檬酸盐还原法和简单的沉淀法,结合可编程辊球磨机的机械使用。使用透射电子显微镜 (TEM)、配备能量色散 X 射线 (EDX) 和傅里叶变换红外光谱 (FTIR) 的场发射扫描电子显微镜 (FESEM) 对合成的共轭纳米材料的物理化学性质进行了表征。然而,细胞机制的复杂性对 Au-CSCaCO3NP 等纳米材料具有挑战性,因此需要进行细胞毒性评估。得到的球形纳米粒子(浅绿色紫红色)的平均粒径为35 ± 16nm,碳氧成分较高。共轭纳米材料还具有独特的文石多晶型和羧酸键光谱,显着支持共轭纳米粒子之间的相互作用。负表面电荷和光谱吸收突出了它们的稳定性。合成的球形共轭Au-CSCaCO3NPs有望成为一种很好的生物医学纳米材料。
背景
单分散纳米粒子的生产在电子、光学、生物医学和磁性应用中具有重要意义 [1,2,3,4]。它们的进化和生物材料的进化已经有利地增强了药物 [5]、生物医学系统 [6]、药物输送系统 [7]、化妆品和水处理 [7,8,9]。同样,生物相容性、生物源性和无毒共轭材料的开发可能对生物科学和生物医学领域做出宝贵贡献 [10]。此外,生物相容性金属共轭生物和纳米材料可以促进生物医学应用的更多科学进步,例如组织工程 [5]、治疗学 [11] 和药物递送 [12]。这在最近的工作中已经得到了详细的展示,例如使用可注射的自组装胶原-金混合水凝胶[13]、胶体金-胶原核-壳纳米偶联物[14],以及用于抗肿瘤治疗的共组装无载体纳米药物[15]。许多研究还证明,金属纳米粒子可以在具有无机非二氧化硅多孔材料的电化学生物传感器中产生酶电极 [16]。此外,合成的氧化石墨烯-白蛋白纳米杂化物也显示出它们对增强光动力疗法的潜在益处[17]。总而言之,这只是激发了人们对其他可能的应用的兴趣,例如生物医学成像和生物传感系统 [16, 18]。
碳酸钙作为一种原始的天然矿物,已被广泛用于生物医学、工业和纳米技术等领域 [10, 19,20,21]。文石作为一种碳酸钙多晶型物,丰富地存在于海扇壳中(Anadara granosa ),一种流行的软体动物,也发现于马来西亚 [22]。与方解石和球霰石的其他碳酸钙多晶型物不同,文石是生物成因的,占海扇壳的 95-98%。碳酸钙是一种文石多晶型物的无机材料,天然且普遍存在于海扇壳中 [23]。文石多晶型物由于其生物相容性特性和在抗癌药物递送系统 [24] 和生物医学成像 [25, 26] 的开发中具有广阔的潜力而越来越受到研究领域的关注。目前,大多数先前的研究主要揭示了碳酸钙的两种生产方法[26]。它们包括在受控环境下通过氢氧化钙对 CO2 气体进行共沉淀或复分解和碳酸化,遗憾的是没有产生生物碳酸钙 [26,27,28]。因此,该产品含有大量方解石和球霰石的混合物,因其非生物相容性和高毒性报告而不适用于生物医学用途[26]。
然而,随着纳米技术在生物医学应用中的应用越来越多,本研究的重点是使用十二烷基二甲基甜菜碱 (BS-12) [29] 合成具有独特尺寸和形状的受控海扇壳衍生碳酸钙纳米粒子 (CSCaCO3NPs)。这是受到先前工作的启发,这些工作利用 BS-12 作为生物矿化催化剂合成 CSCaCO3NPs,可以轻松操作用于生物应用、具有成本效益和相对纯净的纳米粒子 [30]。合成纳米颗粒的形态和尺寸对于确定其理化性质至关重要,鉴于金属纳米颗粒具有巨大的生物医学应用潜力,因此重点关注金属纳米颗粒 [31]。金纳米粒子 (AuNPs) 由于其光学特性、不同的尺寸范围和颜色而被持续使用,这些取决于吸收最大值的变化或所采用的合成方法 [32]。 AuNPs 的大小和形状会影响它们在可见光光谱中的吸收和发射特性,使它们从可见光到近红外区域变化。因此,由于它们的合成 [33]、物理化学特性 [34]、生物相容性 [35] 和表面功能化 [36],它们可以针对不同和特定的应用进行操作 [37]。此外,也有人指出,在医学诊断中,它们并没有被完全使用,它们的价值可能模糊不清[37]。
因此,也许在适当的功能化后,它们可以重新设计用于癌症成像 [38]、癌症治疗 [39]、药物递送 [40] 和感官小工具 [41]。涂层对于制造具有功能化特性的纳米混合生物材料至关重要,例如与多孔碳酸钙纳米球结合的金纳米粒子 (AuNPs) [16, 42]。由此产生的共轭金-碳酸钙纳米材料或纳米复合杂化物,可以保留有利的亲本特性,如生物相容性、良好的溶解性和在溶液中的分散性[16]。表现出强烈颜色变化和局部表面等离子体共振 (LSPR) 的共轭金纳米粒子可能是潜在的多受体系统(如适体、肽和抗体)的优秀候选者 [35, 43,44,45]。水溶性共轭聚合物的制备及其在生物传感器、荧光成像和药物输送中的应用已成功实现[46,47,48]。然而,近年来共轭纳米粒子或纳米材料除了制备更友好[51]和分离特性[48]外,还具有光稳定性[48, 49]和低细胞毒性[50]等优点。
因此,AuNPs 和 CSCaCO3NPs 是可控合成的,用于制造和表征生物共轭金-蚬壳衍生的碳酸钙纳米粒子 (Au-CSCaCO3NPs),其直径大小范围为 19-51 nm。最初,AuNPs 的制备受到经典 Turkevich 方法 [52] 和使用十二烷基二甲基甜菜碱合成方法 [26] 的海扇壳衍生纳米粒子的启发。合成参数(如浓度)的修改可以有效地减少或增加它们的大小。因此,对合成的纳米材料进行了表征和细胞毒性研究。 Au-CSCaCO3NPs 制备的附加优点是;合成简单,成本效益高。
方法/实验
材料和化学试剂
金盐(含 49% 金溶液的四氯金酸)和柠檬酸三钠购自 prima nexus Sdn Bhd(马来西亚)。新鲜海扇壳购自当地市场(Pasar borong, Seri Kembangan, Selangor, Malaysia)。十二烷基二甲基甜菜碱 (BS-12) 和吲哚菁绿染料 (ICG) 购自 Sigma-Aldrich (Steinheim, Germany)。 Dulbecco 改良 Eagle 培养基 (DMEM)、胎牛血清 (FBS)、抗生素组合(谷氨酰胺 100 mmol/L、青霉素 100 U/mL 和链霉素 100 μg/mL)、磷酸盐缓冲盐水 (PBS)、二甲基亚砜 (DMSO) ) 和 MTT(3-二甲基噻唑-2,5-二苯基四唑溴化物染料)购自 Naclai tesque, Inc.,Kyoto,Japan。其他试剂均为分析纯。
金纳米粒子的合成
该合成是使用 Verma 等人先前描述的方法实现的。 [53] 浓度略有变化,1% 四氯金酸含 49% 金溶液。大约 0.1% 的金溶液分别在不同的锥形瓶中制备并稀释为 15、25 和 20 mM 的一系列浓度。然后将溶液在加热板上连同磁力搅拌(6 位,WiseStir ® Korea)在 100°C 下加热。然后,在连续磁力搅拌下将约1%的柠檬酸三钠加入沸腾的溶液中,直到观察到颜色转变(金黄色溶液变成无色然后变成黑色,最后变成亮红色)。 15 分钟后关闭加热并使其在室温下冷却。然后将合成的金纳米粒子储存在 - 4°C 以备进一步使用。反应式如下:
$$ 2{\mathrm{H}\mathrm{AuCl}}_4+3{\mathrm{C}}_6{\mathrm{H}}_8{\mathrm{O}}_7\left(\mathrm{citric} \\mathrm{酸}\right)\to 2\mathrm{Au}+3{\mathrm{C}}_3{\mathrm{H}}_6{\mathrm{O}}_5\left(3-\mathrm {酮戊二酸}\ \mathrm{酸}\right)+8\mathrm{HCl}+3{\mathrm{C}\mathrm{O}}_2 $$鸟蛤壳衍生的碳酸钙纳米颗粒 (CSCaCO3NPs) 的制备和合成
三公斤新鲜获得的海扇贝壳被彻底清洗、擦洗和清洗。扇贝壳粉是根据Islam等人描述的方法生产的。 [54]。将清洁的海扇壳在烘箱(Memmert UM500,GmbH Co,Germany)中在 50°C 下干燥 7 天。使用搅拌机(Blender HCB,550,美国)将海扇壳研磨成粉末,并用孔径为 90 μm 的不锈钢实验室测试筛(Endecott Ltd.,英国伦敦制造)筛分以获得微米级粉末。粉末在烘箱中在 74°C 下干燥 7 天。粉末进一步包装在密封的聚乙烯塑料袋中以备后用。根据Islam等人描述的方法合成了海扇壳衍生的碳酸钙纳米颗粒。 [55],对方法和合成参数略有修改。将2克海扇壳粉放入250毫升锥形瓶中,然后加入50毫升双去离子水,向锥形瓶中加入浓度为0.5毫升的BS-12。使用系统的多加热板和带有小磁棒的磁力搅拌器,将锥形烧瓶中的混合物在 50°C 的温度下以 1000 rpm 剧烈搅拌 135 分钟。使用尺寸为 125 毫米的双环滤纸(Filtres Fioroni,中国)将制备的样品与母液分离。然后彻底洗涤残余物以除去过量的BS-12。最终产品 CSCaCO3NP 粉末装入干洗容器中并在 74°C 下干燥 3 天(Oven Memmert UM500,GmbH Co,Germany)。在容器内加入多个小大理石球后,容器被妥善包裹并用Para膜密封。将容器以 200 rpm 的速度放置在可编程滚球磨机(BML-6,Wisemix ® Korea)上 5 天。样品保存在密封的聚乙烯烘箱中备用。
共轭金-鸟蛤壳衍生的碳酸钙纳米颗粒 (Au-CSCaCO3NPs) 的合成与近红外 (NIR) 染料的协同作用
在此过程中,将 0.2 g CSCaCO3NPs 和 5 mg 近红外 (NIR) 吲哚菁绿染料 (ICG) 分散在 20 ml 金胶体溶液(pH 7)(AuNPs 溶液)中,与 Cai 等人的描述类似。 [16],在一个干净的空锥形瓶中。进行了进一步的合成修改,其中将样品超声处理 20 分钟,然后在带有小磁棒的磁力搅拌器上以 200 rpm 的速度孵育 3 天。将样品以 10,000 rpm 的速度超离心 10 分钟,以获得浅绿色-紫色的 Au-CSCaCO3NP 复合材料。倒出上清液,用一系列去离子水洗涤沉淀。制备的复合材料在烘箱中干燥4天,并在烘箱中储存在密闭的聚乙烯中以备进一步分析。
共轭金-海扇壳衍生的碳酸钙纳米颗粒 (Au-CSCaCO3NPs) 的表征
使用透射电子显微镜(TEM)分析纳米材料的粒径和形貌。将纳米材料分散在无水酒精中并超声处理 40 分钟。将大约 5 μl 的悬浮样品溶液移出到铜握试样架上。在 TEM (Hitachi H-7100) 下观察样品。场发射扫描电子显微镜(FESEM)(JOEL 7600F 型)在 5 KV 的电压下运行并配备能量色散 X 射线光谱仪(EDX)。这用于表征 Au-CSCaCO3NP 的表面特征。将材料分散在无水酒精中并超声处理 1 小时。将大约 50 μl 的悬浮样品溶液移出到铜夹样品架上,干燥过夜,并使用电子束扫描。此外,还利用傅里叶变换红外光谱仪(FTIR)对合成的共轭纳米材料进行了功能分析;纳米材料在 400–4000 cm -1 范围内在 Ker(FTIR 模型 100,Perkin Elmer)中以 1 wt% 进行校准 .此外,使用zetasizer(Nano ZS,Malvern Instruments)对合成的纳米缀合物尺寸和zeta电位进行分析。将材料悬浮在去离子水中并超声处理 50 分钟;将均匀悬浮液置于 zetasizer 比色皿中并检查粒度和 zeta 电位。使用紫外-可见分光光度计 (UV - 2600) 在 300 至 800 nm 的不同波长下监测共轭纳米复合材料中不同分析物的存在。
细胞培养和细胞毒性研究
人乳腺腺癌细胞系(JCRB:MCF-7)和小鼠成纤维细胞系(JCRB:NIH3T3)在补充有 10% FBS 和抗生素组合(谷氨酰胺 100 mmol/L,青霉素 100 U/ mL 和链霉素 100 μg/mL)。培养瓶(Eppendorf culture T-25 和 T-75)在 5% 二氧化碳中 37°C 培养,80-90% 汇合的细胞用于接种和处理过程。
细胞接种和处理
将细胞以5 × 10 3 的密度接种于96孔无菌板中 细胞每孔并孵育 24 小时过夜。去除每个孔中的培养基,将细胞处理并与共轭纳米复合悬浮液 (Au-CSCaCO3NP) 重复共培养 24、48 和 72 小时。处理暴露完成后,将孔内培养基吸出并用PBS洗涤,然后更换为另一种新鲜培养基进行实验处理。
用于治疗的 Au-CSCaCO3NP 的制备
在 10% 无血清 DMEM 培养基中制备浓度为 1 mg/ml 的 Au-CSCaCO3NP 储备溶液。将 MCF-7 细胞和 NIH3T3 细胞接种到 96 孔板中后,用不同浓度的 Au-CSCaCO3NPs 溶液处理培养板,微克(100–1.56)。
(MTT) 3-Dimethylthiazo-2, 5-diphynyltetrazolium Bromide 试剂制备和方案
通常,将 5 毫克 MTT 试剂粉末溶解在 1 毫升 PBS 中,通过超声涡旋促进均匀混合。细胞接种和处理后,清除孔板并向每个孔中加入 20 μl MTT 试剂。紧接着,让平板孵育 3-4 小时,使 MTT 与细胞的线粒体结合。孵育后,将 1 ml DMSO 添加到每个孔中,将有色产物释放到溶液中。将板在暗室中放置 30 分钟,并用微孔板读取器在 570 nm 波长处测量溶液的光密度 (OD) [56]。对每个细胞系一式三份进行实验,并记录平均值。使用以下公式确定细胞活力的百分比。
$$ \mathrm{Percentage}\ \mathrm{of}\ \mathrm{cell}\ \mathrm{viability}=\left(\A\Sample/A\Control\right)\times 100 $$其中 A 样品是两种细胞系和 A 的不同孵育处理细胞的平均 OD 读数 对照是仅在完全培养基中不同孵育细胞的平均 OD 读数。然后从平均三次重复值评估细胞的细胞毒性,并显示为平均值 ± 标准偏差(SD)。
统计分析
使用 SPSS 软件(第 10 版,芝加哥,美国)进行统计数据分析。实验一式三份进行并表示为平均值 ± 标准偏差(M ± SD)。显着性阈值为 p <0.01.
结果与讨论
共轭 Au-CSCaCO3NPs 的理化性质
透射电子显微镜
TEM 显微照片的目的是评估合成的共轭 Au-CSCaCO3 NPs 的尺寸,其显示在 (19-51 nm) 范围内平均直径尺寸为 35 ± 16 nm 的分散良好的纳米粒子。由合成条件引起的尺寸差异如图1所示。
<图片>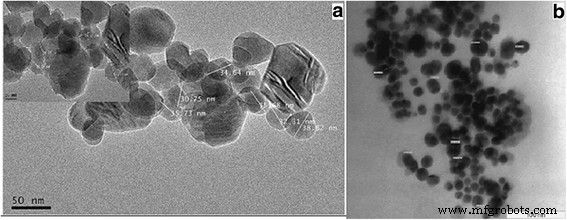
透射电镜 (a , b ) 表征纳米颗粒不同尺寸的 Au-CSCaCO3NPs 的图像
纳米共轭物的 TEM 显微照片显示直径范围为 19-51 nm 和分散的纳米粒子。独特获得的纳米尺寸可归因于所采用的受控合成条件。对纳米颗粒分散性的另一种可能解释可能是由于柠檬酸根离子的带负电荷层有助于纳米颗粒相互排斥,此外,由于静电排斥和共轭水合表面层防止聚集和增加共轭稳定性,如类似报道由 Jazayeri 等人撰写。 [56]。此外,柠檬酸盐封端试剂在合成中发挥作用,如 Rawat 等人报道的那样,这使得纳米颗粒缀合物具有更高的分散性和稳定性。 [57]。独特的粒径表明碳酸钙纳米球基质内吸收了不同的金纳米颗粒,类似于蔡等人所做的工作。 [16],有助于观察到的所得粒度。然而,这一结果也证实了方解石容纳金纳米粒子的能力较差的报道[16]。
场发射扫描电子显微镜 (FESEM) 和能量色散 X 射线光谱 (EDX)
FESEM 显微照片评估了合成纳米粒子的形态和形状,显示球形和链状 Au-CSCaCO3NPs 纳米粒子具有小聚集程度,如图 2 所示。元素光谱(图 2b)分析了元素组成共轭纳米粒子显示出 64.98% 的碳、13.53% 的氧、0.02% 的钙、17.63% 的铜和 3.85% 的金,如表 1 所示。
<图片>
FESEM a 描述形态的 Au-CSCaCO3NPs 的 FESEM 显微照片。 b Au-CSCaCO3NPs的EDX光谱
FESEM 显微照片将独特的形态描述为球形、光滑的表面和链状结构的共轭纳米粒子,其物理或化学性质可以解释为制备条件和合成方法的结果 [58]。类似地,共轭纳米颗粒显示的球形结构性质与 Verma 等人报道的相似。 [53],但与所呈现的小程度聚合相反。造成这种结果的一个可能原因可能是金纳米粒子和海扇壳衍生的碳酸钙纳米粒子之间的疏水和静电相互作用导致强结合 [48]。此外,BS-12 在合成中的作用反映在纳米颗粒分解成球形的过程中,类似于 Islam 等人记录的工作。 [55]。基本概况(表 1)显示没有与预期结果相反的显着变化。同样,如先前工作[26, 54]中所示,观察到的共轭纳米粒子化学成分的发现也被记录在案。
按强度划分的表面电荷和尺寸分布
完成共轭纳米粒子的 zeta 电位,以通过强度评估它们的表面电荷、稳定性和尺寸分布,显示负电荷为 - 16.4 ± 3.81 mV,共轭纳米粒子平均尺寸为 57.97 nm,如图 3 和表 2.
<图片>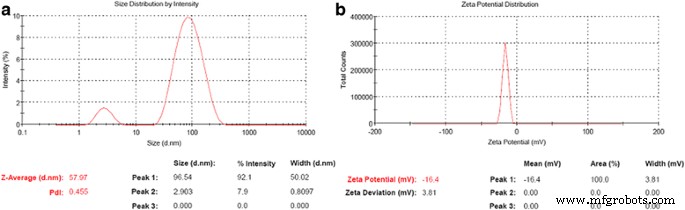
一 Au-CSCaCO3NPs 强度的粒度分布。 b Au-CSCaCO3NPs的Zeta电位显示表面电荷
Zeta 电位是评估使用 zeta sizer 确定的纳米颗粒表面静电荷的重要分析。这进一步解释了纳米材料在溶液中的分散性,使我们能够了解整体稳定性、纳米粒子保质期、带电粒子之间的粒子相互作用及其影响 [59]。共轭纳米材料的 zeta 电位评估表明纳米颗粒在 - 16.4 mV 下具有稳定性,并且多分散指数 (PdI) 小于 0.5。一种可能的解释可以归因于在测量过程中悬浮粒子之间存在更多的电排斥。此外,由于合成方法,团聚趋势也可能影响尺寸分布,导致尺寸变大。 Hoque 等人的先前研究。有类似的记录 [60] 高度正或负的 zeta 电位会减少聚集并增加稳定性。此外,合成的纳米粒子的物理化学差异可以归因于所使用的合成方法。 Kanaujia 及其同事的 [61] 工作还强调,zeta 电位的较高负值或正值表明稳定性并避免粒子聚集,因为电排斥使纳米粒子分散体在电学上稳定,Isa 等人也报道了这一点。 [62].
傅立叶变换红外光谱仪 (FTIR)
Au-CSCaCO3NPs 的 FTIR 光谱显示最突出的峰出现在 1455.09 cm -1 随后是在 1059.12 cm -1 处观察到的峰 , 854.80 cm −1 , 和 464.16 cm −1 , 分别。此外,在 706.40 cm -1 处观察到弱峰 和 1785.68 厘米 −1 如图 4 所示。
<图片>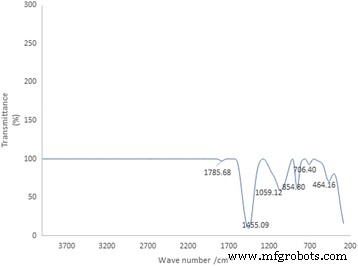
Au-CSCaCO3NPs主要特征峰的傅里叶变换红外光谱图。所有标记对应于文中讨论的频率
Au-CSCaCO3NPs 的 FTIR 光谱显示,最突出的峰出现在 1455.09 cm -1 ,证明存在于金纳米粒子 [14] 和海扇壳纳米粒子的羧基中的氧 - 氢 (O-H) 键,其次是在 1059.12 cm −1 , 854.80 cm −1 , 和 706.40 cm −1 ,已知它们报告了与光谱峰一致的海扇壳衍生纳米颗粒中出现的烷基 [55]。同样,在 1785.68 cm -1 处观察到弱峰 由于羧基的存在 [54],并且在 464.16 cm -1 处观察到一个额外的峰 .所有峰都显示出存在共价键、碳-碳 (C-C)、碳-氧 (C-O) 和碳-氮 (C-N) 键的显着特征,其适当的官能团存在于我们的共轭结构中。纳米粒子。 FTIR 通过获得共轭纳米材料的红外光谱峰并同时在宽光谱范围 (400–4000 cm -1 ) [63]。然而,据报道碳酸钙的方解石多晶型物在 2000 至 2900 cm -1 范围内具有峰 碳化法制备纳米颗粒[64]。
紫外可见分光光度计
合成的共轭纳米粒子在 530 nm 处显示出重吸收峰,如图 5 所示。
<图片>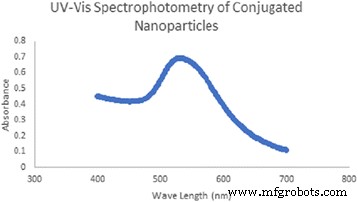
文中讨论的Au-CSCaCO3NPs的紫外可见分光光度计吸收光谱
由于 AuNP 的局部表面等离子体共振效应,金纳米结构具有较宽的光吸收率 [65, 66]。许多报告表明,金颗粒通常在 500-520 nm 之间观察到一个尖锐的吸收峰 [66,67,68,69]。该技术允许进一步评估共轭 Au-CSCaCO3NPs 的大小、浓度和聚集水平 [65]。已知吸收带向更小的波长移动,表明粒径减小,吸收光谱的对称形状表明粒径分布较窄 [70],从而证实了我们的共轭 Au-CSCaCO3NPs 显示出更宽的吸收峰在 500-550 nm 和 530 nm 波长处的最高点之间。在近红外可见光谱区域是可以接受的,在该区域光很容易被组织衰减,吸收峰显着转移到更长的波长 [71]。对此的可能解释可能是由于纳米材料的合成和结合。也与 Srinath 等人一致,他们揭示了吸收带的位置主要取决于颜色变化、聚集和表面吸附物质 [72]。此外,由于金等离子体共振特性,纳米粒子的吸收光谱可能会根据颜色、形态和尺寸发生变化 [73]。具有近红外光热特性的纳米结构具有较强的光散射能力,在生物医学成像中具有重要应用[74, 75]。
细胞毒性研究
MTT(3-Dimethylthiazo-2, 5-diphynyltetrazolium Bromide)
对人乳腺癌细胞 (MCF-7) 和小鼠胚胎成纤维细胞 (NIH3T3) 的细胞毒性研究表明,在 100 μg 剂量下,Au-CSCaCO3NPs 抑制了超过 70% 的细胞增殖,导致癌细胞死亡,并抑制了近 40% 的成纤维细胞。 IC50 和较低浓度的剂量(例如 25 μg)也证明对癌细胞具有毒性,这表明纳米颗粒的细胞活力低,并且还抑制了癌细胞超过 50% 的细胞增殖。另一方面,成纤维细胞的相同浓度剂量显示成纤维细胞的细胞活力增加且一致。 IC50 显示成纤维细胞的细胞活力高达 80%,如图 6 所示。
<图片>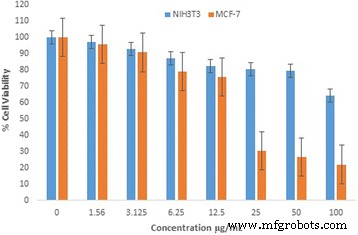
使用MTT法对MCF-7和NIH3T3处理的Au-CSCaCO3NPs细胞进行细胞毒性评估,得出细胞活力百分比
3-Dimethylthiazo-2,5-diphynyltetrazolium Bromide (MTT) 是一种可用于确定细胞活力的比色法 [76]。利用电子传递链中的线粒体酶 [77],代谢活跃的活细胞将 MTT 转化为细胞质中的紫色甲胂晶体 [78]。与死细胞不同,由于无法进行反应的细胞毒性,在添加与活细胞数量成正比的有机溶剂二甲基亚砜 (DMSO) 后,晶体溶解后 [79]。 The conjugated nanoparticles displayed consistent cell death against the cancer cells and reliable cell viability of the fibroblast cells with concentration doses ranging from 25–100 μg. Furthermore, attesting low cytotoxicity and highlighting the biocompatibility of Au-CSCaCO3NPs and potential usefulness for biomedical applications, the cytotoxicity could be due to the internalization of the nanoparticles which possibly triggered intracellular responses and thus induced cellular damage because of interaction with cell organelles. Despite contrary cytotoxicity findings with works done on HeLa cells (human cervical cancer cell line) due to nanoparticles inducing oxidative damage [35, 80], Zhang et al. demonstrated the biocompatibility of the nanoparticles and its likely use for drug delivery systems [80]. Similarly, reports of gold nanoparticles confirmed nontoxic dependent on their size [81] and concentration [39]. Studies strongly confirmed that biogenic gold conjugates are stable and nontoxic nanocarrier used in biomedical application [35, 39] suggesting use for biomedical applications such as drug delivery and cancer therapy [82].
结论
Spherical-shaped conjugated gold-cockle shell-derived calcium carbonate nanoparticles (Au-CSCaCO3NPs) were obtained. The conjugated nanoparticles were synthesized using a simpler, environmental friendly, and cost-efficient synthetic approach. Furthermore, based on the results, the obtained conjugated nanoparticles were relatively pure and stable. The source of material used for the cockle shell-derived nanoparticles is biogenic, readily available, and naturally occurring as seawater mollusca cockle shell. Based on the presented evidences, the conjugated Au-CSCaCO3NPs could be a good biomaterial for biomedical applications.
缩写
- Au-CSCaCO3NPs :
-
Synthesized Conjugated Gold-Cockle Shell Derived Calcium Carbonate Nanoparticles
- AuNPs:
-
金纳米粒子
- BS-12:
-
Dodecyl dimethyl betaine
- C–C:
-
Carbon-carbon bond
- C–N:
-
Carbon-nitrogen bond
- C–O :
-
Carbon-oxygen bond
- DMEM:
-
Dulbecco’s modified Eagle’s medium
- DMSO:
-
Dimethyl sulfoxide
- EDX:
-
Energy dispersive X-ray
- FBS:
-
Fetal bovine serum
- FESEM:
-
Field emission scanning electron microscope
- FRGS:
-
Fundamental Research Grant Scheme
- FTIR:
-
傅里叶变换红外光谱
- HeLa cells:
-
Human cervical cancer cell line
- IC50:
-
50% inhibition concentration
- ICG:
-
Indocyanine green dye
- JCRB:
-
Japanese Collection Research Bioresource
- LSPR:
-
局域表面等离子体共振
- MCF-7:
-
Human breast adenocarcinoma cell line
- MTT:
-
3-Dimethylthiazo-2, 5-diphynyltetrazolium Bromide Dye
- NIH-3T3:
-
Mouse embryonic fibroblast cell line
- 近红外:
-
近红外
- O–H:
-
Oxygen-hydrogen bond
- OD:
-
Optical density
- PBS:
-
Phosphate-buffered saline
- TEM:
-
透射电子显微镜
纳米材料
- 3D 打印的下一步发展——生物医学应用
- 碳酸钙的总体应用
- 碳酸钙母粒的应用。用于制造填充母料的碳酸钙
- 用于改进诊断和治疗应用的多功能金纳米粒子:综述
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 用于合成和生物医学应用的荧光纳米材料的进展和挑战
- 用于超级电容器应用的石墨烯和聚合物复合材料:综述
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- Au@TiO2 蛋黄-壳纳米结构的制备及其在亚甲基蓝降解和检测中的应用
- 银纳米结构的合成方法和应用的最新进展
- 通过多元醇介导工艺制备和表征 ZnO 纳米夹
- 用 Au 纳米粒子定制的二氧化硅硅藻壳可以对用于生物、安全和环境应用的分子进行灵敏分析


