基于二硫化钼纳米复合材料的无酶葡萄糖生物传感器
摘要
医疗保健领域非常需要高性能葡萄糖生物传感器。为了满足这些需求,葡萄糖生物传感器,特别是无酶葡萄糖生物传感器,受到了广泛关注。二维材料,例如石墨烯,具有高表面积、优异的电性能和良好的生物相容性,是过去十年生物传感器研究的主要焦点。本综述介绍了基于二硫化钼纳米复合材料的无酶葡萄糖生物传感器的最新进展。介绍了两种不同的葡萄糖检测技术,重点是电化学葡萄糖生物传感器。还讨论了二硫化钼纳米复合葡萄糖生物传感器面临的挑战和未来前景。
介绍
人体血液中的葡萄糖浓度是一项重要的健康指标。例如,健康人的血糖水平通常在 3.9–6.1 mM(1 mM =∼ 18 mg/dL)左右,超出此范围的葡萄糖浓度可能表明存在肾功能障碍、糖尿病等 [1]。在医疗保健需求不断增长的推动下,基于葡萄糖氧化酶 (GOx ) 自从 Updike 和 Hicks 在 1967 年报道了酶电极 [2]。尽管酶促葡萄糖生物传感器具有简单、高效、高灵敏度和选择性,但仍然无法令人满意地解决两个主要挑战,即高成本和不稳定性。这是因为酶促葡萄糖传感器使用酶,例如 GOx 间接检测葡萄糖,这通常涉及昂贵的催化剂和复杂的设备结构,因此成本相对较高 [3, 4]。此外,像 GOx 这样的酶 由于其固有的热和化学不稳定性,它们容易受到温度、湿度、pH 值和非生理化学物质的影响 [5, 6]。 GOx 的固定 在电极表面上,通常给制造具有良好稳定性和重现性的酶促葡萄糖传感器增加了另一层难度[7, 8]。
随着物联网的发展,低成本、高可靠性的传感器越来越受到人们的关注。在追求满足这些需求的葡萄糖传感器的过程中,无酶电化学生物传感器因其简单、高灵敏度和稳定性等诸多优点而广受欢迎[9,10,11,12]。无酶电化学生物传感器通过电催化氧化直接检测葡萄糖,避免使用昂贵的酶,并提高了环境条件下的稳定性。预计此类生物传感器将为与便携式设备和实时葡萄糖检测结合提供新的机会 [13]。实现实用的无酶葡萄糖传感器的关键是廉价、可靠、生物相容性和丰富的催化剂。为此,纳米复合材料,例如二维材料和纳米颗粒的复合材料,已被广泛用作生物传感器电极材料 [14]。特别是基于二维 (2D) 材料的生物电子学由于二维材料具有许多独特的物理和化学性质,包括大的比表面积、优异的导电性和易于合成,成为一个令人兴奋的跨学科新领域。例如,二维材料的大比表面积可以通过杂化轻松实现表面功能化。高电导率允许在二维材料中进行有效的电荷转移和收集。在各种二维材料中,石墨烯及其衍生物无疑是生物传感器中研究最多的材料[15]。另一种在电子和光电子领域被广泛探索的二维材料也显示出作为生物电子材料的优点。过渡金属二硫属化物 (TMD),尤其是二硫化钼 (MoS2),具有类似的比表面积大、化学惰性和表面功能性等优点。鉴于其独特的原子结构,可以很容易地将外来离子或分子插入到 TMD 纳米片中 [16]。使 MoS2 从其他二维材料中脱颖而出的一个重要特性是其高催化活性来自暴露的边缘 [13]。但是,MoS2 的劣势也相当明显。与石墨烯相比,二维二硫化钼片的电导率要低得多。 MoS2纳米片的重新堆叠进一步限制了电荷转移以及活性反应位点。
直到最近几年,才在基于 2D MoS2 的无酶葡萄糖传感器方面做出了有限的努力。通过使用许多成功解决低本征电导率的方法,已经很好地解决了基于 MoS2 的电化学装置性能不佳的问题。已经报道了一些基于 MoS2 的电化学葡萄糖生物传感器的性能超过其石墨烯对应物 [17]。除了电化学生物传感器外,最近还研究了二维 MoS2 的低成本非电化学方法,利用 MoS2 在电子和光电子学中取得的进展 [18]。在这篇综述中,我们总结了基于二硫化钼的葡萄糖生物传感器的最新进展。特别关注基于 MoS2 的电化学葡萄糖生物传感器,其在“基于电化学葡萄糖生物传感器的 MoS2 纳米复合材料”部分中有所描述。在“使用MoS2场效应晶体管进行高灵敏度葡萄糖检测”部分,简要介绍了用于葡萄糖检测的MoS2场效应晶体管。最后,提出了二硫化钼纳米复合葡萄糖生物传感器的研究结论和未来展望。
基于电化学葡萄糖生物传感器的二硫化钼纳米复合材料
几十年来,金属或合金一直是葡萄糖直接电催化氧化的主要催化剂选择 [19]。在过去的十年中,具有大表面积以及独特的化学和物理性质的二维材料为包括电化学传感、能量存储和电子学在内的许多领域开辟了新的机遇 [20]。在电化学生物传感方面,不同二维材料和催化剂的纳米复合材料显示出明显优于传统催化剂的优势。这些材料之间的协同耦合,即协同效应,可以显着提高催化活性 [21]。大量此类纳米复合材料,特别是那些基于石墨烯或石墨烯衍生物的纳米复合材料,已被开发并应用于无酶葡萄糖传感器。预计层状 MoS2 具有类似的优势,因为它具有石墨烯的材料特性。特别是层状MoS2纳米片具有大量的边缘,类似于功能化石墨烯片,作为催化反应的活性位点[22, 23]。
事实上,黄等人。通过水热法合成二硫化钼纳米花 [24]。用二硫化钼纳米花和壳聚糖/金纳米颗粒复合材料修饰的玻碳电极对双酚 A 氧化显示出明显的过电位降低。纳米复合传感器显示出双酚 A 的有效电催化氧化,循环伏安图中电流显着增加就证明了这一点。双酚 A 传感获得了 0.05 到 100 μM 的良好线性检测范围。此外,估计检测限为 5 nM。这项工作清楚地证明了 Au/MoS2 纳米复合材料优异的电催化活性和协同效应。同样,基于二硫化钼的纳米复合材料已用于无酶葡萄糖检测。使用十六烷基三甲基溴化铵 (CTAB) 作为表面活性剂,通过水热法合成了具有大表面积的二硫化钼花 [25]。微花的形态可以通过反应溶液的pH值、CTAB表面活性剂的浓度和退火温度来控制。在 500 °C 的退火温度下获得的 MoS2 微花显示出良好的结晶质量,因此改善了电荷转移。有趣的是,电化学无酶葡萄糖传感测试表明,没有任何功能化的 MoS2 微花电极可以提供 570.71 μA mM -1 的高灵敏度 cm −2 .此外,该传感器具有高达 30 mM 的宽线性检测范围。
掺杂或杂化外来金属(如 Cu、Ni、Co 和 Fe)的 MoS2 催化剂的协同效应也适用于增强的葡萄糖电化学催化。黄等人。设法结合了铜对葡萄糖氧化的强电催化活性和二硫化钼纳米片的大表面积和活性边缘位点的优点[26]。 Cu纳米颗粒装饰的MoS2纳米片显示出对葡萄糖氧化的电催化活性。 1055 μA mM −2 的高灵敏度 cm −2 据报道,Cu/MoS2 纳米复合葡萄糖传感器的线性检测范围高达 4 mM。灵敏度几乎是从 MoS2 微花电极测量的值的两倍。该传感器在检测葡萄糖对抗尿酸、抗坏血酸和多巴胺方面也表现出良好的选择性。这些化学物质引起的干扰电流仅为葡萄糖的2.1-5.2%左右,如此低的干扰电流水平在生理浓度下可以忽略不计。
另一个有吸引力的候选者是镍 (Ni),它已被广泛研究用于 Ni/石墨烯杂化物。与铜相似,镍也是地球上含量丰富的金属。 Ni 3+ 的氧化还原对 /Ni 2+ 在碱性介质中提供令人印象深刻的催化活性。因此,黄等人。使用二硫化钼纳米片作为催化剂载体来固定镍纳米颗粒 [27]。 MoS2 纳米片是由 MoS2 粉末在乙醇/水混合溶剂中通过液体剥离合成的。在加入 NiCl2·6H2O 前驱体和 N2H4·H2O 和 NaOH 溶液后,通过在 60 °C 下加热 MoS2 纳米片-乙二醇溶液 1 小时,在 MoS2 纳米片上还原 Ni 纳米颗粒。通过在玻璃碳电极上沉积 Ni-MoS2 杂化物制备葡萄糖传感器电极。 Ni/MoS2 混合修饰电极的循环伏安图清楚地显示葡萄糖氧化作用比 Ni 修饰参比电极更高。电催化活性的提高归因于二硫化钼纳米片上更多的活性位点以及二维材料载体上镍纳米颗粒聚集的减少。电流分析结果证实了良好的线性检测范围,高达4 mM,灵敏度高达1824 μA mM -1 cm −2 ,以及 0.31 μM 的低检测限,信噪比为 3 (S/N =3)。与 Cu/MoS2 纳米复合葡萄糖传感器相比,使用 Ni/MoS2 纳米复合材料进一步提高了灵敏度。干扰物质(包括多巴胺、抗坏血酸和尿酸)对葡萄糖感应的影响也被发现是微不足道的。更重要的是,该传感器表现出良好的重现性和高稳定性。在环境储存 4 周后测得的传感器响应降低了 3.4%,可以忽略不计。此外,安德森等人。通过将胶体银纳米颗粒与 MoS2 结合,报道了一种高度灵敏的非酶葡萄糖生物传感器 [28]。 Ag 纳米粒子的引入是为了解决 MoS2 固有的导电性差的问题。 9044.6 μA mM −1 的出色灵敏度 cm −2 据报道,低检测限为 0.03 μM。但线性检测范围仅为1 mM。
通过与石墨烯杂交,可以进一步提高 MoS2 的电催化活性。 MoS2 的低固有电导率破坏了其高催化活性。在电化学反应或一般电子应用中,MoS2 纳米材料之间的电荷转移很慢。另一方面,石墨烯具有优异的导电性,可以作为减缓 MoS2 纳米材料中电子传输的直接解决方案 [29]。郑等人。通过一锅水热法制备三维 (3D) MoS2/石墨烯气凝胶纳米复合材料 [13]。尽管与 2D 参考样品相比,通过使用 3D 多孔结构已经观察到增强的电催化活性,但葡萄糖氧化酶的使用使制造复杂化并且面临与酶传感器相同的问题。耿等人。通过一种简便且可扩展的方法合成了装饰在还原氧化石墨烯(Ni-MoS2/rGO)上的 Ni 掺杂的 MoS2 纳米粒子 [30]。如图 1a 所示,通过 Hummers 和 Offeman 方法合成的氧化石墨烯与 CH3COOH 和去离子水混合。 Ni-Mo前驱体溶液是通过将不同摩尔比的(NH4)2MoS4和Ni(CH3COO)2·4H2O加入到氧化石墨烯溶液中制备的。 Ni-MoS2/rGO 悬浮液在 80 °C 下离心和干燥后获得。然后将收集的 Ni-MoS2/rGO 悬浮液在 N2 气氛中在 600 °C 下煅烧 4 小时。获得的 Ni-MoS2/rGO 纳米复合材料用于非酶葡萄糖传感。图 1b 显示了由 Ni-MoS2/rGO 纳米复合材料修饰的传感器电极对连续添加葡萄糖溶液的电流响应。每次加入葡萄糖后都观察到电流明显增加。此外,图 1b 中的插图显示传感器能够响应低至 5 μM 的葡萄糖浓度。作为葡萄糖浓度函数的精确电流信号绘制在图 1c 中,它清楚地显示了传感器的广泛线性检测范围,0.005-8.2 mM,很好地覆盖了典型的人类血糖水平。计算的灵敏度和检测限为256.6 μA mM −1 cm −2 和 2.7 μM (S/N =3),分别。尽管传感器的灵敏度和检测限明显低于早期的传感器,但线性检测范围得到了很好的提高。该工作进一步报告了电子传输速率和电催化活性的提高,扩散系数为 1.83 × 10 -3 厘米 2 s −1 催化速率常数为 6.26 × 10 5 厘米 3 mol −1 s −1 通过使用 Ni-MoS2/rGO 复合材料。如图1d所示,当传感器在干燥条件下储存时,其对1 mM葡萄糖的电流响应在15 天内几乎保持不变,显示出良好的稳定性。还研究了常见干扰化学品 NaCl、多巴胺、尿酸、抗坏血酸和 VB 的影响。结果如图 1e 所示,这些化学品对信号电流的影响很小。 0.1 mM NaCl、多巴胺、尿酸、抗坏血酸和VB(正常血清中干扰化学物质的典型浓度)引起的电流变化仅为0.76%、2.77%、6.03%、0%、2.51%和2.5 mM 葡萄糖的电流响应的 0.63%。最后,该工作证明了 Ni-MoS2/rGO 传感器测量的浓度与报告的医院值之间的良好匹配,显示了该传感器在实际应用中的巨大潜力[30]。
<图片>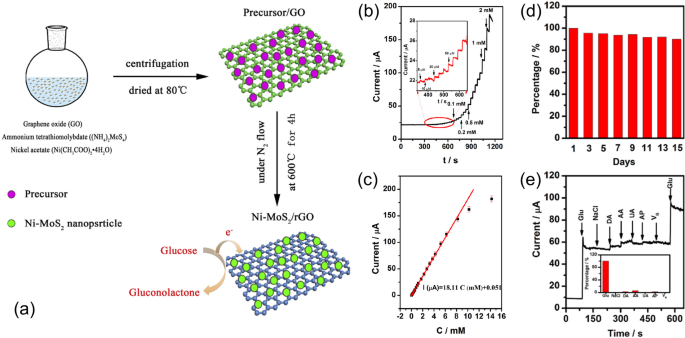
一 Ni-MoS2/rGO 复合材料的合成示意图。 b Ni-MoS2/rGO 传感器对连续添加葡萄糖的电流响应。 c 提取的对不同葡萄糖浓度的响应电流。 d 通过安培测量对传感器进行 15 天的稳定性测试。 e 2.5 mM 葡萄糖和 0.1 mM 干扰化学品的电流响应比较。转载自 [25],版权所有 2017,经 Elsevier 许可
改善 MoS2 纳米复合材料中电荷转移的另一种方法是与另一种高导电性和生物相容性碳材料碳纳米管 (CNT) 杂交。同时,这种方式可以很好地限制二硫化钼纳米材料的重新堆积,从而提供更多的活性反应位点。碳纳米管也被广泛地合成为 3D 结构,并应用于能量存储、能量收集、传感等 [31,32,33]。李等人。制备了 MoS2 纳米片与氧化钴纳米颗粒和 CNT 杂化的 3D 纳米复合材料 [34]。氧化钴纳米颗粒用于提高电催化活性,碳纳米管用于提高电导率。用于合成 Co-MoS2/CNT 纳米复合材料的一锅水热法如图 2a 所示。将 CNT、0.1 mmol Co(CH3COO)2·4H2O、1.35 mmol Na2MoO4 和 7.5 mmol l-半胱氨酸的混合物转移到衬有聚四氟乙烯的不锈钢高压釜中,并在 180 °C 下保持 24 小时。然后将产物冷却、离心并用去离子水和无水乙醇冲洗。清洁后的 Co-MoS2/CNT 纳米复合材料最终在真空烘箱中在 60 °C 下干燥 6 小时。 Co-MoS2/CNT 纳米复合材料的扫描电子显微镜(SEM)和透射电子显微镜(TEM)图像如图 2b、c 所示。观察到直径约为 20 nm 的典型 3D 成束 CNT。 TEM 图像清楚地显示了附着在 MoS2 纳米片上的中空 CNT。这种结构可作为高导电性基质来支撑 MoS2 纳米片并固定 Co 纳米颗粒。这种密集堆积的 Co-MoS2/CNT 纳米复合材料不仅提供了大量的催化活性边缘,而且还允许在反应过程中进行有效的电荷转移。更重要的是,密集堆积的 Co-MoS2/CNT 结构和相当大的 MoS2 层间距为 0.65 nm(大于 CNT 的 0.34 nm)有效地抑制了 MoS2/CNT 复合材料的重新堆叠。进行了典型的循环伏安法和电流法测量,以检查由 Co-MoS2/CNT 纳米复合材料制成的无酶传感器的性能。在连续添加葡萄糖的情况下测量的 Co-MoS2/CNT 传感电极的电流响应(在 0.65 V 对 Ag/AgCl 下)如图 2d 所示。观察到对葡萄糖添加的响应电流有明显的阶跃增加。实现了良好的线性检测范围,最高可达 5.2 mM,如图 3 和图 5 所示。 2e。计算出的灵敏度为 131.69 μA mM −1 cm −2 .尽管灵敏度相对较低,但从图 2f 中获得了 80 nM 的极低检测限(S/N =3)。
<图片>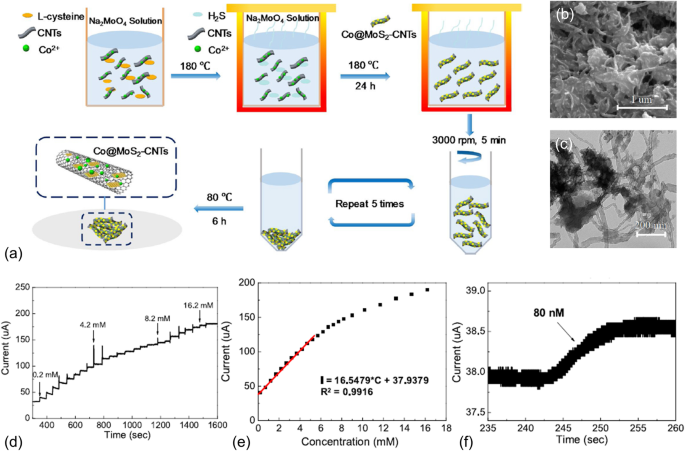
一 Co-MoS2/CNTs 的水热组装示意图。 b SEM 和 c 合成的 Co-MoS2/CNTs 的 TEM 图像。 d Co-MoS2/CNT 传感器对连续添加葡萄糖的电流响应。 e 提取的对不同葡萄糖浓度的响应电流。 f Co-MoS2/CNT 传感器对 80 nM 葡萄糖的电流曲线。转载自 [29],版权所有 2019,经爱思唯尔许可
与金属-2D 材料杂化所显示的协同效应类似,双金属合金和纳米结构也显示出改进的催化性能,并在许多应用中显示出良好的潜力,包括传感 [35]、能量收集 [36, 37] 等。 Li 等人.最近合成了用于非酶促过氧化氢和葡萄糖传感的 Au-Pd 双金属纳米粒子 [5]。 Au-Pd/MoS2 传感器电极的制造如图 3a 所示。 MoS2 纳米片是通过液体剥离制备的。 Au-Pd双金属纳米颗粒通过化学还原合成。然后将制备的 Au-Pd/MoS2 纳米复合材料沉积在玻璃碳电极上用于化学传感。如图 3b 所示,在连续添加葡萄糖的情况下观察到良好的电流步骤。测量为 0.5-20 mM 的线性检测范围远远超出正常人的血糖水平(图 3c)。 Ma 等人没有使用通常由昂贵金属制成的传统双金属纳米粒子。设计了一种金纳米颗粒-聚吡咯 (PPY) 共装饰的二硫化钼纳米复合材料 [38]。金属/导电聚合物混合物也有望提高传感器电极的表面积和电导率。此外,导电聚合物的使用可以进一步降低电化学传感器的成本。制造的 MoS2-PPY-Au/玻碳电极显示出令人难以置信的 0.08 nM 低检测率、几乎无干扰的选择性和超过 3 周的长期稳定性。然而,传感器灵敏度仅为37.35 μA·μM –1 ·cm –2 并且检测范围相当有限(0.1-80 nM)。
<图片>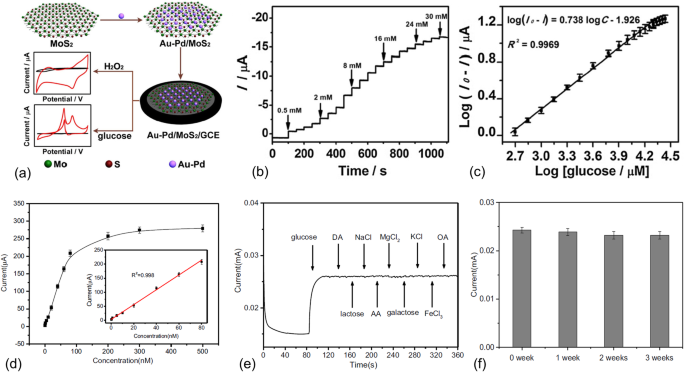
一 图解 Au-Pd/MoS2 纳米复合材料的合成和组装在玻碳电极上,用于 H2O2 和葡萄糖的非酶电化学传感。 b Au-Pd/MoS2 纳米复合传感器对连续添加葡萄糖的电流响应。 c 提取的对不同葡萄糖浓度的响应电流。转载自 [5],版权所有 2017,经 Elsevier 许可
除了金属之外,还尝试使用具有高催化活性的金属氧化物来改进电化学催化。除了其高电催化活性外,金属氧化物的低成本是低成本电化学传感器的另一个优势。在各种金属氧化物中,具有不同形貌的 Cu2O 纳米材料有望在各种应用中催化。方等人。已经研究了用 Cu2O 纳米颗粒装饰的 MoS2 用于非酶葡萄糖传感 [39]。 Cu2O/MoS2 混合修饰电极的电流测量显示出良好的线性范围,从 0.01 到 4 mM。提取的检测限约为1 μM。计算灵敏度高达3108.87 μA mM -1 cm −2 ,高于大多数基于二硫化钼的非酶葡萄糖传感器。结果还表明金属氧化物在低成本非酶葡萄糖传感器方面具有良好的潜力。基于MoS2纳米复合材料的无酶葡萄糖生物传感器的比较见表1。
使用二硫化钼场效应晶体管的高灵敏度葡萄糖检测
MoS2 场效应晶体管 (FET) 具有许多优点,例如高开关电流比、低漏电流、小亚阈值摆幅和高迁移率 [41, 42]。由于其出色的电子特性和机械强度,MoS2 晶体管在低能耗、低成本和可穿戴电子产品方面显示出良好的前景 [43, 44]。最近报道了生物传感器、光电探测器、气体传感器及其基于 MoS2 晶体管的灵活对应物 [45]。 MoS2 晶体管的优点使这些传感器具有高灵敏度、低功耗、便携等优点。 MoS2 FET 已被报道为各种湿度、H2O2、NO、NO2、NH3、DNA 等传感器 [46,47,48, 49]。山等人。报道了第一个用于葡萄糖检测的基于 MoS2 的场效应晶体管 [40]。如图 4a 所示,在 SiO2/Si 衬底上制造了一个背栅 MoS2 FET。通过光刻和电子束光刻对源电极和漏电极进行图案化。 Au/Ni(70 nm/10 nm)触点通过蒸发沉积。应该注意的是,大约 2 μm × 3 μm 的 MoS2 通道材料被机械剥离并转移到预先图案化的电极上,如图 4b 所示。将制作好的晶体管放入样品池中进行测试。
<图片>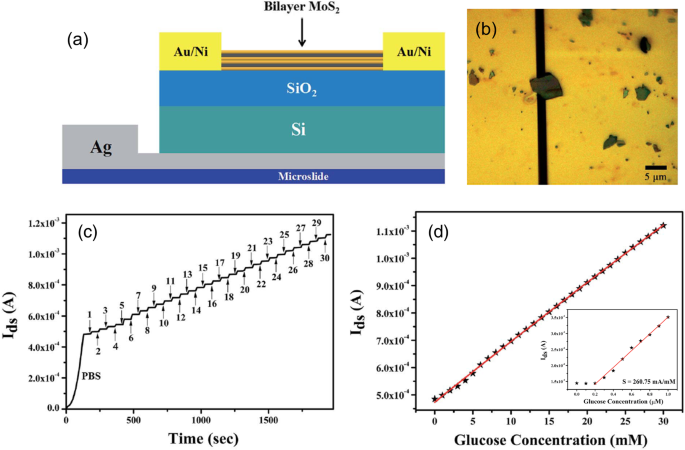
一 背栅式 MoS2 晶体管的示意图。 b 源电极和漏电极之间的 MoS2 通道材料的光学显微镜图像。 c 对不同葡萄糖浓度的实时电流响应。 d 响应电流I MoS2 FET 的 ds 作为葡萄糖浓度的函数,从 0 到 30 mM。插图显示了从 0 到 1.0 μM 的较低葡萄糖浓度提取的响应电流。转载自 [44]
在 CC BY-NC 3.0 下测量的 I ds–V 不同浓度葡萄糖溶液的ds曲线清楚地显示源漏电流随着葡萄糖浓度的增加而增加。需要注意的是,GOx 将酶加入葡萄糖浓度。因此,传感并非完全不含酶。增加葡萄糖浓度后增强的通道电流归因于酶促葡萄糖氧化。反应产生的电子被转移到 n 型 MoS2 通道,从而增加了其电导率。为了说明传感器对葡萄糖的响应,实时 I ds 测量是通过连续添加不同浓度的葡萄糖进行的,如图 4c 所示。测量开始于纯 PBS 溶液和更高浓度的溶液,每分钟放置前一个溶液,其中含有 1 mM 多的葡萄糖。对不同浓度葡萄糖的源漏电流响应绘制在图 4d 中。显然,MoS2 FET 传感器显示出非常大的葡萄糖检测线性范围,高达 30 mM。对低浓度葡萄糖溶液重复测试,以探测 MoS2 FET 传感器的检测极限和灵敏度。如图 4d 的插图所示,传感器可以清楚地检测到浓度低至 300 nM 的葡萄糖的存在。 MoS2 FET葡萄糖生物传感器的灵敏度计算为260.75 mA mM −1 .除了高灵敏度和低检测限外,该设备还表现出长达 45 天的高稳定性。不过目前的设备还得涉及到GOx的添加 被测葡萄糖溶液中的酶,这使得它在便携式应用中不太实用。
结论与展望
这篇小型评论介绍了最近为开发基于无酶生物传感器的二硫化钼纳米复合材料所做的努力。这些出版物在灵敏度、线性检测范围和检测极限方面都为高性能葡萄糖传感器提供了简便和低成本的方法。这些研究无疑为低成本和灵敏的葡萄糖传感器开辟了新的机会。这些进步在很大程度上取决于最近在合成二维材料、金属纳米材料和催化氧化物纳米颗粒的新型纳米复合材料方面取得的进展。预计在这方面会投入更多的精力,积累的经验对未来传感应用相关材料的研究非常有益。
然而,与此同时,人们应该意识到,临床或任何其他实际应用还需要付出很多努力。这些设备的稳定性和可重复性还有待提高。到目前为止,要么使用有限的储存时间,要么在干燥条件下使用。其次,化学合成方法简便且成本低,但该方法是否具有可扩展性尚不清楚。喷墨打印等新技术可用于可重复的大规模传感器制造。尽管与基于碳材料的电化学传感器相比,基于 MoS2 的电化学传感器显示出具有竞争力的性能,但其优势(例如 MoS2 的催化边缘位点)并不显着。显然还有很大的空间可以真正利用二硫化钼的独特特性来进一步改进非酶促葡萄糖传感。此外,基于葡萄糖生物传感器的柔性MoS2纳米复合材料的开发对于医疗领域的柔性传感具有重要意义,应该在市场上更具竞争力,必将成为未来的研究热点。
最后,基于 MoS2 FET 的传感器在葡萄糖传感方面表现出优异的性能。鉴于最近 MoS2 FET 的发展,这个方向在开发低成本葡萄糖传感器和其他类型的化学传感器方面似乎非常有前途。应该强调的是,目前报道的关于 MoS2 FET 葡萄糖传感器的工作仅对 GOx 起作用 -掺杂的葡萄糖溶液。未来的工作需要寻找替代方案来避免使用 GOx MoS2 FET葡萄糖传感器的更实际部署。
数据和材料的可用性
不适用。
缩写
- 二维:
-
二维
- 3D:
-
三维
- CNT:
-
碳纳米管
- CTAB:
-
十六烷基三甲基溴化铵
- FET:
-
场效应晶体管
- GOx :
-
葡萄糖氧化酶
- 首字母:
-
全名
- MoS2:
-
二硫化钼
- Ni:
-
镍
- SEM:
-
扫描电镜
- TEM:
-
透射电子显微镜
- TMD:
-
过渡金属二硫属化物
纳米材料


