增强新型阳极 PdAu/VGCNF 催化剂在甘油燃料电池中的电氧化性能
摘要
本研究提出了一种新型阳极 PdAu/VGCNF 催化剂,用于甘油燃料电池中的电氧化。反应条件是影响甘油电氧化性能的关键问题。本研究介绍了催化剂负载、温度和电解质浓度的影响。 PdAu/VGCNF 催化剂在阳极侧的甘油氧化性能通过循环伏安法测试,3 mm 2 活动区。使用 X 射线衍射 (XRD)、场发射扫描电子显微镜 (SEM) 和能量色散 X 射线 (EDX) 光谱检查催化剂的形貌和物理性质。然后,使用响应面法和中心复合实验设计进行优化。电流密度通过实验获得,作为一组实验实验室测试的响应变量。催化剂负载量、温度和 NaOH 浓度被视为独立参数,这些参数在之前的筛选实验中进行了评估。最高电流密度158.34 mAcm −2 在 3.0 M NaOH 浓度、60 °C 温度和 12 wt.% 催化剂负载的最佳条件下获得。这些结果证明PdAu-VGCNF是一种潜在的甘油燃料电池阳极催化剂。
背景
化石燃料等传统能源是有限的,总有一天会枯竭。尽管化石燃料的消耗仍然是必需的,但我们用作燃料的可燃材料无法快速更换以满足未来的能源需求 [1, 2]。燃料电池是一种很有前途的可再生能源技术,它结合氢和氧来产生电、热和水。此前,氢已被用作燃料电池的基本燃料。不幸的是,氢的处理和储存困难,需要进一步研究以液体燃料代替氢作为能量载体并将氢输送到燃料电池[3]。
在早期的研究中,甲醇是燃料电池中最常用的燃料,因为它具有高能量密度和简单的分子结构。然而,主要焦点已转向环保材料。因此,甲醇不适合用作燃料,因为它具有高毒性 [4]。此外,作为提供给阳极的燃料,甲醇显示出氧化效率低、开路电位低以及从阳极到阴极的交叉等局限性[5]。因此,为了避免甲醇的问题,甘油已成为燃料电池的一个有前途的候选者。生物柴油的主要产物甘油含量丰富,能量密度高,毒性低,使其成为燃料电池应用的良好替代品[6]。
甘油的复杂分子结构和氧化过程中的众多中间物质是阻止甘油在燃料电池中使用的主要障碍。因此,催化剂和反应条件的选择对于确保预期结果很重要。甘油氧化使用碱性介质,而不是酸性介质,以克服氧化反应过程中的动力学限制 [7]。在阳极,催化剂提供了将燃料的化学能转化为电能的基础。由于钯基材料在碱性介质中是有效的阳极材料,因此在本研究中,负载在气相生长碳纳米纤维 (VGCNF) 上的双金属 PdAu 纳米颗粒被用作甘油氧化的催化剂。 PdAu 纳米粒子本身的特性具有很高的团聚倾向,因此使用催化剂载体对于提高催化剂的性能、利用率和寿命非常重要 [8]。此外,除了它们的机械强度和表面积在 10–200 m 2 g −1 , VGCNF 具有独特的结构,在晶格和基底区域具有大量边缘,为金属-支撑相互作用提供了表面 [9, 10]。 VGCNF作为载体材料的存在可以提高金属催化剂的分散性和电催化性能[11]。
在一些研究中已经研究了乙醇的电氧化对电解液温度和 NaOH 浓度的依赖性。 Tripković、Štrbac 和 Popović [10] 指出,将温度从 295 K 提高到 333 K 会增加 Pt 和 PtRu 催化剂的 MOR 活性。 Habibi 和 Razmi [12] 研究了 NaOH 浓度在 0.5 M 到 6.0 M 范围内和温度在 25°C 到 80°C 范围内对制备的负载在改性碳陶瓷电极上的 Au、Pd 和 Pt 纳米粒子的影响( CCE)。作者报告说,NaOH 浓度和温度直接影响甘油的氧化。催化剂负载量也影响醇氧化性能。基本上,减少催化剂负载对醇氧化的影响,特别是对于复杂分子如甘油,是一项重大挑战。许多研究 [13] 开发了 10% 至 20%重量的 Pd/C 和 PdAu/C 金属催化剂,用于乙醇和甘油的氧化。乙醇和甘油等多元醇在氧化过程中涉及许多中间反应机制,其复杂性使得使用较低的催化剂负载量变得困难。
这些观察结果启发了对甘油氧化反应条件的优化研究。通过响应面法 (RSM) 分析了电解液温度、NaOH 浓度和催化剂负载量对使用 PdAu/VGCNF 进行甘油氧化的性能的影响。结果,通过一次改变一个参数,从实验数据生成了一个预测模型。 RSM 是一种用于实验设计的应用统计技术,用于战略性地计划和执行实验,从而减少优化甘油氧化操作条件所需的实验数量。 RSM 是基于多项式方程与实验数据拟合的数学和统计技术的集合 [14, 15]。 RSM 的使用更实用,因为它可能包括变量之间的交互作用,并最终描述参数对过程的整体影响 [16]。对合金电催化剂的操作条件的研究非常有限。此外,从未研究过使用 PdAu/VGCNF 催化剂对碱性介质中甘油氧化的半电池性能的 RSM 优化。大多数研究都集中在单个电池的性能上。然而,半电池测试中参数的优化可能会提供一个可应用于单电池操作的基准。
实验
材料和化学品
所有前体金属盐和化学试剂,如三水氯化金 (III) (HAuCl4·3H2O)、氯化钯 (PdCl2)、柠檬酸三钠 (Na3Ct)、硼氢化钠 (NaBH4)、碳纳米纤维、氢氧化钠、甘油、2-丙醇和 5 wt.% Nafion 溶液购自 Sigma-Aldrich/USA。
仪器
对于电催化剂的物理分析,使用 X 射线衍射 (XRD)、场发射扫描电子显微镜 (FESEM)、能量色散 X 射线 (EDX) 光谱和透射电子显微镜 (TEM) 等技术来检查电催化剂结晶、结构、形态、元素组成、尺寸和原子分布。 XRD 用于鉴定结晶材料的相。这项工作中使用的仪器是配备了 40 kV 和 40 mA 的 CuKα 辐射源的 Bruker D8 Advance 衍射仪。以 2° min -1 的速率扫描电催化剂 30° 到 90° 之间。 Scherrer 方程用于确定粉末中结晶颗粒的尺寸。纳米结构催化剂的形貌和元素信息是使用配备能量色散 X 射线光谱仪的 Gemini SEM 500 场发射扫描电子显微镜获得的,该显微镜可以提供三维图像并提供有关样品元素组成的信息。分析。透射电子显微镜 (TEM) 使用 Philips CM12 显微镜在 120 kV 下运行。在分析前,将样品催化剂置于乙醇中超声浴中 30 分钟。
催化剂合成
本研究中使用的合成电催化剂的方法是基于还原和浸渍的混合技术 [17]。这是最简单的方法,可以形成负载在气相生长碳纳米纤维 (VGCNF) 上的 PdAu 双金属合金。电催化剂合成以 2 ml PdCl2 (0.05 M) 与 7 ml 三水合氯化金 (III) (HAuCl4·3H2O) (0.012 M) 混合开始。将混合溶液滴加到一定量的柠檬酸三钠(0.5M)中。柠檬酸三钠作为稳定剂通过降低固体颗粒和溶剂之间的表面张力来控制纳米颗粒的聚集。随后,将混合溶液滴加到搅拌的 VGCNF 浆液(异丙醇 + 去离子水)中并搅拌 3 小时。使用过量的新鲜制备的冰冷 (0.5 M) 硼氢化钠 (NaBH4) 进行金属前体的还原,并将溶液搅拌过夜。较长的反应时间使硼氢化钠具有很强的还原能力,可以与产物发生反应。 NaBH4与金属离子的摩尔比为5比15,这为PdAu双金属合金纳米粒子提供了更好的催化剂分散和表面组成。将溶液保持在磁力搅拌下过夜、过滤、用去离子水洗涤数次以除去所有溶剂并在 80°C 下干燥 10 小时。在制备负载在 VGCNF 上的电催化剂 PdAu 双金属合金时,金属负载量在 10 wt.% 和 30 wt.% 之间变化。
循环伏安测试
进行循环伏安实验以对电催化剂进行电化学分析。在室温下使用 Autolab (PGSTAT101) 电化学工作站进行循环伏安法测量。通过将 5 mg 电催化剂溶解在蒸馏水、异丙醇和 5 wt.% Nafion® 的混合物中来制备催化剂油墨。使用微量移液管将 2.5 μl 等分的电催化剂墨水沉积在玻璃碳电极上,然后在室温下干燥。电催化剂的电化学表征是通过循环伏安法 (CV) 测试在 - 0.8 至 0.4 V 的电位范围内在 1 M NaOH 中以 50 mVs - 1 的扫描速率进行的 在 0.5 M 甘油/0.5 M NaOH 溶液中。 NaOH 电解质的浓度和温度分别在 0.5 到 6.0 M 和 25 到 80 °C 之间变化。两种溶液都通过在 200 ml min − 1 下用 N2 鼓泡来脱氧 在对甘油氧化反应进行任何测量之前保持 30 分钟。
实验设计
使用 Design Expert 8.0 进行中心复合设计 (CCD),以确定使用 PdAu/VGCNF 电催化剂的甘油氧化反应的优化因素。 CCD 是一种用于顺序实验的设计工具,当存在足够数量的实验数据点时,它允许对合理的信息量进行测试以防止拟合不足 [18]。本工作中使用的三个因素和范围列于表 1 中,包括 NaOH 电解质浓度、电解质温度和金属负载。响应设置为循环伏安分析得到的甘油氧化峰电位处的电流密度。
使用表 2 中所列的组合设计矩阵制备用于优化的催化剂,共进行 20 次实验,包括因子、轴向和中心点。实验数据拟合二阶多项式回归模型,由方程表示。 1:
$$ Y=\beta o+{\sum}_{i=1}^n\beta i\times Xi+{\sum}_{i=1}^n\beta ii\times X{i}^2+{ \sum}_{i=1}^n{\sum}_{j>1}^n\beta ij\times Xi Xj $$ (1)其中 Y 是预测的响应变量; n 是变量的数量;和 β 0, β i, β ii, 和 β ij 分别是线性参数、二次参数和交互作用参数的系数。上述多项式模型的确定性可以通过决定系数R来估计 2 .实验顺序随机,避免系统误差。
结果与讨论
催化剂的物理特性
为了验证 VGCNF 上负载的 PdAu 合金的形成,通过 XRD 分析了选定的样品(样品 Run-15)(见图 1)。如图 1 所示,第一个衍射峰以 26.0° 为中心,可以归因于原始 VGCNF 中的石墨结构碳,特别是六方石墨的 (002) 衍射面(JCPDS Card No. 41–1487)[10 ]。第二个峰对应于单个面心立方 (fcc) 相,表明 Pd 和 Au 高度合金化以形成高度合金化的 PdAu 双金属合金纳米粒子。样品在 39.06°、45.14°、66.17° 和 79.60° 处显示出 XRD 峰,对应于 fcc 结构中的(111)、(200)、(220)和(311)面。 PdAu双金属合金的XRD图谱可以索引到Fm3m空间群和JCPDS卡号96-151-0339的粉末衍射数据。由于第二种金属与 Pd 的相互作用,添加第二种金属,即 Au,将衍射峰移动到较低的值。此外,由于小尺寸(纳米级)材料,两个样品的 XRD 峰更短和更宽。使用 Scherrer 方程估算微晶尺寸,结果表明 Run-15 样品的微晶尺寸为 4.5 nm。
<图片>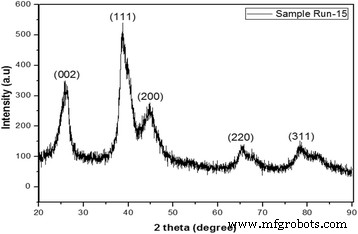
样品 Run-15 的 XRD 图
为了研究 VGCNF 上负载的 PdAu 颗粒的形态,使用 FESEM 观察样品。在图 2a 中,可以发现负载在 VGCNF 上的 PdAu 颗粒在 VGCNF 上有中等程度的团聚,它们的形状难以区分。催化剂样品中的元素组成分布通过 EDX 测量,如图 2b 所示。当进料溶液中 PdCl2:HAuCl4·3H2O 的比例为 1:1 时,Pd:Au 元素比确定为 55:44,接近预期的比例。这无疑证实了 Pd 和 Au 纳米颗粒的存在,并且与进料溶液中两种金属盐的存在非常吻合。
<图片>
一 FESEM 图像和 b 样品 Run-15 的 EDX 数据
图 3 显示了 PdAu/VGCNF(样品 Run-15)的 TEM 图像。样品图像显示 PdAu 纳米粒子在 VGCNF 上分布良好,在团聚和聚集的混合物中具有小粒径。团聚颗粒不会形成硬聚集体,而是由通过范德华力和毛细管粘附力弱附着的初级颗粒组成的软团聚体 [19]。这可能是由于粒子之间的长程磁偶极-偶极相互作用。此外,在 TEM 样品制备的干燥步骤中也观察到了这一结果,这是由溶剂蒸发过程中的毛细管力引起的 [20]。粒度分布直方图范围在 2.5 到 9.5 nm 之间,平均直径为 4.5 ± 1.0 nm。这些值与XRD分析得到的微晶尺寸接近。
<图片>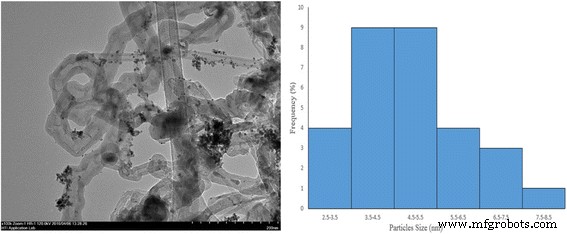
样品 Run-15 的 TEM 图像
优化研究
表 2 显示了甘油氧化反应峰值电位处的电流密度响应。甘油氧化峰值电位处的电流密度由方程给出的二阶多项式回归建模。 1. 拟合汇总模型统计结果从方程获得。 1 如表 3 所示。二阶多项式回归的建模用于最大化调整和预测的 R 2 值。如表 3 所示,二次模型具有最高的调整 R 2 和预测的 R 2 值和最低 p 价值。
表 4 显示了甘油氧化反应电流密度的方差分析 (ANOVA) 结果。模型的 p 值 <0.0001,表明模型显着 [21]。本研究中使用的因素,即 NaOH 浓度、电解质温度和催化剂负载,在甘油氧化反应模型中都很重要。该模型还具有较高的 R 2 决定系数,值为 0.9859,表明模型与观测数据拟合良好,响应的变异性仅为 0.0141%。如果模型具有R,则经验模型是足够的并且表明模型性能良好 2 值至少为 0.75 [22]。失拟的 p 值为 0.0844,大于 0.05;这也表明模型拟合良好,参数与输出响应 [23] 之间存在显着相关性,如表 4 所示。预测 R 之间的差距 2 并调整了 R 2 不大于 0.3,这意味着非显着项不会干扰二次模型。自由度 (F test) 在模型中的值为 4303.03,这意味着该模型是显着的,并且这个大 F 的可能性只有 0.01% 值可能因噪声而出现。开发了编码因子模型以拟合方程中获得的二次模型。 2;
$$ \mathrm{Current}\ \mathrm{Density}=157.49+{10.76}^{\ast }{\mathrm{X}}_1+{21.91}^{\ast }{\mathrm{X}}_2+{8.87 }^{\ast }{\mathrm{X}}_3-{5.37}^{\ast }{\mathrm{X}}_1{}^2-{29.43}^{\ast }{{\mathrm{X }}_2}^2-{36.43}^{\ast }{{\mathrm{X}}_3}^2-{9.11}^{\ast }{{\mathrm{X}}_1}^{\ast }{\mathrm{X}}_2+{0.78}^{\ast }{{\mathrm{X}}_1}^{\ast }{\mathrm{X}}_3-{1.51}^{\ast }{ \mathrm{X}}_2\ast {\mathrm{X}}_3 $$ (2)图 4a 显示了学生化残差的正态概率图。该图显示数据点近似线性,表明误差项中所需的正态性。图 4b 显示了实际响应数据与甘油氧化反应氧化峰处预测电流密度的关系图。预测与实验电流密度 (mAcm −2 ),完全符合回归模型,在操作变量范围内与观察到的密度非常吻合。图 5 显示了原始数据的残差与预测值的关系图。该图用于检查模型的充分性。在图 5 中,标准化残差与运行顺序的关系图显示残差沿直线随机分布。该结果表明原始观测值的方差对于所有响应值都是恒定的。
<图片>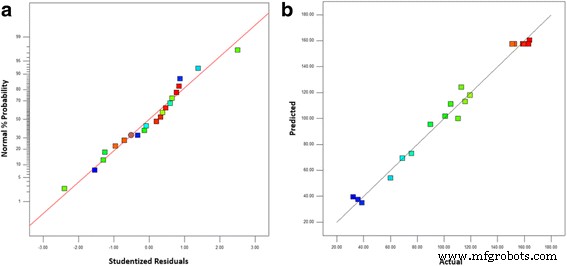
一 响应面方法 (RSM) 中学生化残差的正态概率图。 b 甘油氧化反应氧化峰电流密度的实际响应数据与预测数据对比
<图片>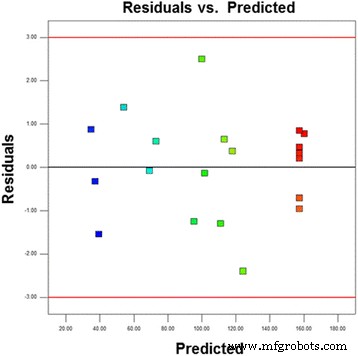
原始数据的残差与预测图
不同交互参数条件下甘油氧化性能
图 6、7、8 和 9 显示了 PdAu/VGCNF 催化剂氧化甘油氧化峰处电流密度的等高线图,作为金属催化剂负载量 (wt.%) 和 NaOH 电解质浓度 (M) 的函数不同的电解液温度范围为 25 至 80°C。图 6a 显示了电解液温度设置为 25°C 时的等高线图。如图 6a 所示,随着 NaOH 浓度和金属催化剂负载量的增加,电流密度略有增加。然而,当金属催化剂负载量超过 22 重量%时,电流密度会降低。等高线图显示,在 25°C 下获得的最高电流密度为 120 mAcm -2 .在此电流密度下,需要 18-24 重量%的金属催化剂负载和 5.5-6.0 M 的 NaOH 浓度。在图 6b 中观察到在 30°C 甘油氧化反应的氧化峰处的电流密度等高线图的相同模式。当金属负载量超过 24 重量%时,电流密度趋于降低。当 130 mAcm −2 时出现高电流密度区域 .该区域需要 5.0-6.0 M 的 NaOH 浓度和 18 重量%至 24 重量%的金属催化剂负载。在 25°C 和 30°C 下都可以达到类似的高电流密度,但 NaOH 浓度必须降低到 5.0 M,才能为甘油氧化反应的氧化峰获得高电流密度。
<图片>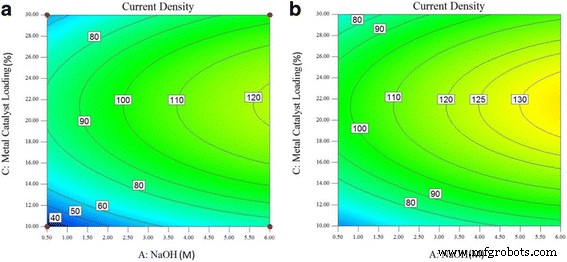
在电解质温度为 (a ) 25°C 和 (b ) 30°C
<图片>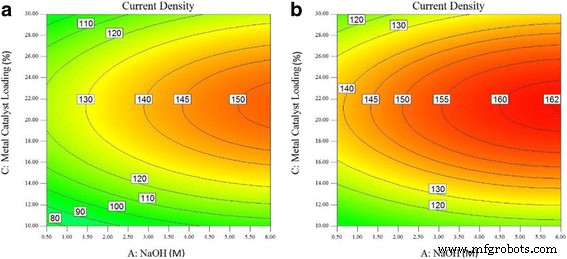
在电解质温度为 (a ) 40°C 和 (b ) 50°C
<图片>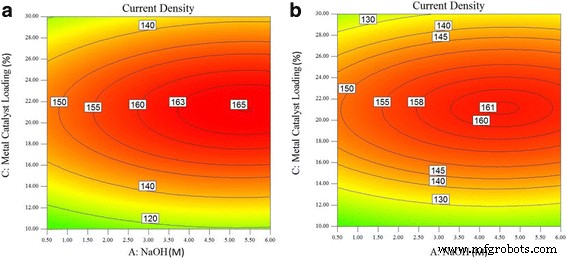
在电解质温度为 (a ) 60°C 和 (b ) 70°C
<图片>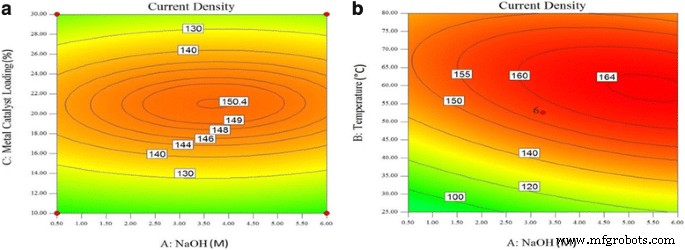
甘油氧化反应氧化峰处的电流密度图 (a ) 作为金属催化剂负载 (wt.%) 和 NaOH 浓度 (M) 在电解质温度为 80 °C 和 (b ) 作为电解质温度 (°C) 和 NaOH 浓度 (M) 的函数,在 20% 金属催化剂负载下
图 7a 显示了在 40°C 电解质温度下甘油氧化反应的氧化峰电流密度的等高线图。在此温度下可达到的最高电流密度为 150 mA/cm 2 ,相对于 130 mA/cm 2 在 30°C 下达到。与 30 °C 电解液温度相比,金属负载量可以在 16-29 wt.% 范围内,NaOH 浓度范围从 1.50 到 6.0 M,以获得 130 mA/cm 2 电解液温度为 40°C 时的电流密度。然而,使用 5.0 至 6.0 M 的 NaOH 浓度且金属催化剂负载量减少 2%(20-24%)将实现 150 mA/cm 2 的最高电流密度 在 40 °C 电解液温度下; 30 °C 的温度可以实现仅 130 mA/cm 2 的电流密度 .电解液温度从 30 到 40 °C 的变化增加了甘油氧化反应氧化峰处的电流密度。
当电解液温度进一步升高到 50°C 时,甘油氧化反应的氧化峰电流密度的等高线图如图 7b 所示。此温度下的最高电流密度为 162 mA/cm 2 ,但面积小,需要金属催化剂负载量和 NaOH 浓度分别为 21-22%wt.% 和 5.75-6.0 m。在 50°C 的电解液温度下,使用相同范围的金属催化剂负载量 (20–24 wt.%) 将 NaOH 浓度移动 0.5 M (4.5–6.0 M) 以获得 160 mA/cm2 .在相同的金属催化剂负载量和NaOH浓度范围内,温度的影响使电流密度增加到较高值。
图 8a、b 和 9a 分别显示了在 60、70 和 80°C 下甘油氧化反应的氧化峰处电流密度的等高线图。在图 8a 中,电流密度的最大值为 165 mAcm − 2 与 70 和 80°C 相比,60°C 下的电流密度为 161 mAcm − 2 和 150.4 mAcm − 3 , 分别。 PdAu/VGCNF 催化剂在 60°C 的甘油氧化反应的氧化峰处获得最高电流密度。在高于 60°C 的温度下,电流密度会降低。在图 8a 中,获得最高电流密度所需的 NaOH 浓度在 5.0-5.5 M 范围内。然而,获得 160 mA/cm 2 的电流密度 需要低至 3 M 的 NaOH 浓度,这是本研究中发现的最低浓度。电解液温度为 70 °C 时的最高电流密度降至 161 mA/cm 2 , NaOH 浓度范围约为 4.0–5.0 M。将温度升高至 80 °C 将最高电流密度降低至 150.4 mA/cm 2 以及 NaOH 浓度在 3.5-4.0 M 范围内。
在 60 至 80°C 的温度范围内获得最高电流密度所需的金属催化剂负载量似乎相同,约为 20-24 重量%。进一步增加金属负载只会降低电流密度。相同的条件也适用于其他温度。将金属催化剂负载增加至超过 24 重量%可能会阻断甘油氧化反应的活性位点。催化剂具有活性,可以将甘油吸附到催化剂表面。然而,必须考虑载体上催化金属的量。由于大体积的碳载体,高催化剂负载将影响燃料电池催化剂层的厚度。此外,增加金属负载量会导致电化学活性表面积 (EASA) [24] 的饱和。这可能是由于 Pd 聚集的可能性很高,即使在支持的情况下也是如此。因此,高金属负载量会增加纳米颗粒的聚集程度并降低孔隙率,这可能会导致传质受限并降低催化活性 [25]。如果温度和催化剂负载量同时增加,电流密度的降低可能导致 PdAu 合金颗粒聚集,由于 PdAu 催化剂的氧化还原金属转移反应的反应速度非常快,导致质量活性有限[26 ]。图 9b 显示了甘油氧化反应的氧化峰处的电流密度,金属催化剂负载量为 20 重量%,作为电解质温度和 NaOH 浓度的函数。通过将金属催化剂负载常数设置为 20 wt.%,可以改变电解液温度和 NaOH 浓度以获得最佳电流密度。
由于扩散系数、反应物的传质和反应动力学的改进,电流密度的增加是由电解质的温度引起的。当引入热量时,甘油分子移动得更快,从而使甘油能够更快地传输到阳极催化剂。然而,将温度提高到 65°C 以上对电流密度没有显着影响;更准确地说,由于中间物种的形成,电流密度变得停滞,这可能会阻塞活性位点并降低催化剂的性能 [27]。在电解质温度恒定的情况下,随着 NaOH 浓度的增加,也观察到了这一点。电流密度增加到 123.33 mAcm − 2 如图 9b 所示,NaOH 浓度为 6.0 M,温度为 25°C。由于 OH − 的增加,电流密度增加 碱性电解质环境中的浓度可能会产生更大的 OH − 覆盖在催化剂表面。 OH − 的存在 促进甘油在催化剂活性位点上的吸附,增加 OH − concentration to a certain value will prevent the adsorption of glycerol on the catalyst sites and decrease the reaction rate of the glycerol oxidation [28]. Figure 9b shows the decrease in the current density when the temperature and NaOH concentration approach 80 °C and 6.0 M, respectively. In general, the performance of the catalyst increases with increasing temperature and electrolyte concentration. However, at a certain point, these two operating conditions will have an adverse effect on the current density. Temperatures and NaOH concentrations that are too high will lead to a higher coverage of the active layer on the anode catalyst and a decrease in the cell performance [27]. The highest current density is 164 mAcm − 2 , recorded at a NaOH concentration of 6.0 M and a temperature of 60 °C.
Confirmation test
Two additional confirmation experiments were conducted to validate the RSM model and ensure that the model provides an adequate approximation to the real system. The chosen conditions for the temperature, NaOH concentration and catalyst loading, together with the predicted and experimental results, are listed in Table 5. Figure 10 shows the experiments that were performed to verify the accuracy of the developed model. The predicted and experimental values were compared, and the margin of the error was in the permissible range. The maximum current density of 164.10 mAcm − 2 was recorded during the cyclic voltammetry test at a NaOH concentration of 6.0 M, temperature of 50 °C and catalyst loading of 20 wt.%. These conditions affected the glycerol oxidation performance of the catalyst, producing the best current density. For the second set of conditions, the NaOH concentration and temperature were set to the minimum values, with a NaOH concentration of 0.5 M, temperature of 45.21 °C and catalyst loading of 20 wt.%. The maximum current density achieved in the experiment was 143.94 mAcm − 2 . Although the current density was slightly lower, the system can be run with minimal operational cost. In addition, reducing the temperature reduces the heat or energy of the system. Reducing the energy usage directly decreases the operational cost. One optimal condition, NaOH concentration of 5.24 M, temperature of 60 °C and minimal catalyst loading of 12 wt.%, was found that led to a current density of 158.34 mAcm − 2 during glycerol oxidation. Compared to the conditions used before the optimization, the catalyst loading can be minimized by up to 8%, and the current density can be increased by more than 40% (Fig. 10). The parameters chosen for the optimum conditions are suitable for single-cell operation. Table 6 presents a comparison of our Pd-based catalyst with that used in a previous study and shows that the oxidation of glycerol is remarkably enhanced when using the PdAu/VGCNF catalyst after optimizing several of the reaction parameters.
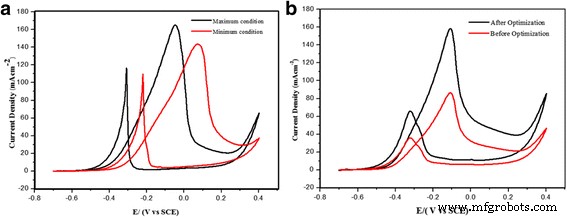
Plot of the current density for (a ) the maximum and minimum conditions and (b ) before and after optimization of the reaction conditions
结论
Response surface methodology using central composite design is a powerful method for the examination and optimization of multivariable procedures. In this study, the Design Expert RSM tool generated 20 experiments to analyze the effects of temperature, NaOH concentration and catalyst loading on the current density of the glycerol oxidation reaction via cyclic voltammogram testing. According to the F values in the analysis of variance (ANOVA) evaluation, the NaOH concentration and temperature of the electrolyte had significant effects on the response. High temperatures improved the reaction kinetics of the glycerol reaction. Meanwhile, a high NaOH concentration provided OH − ions that facilitated the glycerol oxidation reaction. The best expression or optimal conditions subject to the highest current density of 158.34 mAcm − 2 were found to be at a NaOH concentration, temperature and catalyst loading of 5.24 M, 60 °C and 12 wt.%, respectively. In conclusion, using RSM to optimize an analytical method verified and successfully determined the optimum conditions for glycerol oxidation when using PdAu/VGCNF as the catalyst.
纳米材料
- 增强智能产品分析的传感器燃料竞赛
- 用于增强药物递送的纳米纤维和细丝
- LiNi0.8Co0.15Al0.05O2/碳纳米管的机械复合材料具有增强的锂离子电池电化学性能
- 提高阳极 TaO x 纳米管阵列的生物相容性
- 通过静电纺丝法制备用于直接甲醇燃料电池的新型复合二氧化钛碳纳米纤维阳极催化剂的制备和表征
- 具有增强光催化性能的新型 Bi4Ti3O12/Ag3PO4 异质结光催化剂
- 基于叶酸和 gH625 肽的 Fe3O4 磁性纳米颗粒功能化增强细胞内化的比较
- 掺杂 Sb2O3 纳米晶体:一种用于有机降解的高效可见光催化剂
- 支持直接甲醇燃料电池的新型阳极催化剂:表征和单电池性能
- 用于染料降解的新型 p-Ag3PO4/n-BiFeO3 异质结复合材料的简便合成和增强的可见光光催化活性
- 自噬抑制剂 (LY294002) 和 5-氟尿嘧啶 (5-FU) 基于组合的纳米脂质体,可增强对食管鳞状细胞癌的疗效
- 一种用于高灵敏度检测阿特拉津的新型磁弹性纳米生物传感器


