生物相容性 5-氨基乙酰丙酸/金纳米颗粒负载的 Ethosomal 囊泡用于肥厚性疤痕的体外透皮协同光动力/光热疗法
摘要
生物相容性 5-氨基乙酰丙酸/Au 纳米颗粒负载的乙醇酸囊泡 (A/A-ES) 是通过超声制备的,用于肥厚性瘢痕 (HS) 的协同透皮光动力/光热疗法 (PDT/PTT)。利用超声处理,Au 纳米粒子 (AuNPs) 被合成并同时加载到无毒剂的 ethosomal 囊泡 (ES) 中,并且 5-氨基乙酰丙酸 (ALA) 也以 20% 的截留效率 (EE) 加载到 ES 中。由于同一 A/A-ES 中相邻 AuNPs 之间的等离子体耦合效应,制备的 A/A-ES 在 600-650 nm 显示出强吸收,这可以同时刺激 A/A-ES 产生热量并提高量子产率活性氧 (ROS) 使用 632 nm 激光。体外透皮渗透性研究表明,A/A-ES 作为一种高效的药物载体,可增强 ALA 和 AuNPs 对 HS 组织的渗透。 以人肥厚性瘢痕成纤维细胞 (HSF) 为治疗靶点,HS 的协同 PDT/PTT 表明 A/A-ES 可以通过光热效应和 AuNPs 的局域表面等离子体共振 (LSPR) 提高 ROS 的量子产率,导致高水平细胞凋亡或坏死。总之,制备的 A/A-ES 对 HSF 的 PDT/PTT 协同效率优于单独的 PDT 和 PTT,为 HSF 的治疗提供了令人鼓舞的前景。
背景
肥厚性瘢痕 (HS) 是皮肤真皮损伤后常见且不可避免的问题,其纤维化真皮比正常皮肤厚得多 [1, 2]。组织病理学上,HS 表现为增生性瘢痕成纤维细胞 (HSF) 增多,呈波浪状排列,朝向上皮表面并形成结节结构 [3]。尽管临床上有多种治疗方法,但由于存在诸多限制,HS 治疗仍面临许多挑战。病灶内注射疗法广泛用于临床实践。然而,它受到不舒服的操作和副作用的限制,例如永久性色素减退和皮肤萎缩 [4]。压力疗法的副作用有限,例如组织缺血以及降低组织代谢 [5]。为了克服这些限制,激光治疗作为一种局部和非侵入性方式,通过利用激光照射的优势,已在 HS 治疗中开发和应用超过 25 年 [6]。一般来说,激光疗法根据原理的不同可分为光动力疗法(PDT)和光热疗法(PTT)。
PDT具有选择性高、副作用少等优点,已被用于治疗HS[7]。其原理演变为两个步骤:(a) 光敏剂优先聚集在 HSF 中;(b) 在适当的激光照射下,光敏剂产生细胞毒性活性氧 (ROS),导致 HSF 细胞凋亡 [8, 9]。在各种光敏剂中,5-氨基乙酰丙酸 (ALA) 被证明是皮肤病学局部治疗方式的极好候选者,没有明显的副作用。因此,基于 ALA 的 PDT(ALA-PDT)已于 2010 年获得美国食品和药物管理局的上市许可,广泛用于 HS 治疗 [10]。然而,它的效率因两个限制而存在争议:(a)ALA 对 HS 组织和 HSF 的渗透性差,以及(b)ROS 的低量子产率。为了产生显着的效果,临床上应用了大剂量ALA或高强度激光。不幸的是,高剂量的 ALA 会导致皮脂腺和表皮的损伤,而高强度的激光往往会导致健康组织受损。因此,在 PDT 治疗 HS 中,提高 ALA 的渗透性和 ROS 的量子产率受到了很多关注。最近,发现一种专门设计的脂质体 ethosomal vesicles (ES) 能够克服 HS 中的障碍,用于局部给药并取得显着进展 [11, 12]。在我们之前的工作中,与传统的水醇溶液系统相比,制备的负载 ALA 的 ES(ALA-ES)能够将更多的 ALA 输送到 HS 中 [13]。因此,ES 可以增强 ALA 的渗透性,从而提高 HS 的 PDT 疗效。同时,一种新的PDT与PTT相结合的协同治疗方式有望同时提高ROS的量子产率和HS的治疗效果。
PTT 也是治疗各种疾病的非凡治疗方法 [14, 15]。目前已成功应用于HS的临床治疗[16]。其机制演变为收集光能、产生热量,然后导致组织汽化、凝固、HSF 细胞凋亡和胶原变性。然而,PTT 对 HS 组织的高强度激光选择性较差,因此在 HS 治疗中具有严重的副作用,如渗出、溃疡和灼烧不适[4]。最近,桥接纳米技术 PTT 被认为是一种具有高选择性和微创光热效应的潜在 HS 治疗方法。更重要的是,基于 Au 纳米粒子 (AuNPs) 作为有效的光吸附剂,PTT 已被证实可提高 ROS 的量子产率,原因有两个:(a) 热 PDT 通过在一定温度下增强 ROS 的产生来显着增加细胞凋亡依赖的方式,以及 [17] (b) AuNPs 可以与 ALA 共轭并由于局部表面等离子体共振 (LSPR) [18, 19] 提高 ROS 的量子产率。因此,基于ALA/AuNP的协同光动力/光热疗法(PDT/PTT)有望克服目前PDT和PTT在HS治疗中的局限性。
最近,基于 AuNP 的协同 PDT/PTT 已通过注射方式广泛用于各种癌症治疗 [20, 21]。与癌症不同,HS 适合使用局部给药 [22]。然而,HS真皮中的胶原束对ALA和AuNPs的渗透存在很大障碍,这限制了HS的PDT/PTT协同治疗效率。因此,如何使 ALA 和 AuNPs 同时渗透到 HS 中对于协同 PDT/PTT 具有最大疗效和最小副作用至关重要 [23, 24]。此外,合适的基于 ALA/AuNP 的协同 PDT/PTT 还应满足以下条件:(a)AuNPs 可以通过 ALA-PDT 中使用的 He-Ne 激光产生热量,以及(b)传递系统应该是高生物相容。然而,报道的各种光敏剂/AuNPs由于渗透性和生物相容性差而不能通过局部透皮给药和HS处理来应用[25]。
在此,本研究开发了具有优异生物相容性和渗透性的 ALA/AuNP 负载 ES(A/A-ES)用于 HS 的协同 PDT/PTT。生物相容性 A/A-ES 由 AuNPs 和负载 ALA 的 ES 通过超声波处理制备, 没有任何毒剂。制备的 A/A-ES 在 600-650 nm 范围内显示出强吸光度,这是由于 A/A-ES 中共载的相邻 AuNP 之间的等离子体耦合。这使得可以使用 He-Ne 激光刺激 A/A-ES 同时产生热量和 ROS,从而促进 HSF 细胞凋亡。在体外研究中,A/A-ES 显示出优异的渗透性,可以同时将 ALA 和 AuNPs 输送到 HS 中。最后,以HSF为靶点,通过细胞内原卟啉IX(PpIX)的积累、ROS的量子产率和HSF的凋亡研究了HS的体外PDT/PTT效率。此外,还通过 TEM 观察到了对 HSF 的渗透性。由于协同效应,A/A-ES 促进 ALA 和 AuNPs 同时渗透到 HS 和 HSF,与单独的 PTT 或 PDT 相比,导致更高水平的细胞凋亡。总之,A/A-ES是一种很有前景的ALA和AuNP外用透皮给药系统,在HS协同PDT/PTT方面具有巨大潜力,为HS治疗打开了一扇新窗口。
结果和讨论
A/A-ES 的特征
超声波是制备 A/A-ES 的关键参数,原因有二:(a) AuNPs 可以在没有任何毒剂的情况下通过超声波形成,这赋予了 A/A-ES 生物相容性; (b) 超声处理可以重新排列脂质双层以形成更多小尺寸和相对较大内部核心的囊泡,这可以加载更多的 ALA 和 AuNP。在这项工作中,AuNPs 是按照以下方案形成的:(a)高反应性的 H• 和 OH• 自由基在气泡内通过 H2O 的均解(方程 1)产生,(b)氧化性自由基 H• 可以提取CH3CH2OH的αH并形成还原自由基CH2•CH2OH(方程式2),并且(c)在气泡内的热解过程中,自由基CH2•CH2OH可以还原Au 3+ 形成AuNPs(方程3)[26]。
$$ {\mathrm{H}}_2\mathrm{O}\to \mathrm{H}\bullet +\mathrm{OH}\bullet $$ (1) $$ \mathrm{H}\bullet +{\mathrm {CH}}_3{\mathrm{CH}}_2\mathrm{OH}\to {\mathrm{CH}}_2\bullet {\mathrm{CH}}_2\mathrm{OH}+{\mathrm{H} }_2 $$ (2) $$ {\mathrm{Au}}^{3+}+{\mathrm{CH}}_2\bullet {\mathrm{CH}}_2\mathrm{O}\mathrm{H} +\mathrm{OH}\bullet \to \mathrm{AuNPs}+{\mathrm{CH}}_3{\mathrm{CH}}_2\mathrm{O}\mathrm{H}+{\mathrm{H}} _2\mathrm{O} $$ (3)首先,A/A-ES 是通过 UV-Vis 验证的(图 1a)。由于同一 A/A-ES 中相邻 AuNP 之间的等离子体耦合,它在 600-650 nm 范围内具有很强的吸光度 [20]。因此,它可以使用 632 nm 激光照射同时对 HS 进行 PDT 和 PTT。此外,根据图 1b 中的 DLS 分析,A/A-ES 表现出相对窄的尺寸分布,平均尺寸为 166 ± 83 nm。有趣的是,两种尺寸分布归因于卸载的 AuNP 和 A/A-ES。此外,两种分布之间的巨大差异表明 A/A-ES 的数量远多于未加载的 AuNPs。 PDT 效率取决于 A/A-ES 中加载的 ALA 量。受益于跨膜 pH 梯度主动加载方法,ALA 的 EE 为 20%,高于已报道的工作(小于 10%)[27]。还研究了 A/A-ES 的形态。在 SEM 图像上(图 1c),A/A-ES 表现为完整的球形层状囊泡,尺寸为 200 nm,并且可以清楚地观察到 AuNPs 并加载到 ES 中。除了AuNPs,薄片延伸到图1d 中的AuNP 表面,这是ES 的特征[28, 29]。此外,加载不同数量的 AuNP 的制备的 A/A-ES 在附加文件 1 中具有相似的大小:图 S1。因此,A/A-ES 在超声作用下被调整为稳定可变形的结构,这有利于 A/A-ES 挤过 HS 的狭窄空间。综上所述,A/A-ES 已成功制备,其中含有 20% 的 ALA EE,并且在 600-650 nm 处具有强吸光度。其形态也非常有利于穿透性,这与以下体外PDT/PTT研究一致。
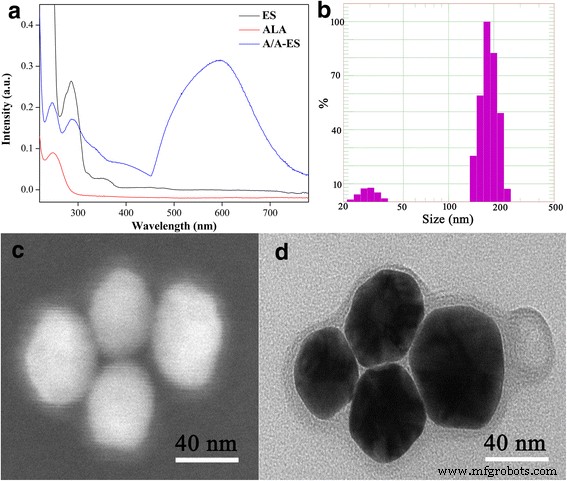
一 ES、ALA 和 A/A-ES 的 UV-Vis 光谱。 b 制备的 A/A-ES 的尺寸分布。 c , d A/A-ES的SEM和TEM图像
A/A-ES 的体外透皮渗透性研究
A/A-ES 的保留是评估 A/A-ES 渗透性和处理效率的重要参数。因此,使用 Franz 扩散池研究了不同时间 ALA 和 AuNPs 在 HS 中的保留量。如图 2a 所示,由于 ES 的渗透增强功能,ALA 和 AuNPs 在前 2 小时迅速达到最大保留。达到最大值后,由于 A/A-ES 穿透了整个 HS,ALA 和 AuNPs 的保留量不断下降。结果表明A/A-ES具有足够的渗透性。与ALA的应用剂量(2mg)相比,48%的ALA存在于HS组织中,这有利于HS的PDT。此外,ALA 和 AuNPs 之间相同的保留变化表明 ALA 和 AuNPs 都加载到 ES 中,这与显微镜的结果一致。根据结果,2 h 是 A/A-ES 最大保留量的局部使用的合适给药时间。在我们之前的工作中,ES 被认为是一种高效的药物载体,可以增强药物渗透到 HS 组织中 [13]。因此,本工作还利用透射电镜研究了 A/A-ES 在 HS 中的分布和作用。如图 2b 所示,A/A-ES 作为完整的结构存在于真皮中,表明 A/A-ES 可以稳定地穿透表皮并进入 HS 真皮。在图 2c 所示的真皮下部,ES 和 AuNPs 被观察为分离状态,表明 A/A-ES 会同时释放 ALA 和 AuNPs。有趣的是,AuNPs 可能在真皮中聚集,即使它们没有加载到 ES 中。此外,在图 2d 中发现更多的 AuNPs 积累在真皮中,这可以提供相邻 AuNPs 之间的等离子体耦合以收集光能并产生热量。简而言之,体外透皮渗透性研究表明 A/A-ES 是一种高效的药物载体,可增强 ALA 和 AuNP 对 HS 组织的渗透,并且真皮中的聚集 AuNPs 有利于产生热量 [20]。因此,A/A-ES在HS协同PDT/PTT方面显示出巨大的潜力。
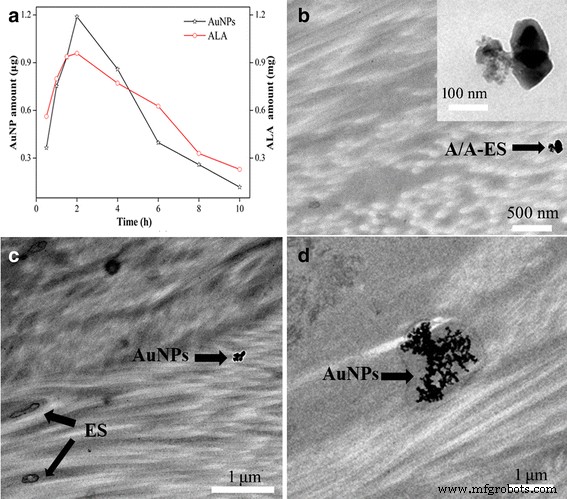
一 ALA 和 AuNPs 的保留量。 b A/A-ES 在 HS 组织中的分布。 c ES和AuNPs在HS组织中的分布。 d AuNPs在HS组织中积累
HSF 体外 PDT/PTT
生物相容性测定
尽管 AuNPs 的生物相容性已在报道的工作中得到很好的证明,但这项工作还应研究 A/A-ES 对 HSF 的生物相容性 [30, 31]。不同浓度的 ALA-ES、Au-ES 和 A/A-ES(基于 0.1 至 10 mM 的 ALA 浓度,Au-ES 与 A/A-ES 的 AuNP 浓度相同)与 HSF 一起孵育 12 小时无需辐照。结果表明,在不超过 2.0 mM 的浓度下没有暗细胞毒性,细胞存活率超过 90%。当浓度高于 2.0 mM 时,检测到细胞存活率略有下降。结果表明,A/A-ES 具有良好的生物相容性,后续研究中 PDT/PTT 应在 2.0 Mm 浓度下进行(约 14% A/A-ES 在培养基中,v /v .) 图 3.
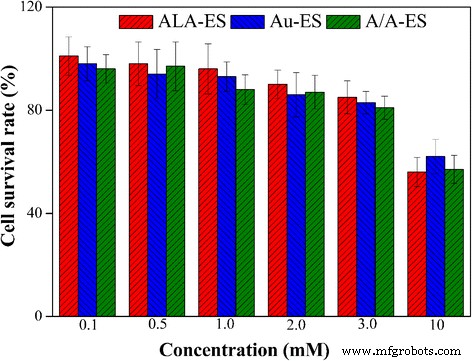
HSF在暗处用ALA-ES、Au-ES和A/A-ES处理12小时后的细胞活力
HSF 的 PDT/PTT
A/A-ES 可以通过 A/A-ES 与 HSF 膜的融合克服表面通透性障碍,然后将 ALA 和 AuNPs 直接释放到细胞质中 [32]。根据ALA-PDT的机制,A/A-ES释放的ALA可以在HSF细胞质中转化为PpIX。使用激光,PpIX 产生细胞毒性 ROS,导致细胞凋亡。因此,CLSM 用于研究图 4 中 PpIX 和 ROS 的积累 [33, 34]。在激光照射前,PpIX 的红色荧光主要分布在 HSF 的细胞质中。 ALA-ES和A/A-ES处理的HSF中的PpIX远多于Au-ES处理的HSF中的自体PpIX。而且,在没有激光照射的情况下,几乎没有在所有HSF中发现ROS,这也是合理的。激光照射后,ALA-ES和A/A-ES处理的HSF中PpIX强度降低,这些细胞中的ROS很容易以强强度被发现。同时,Au-ES 处理的 HSF 在 PpIX 和 ROS 中没有反应,因为它们没有足够的自体 PpIX。有趣的是,在 ROS 强度的比较中,A/A-ES 可以比 ALA-ES 促进更多的 ROS 生成,这归因于 AuNP。此外,细胞形态也提供了更多信息。 ALA-ES 处理的 HSF 具有优态性,而 Au-ES 处理的 HSF 显示出不健康的质膜突起。相比之下,A/A-ES 处理的 HSF 表现为突出和收缩的“气泡”,这是死亡细胞的特征 [35]。这些 ROS 生成和细胞形态的差异归因于基于 AuNPs 的 PTT,这也在图 5 中通过红外成像进行了研究。根据 AuNPs-PTT 的机制,HSF 细胞质中的 AuNPs 可以吸收 632 nm 激光并产生足够的热量使细胞在照射下发生凋亡或坏死。因此,使用红外热像仪监测 ALA-ES、Au-ES 和 A/A-ES 的光热效应。与 ALA-ES 相比,Au-ES 和 A/A-ES 在辐照时具有明显更高的温度(Au-ES 和 A/A-ES 为 41.3°C,ALA-ES 为 36.5°C)。移除激光后,所有温度在 1 分钟内迅速下降至正常值,表明激光照射治疗是安全的 [36]。因此,加载在 ES 中的 AuNPs 可以提供有效的 PTT,这也由细胞凋亡和坏死测定提供。综上所述,A/A-ES可以提高ROS的量子产率并提供光热效应,从而实现PDT/PTT协同处理HSF的优异效率。
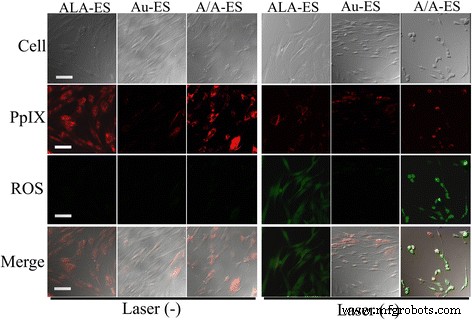
用 ALA-ES、Au-ES 和 A/A-ES 处理 6 小时的 HSF 共聚焦图像,然后在没有/有辐射的情况下进行跟踪。比例尺为 100 μm
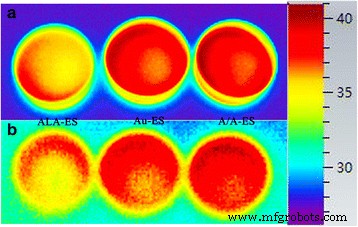
.用 ALA-ES、Au-ES 和 A/A-ES 在 (a ) 和辐照后 (b )
细胞凋亡和坏死分析
通过ALA-ES、Au-ES和A/A-ES在激光照射下处理HSF的凋亡和坏死,进一步研究了PDT/PTT的效率。通过使用膜联蛋白 V-FITC 和碘化丙啶 (PI) 双染色的流式细胞术分析进行细胞凋亡测定(图 6)。对照结果显示激光照射不影响细胞活力(图 6a)。在照射前,ALA-ES、Au-ES 和 A/A-ES 表现出良好的生物相容性。辐照后,ALA-ES、Au-ES和A/A-ES处理的HSF坏死和凋亡比例均有显着差异。简而言之,A/A-ES 处理的 HSF 坏死和凋亡的比例最高,这与 CLSM 的结果一致。在图 6e 中,实验的统计分析显示,用 A/A-ES 处理的坏死细胞死亡增加到 61.8%,表明 A/A-ES 对 HSF 的协同 PDT/PTT 效率比单独的 PDT 更好。 47.7% 坏死细胞死亡)和 PTT(24.3% 坏死细胞死亡)。有趣的是,结果还表明,与 PTT 相比,PDT 在 HS 治疗中发挥了更有效的作用,并且基于 AuNP 的 PTT 可以帮助 PDT 效果。这些结果可能被解释为 A/A-ES 可以提高 ROS 的量子产率并提供光热效应以实现 PDT/PTT 协同处理 HSF 的优异效率。尽管 A/A-ES 中 ALA 的 EE 远低于 ALA-ES(20% vs. 54%),但 A/A-ES 和 ALA-ES 的坏死细胞死亡相似(61.8 vs. 78 %)。这一结果可以解释为A/A-ES可以通过光热效应和AuNPs的LSPR提高ROS的量子产率。
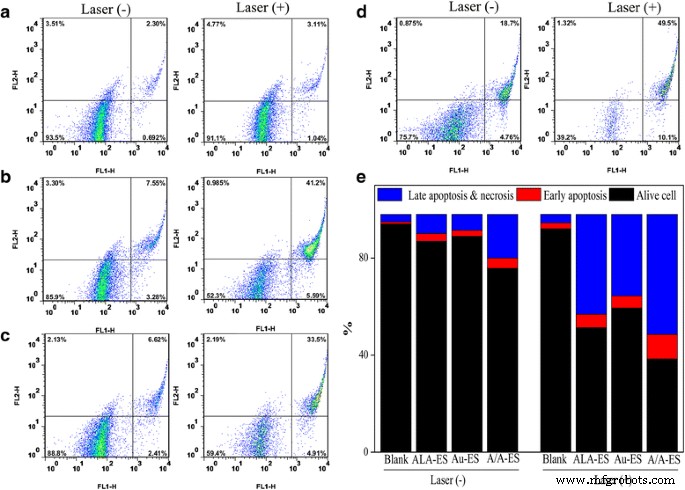
ALA-ES 处理 HSF 的细胞凋亡测定 (b ), Au-ES (c ), 和 A/A-ES 无/有激光照射 (d ),以及存活、早期凋亡和晚期凋亡和坏死的统计分析 (e )。 一 是控制。激光 (-) 和 (+) 表示无/有激光照射
HSF 中 A/A-ES 的可视化
PDT/PTT引起的HSF形态和结构的细节变化也在图7中通过光学显微镜和TEM进行了研究。辐照前,HSF经A/A-ES处理后生长良好,变态牢固粘附,表明A/A-正如预期的那样,ES 具有出色的生物相容性(图 7a)。在他们的TEM图像中,除了正常细胞质中的各种细胞器外,处理过的HSF在细胞质中聚集了大量AuNP(图7c中的空白框)。可以解释的是,A/A-ES 与细胞膜的融合可以将更多的 AuNPs 和 ALA 输送到 HSF。因此,由于更强的等离子体耦合效应,AuNPs 可以作为更有效的光热源,并通过 LSPR 提高 ROS 的量子产率。有趣的是,如图 7c 中的虚线框所示,一些 AuNP 由于胞吐作用而脱离了 HSF,这再次证明了 A/A-ES 的优异生物相容性。辐照后,HSF 显示出细胞死亡的特征,即质膜的突起(图 7b)[37]。由于 ROS 和光热效应,在 HSF 细胞质中发现了膨胀的线粒体和破裂的外膜,作为 HSF 死亡的其他指标(图 7d)[35]。此外,还发现 ES 具有其特征膜结构(图 7d 中的红色框)。综上所述,A/A-ES可以通过协同PDT/PTT促进ALA和AuNPs渗透到HSF中并破坏HSF。

之前用 A/A-ES 处理的 HSF 的光学显微镜图像 (a ) 和辐照后 (b )。之前用 A/A-ES 处理过的 HSF 的 TEM 图像 (c ) 和辐照后 (d )
结论
生物相容性 A/A-ES 通过渗透到 HS 和破坏 HSF 轻松制备用于 HS 的体外协同 PDT/PTT。利用超声波处理,在没有任何有毒物质的情况下同时合成和加载 AuNP。 A/A-ES 在 600-650 nm 具有强吸光度,因为 ES 中相邻 AuNP 之间的等离子体耦合效应与 ALA 的高 EE(约 20%)。体外透皮渗透性研究表明,A/A-ES 是一种高效的药物载体,可增强 ALA 和 AuNP 对 HS 组织的渗透。 HSF 的体外 PDT/PTT 表明 A/A-ES 可以通过光热效应和 AuNPs 的 LSPR 提高 ROS 的量子产率,导致高水平的细胞凋亡或坏死。总之,与单独的 PDT 和 PTT 相比,生物相容性 A/A-ES 对 HSF 具有更好的协同 PDT/PTT 效率,令人鼓舞的治疗 HS 前景。进一步的工作将集中在疤痕模型中HS协同PDT/PTT的体内研究,相关工作正在进行中。
实验与方法
A/A-ES的准备
180 毫克磷脂酰胆碱(PC,95.8% 大豆卵磷脂,Lipoid GmbH,德国)溶解在 1.8 mL CH3CH2OH、0.6 mL HAuCl4(10 mM,Aladdin,中国上海)和 3.6 mL ALA-柠檬酸缓冲溶液(CBS, 0.01 M,12 mg ALA,pH 4.0),依次滴加到 PC 溶液中。将混合物以 700 rpm 搅拌 10 分钟以制备前体溶液。如方案 1 所示,将前体溶液置于 200 W 的超声波环境中 30 分钟,直至呈现明亮的酒红色。然后,将反应溶液用离心机(8000 rpm,20 分钟)进行以去除残留的 HAuCl 4 和 PC。最后,根据我们之前的工作,将沉积物重新分散在 3 ml ALA 水醇溶液(ALA-HA,2 mg/ml ALA,30% 乙醇)中,并通过跨膜 pH 梯度主动加载方法进行孵育 [13]。在孵化过程中,大量外部未结合的 ALA 通过 ES 双层扩散到 ES 的内部酸性水核中,然后,它们被质子化并被困在 ES 中。孵育后,A/A-ES 已制备完毕。在这项工作中,ALA-ES 是根据我们之前的工作制备的,其 ALA 浓度与 A/A-ES 相同。负载AuNP的ES(Au-ES)制备成A/A-ES,不含ALA,AuNP浓度与A/A-ES相同。
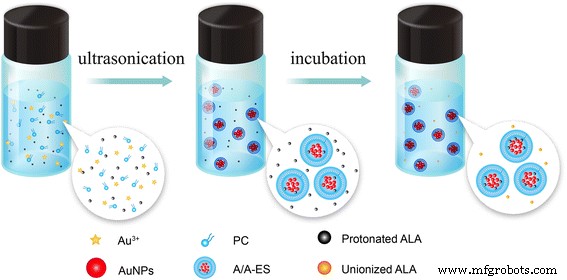
A/A-ES制备示意图
A/A-ES 的特征
A/A-ES 用磷钨酸 (1.5 wt%) 负染色,然后通过透射电子显微镜(TEM,JEOL,日本,加速电压为 120 kV)观察。还通过扫描电子显微镜(SEM,JEOL,日本,10 kV 加速电压)检查了 A/A-ES。 A/A-ES 尺寸分布是通过在 NiComp 380ZLS 检测系统(Nicomp,美国)中进行动态光散射 (DLS) 分析来确定的。 ALA 是通过荧光胺衍生方法测定的,详细信息显示在附加文件 1 中。通过超滤方法测定的 ALA 的截留效率 (EE) 显示在附加文件 1 中。最后,UV-Vis 光谱在一个Varian Cary 50 紫外-可见分光光度计(美国珀金埃尔默)。
Franz 扩散池的体外渗透性研究
A/A-ES 的渗透性研究是通过使用 2.8 cm 2 的 Franz 扩散池进行的 有效渗透面积包括供体和受体隔室的受体细胞通过循环水浴保持在 37°C。在上海第九人民医院知情同意和上海第九人民医院批准的 1975 年赫尔辛基宣言的伦理指南的情况下收集 HS 组织。将不含脂肪组织的新鲜 HS 组织(切除后不到 24 小时)安装在受体隔室上,角质层向上至供体隔室。将一毫升 A/A-ES 加入供体室,然后用石蜡膜覆盖供体室以防止蒸发。不同时间渗透后,迅速清洗HS组织以去除HS表面残留的A/A-ES。为了在 HS 中积累 ALA 和 AuNPs 的保留量,将 HS 组织切成小块,并通过在 PBS 中透析 24 小时来提取 HS 组织中的 ALA。分析提取溶液中 HS 组织中 ALA 的保留量。还通过电感耦合等离子体质谱法 (ICP-MS) 分析了保留在透析袋中的 HS 组织的 AuNP 保留量。在被 ALA-ES 渗透 2 小时后,HS 组织被洗涤、固定、脱水、渗透和后固定。包埋在环氧树脂中后,将它们切成超切片(50 nm 厚,垂直于表皮),并在 120 kV 加速电压下使用 TEM 进行观察。
HSF 体外 PDT/PTT
细胞培养
HSF的分离培养采用以下常用方法:新鲜HS组织切片(1mm 3 ,切除后不到 6 小时)通过使用 I 型胶原酶(Invitrogen,美国)消化以获得单细胞悬浮液。 HSF 在含有 10% 胎牛血清(FBS,Gibco,美国)和 5% CO2 的 Dulbecco 改良 Eagle 培养基(DMEM,Invitrogen,美国)中生长。应每 3 天更换一次培养基,细胞在 80% 汇合时传代。传代二、三细胞用于后续实验。
生物相容性分析
在评价A/A-ES的生物相容性时,HSF以2 × 10 3 接种于96孔板中。 细胞/孔。培养基分别更换为不含 FBS 的培养基和新鲜制备的不同浓度的 ALA-ES、Au-ES 和 A/A-ES。 12 小时后,按照制造商的说明,使用细胞计数试剂盒-8(CCK-8,Dojindo,日本)测量细胞活力。
PDT/PTT程序
HSF以4 × 10 4 接种于12孔板 细胞/孔。 12 小时后,培养基分别含有新鲜制备的 ALA-ES、Au-ES 和 A/A-ES(14%,v /v ),用不含 FBS 的培养基替换 6 小时。处理后,HSF 用 PBS 洗涤并在培养基中孵育 1 小时。然后,它们被 He-Ne 激光(632 nm 波长,40 mW/cm 2 ,上海激光技术研究所,中国)20 分钟。然后,将培养基更换为含有 10% FBS 的新鲜 DMEM 再培养 24 小时,为后续实验做准备。此外,HSF经A/A-ES和辐照后进行前缀、脱水和包埋,制备用于TEM检查的超切片。
细胞内 PpIX 和 ROS 生成分析
通过使用共聚焦激光扫描显微镜(CLSM,Leica TCS SP5,德国)检测 HSF 中细胞内 PpIX 的积累和 ROS 的产生。使用 DCFH-DA 进行 ROS 生成测定并遵循制造商的说明。将带有细胞的盖玻片安装在载玻片上,并在 405 nm 激发/635 nm 发射下观察 PpIX 和 488 nm 激发/560 nm 发射下 ROS。所有数据均采用LAS AF软件进行分析。
细胞凋亡和坏死检测
经Annexin V-FITC双染和碘化丙啶(PI)双染后,流式细胞仪分析HSF的凋亡和坏死情况。根据Annexin V-FITC/PI细胞凋亡检测试剂盒的方案制备样品,然后通过BD FACSCalibur(BD Biosciences,Mountain View,USA)进行分析。数据分析采用FlowJo 7.6软件。
统计分析
除非另有说明,数据均表示为平均值 ± SD。使用双尾学生测试 (P <0.05) 除非另有说明。
缩写
- A/A-ES:
-
5-氨基乙酰丙酸/Au纳米颗粒负载的乙醇型囊泡
- ALA:
-
5-氨基乙酰丙酸
- ALA-ES:
-
加载 ALA 的 ES
- ALA-PDT:
-
基于ALA的PDT
- Au-ES:
-
负载AuNP的ES
- AuNPs:
-
金纳米粒子
- CLSM:
-
共聚焦激光扫描显微镜
- DLS:
-
动态光散射
- DMEM:
-
Dulbecco 改良 Eagle 培养基
- EE:
-
包封率
- ES:
-
嗜酸性囊泡
- FBS:
-
胎牛血清
- HS:
-
增生性瘢痕
- HSF:
-
增生性瘢痕成纤维细胞
- ICP-MS:
-
电感耦合等离子体质谱法
- LSPR:
-
局域表面等离子体共振
- PDT:
-
光动力疗法
- PDT/PTT:
-
光动力/光热疗法
- PpIX:
-
原卟啉Ⅸ
- PTT:
-
光热疗法
- ROS:
-
活性氧
- SEM:
-
扫描电镜
- TEM:
-
透射电子显微镜
纳米材料
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 用于 NIR-II 光热疗法的 BSA 涂层金纳米棒
- 环境响应金属-有机框架作为肿瘤治疗的给药系统
- 用聚苯乙烯-共-丙烯酸复合纳米球检测霍乱弧菌 DNA 的超灵敏生物传感器
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- 5-氨基乙酰丙酸-角鲨烯纳米组件用于肿瘤光检测和治疗:体外研究
- 用于新型隐球菌诊断和光热治疗的抗体偶联二氧化硅修饰金纳米棒:体外实验
- 用于光热疗法的聚多巴胺碳点的简便一锅法合成
- Carbon Dots @ Platinum Porphyrin Composite 作为用于有效光动力癌症治疗的治疗诊断纳米剂
- 用于超声介导多柔比星靶向递送的生物相容性壳聚糖纳米泡
- 基于铂和镍锯齿状纳米线的用于检测咖啡酸的超稳定电化学传感器


