苯甲醇在 TiO2 上沉积的 Au-Pd 双金属上的无溶剂催化氧化:金红石、板钛矿和锐钛矿的比较
摘要
TiO2(P25)负载的Au-Pd双金属纳米粒子在无溶剂苯甲醇催化氧化中表现出优异的性能。然而,很少有研究关注研究 TiO2 形式对 Au-Pd/TiO2 催化活性的影响。在目前的研究中,成功合成了金红石、板钛矿和锐钛矿 TiO2,并随后作为载体通过沉积沉淀法负载 Au-Pd 纳米颗粒。实验结果表明,采用金红石型TiO2负载Au-Pd催化剂的苯甲醇转化率高于负载锐钛矿和板钛矿型TiO2负载Au-Pd催化剂的转化率。然而,Au-Pd/TiO2-金红石分别对苯甲醛和甲苯显示出最低和最高的选择性。进行 ICP-AES、XRD、XPS 和 TEM 来表征这些催化剂。相应的实验结果表明,Au-Pd/TiO2-金红石催化剂的优异性能归因于较小的Au-Pd纳米粒径分布以及较高的Oα和Pd 2+ 浓度。 催化剂表面的物种。在循环实验中,与 Au-Pd/TiO2-锐钛矿和 Au-Pd/TiO2-板钛矿相比,Au-Pd/TiO2-金红石催化剂表现出较低的反应稳定性,这可能是由于覆盖了大量的醛产物表面上。
介绍
长期以来,黄金一直被认为是化学惰性的,直到 Hutchings 和 Haruta 分别独立发现它们在乙炔氢氯化和低温 CO 催化氧化中具有出色的催化活性 [1, 2]。金作为活性成分,在许多反应中得到了广泛的研究,包括水煤气变换反应、由 O2 和 H2 直接合成 H2O2 以及肉桂醛的选择性加氢 [3,4,5]。此外,Au 基催化剂的反应活性和稳定性可以通过将它们与 Pd 结合来显着提高。例如,哈钦斯等人。发现固定在TiO2(P25)上的Au-Pd双金属催化剂在无溶剂条件下对苯甲醇氧化的催化活性远高于负载型Au或Pd催化剂[6]。
人们普遍认为,负载型Au-Pd双金属催化剂的催化活性与载体性质、纳米颗粒尺寸和制备方法密切相关。 TiO2、CeO2、Fe2O3等可还原金属氧化物作为催化剂载体,由于金属与载体之间相互作用强,分子氧易于活化,被广泛采用。 TiO2 作为典型的载体候选物,已被广泛研究用于支持 Au-Pd,它还显示出出色的苯甲醇氧化催化活性。例如,哈钦斯等人。首先采用溶胶固定法制备了Au-Pd/TiO2,并将其应用于醇类选择性催化氧化成醛类。相应的结果表明,与 Au 催化剂相比,将 Au 与 Pd 合金化可以使活性提高 25 倍,同时保持选择性 [6]。查德威克等人。最近通过在无钠钛纳米管上使用胶体合成和固定化制备了双金属 Au-Pd/TiO2 纳米管,该纳米管对苯甲醇氧化成苯甲醛显示出优异的催化性能 [7]。郑等人。通过两步光沉积方法开发了一系列具有高度分散的 Pd 的 Au@Pd/TiO2 催化剂,该催化剂还可作为无溶剂条件下苯甲醇有氧氧化的高活性催化剂 [8]。李等人。采用桔梗提取物的生物还原方法制备Au-Pd/TiO2,然后将其应用于苯甲醇的无溶剂氧化。该催化剂表现出优异的催化性能、耐久性和可重复使用性[9]。
最广泛使用的 TiO2 类型是 P25。然而,公认的是二氧化钛包含三种不同的形式:金红石、板钛矿和锐钛矿。迄今为止,仅在光催化反应和气固催化氧化反应中报道了TiO2形态对催化活性的影响,如CO2光催化还原、CO催化氧化和NH3选择性催化还原NO<我> x [10,11,12]。众所周知,锐钛矿型TiO2作为载体,通常表现出比金红石型和板钛矿型TiO2更好的催化活性。然而,这种观点与一些实验结果相反。戴等人。使用沉积沉淀法分别将 Au 负载到锐钛矿、金红石、板钛矿 TiO2 和 P25 的表面上,并研究了它们对 CO 氧化的催化活性。相应的结果表明,板钛矿 TiO2 负载的金催化剂由于表面上较小的 Au 纳米粒子而保持最高的催化活性 [11]。姚等人。用传统的初湿浸渍法制备了CeO2/锐钛矿、CeO2/板钛矿和CeO2/金红石,并比较了它们的NH3-SCR催化性能。实验结果表明,CeO2/金红石可以得到最佳的催化性能,这可能是由于其优异的氧化还原性能,较高的酸性位点浓度,Ce 3+ 物种,并吸附在催化剂表面上的氧物种 [12]。李等人。研究了水蒸气在金红石、锐钛矿和板钛矿 TiO2 上的 CO2 光还原;实验结果表明,板钛矿TiO2的光催化性能优于锐钛矿和金红石,这与板钛矿表面氧空位形成能垒最低有关[10]。
尽管 Au-Pd/TiO2 催化剂在苯甲醇氧化中表现出出色的催化活性,但目前尚未研究负载 TiO2 的 Au-Pd 形式对催化性能的影响。因此,有必要进行对比实验以研究催化活性的差异,并揭示 TiO2 负载的 Au-Pd 对金红石、板钛矿和锐钛矿 TiO2 催化性能不同的原因。目前的工作研究了苯甲醇氧化对分别负载在锐钛矿、金红石和板钛矿上的双金属 Au-Pd 的催化活性。同时,利用XRD、ICP-AES、XPS和TEM等手段揭示了TiO2形态对Au-Pd/TiO2理化性质的影响。
方法
所有化学试剂均购自阿拉丁公司(中国上海)并按原样使用:尿素(99.9% 金属基)、二氢氧化钛双(乳酸铵)水溶液(待定,50% 水溶液)、TiCl4(99.99% 金属基) 、乙醇(≥ 99.5%,纯度)、H2SO4(> 98%,纯度)、PdCl2(99.99% 金属基础)、HAuCl4·3H2O(≥ 99.9% 微量金属基础)、苯甲醇(99.8%,纯度)。 O2(99.999%,纯度)由太原钢铁公司提供。
Brookite 和锐钛矿 TiO2 的合成 [13]
为了制备板钛矿 TiO2,首先将 8 mL 的 TBD 溶液(50%)和 17 g 尿素混合,然后通过添加额外的去离子水将混合溶液调节至 80 mL。随后,将所得溶液转移到 200 mL 内衬聚四氟乙烯的高压釜中,将其封装并在 160 °C 下保持 24 小时。当高压釜冷却至室温时,将沉淀物过滤、洗涤并干燥。最后将所得粉末在500℃下煅烧5 h。
在制备锐钛矿型TiO2时,我们仅将尿素用量从17g调整为0.48 g,并重复上述步骤。
金红石二氧化钛的合成[10]
对于金红石 TiO2,在搅拌下将所需量的 TiCl4 溶解在乙醇中。形成黄色溶胶后,在上述溶液中滴加水,同时搅拌。 TiCl4、乙醇和水的摩尔比控制在2:20:280。将所得混合物再搅拌 3 小时,并在密闭的高压釜中在 50°C 下老化 24 小时。随后,将白色沉淀物离心、洗涤并干燥。最后,所得产物也在500℃下煅烧5 h。
制备沉积在布鲁克石、锐钛矿和金红石上的 Au-Pd
为了保持 Au:Pd 摩尔比为 1:1,Au-Pd/TiO2 催化剂上 Au 和 Pd 的标称负载量分别为 1.00 wt% 和 0.54 wt%。 1.00 wt% Au-0.54 wt% Pd/TiO2(板钛矿、锐钛矿和金红石)采用沉积-沉淀法制备,尿素为沉淀剂。通常,为了制备 Au-Pd/TiO2-板钛矿,2 mL HAuCl4 水溶液(5 mg Au/mL)、1.08 mL PdCl2 水溶液(5 mg Pd/mL)、0.985 g 板钛矿 TiO2 和 3.48 mL PdCl2 水溶液在室温搅拌下,将尿素加入 100 mL 去离子水中。将混合物溶液在 80°C 搅拌 6 h。然后,将所得溶液在室温下再老化 12 小时。随后,将沉淀物离心、洗涤并干燥。最后将所得产物在300℃下以2℃/min的升温速率煅烧2 h。
为简单起见,制备的 TiO2-板钛矿、TiO2-金红石、TiO2-锐钛矿催化剂 Au-Pd/TiO2-板钛矿、Au-Pd/TiO2-金红石和 Au-Pd/TiO2-锐钛矿样品表示为 TiO2-B、TiO2 -R、TiO2-A、ATB、ATR和ATA。
苯甲醇氧化
苯甲醇催化氧化在机械搅拌反应器中使用 50 mL 搪玻璃 min claves(安徽凯米机械科技有限公司,中国)进行。通常,将15 mL苯甲醇和0.05 g催化剂加入反应器中,将反应器密封并用O2吹扫5次。随后,在室温下用 O2 将反应器加压至 0.3 MPa。以1000 rpm将反应混合物加热至所需温度。反应器还与储氧器相连,用于补充反应过程中消耗的氧气。反应产物通过配备火焰离子化检测器(FID)和DM-5色谱柱(30 m×0.25 mm×0.25 μm)的GC(FuLi GC9790,浙江,中国)进行分析。为保证数据的可靠性,每组实验至少重复2次,每个数据点GC测定3次。
为了研究催化活性的稳定性,重复使用的催化剂在三个催化循环内进行。每次运行后,收集催化剂并用丙酮洗涤,然后在80°C下加热16 h。
特征化
粉末 XRD 在 Rigaku D/max-RC 衍射仪上进行,CuKα 辐射在 40 kV 和 25 mA (λ =0.15418 nm)。以 8°/min 的速度在 10-90° 的扫描范围内记录强度。在 Agilent 735-ES 仪器上进行 ICP-AES 以定量测定所制备催化剂的化学成分。在测量之前,将催化剂溶解在王水中约 24 h。 X 射线光电子能谱测量在 PHI-1600ESCA System XPS 光谱仪(Perkin-Elmer,美国)上进行,使用非单色 Mg-Kα 辐射,在 15 kV 和 10 -7 下运行 Pa 压力,光电子能量设置为 1254 eV。报告的结合能参考了 C1s 结合能 284.6 eV。 TEM 在 JEM-2100 电子显微镜上进行,操作电压为 200 kV。分析前,用乙醇在超声波的辅助下分散样品粉末,然后将混合溶液沉积在带有碳膜的网格上。
结果与讨论
进行 XRD 以研究 TiO2 载体的晶型和 Au-Pd/TiO2 催化剂上的 Au-Pd 分散状态。如图1所示,制备的锐钛矿型TiO2在25.4、37.8、48.1、54.1、55.2、62.9、68.8、70.4、75.1和82.7°处检测到10个衍射峰,与标准PDF卡(No . 21-1272)。还可以发现在 25.4, 30.9, 32.8, 36.3, 37.4, 40.2, 42.4, 46.2, 48.2, 49.3, 54.4, 55.3, 57.4, 60.2, 6.7, 60.2, 6.7, 60.2, 6.1, 6.7在制备的板钛矿 TiO2 载体上检测到 、77.2、82.7 和 87.0°,这与标准板钛矿 PDF 卡(板钛矿 TiO2 PDF 29-1360)非常吻合。制备的金红石型TiO2在27.5、36.1、39.2、41.3、44.2、54.3、56.6、62.7、64.1、69.1、69.9、76.6、82.4、84.3°的TiO2均表现出相应的峰(也与金红石型TiO2相一致,PDF°也为84.3)。金红石二氧化钛 PDF 21-1276)。上述XRD结果证实成功制备了具有金红石、板钛矿和锐钛矿形式的TiO2。同时,基于不同位置的衍射峰信息(2θ =TiO2-A 为 25.4°,TiO2-B 为 30.9°,TiO2-R 为 27.6°);计算结果表明,TiO2的纳米粒径排列顺序为:TiO2-R(27.6 nm)>TiO2-B(18.9 nm)>TiO2-A(11.2 nm)。在 TiO2 载体表面负载 Au-Pd 双金属纳米粒子后,在制备的 Au-Pd/TiO2 图案上没有检测到 Au 或 Pd 的衍射峰。这种现象不仅表明 Au 和 Pd 高度分散成更小的粒径(例如 3~5 nm),这在 XRD 中无法观察到,而且表明 TiO2 载体的晶体结构不受 Au 负载的影响和钯。
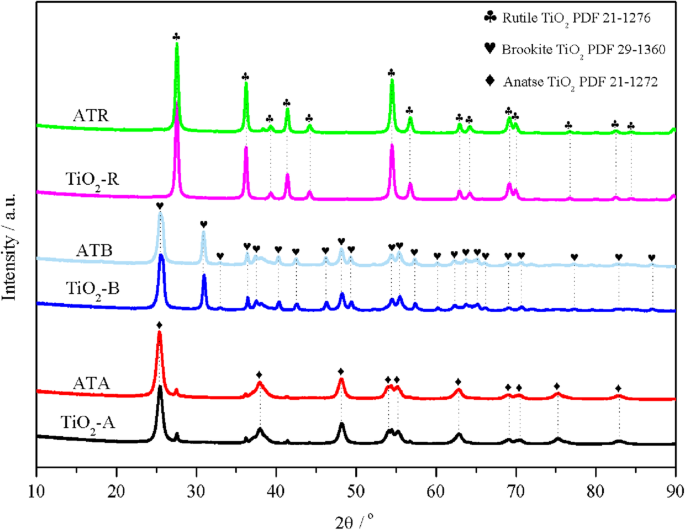
TiO2-A、ATA、TiO2-B、ATB、TiO2-R和ATR样品的XRD图
为了确定所制备的 Au-Pd/TiO2 催化剂上 Au 和 Pd 的实际含量,进行了 ICP-AES。相应的结果列于表 1。发现实际块体金属浓度低于标称值,这可能是由于过滤或洗涤过程中弱吸附的 Au-Pd 纳米颗粒浸出所致。
<图>XPS 作为一种表面敏感探针技术,用于检测表面元素组成和化学状态。图 2 显示了负载在 TiO2 催化剂上的 Au-Pd 纳米粒子的 Au (4f)、Pd (3d)、O (1 s) 和 Ti (2p) 光谱。如图 2.1 所示,在每个催化剂的两个位置检测到 Au 4f 光谱,但两个峰的具体位置略有不同。人们普遍认为,金属态 Au 4f 光谱通常显示出两种贡献(4f7/2 和 Au 4f5/2),分别位于 84.0 和 87.7 eV [14]。观察到的这三种 Au-Pd/TiO2 催化剂的 Au 4f 光谱负移可以通过 Pd 物种对 Au 物种的电子修饰来解释,这也表明 Au 和 Pd 物种之间的强相互作用。此外,在制备的Au-Pd/TiO2催化剂上未检测到离子型Au物质。
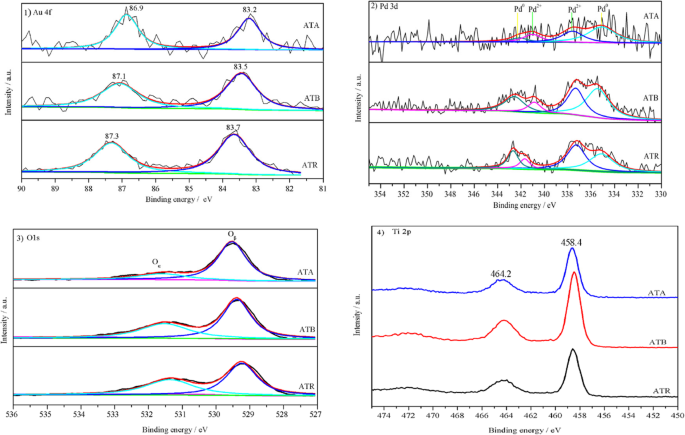
(1 ) 金 4f , (2 )Pd 3d, (3 ) O1 和 (4 ) Ti 2p) 对于 ATA、ATB 和 ATR 样本
图 2.2 显示了 ATA、ATB 和 ATR 样品的 Pd 3d 核心水平区域的 XPS 光谱。根据之前的报道,Pd 3d 的波段可以解卷积为四个子峰;在 335 和 341 eV 附近的 Pd 3d3/2 和 3d5/2 峰归因于金属 Pd 0 [15] 以约 337 和 342 eV 为中心的 Pd 3d5/2 和 3d7/2 归因于 Pd 2+ [16]。显然,Pd 0 和 Pd 2+ 根据分析结果,共存于催化剂表面。 Pd 2+ 的百分比 通过XPS拟合区域Pd 2+ 得到Au-Pd/TiO2催化剂上的物种 /(Pd 2+ +Pd 0 )。 Pd 2+ 的内容 在催化剂表面上的排列顺序如下:ATR (55.4%)> ATB (48.2%)> ATA (34.8%)。一般认为 Pd 2+ 的形成 催化剂表面的物质与干燥和煅烧过程密切相关[17]。然而,较高的 Pd 2+ ATR和ATB表明TiO2载体在促进Pd 2+ 的形成中也发挥了重要作用 , 可提供氧气以辅助 Pd 2+ 的产生 . Pd 2+ 的存在 物种进一步证明一些 Pd 不能与 Au 合金;这种现象在类似的Au-Pd/CeO2催化剂中已有报道[18]。
O1s 在 ATA、ATB 和 ATR 催化剂上的 XPS 光谱如图 2.3 所示。据报道,O1s 峰可以拟合成两个子峰。较低带能(529.1 eV)的子带可归因于晶格氧(Oβ),而较高结合能(531.0 eV)的子带可归因于表面吸附的氧(Oα)。在传统的催化氧化反应中,由于其较高的迁移率,表面吸附的氧通常比晶格氧表现出更高的反应性 [19]。因此,这三种 Au-Pd/TiO2 催化剂的 Oα 比率通过 XPS 拟合面积 Oα/(Oα+Oβ) 计算。发现 ATR 上的 Oα 比率(43.8%)高于 ATB(38.7%)和 ATA(20.2%)上的 Oα 比率。 Oα比值还可用于估算催化剂表面氧空位的含量,这在稳定催化剂上的Au-Pd纳米颗粒和提高催化活性方面起着关键作用。 Oα比值与Pd 2+ 一致 催化剂表面的浓度。图 2.4 显示了 Ti2p XPS 光谱。峰集中在大约 464.2 和 458.4 eV;这可能归因于 Ti 4+ 的 Ti 2p1/2 和 Ti 2p3/2 分别在 TiO2 中,表明 Ti 的氧化态为 +4 [20]。
从 XPS 表征结果获得的表面原子浓度总结在表 2 中。 与通过 ICP-AES 测定的 Au-Pd 本体组成相比,可以发现 Au-Pd/TiO2 催化剂表面的 Au 含量低于相应的批量。除了 ATR 上的 Pd 之外,催化剂表面上 Pd 的浓度也表现出类似的趋势。根据确定的催化剂表面 Au 和 Pd 浓度,计算 Au/Pd 的摩尔比并按 ATA> ATB> ATR 排序。发现这些值低于标称和体相 Au/Pd 值,这表明金属纳米粒子和 TiO2 之间的相互作用与载体形式密切相关。
<图>进行TEM以研究催化剂的形态和催化剂表面上Au-Pd纳米颗粒的尺寸分布。相应的 TEM 图像和 Au-Pd 分布的直方图如图 3 所示。值得注意的是,测量了 100 多个纳米粒子以计算平均粒径。如图 3a 所示,在 ATA 催化剂上观察到的载流子团聚现象和 Au-Pd 纳米颗粒尺寸分布可以使用对数正态分布来描述,平均尺寸约为 4.6 nm。同时,发现板钛矿TiO2呈棒状,ATB上的Au-Pd纳米颗粒平均尺寸小于ATA上的纳米颗粒尺寸。这一结果与戴的报告一致[11]。对于 ATR 催化剂,Au-Pd 纳米粒子在催化剂表面的分散最均匀,平均粒径最小(4.1 nm)。 TEM结果表明平均粒径和粒径分布与催化剂载体的性质和形态密切相关。
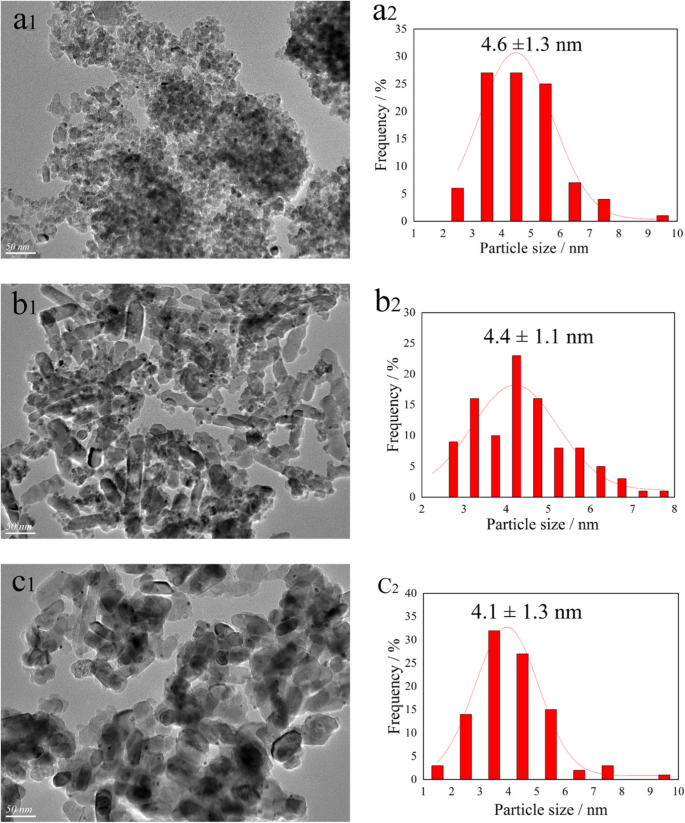
ATA 的 TEM 图像和 Au-Pd 粒度分布直方图 (a 1 , a 2 ), ATB (b 1 , b 2 ) 和 ATR (c 1 , c 2 ) 催化剂
催化活性测量
研究了负载在不同形式 TiO2 上的 Au-Pd 纳米粒子的苯甲醇氧化,在 0.3 MPa 纯氧和 120°C 下无溶剂条件下。相应的结果如图4所示。从图中可以看出,反应3 h后苯甲醇在ATR催化剂上的转化率达到了约65.11%。然而,在相同条件下,ATB 和 ATA 催化剂只能获得 60.01% 和 51.75% 的苯甲醇转化率。此外,发现在整个调查期间,苯甲醇转化可以按以下顺序排列:ATR> ATB> ATA。根据 XPS 表征结果,我们可以发现 Oα 和 Pd 2+ 比率也表现出相似的趋势,这表明 Oα 和 Pd 2+ 比率在决定催化性能方面起着关键作用。此外,TEM 结果表明在 ATR 上获得了更小的 Au-Pd 粒径,这也有助于提高催化活性。众所周知,苯甲醇氧化反应的主要产物是苯甲醛和甲苯,其余副产物有苯、苯甲酸和苯甲酸苄酯。所有这些产物都是在我们的实验中检测到的,典型情况列于表 3 中,这与已发表的 Au-Pd 固定催化剂上苯甲醇氧化的文献一致 [21, 22]。同时可以发现,在整个反应过程中,与ATA和ATB催化剂相比,ATR催化剂对甲苯的选择性更高,对苯甲醛的选择性更低(图5)。
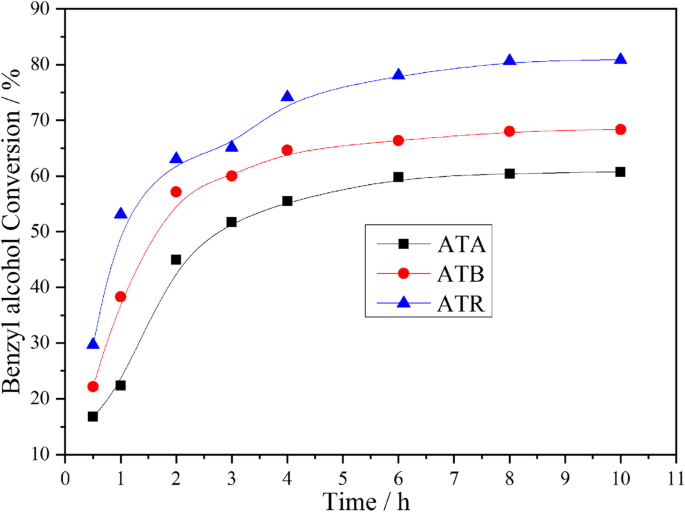
在 ATA、ATB 和 ATR 上实现的苯甲醇转化率随时间的变化
<图>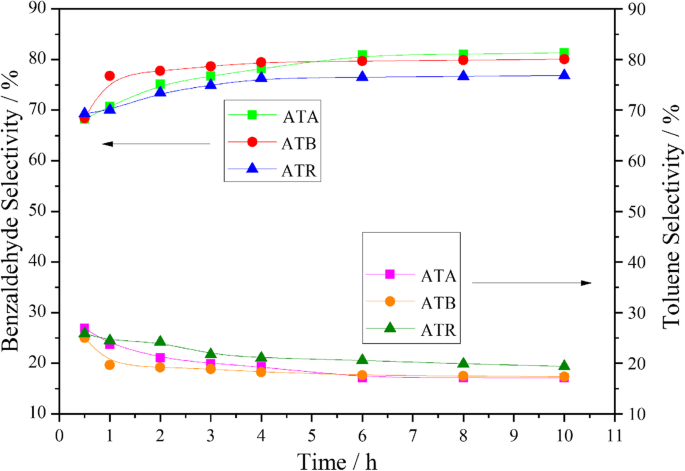
在 ATA、ATB 和 ATR 上获得的苯甲醛和甲苯选择性随时间的变化
为了进一步研究 Au-Pd/TiO2 催化剂在苯甲醇氧化中的稳定性,对 ATA、ATB 和 ATR 催化剂的催化性能进行了重复使用研究。相应的结果如图 6 所示。每次活性评估后,通过离心将催化剂从混合物溶液中分离出来,然后用丙酮洗涤,并在 80°C 下加热 16 h。发现与 ATR 样品相比,ATA 和 ATB 样品显示出更高的催化稳定性。在第一次、第二次和第三次循环中,ATA 催化剂的苯甲醇转化率分别为 51.28%、51.06% 和 51.49%,ATB 样品的苯甲醇转化率分别为 59.78%、59.54%、58.76%。然而,在每个循环后,ATR 样品的苯甲醇转化率均显着下降;催化活性从最初的 65.11% 下降到最终的 59.22%,这可能是由于 Pd 中毒。当催化剂在反应过程中被产物饱和时,Pd 中毒。据广泛报道,由于醛产物在催化剂表面的解吸问题,Pd 基催化剂很容易失活 [22,23,24,25]。在我们的案例中,通过 XPS 测量发现 ATR 在催化剂表面含有最高浓度的 Pd(0.65 原子%)。
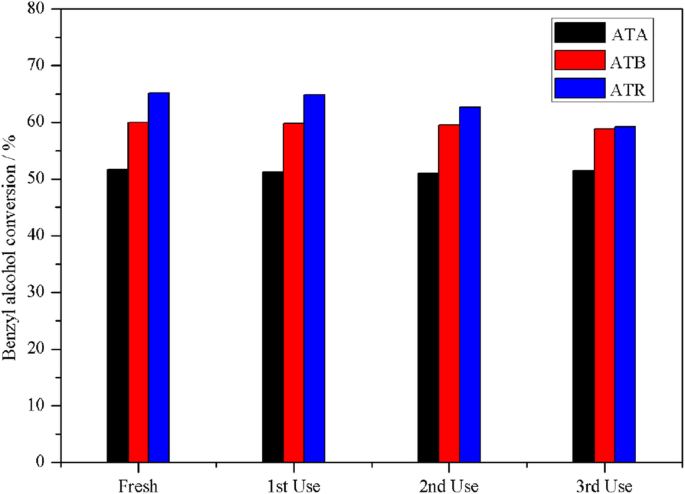
ATA、ATB和ATR催化剂在无溶剂苯甲醇氧化中的再利用
结论
总之,摩尔比为 1:1 的 Au-Pd 纳米粒子通过沉积-沉淀法沉积在不同形式的 TiO2 上。选择苯甲醇氧化作为探针反应以研究无溶剂下的催化活性。根据表征和活性评价结果,可以发现 Au-Pd/TiO2 催化剂的催化活性与 TiO2 形态密切相关。 XPS和TEM表征结果表明ATR表面含有较大的Oα和Pd 2+ 与 ATB 和 ATA 催化剂相比,Au-Pd 纳米颗粒尺寸更小,这在获得高苯甲醇转化率方面发挥了关键作用。然而,与ATA和ATB催化剂相比,ATR催化剂表现出较低的催化稳定性,这可能与反应过程中大量醛类产物覆盖在表面有关。
数据和材料的可用性
所有数据完全可用,不受限制。
缩写
- ATA:
-
Au-Pd/TiO2-锐钛矿
- ATB:
-
Au-Pd/TiO2-板钛矿
- ATR:
-
Au-Pd/TiO2-金红石
- FID:
-
火焰电离检测器
- GC:
-
气相色谱
- ICP-AES:
-
电感耦合等离子体原子发射光谱法
- 待定:
-
双(乳酸铵)二氢氧化钛
- TEM:
-
透射电子显微镜
- TiO2-A:
-
TiO2-锐钛矿
- TiO2-B:
-
TiO2-板钛矿
- TiO2-R:
-
TiO2-金红石
- XPS:
-
X射线光电子能谱
- XRD:
-
X射线粉末衍射
纳米材料
- 走向 TiO2 纳米流体——第 1 部分:制备和性质
- SrTiO3 改性金红石型 TiO2 纳米纤维的一步静电纺丝路线及其光催化性能
- Sb/坡缕石 (PAL) 纳米颗粒的制备和增强催化氢化活性
- 迈向 TiO2 纳米流体——第 2 部分:应用和挑战
- TiO2 中金纳米粒子分布对染料敏化太阳能电池光学和电学特性的影响
- 有机太阳能电池中纳米孔型和纳米柱型图案化金属电极的比较
- 用于有色冷色颜料的 Cr 掺杂 TiO2 的结构和可见近红外光学特性
- TiO2 纳米管阵列:由软硬模板制造和场发射性能的晶粒尺寸依赖性
- 使用表面光谱分析测定过渡金属掺杂的 TiO2 纳米颗粒的催化活性
- 一维混合二元氧化物 CeO2-LaO x 支持的金催化剂的合成和 CO 氧化活性
- 酸性胶溶剂对 TiO2 纳米颗粒锐钛矿-金红石比和光催化性能的影响
- 珩磨和研磨的比较


