根据 Fe3O4-Au 核壳纳米颗粒的多种抑制剂评估细胞摄取效率:控制结肠直肠癌细胞特定内吞作用的可能性
摘要
磁铁矿 (Fe3O4)-金 (Au) 核壳纳米粒子 (NPs) 具有独特的磁性和光学特性。当与生物部分结合时,这些 NP 可以为生物医学应用提供新的策略,例如药物递送和癌症靶向。在这里,我们提出了一种有效的方法,用于与生物部分相结合的磁性核壳 NP 系统的可控细胞吸收。波形蛋白是结构蛋白,已被生化证实可有效影响吞噬作用。此外,即使在生物部分的多重抑制下,波形蛋白也会影响外源物质内化到细胞中。在这项研究中,我们展示了使用生物部分组合进行表面改性的 Fe3O4-Au 核壳 NPs 的细胞内化性能。波形蛋白标记的 NPs 的光荧光在多次抑制测试中保持不受影响,表明 NPs 受制霉菌素、dynasore、细胞松弛素 D 甚至 Muc1 抗体 (Ab) 的影响最小。因此,该结果表明 Muc1 Ab 可以靶向特定分子并可以控制特定的内吞作用。此外,我们还展示了控制大肠癌细胞特异性内吞作用的可能性。
介绍
纳米材料为临床诊断和治疗开辟了新途径。特别是,纳米颗粒 (NPs) 是最重要的工具之一,已被用于生物传感器 [1, 2]、诊断 [3, 4] 和靶向给药系统 [5, 6] 等应用。对于生物医学应用,纳米颗粒通常由围绕核心材料表面的有机材料组成 [7,8,9]。由磁性材料、半导体材料或其他类型的材料组成的核心材料具有有用的物理化学性质,外有机表面为纳米颗粒提供化学稳定性和功能性。对于在生物靶向系统中的应用,不仅物理化学特性而且为靶向而生物功能化的外有机表面都是关键参数。用于功能化的靶向部分的例子是对靶标具有特异性的抗体或配体。根据外表面的生物功能化材料,确定了 NPs 的内吞机制。由于纳米颗粒在纳米医学应用中的重要性,NPs 进入细胞的机制已成为许多近期研究工作的主题[10,11,12,13,14,15]。
特别是,磁性 NPs 已广泛用于许多特定的位点靶向应用,包括细胞分选 [16, 17]、MRI [18]、DNA 分离 [19]、药物递送 [20]、热疗 [21] 和癌症目标 [22]。在各种磁性纳米颗粒中,磁铁矿纳米晶体因其生物相容性和化学稳定性而在生物医学应用中得到最广泛的应用。尽管已经为使用磁性纳米颗粒的生物医学应用做出了许多努力,但仍然存在一些关键问题,例如在水溶液中的良好分散性、功能性和生物相容性。为了克服这些问题,许多研究都集中在使用各种官能团(例如羧基和胺基团)对 NP 进行表面改性 [23]。然而,将官能团连接到磁铁矿纳米颗粒表面是一个耗时且费力的过程。鉴于此,核壳型 Au 包覆磁性 NPs 具有吸引力,因为 Au 表面很容易与生物分子和有机材料连接。
特别是,磁芯-Au 壳纳米粒子的磁性能够实现磁分离,提高 MRI 成像的分辨率,并可应用于热疗。此外,金优越的化学结合特性有利于构建受体介导的特定癌症靶向递送系统[24,25,26]。
在过去的几十年里,许多研究人员报道了受体介导的癌症靶向递送系统[27,28,29]。
受体介导的癌细胞靶向是主动靶向的一种形式。靶标的选择是有效主动靶向的关键,靶标必须在细胞外膜上过表达。大多数研究人员已将单克隆抗体用于癌症治疗,当单克隆抗体治疗与常规化疗相结合时,治疗效果可大大提高[30]。尽管单克隆抗体治疗取得了成功,但单克隆抗体在癌症靶向方面存在一些局限性。它们的大尺寸(大约 150 kDa)是肿瘤渗透的主要障碍 [31, 32],并且它们的低稳定性和低溶解度阻碍了它们的广泛应用 [33]。它们在靶向载体上的不均匀方向也被认为是非特异性结合的障碍。为了产生具有改善的肿瘤渗透性的抗体,已经设计和测试了广泛的抗体形式[34]。除了经典抗体外,骆驼科物种中还存在一种独特的抗体形式。所谓的重链抗体 (HCAb) 天然存在于这些物种的外周血和乳汁中。这种 HCAb 的抗原结合片段由一个单一结构域组成,即骆驼科动物 HCAb (VHH) 的重链可变结构域 (VH)。在细菌或真菌中克隆和表达后重组获得的 VHH 称为纳米抗体。它的分子量为 11–15 kDa,是所有 mAb 中最小的抗体 [35,36,37]。不仅它们的小尺寸使其可能适合作为针对孤立位置抗原的靶向探针,而且其易于修饰的末端对于癌症靶向应用具有吸引力。
具有适当靶向和细胞内化的纳米颗粒的有效递送也是递送系统中的重要因素。据报道,波形蛋白作为病原体附着和细胞内进入途径的组成部分发挥着重要作用。波形蛋白基因表达的沉默抑制吞噬作用 [38],而裂解的波形蛋白是一种显着增加吞噬作用的信号 [39]。因此,中和由细胞表面波形蛋白引起的细胞吞噬抵抗对于纳米颗粒的高效递送具有重要意义。
在这项研究中,我们研究了用不同长度的 PEG(聚乙二醇)间隔物修饰的纳米体标记的 Fe3O4-Au 核壳 NPs 的内吞途径。生化实验中已知对吞噬作用有很强作用的波形蛋白[39]作为对照,证实其有效作用于细胞内化NPs。此外,Muc1 是一种细胞表面糖蛋白,在胰腺癌、乳腺癌、肺癌和胃癌等多种癌症中过表达,被用作癌症靶向生物标志物。我们证实了 Fe3O4Au 核壳 NPs 的有效内化以及通过结肠细胞中 Muc1 受体介导的内吞作用途径可控靶向癌细胞的方法。
材料和方法
材料
醋酸金(III)(Au(OOCCH3)3,99.9%)得自Alfa Aesar。其他化学品包括乙酰丙酮铁 (III) (Fe(acac)3, 99.9%)、1,2-十六烷二醇 (C14H29CH(OH)CH2(OH), 90%)、聚(乙二醇)-嵌段-聚(丙二醇) )-嵌段聚(乙二醇)(PEG-PPG-PEG)和辛基醚(C8H17OC8H17,99%)购自 Sigma-Aldrich 并按原样使用。 α-吡啶基-2-二硫-ω-羧基琥珀酰亚胺酯聚(乙二醇)(OPSS-PEG-NHS)(2K、5K 和 10K)购自 Nanocs。碳酸氢钠、WST-1、氯丙嗪、制霉菌素、细胞松弛素 D、dynasore、布雷菲尔德菌素 A (BFA)、莫能菌素和台盼蓝购自 Sigma-Aldrich。 Cy3 和 Cy7.5 购自 Lumiprobe。 Anti-Muc1 Ab 购自 Abcam Inc. (Cambridge, MA)。磷酸盐缓冲液(PBS)、Dulbecco's改良Eagle's培养基、胎牛血清购自Invitrogen Corp.
Fe3O4-Au 核壳纳米粒子的合成
Fe3O4-Au 核壳纳米粒子是通过纳米乳液法合成的。核壳 NPs 的合成过程包括两个步骤:(1)Fe3O4 核 NPs 的形成和(2)在磁性 NPs 上涂覆 Au 壳。在第一步中,Fe3O4 NPs 由 Fe(acac)3(0.1766 g 或 0.5 mmol)、1,2-十六烷二醇(0.6468 g 或 2.5 mmol)和嵌段共聚物(聚(环氧乙烷) -聚(环氧丙烷)-聚(环氧乙烷);PEO-PPO-PEO)(0.4 ~ 1.2 g)在辛醚中。将混合溶液在 300 °C 下加热以还原 Fe 前体。通过冷却加热的溶液完成 Fe3O4 核 NPs 的形成。在磁芯形成之后,没有任何净化过程连续进行第二个过程。将 Au 前驱体(0.2338 g 或 0.62 mmol)和 1,2-十六烷二醇(0.88 g,3.4 mmol)加入由 Fe3O4 NPs 组成的乳液中,然后将混合溶液在 230 °C 下加热。冷却至室温后,离心沉淀乳液,分离核壳纳米颗粒。
重组抗Muc1-VHH 5-24 K10表达载体的构建
使用正向引物 5'-CCGAATTCGCCGATGTGCAGCTGACCGAG-3' 和反向引物 5'-CGG CTCGAGCTTCTTCTTCTTCTTCTTCTTCTTCTTCTTGCCTGAGGAGACGGTGACCTG-3' 进行聚合酶链反应 (PCR)。 PCR 产物用 EcoRI 和 XhoI 消化,并使用 QIA 快速凝胶提取试剂盒(QIAGEN,Valencia,CA,USA)进行凝胶纯化。将纯化的 PCR 产物克隆到 EcoRI/XhoI 消化的 pET-23a (Novagen, Darmstadt, Germany)。 大肠杆菌 (大肠杆菌 )DH5α(RBC Bioscience,Xindian,Taiwan)通过热休克用得到的构建体转化,并在含有 100 μg/mL 氨苄青霉素(Duchefa Biochemie,Haarlem,The Netherlands)的 LB 琼脂平板上进行选择。
重组蛋白的表达与纯化
为了表达和纯化重组抗 Muc1-VHH 5-24 K10 蛋白,E.大肠杆菌 BL21 菌株(RBC Bioscience,Xindian,Taiwan)用 pET-23a-anti-Muc1-VHH 5-24 K10 转化。然后细菌在含有氨苄青霉素 (100 μg/mL) 的 LB 肉汤中生长。蛋白质表达由异丙基 β-d-硫代半乳糖苷 (IPTG) (Duchefa Biochemie, Haarlem, The Netherlands) 在 37 °C 下以 0.4 mM 的终浓度诱导 5 小时。将细菌沉淀重悬在裂解缓冲液(50 mM NaH2PO4,pH 8.0;300 mM NaCl)中,然后在冰上超声处理 10 分钟。超声裂解液以 20,000×g 离心 在 4 °C 下持续 20 分钟,然后使用 Ni-NTA His·Bind 树脂(Peptron,大田,韩国)。用洗脱缓冲液(50 mM NaH2PO4,pH 8.0;300 mM NaCl;150 mM咪唑)洗脱与树脂结合的带His标签的蛋白质。纯化后的蛋白在15% SDS-PAGE凝胶上分离。
核壳 Fe3O4-Au 纳米颗粒的改性
将不同长度(2、5 和 10 K)的 OPSS-PEG-NHS 溶解在 0.1 M 碳酸氢钠中以激活硫醇基团。将活化的 OPSS-PEG-NHS 添加到合成的核壳 Fe3O4-Au NPs 溶液中,并在 4 °C 下搅拌 12 小时。活化的 OPSS-PEG-NHS 的硫醇基团共价连接到核壳 NPs 的 Au 表面。然后,将纳米抗体溶液 (0.25 mg/mL) 添加到聚乙二醇化的 Fe3O4-Au 核壳 NPs 中,在 4 °C 下保持 12 小时。在pH 8.3时,末端的十个赖氨酸(K)尾的胺基团与OPSS-PEG-NHS的NHS基团共价连接。 Cy3和Cy7.5被标记到纳米抗体的残留氨基上。
内化曲线
CT26细胞以5×10 3 接种 在透明底部 96 孔板中每孔培养细胞,并在 250 μL 培养基中,在 37 °C 和 5% CO2 中避光培养 24 小时。去除培养基,并在每个孔中加入 250 μL 的新鲜培养基,其中含有 50 μg/mL Cy3 标记的 Fe3O4-Au NPs 和 PEG-Cy3 或 PEG-纳米抗体-Cy3 标记的 NPs。将细胞进一步孵育不同的时间段(0、10、20、30、60、120 和 360 分钟)。然后用 PBS 洗涤细胞 3 次以去除游离的 NP,并通过 SpectraMAX GEMINI(Molecular Devices,CA,USA)用台盼蓝作为膜不可渗透的荧光猝灭剂测量每个孔的荧光。每个实验用等量的NPs(50 μg/mL)进行,重复3次[40]。
抑制测试
CT26细胞以5×10 3 接种 在透明底部 96 孔板中每孔培养细胞,并在 250 μL 的培养基中在 37 °C 和 5% CO2 条件下避光孵育 24 小时。除去培养基并加入 250 μL 新鲜培养基,其中含有 20 μg/mL 氯丙嗪 (CPZ)、50 μg/mL 制霉菌素、20 μg/mL 细胞松弛素 D、25 μg/mL dynasore、20 μg/mL BFA, 20 μg/mL B加入mL莫能菌素或5 μM抗Muc1 Ab,孵育细胞1 h。
再次去除培养基,加入250 μL培养基,其中含有50 μg/mL Cy3-标记的Fe3O4-Au NPs、PEG-Cy3-标记的NPs、PEG-纳米抗体-Cy3-标记的NPs或波形蛋白-Cy3-标记的NPs .
在 37 °C 和 5% CO2 条件下 1 h 后,用 PBS 洗涤细胞 3 次以去除游离 NPs,并通过 SpectraMAX GEMINI (Molecular Devices, CA, USA) 用台盼蓝作为膜不可渗透的荧光猝灭剂测量荧光)。每个实验用等量的NPs(50 μg/mL)进行,重复4次。
结果与讨论
核壳纳米颗粒是通过公开的方法合成的 [16, 17]。图 1a、b 中的透射电子显微镜 (TEM) 观察表明 Fe3O4-Au 核壳纳米颗粒呈球形,平均直径为 13.5 nm,粒径分布窄。
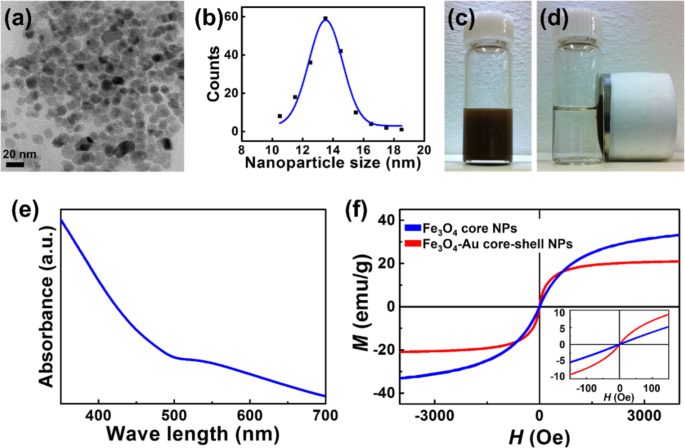
合成的 Fe3O4-Au 核壳 NPs 的表征。 一 , b 合成的 Fe3O4-Au 核壳 NPs 的 TEM 观察。 c , d 在施加外部磁场之前和之后,水溶液中的纳米颗粒。 e 合成的核壳 NPs 的紫外吸收峰出现在 ~ 530 nm。 f Fe3O4核磁滞回线
核NP(Fe3O4)从~ 8.5 nm的增加源于核表面上~ 2.5nm厚的Au壳的涂层,导致核壳NP。 Fe3O4-Au 核壳 NP 的快速傅立叶变换 (FFT) 分析的高分辨率 TEM 图像包含在补充信息图 S1 中。
有机溶剂制得的产物经磁分离纯化后转移至水中。
由于纳米颗粒上存在残留的嵌段共聚物,核壳纳米颗粒在没有任何表面改性的情况下在水中分散良好且稳定。
图 1c 和 d 显示了在施加外部磁场之前和之后水溶液中的纳米颗粒。在外磁场作用下,核壳纳米颗粒迅速从均匀的分散体(图1c)转变为清澈透明的溶液(图1d)。
使用 UV-Vis 光谱法研究核壳 NPs 的吸收带。如图1e所示,吸收峰出现在~530 nm处,表明纳米颗粒表面存在Au(补充信息图S2包括Fe3O4-Au核壳纳米颗粒的EDX数据结果)。随着样品的纯化,光学结果表明形成了核壳结构。
通过振动样品测量获得磁滞回线,以研究 Fe3O4 核和核壳 NP 的磁性。两种纳米颗粒均表现出超顺磁性,室温下矫顽力接近0 Oe(图1f)。
正如之前的工作所报道的,核壳 NPs 的磁化率高于磁铁矿 NPs,部分原因可能是邻近效应和独特的空间配置 [41, 42]。此外,核NPs和核壳NPs的饱和磁化强度分别为~37 emu/g和~21 emu/g,在10 kOe下。 Ms的差异源于核壳NPs中存在非磁性成分(Au)。
VHH 5-24 K10 基因被框内克隆以在 PCR 扩增后产生 pET-23a-anti-Muc1-VHH 5-24 K10(图 2a)。重组蛋白在大肠杆菌中表达。大肠杆菌 BL21用IPTG诱导后用pET-23a-anti-Muc1-VHH 5-24 K10转化,经Ni-NTA His·Bind Resin纯化。重组抗 Muc1-VHH 5-24 K10 在大肠杆菌中很容易表达。大肠杆菌 作为可溶性 18-kDa 蛋白质。从 1-L 培养物中,我们获得了 1 ± 0.5 mg 纯化的重组抗 Muc1-VHH 5-24 K10。
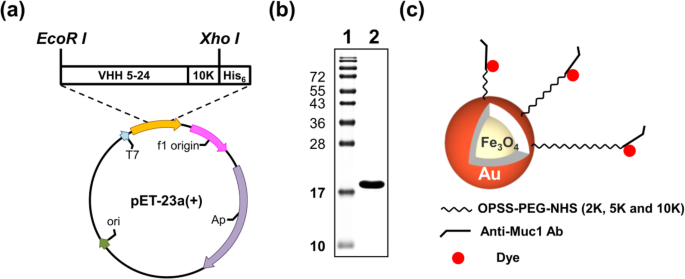
抗Muc1-VHH 5-24 K10融合蛋白的表达和纯化。 VHH 5-24 K10 基因框内克隆产生a b 后 pET-23a-anti-Muc1-VHH 5-24 K10 Muc1-VHH 5-24 K10 融合蛋白的纯化。在 15% SDS-PAGE 上分离纯化的蛋白质。泳道 1 蛋白质阶梯。泳道2纯化的蛋白质。 c 本研究中使用的PEG-纳米抗体染料标记的NPs示意图
纯化的蛋白质通过 15% SDS-PAGE 凝胶验证。纯化蛋白质的考马斯蓝染色显示其纯度> 95%(图 2b)。合成的 Fe3O4-Au NPs 分三步进行修饰,即聚乙二醇化、抗体标记和染料标记(图 2c)。在每个修改步骤之后,测量 zeta 电位以确认修改成功。表 1 显示了修饰对相应 zeta 电位的影响。裸核壳 NP 的 zeta 电位为 - 19.8 ± 6.68 mV。使用 OPSS-PEG-NHS 进行 NPs 的聚乙二醇化。为了制备一系列不同尺寸的纳米复合物,使用了不同长度(2 K、5 K和10 K)的OPSS-PEG-NHS。
<图>PEG化后,zeta电位降低(分别为-44.9±8.19 mV、-40.7±7.88 mV和-39.6±8.74 mV,分别为2 K、5 K和10 K)。
有趣的是,在纳米抗体标记后,zeta 电位明显增加(对于 2 K、5 K 和 10>K,分别为 - 38.5 ± 5.61 mV、- 23.3 ± 8.61 mV 和 - 31.8 ± 7.37 mV)。
染料标记后,zeta 电位也增加(分别为 - 12.5 ± 7.25 mV、- 17.7 ± 3.94 mV 和 - 10.6 ± 4.72 mV,分别为 2、5 和 10 K)。
裸 Fe3O4-Au 核壳 NPs 的 zeta 电位为 - 19.8 ± 6.68 mV。聚乙二醇化后,zeta 电位降低到接近 - 40 mV。这些结果表明 PEG 分子与核壳 NP 的 Au 壳共价键合良好,因为 PEG 分子具有带负电荷的 N-羟基琥珀酰亚胺官能团。同时,在对纳米抗体进行染料标记后,zeta 电位增加(NP-PEG2 K-纳米抗体为-38.5±5.61 mV,NP-PEG2 K-纳米抗体-染料为-12.5±7.25 mV)。这个结果是合理的,因为重组纳米抗体在末端有十个赖氨酸尾巴。通过zeta电位测量对每种类型的纳米抗体进行分类,为了确定抗体与纳米抗体的结合,我们测量了每种纳米抗体类型的荧光。
如图 3 所示,我们证实所有类型的纳米颗粒和纳米抗体在没有抑制剂限制的情况下都具有良好的细胞吸收和内化。从在 50 μg/mL Cy3 标记的 Fe3O4-Au NP、PEG-Cy3 标记的 NP 和 PEG-纳米抗体-Cy3 标记的 NP 存在下培养不同时间(0 到 360 分钟之间)的细胞获得细胞内化曲线)除去培养基,洗掉游离的NPs,最后用台盼蓝测量细胞的总荧光(图3)。
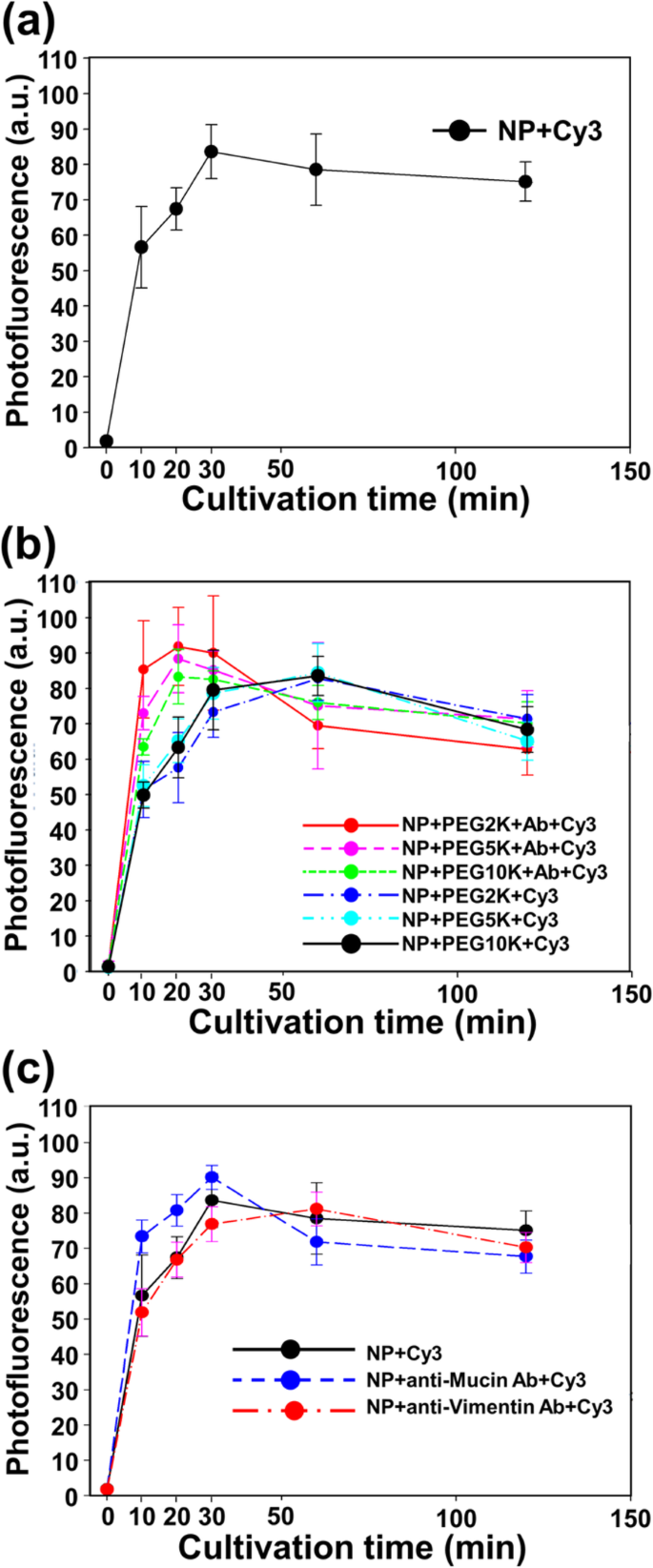
与 50 μg/mL a 孵育后 CT26 粘蛋白细胞的归一化光荧光 Fe3O4-Au 纳米粒子,b 聚乙二醇化 NPs 和 PEG 纳米抗体标记的 NPs,以及 c Fe3O4-Au NPs、纳米抗体标记的 NPs 和波形蛋白标记的 NPs 在 37 °C 和 5% CO2 中不同时期(10、20、30、60、120 和 360 分钟)
根据荧光强度测量结果,我们可以确定纳米颗粒在 1 h 内被内化到细胞中(图 3a)。 NP的荧光强度在1 h内达到最大值,达到稳态后荧光强度逐渐降低。尽管根据 Ab 的存在存在轻微的时间差异,但每个培养时间的荧光强度与裸 NP 的结果没有显着差异(图 3b)。如图3c所示,通过使用Muc1和波形蛋白的异质性Ab,证实了Ab对NP的细胞摄取和内化的影响可以忽略不计。
使用 WST-1 测定,根据 Fe3O4-Au 核壳 NPs 的浓度和表面改性,在不同的暴露时间后估计 CT26 粘蛋白细胞的活力(%)(图 4a,b)。 CT26 细胞的活力在暴露 24 小时和 48 小时后没有显示出任何显着差异,无论是在不同剂量下还是在 NPs 表面改性后。裸Fe3O4-Au NPs(图4a)和表面修饰的NPs(图4b)的细胞活力均大于90%。
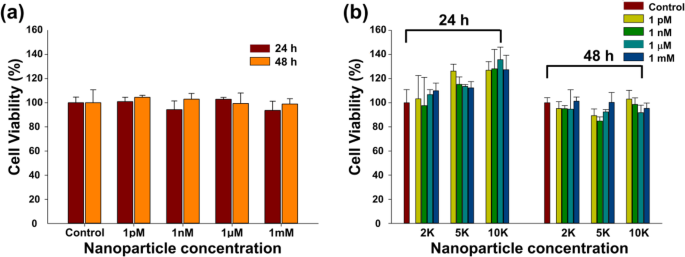
用不同浓度的裸 Fe3O4-Au 核壳 NPs 和表面修饰的 Fe3O4-Au NPs 处理的 CT26 粘蛋白细胞的活力。 一 Fe3O4-Au NPs 和 b PEG-纳米抗体-Cy3 标记的 NP。每个实验图代表一系列四个不同实验的平均值
图 5 表明 NPs 通过各种内吞途径(网格蛋白介导的、小窝介导的和吞噬作用/巨噬细胞作用途径)进入 CT26 粘蛋白细胞。有趣的是,图 5b 显示抗 Muc1 Ab 也主要影响 PEG-纳米抗体-Cy3 标记的 NPs 的内吞作用。为了了解 NP 内化的途径,我们尝试用特定的化学抑制剂抑制内吞途径(图 5)。众所周知,内吞作用的途径分为三种类型:网格蛋白介导的、小窝介导的和巨胞饮/吞噬作用。
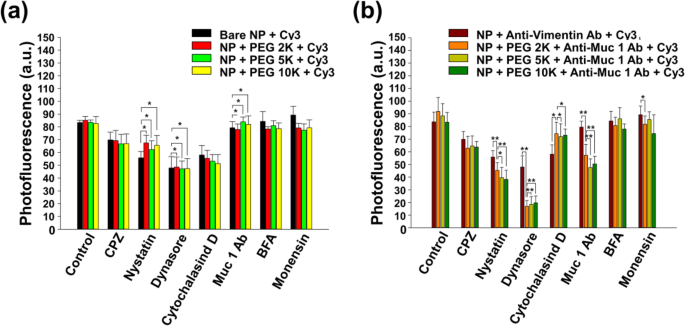
用化学内吞抑制剂处理 1 h 并与 50 μg/mL a 孵育的 CT26 粘蛋白细胞的归一化光荧光 裸核壳 NPs 和 b 纳米抗体标记的 NPs 在 37 °C 下在 5% CO2 中保持 30 分钟。对内化有统计影响的抑制剂(Student's t 测试,p (*) <0.05 和 p (**) <0.01) 用黑色星号标记
在这项研究中,抑制剂被用作研究纳米抗体标记 NP 内在化的第一种方法。 CPZ(网格蛋白介导的内吞作用抑制剂)、制霉菌素(小窝介导的内吞作用抑制剂)、dynasore(动力蛋白抑制剂)、细胞松弛素 D(吞噬作用/巨噬细胞作用抑制剂)、BFA(高尔基体破坏剂)、莫能菌素(溶酶体抑制剂)或抗 Muc1 Ab(受体/转运蛋白特异性竞争物)与细胞一起孵育 1 小时。 CPZ、制霉菌素、dynasore和细胞松弛素D影响NPs的内吞作用(图5a)。
靶向部分是癌症靶向成功的关键,这在癌症治疗中尤为重要。对于靶向,有效的表面修饰对于提高治疗效率和限制副作用非常重要。纳米抗体标记的 Fe3O4-Au 核壳 NPs 成功地由合成的 NPs 和重组纳米抗体制成。表1清楚地表明,每个修改步骤都成功进行。
细胞活力是纳米材料生物应用的基本要素之一。裸核-壳纳米颗粒和修饰纳米颗粒的细胞活力大于 90%(图 4a、b)。这些结果表明裸Fe3O4-Au NPs和修饰的NPs不会引起显着的浓度和修饰依赖性细胞毒性,修饰的NPs适合生物应用。
NPs 的内化效率和抑制作用的研究为了解 NPs 进入细胞的机制提供了重要信息。与裸 NP 相比,聚乙二醇化 NP 内化到细胞中的速度相对较慢,但纳米抗体标记的 NP 内化到细胞中的速度略快于裸 NP(图 3a、b)。由于聚乙二醇化是众所周知的防止纳米颗粒内化的表面修饰方法,因此很容易解释聚乙二醇化纳米颗粒的内化趋势。此外,纳米抗体诱导了 NPs 的内吞作用。为了检查纳米抗体的特异性,我们确认了波形蛋白 Ab 标记的 NP 的内化率。有趣的是,波形蛋白 Ab 标记的 NPs 没有促进细胞内化(图 3c)。
这些结果表明纳米抗体可以有效地诱导纳米材料内化到 CT26 粘蛋白细胞中,并暗示可以通过对纳米颗粒外膜的特定修饰来控制内化趋势。此外,通过抑制测试和共聚焦显微镜成像清楚地显示了纳米抗体标记的 NPs 的内吞机制。当与 CPZ、制霉菌素或 dynasore 一起培养时,纳米抗体标记的 NPs 和未标记的 NPs 的光荧光显示出相似的下降值(图 5a、b)。 CPZ、制霉菌素和 dynasore 分别在抑制网格蛋白介导的内吞作用、小窝介导的内吞作用和动力蛋白中发挥作用,动力蛋白是一种大型 GTP 酶,参与新生囊泡从母膜的出芽和断裂。因此,两种情况下的光荧光值都迅速下降,因为动力蛋白与网格蛋白介导和小窝介导的内吞作用的囊泡的产生密切相关。如图 5a 所示,未标记的(图 5a)和纳米体标记的 NPs(图 5b)均显示出光荧光的快速下降。
特别是,带有纳米抗体标记的 NPs 在 CPZ、制霉菌素和 dynasore 中显示出显着较低的光荧光值。此外,我们证实,当应用于细胞松弛素 D 时,未标记的 NP 比纳米体标记的 NP 受到的影响更大,细胞松弛素 D 是一种细胞渗透性毒素,可阻止肌动蛋白丝的聚合以进行吞噬作用 [43]。这些结果意味着未标记的 NPs 通过多种机制被内化,例如网格蛋白介导的内吞作用、小窝介导的内吞作用和吞噬作用。因此,纳米抗体标记的 NPs 的细胞内化取决于网格蛋白介导和小窝介导的内吞作用。此外,当细胞与 Muc1 抗体一起培养时,纳米抗体标记的 NPs 的细胞摄取量显着减少(图 5b)。该结果表明,游离的 Muc1 抗体在附着于 CT26 细胞膜时作为纳米抗体的竞争者在修饰的 NPs 上发挥作用,并且 Muc1 抗体在修饰的 NPs 的细胞内化中起重要作用。奇怪的是,波形蛋白 Ab 标记的 NPs 与纳米抗体标记的 NPs 在抑制能力方面表现出明显的差异。波形蛋白标记的 NPs 的光荧光在多次抑制测试中保持不受影响,表明 NPs 受制霉菌素、dynasore、细胞松弛素 D 甚至 Muc1 Ab 的影响最小。这种现象可能是波形蛋白功效的证据,波形蛋白已被生化证实可有效影响吞噬作用 [39]。因此,该结果表明Muc1 Ab可以靶向特定分子并可以控制特定的内吞作用。
如图 6 所示,当细胞用 Cy7.5 标记的裸核壳 NP 和 PEG 纳米抗体标记的 NP 处理时,获得了类似的结果,表明在没有动力抑制的情况下,两种情况下的细胞摄取相似。与裸纳米颗粒相比,Dynasore 抑制显着降低了带有 PEG 纳米抗体标签的纳米颗粒的细胞内化(图 6b,底行)。这些结果意味着存在两种内吞作用机制,即裸纳米颗粒的非特异性内吞作用和纳米抗体标记的纳米颗粒通过动力分子的限制内吞作用。一旦纳米抗体附着在外部细胞膜上,由于网格蛋白和小窝蛋白介导机制的同时激活,纳米抗体标记的 NPs 可以很容易地穿过细胞膜。因此,我们可以假设主要机制是网格蛋白和细胞膜穴样内陷介导的内吞作用,用于纳米抗体标记的纳米颗粒在 CT26 粘蛋白细胞中的内化。
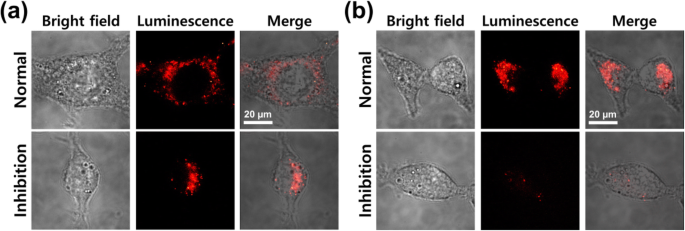
用a孵育的CT26粘蛋白细胞的共聚焦显微成像 Fe3O4-Au NPs 和 b PEG-nanobody-tagged NPs 在 37 °C、5% CO2 培养箱中 1 h,在抑制dynasore 之前和之后 (1 ng/mL)
结论
Nanomaterials for cancer targeting and controllable insertion of exogenic materials such as drugs, genes, and peptides are critical advances in biomedical applications. These familiar but creative concepts can offer strategies for new therapeutic methods. In this paper, we demonstrated enhanced cellular uptake of Fe3O4-Au core-shell NPs after PEGylation with the Muc1 antibody. The main endocytosis mechanisms of nanobody-tagged NPs were demonstrated, showing the possibility of controllable specific endocytosis in colorectal cancer cells. These findings provide insight into the targeting between nanobody-tagged NPs and colorectal cancer cells to aid the design of high-efficiency targeting carriers.
数据和材料的可用性
本研究期间生成或分析的所有数据均包含在这篇已发表的文章中。
缩写
- Fe3O4:
-
Magnetite
- Au:
-
Gold
- NPs:
-
Nanoparticles
- Ab:
-
Antibody
- HCAbs:
-
Heavy-chain antibodies
- VHH:
-
VH of the camelid HCAb
- PEG:
-
Poly(ethylene glycol)
- PPG:
-
Poly(propylene glycol)
- PCR:
-
Polymerase chain reaction
- TEM:
-
透射电子显微镜
- PEO-PPO-PEO:
-
Poly(ethylene oxide)-poly(propylene oxide)-poly(ethylene oxide)
- OPSS-PEG-NHS:
-
Orthopyridyl disulfide PDP PEG succinimidyl ester
- BFA:
-
Brefeldin A
- CPZ:
-
Chlorpromazine
纳米材料
- 高效石墨烯太阳能电池
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 用于癌症应用的基于细胞的药物递送
- 纳米技术灭活癌症干细胞
- 使用多功能 GaN/Fe 纳米颗粒靶向内皮细胞
- 改性超支化聚甘油作为分散剂,用于控制和稳定碳氢化合物中的金纳米粒子
- 嵌入TiO2致密层的不同尺寸和浓度的Ag纳米颗粒对钙钛矿太阳能电池转换效率的影响
- 基于紫杉醇的靶向脂质纳米颗粒的抗增殖和细胞凋亡触发潜力,通过转铁蛋白受体增强细胞内化——白血病细胞研究
- 生长用于形状选择性细胞摄取的金纳米结构
- 石胆酸修饰的金纳米粒子对肝癌细胞的凋亡作用
- 氧化锆纳米粒子对成骨细胞样 3T3-E1 细胞的毒性作用
- 具有疏水修饰的普鲁兰多糖纳米颗粒的米托蒽醌新型递送抑制膀胱癌细胞以及纳米药物大小对抑制效率的影响


