磁性碳微球作为可重复使用的吸附剂从水中去除磺胺
摘要
【摘要】:以葡萄糖为碳源,Fe3O4纳米颗粒为磁性原料,采用水热法制备了新型可重复使用的磁性碳微球(MCMs)。并详细研究了 MCMs 对水中磺胺去除的吸附性能。结果表明,煅烧温度和煅烧时间对MCMs的表面积和体积孔隙率有显着影响。当 MCMs 在 600 °C 下煅烧 1 h 时,MCMs 的表面积和体积孔隙率为 1228 m 2 /g 和 0.448 m 3 /g,分别。吸附结果表明吸附数据符合Langmuir等温线模型,符合准二级动力学。当 pH 值从 4.0 变为 10.0 时,MCMs 对磺胺的吸附容量从 24.6 降至 19.2 mg/g。合成后的MCMs在重复使用4次后的吸附容量达到18.31 mg/g,表现出良好的吸附容量和重复使用性。
背景
药用抗生素在世界范围内被广泛用于治疗疾病和提高动物的生长速度。然而,近年来发现抗生素对水生环境有严重的不良影响,引起越来越多的关注[1,2,3]。在所有的抗生素中,磺胺类抗生素通常在临床、畜牧业和水产养殖中大量使用。它们非常稳定,在消化道中吸收较差,只有一小部分磺胺类抗生素被代谢或吸收。当它们排放到环境中时,经常在污水处理厂、地下水、地表水、土壤、沉积物等中检测到磺胺类抗生素[4,5,6]。磺胺类抗生素残留不仅会破坏环境,还会对人类健康构成重大威胁。因此,有必要研究有效去除水中这些抗生素残留的新技术。
碳材料因其化学惰性、生物相容性和热稳定性而备受关注 [7,8,9],并在分离、催化剂和吸附领域得到了广泛研究 [10,11,12]。然而,传统的碳材料在用作吸附剂时难以从溶液中分离。传统的方法主要是过滤和离心,特别是在工况复杂的情况下,不方便且效率低。近年来,随着纳米技术的发展,与纳米磁性材料相结合的碳材料,即磁性碳微球(MCMs)受到越来越多的关注,它可以很容易地使用磁铁进行分离。这些磁性碳复合材料已被用作去除水中污染物的吸附剂,如甲基蓝 [13] 和苯酚和硝基苯 [14]。朱等人。综述了磁性碳复合材料的合成与应用[15]。
在本文中,我们介绍了一种通过水热法合成具有高表面积的新型磁性碳微球 (MCM) 的新方法,其中以葡萄糖和 Fe3O4 纳米粒子为原料。并详细评价了MCMs对水中磺胺去除的吸附性能。
方法
化学品和材料
FeCl3·6H2O、乙醇、乙二醇、磺胺购自国药化学试剂有限公司 NaAc·3H2O、葡萄糖、KCl、NaOH、HCl购自南京化学试剂有限公司 ZnCl2购自西龙化工有限公司,所有实验均使用蒸馏水。
Fe3O4 纳米颗粒的制备
Fe3O4 纳米粒子是通过水热法制备的,如 [16] 中所报道。将 FeCl3·6H2O(1.35 克)和 NaAc·3H2O(3.60 克)溶解在 40 毫升乙二醇中形成均匀溶液,然后转移到内衬聚四氟乙烯的不锈钢高压釜(100 毫升容量)中,加热至 200°C 8 小时。冷却至室温后,所得产物分别用去离子水和乙醇洗涤3次。
MCM 的准备
将 0.1 g Fe3O4 纳米颗粒、适量葡萄糖和 60 mL 蒸馏水加入 100 mL 烧杯中,然后搅拌使 Fe3O4 纳米颗粒均匀分散。将溶液倒入 100 mL 高压釜中并加热至 200°C 11 小时。得到的MCMs用去离子水和乙醇洗涤两次。
MCM 浸入 40% ZnCl2 溶液中 [17, 18],然后在真空干燥箱中干燥。将合成的 MCM 放入管式炉中并在氮气氛下加热。因此,获得了煅烧和活化的 MCM。将得到的 MCM 洗涤,使用 50 mL 去离子水 5 到 8 次,直到 Zn 2+ 的浓度 小于0.05 mg/L,MCMs在真空干燥箱中干燥用于磺酰胺吸附。
特征化
MCM 使用透射电子显微镜(TEM,Tecnai 12 型,飞利浦公司,荷兰)和场发射扫描电子显微镜(FE-SEM,S-4800 型,日立公司,日本)进行表征。使用振动样品磁强计(VSM,7410 型,Lake Shore Co.,Ltd.,USA)在室温下测量 MCM 的磁特性。使用比表面积分析仪(Model Coulter SA3100,Beckman Co.,Ltd.,USA)进行氮吸附和解吸性能。使用Brunauer-Emmett-Teller(BET)方程计算表面积。表面zeta电位由zeta电位分析仪(ZS90,Malvern Instruments,UK)测量。
吸附程序
吸附实验在 50 mL 锥形瓶中在温控定轨振荡器(QHZ-98A,太仓生物仪器制造有限公司)中进行。为了减少磺胺光降解的可能性,所有锥形瓶都装有磺胺溶液,适当剂量的 MCM 用铝箔密封,并在室温 (300 K) 下以 120 rpm 的速度摇晃。吸附完成后,用磁铁将MCMs与磺胺溶液分离。通过紫外-可见分光光度计(UV-vis,Model 759S,China)在 258 nm 处测量磺胺的浓度和 MCM 的吸附能力(Q e , mg/g) 根据方程计算。 (1):
$$ {Q}_e=\frac{\left({C}_0-{C}_e\right)\times V}{m} $$ (1)其中 Q e 是平衡吸附容量(mg/g); C 0 和 C e 分别表示磺胺的初始浓度和平衡浓度 (mg/L); V 是磺胺溶液的体积 (50 mL); 米 为吸附剂 MCM 的质量 (mg)。
MCM 的复用方法
为了评估 MCM 的可重复使用性,将 1 g/L MCM 添加到 25 mg/L 磺胺溶液中,模拟其在制药厂排水中的浓度。当吸附达到平衡时,计算 MCM 的吸附容量。吸附的 MCM 可以在蒸馏水中分离分散,加入 0.1 mol/L NaOH 解吸至 pH 值达到 10.0,然后在 500 W 超声 10 分钟,重复该过程 3 次 [19, 20]。然后用蒸馏水反复洗涤MCMs,直到pH =7。在所有的实验中,MCMs都被用来从水溶液中分离MCMs。
结果与讨论
MCM 的 TEM
Fe3O4纳米/微球和MCM的TEMs如图1所示。
<图片>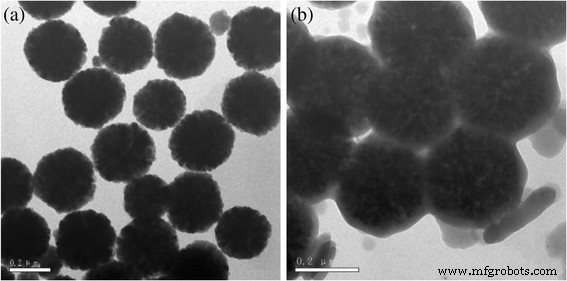
TEM 图像。 一 Fe3O4 纳米/微球。 b MCM
如图 1a 所示,Fe3O4 纳米/微球的尺寸约为 200 nm,并且分散均匀。 Fe3O4 纳米/微球通过水热法与葡萄糖反应后,碳覆盖在 Fe3O4 微球表面(图 1b)。同时,形成了一些碳微球,这与 Cakan 等人先前的工作一致。 [21].
MCM 的 FT-IR 和 XRD 光谱
所得产物 Fe3O4 纳米/微球和 MCM 的 FT-IR 和 XRD 谱如图 2 所示。
<图片>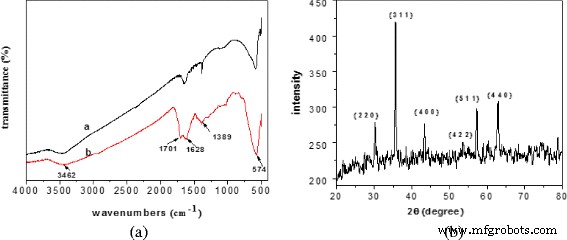
所得产物的 FT-IR 和 XRD 谱。 一 FT-IR 光谱(a:Fe3O4,b:MCM)。 b Fe3O4 的 XRD 谱
得到的 Fe3O4 和 MCM 在 574 cm -1 附近有吸附峰 ,这是 Fe3O4 的特征峰。在 3462 cm -1 附近有一个很宽的吸收峰 对于 Fe3O4 和 MCMs,这表明生成的 Fe3O4 和 MCMs 具有 -OH 官能团。 1701 和 1621 cm −1 的峰值 羰基和烯烃的振动吸收是由于葡萄糖在水热法中碳化所致。
发现所有的反射峰都可以归于(2 2 0)、(3 1 1)、(4 0 0)、(4 2 2)、(5 1 1)和(4 4 0)的衍射) 立方结构的 Fe3O4 晶面 (JCPDS no. 19-0629),表明形成了磁铁矿纳米颗粒 [22]。
MCM 的表面积和多孔体积
制备的 MCM 的 N2 吸附-解吸等温线及其相关的 Brunauer-Emmett-Teller (BET) 孔径分布如图 3 所示,它们的 BET 表面积参数 (S BET)、孔体积和孔径列于表 1。
<图片>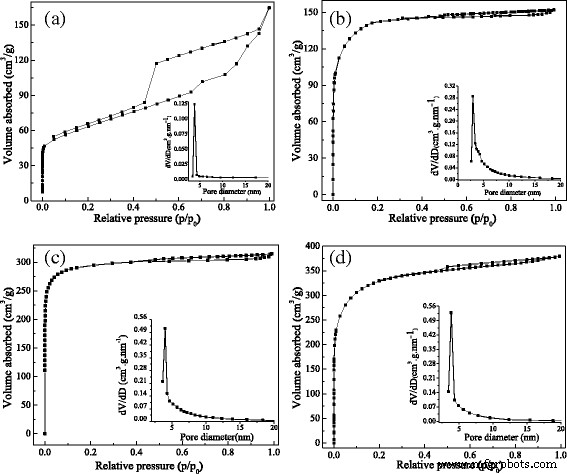
MCMs的氮吸附-解吸等温线和孔径分布。 一 未浸渍 ZnCl2 的 MCM。 b MCM 在没有 ZnCl2 浸渍的情况下在 550°C 下煅烧 1 小时。 c 将 ZnCl2 浸渍 1 小时的 MCM 在 550°C 下煅烧 1 小时。 d 浸渍 1 小时 ZnCl2 的 MCM 在 600°C 下煅烧 1 小时
如图 3a 所示,未经 ZnCl2 浸渍和煅烧的 MCMs 的吸附曲线属于 II 型吸附等温线,通常呈现无孔材料;根据 IUPAC 命名法,滞后回线可以归为 H2 型,这意味着多孔体积是由颗粒堆积形成的 [23]。同时,图 3a 中的样品具有低表面积 (223 m 2 /g) 和低孔隙体积 (0.082 m 2 /g),虽然它具有较大的孔隙尺寸(3.7 nm),这证实孔隙率是填充孔隙率而不是初级孔隙率。
图 3b-d 中的 MCM 样品均在高温下煅烧并具有相似的吸附等温线。如图 3 所示,所有等温线曲线在低相对压力下迅速增加,表明 MCM 样品中存在微孔,有利于强吸附;而在较高的相对压力下,这些曲线表现出一个平台,表明没有发生进一步的吸附,这些曲线是典型的I型吸附等温线。在吸附-解吸过程中,在较高的相对压力下出现滞后回线。该现象表明微孔或中孔的存在和滞后回线可归类为H4型。这种类型的磁滞回线通常出现在活性炭上 [24]。 BJH法计算出的相应孔径分布数据表明,孔径主要分布在3-5 nm以下,这正好证实了MCMs表面存在大量介孔。尽管三种 MCM 样品具有与活性炭相似的吸附等温线,但它们的表面积和多孔体积不同,如表 1 所示。
与 MCM 样品 (c) 和 (d) 相比,MCM 样品 (b) 具有更低的表面积 (356 m 2 /g) 和多孔体积 (0.175 cm 3 /g),在 550°C 下煅烧 1 小时,没有 ZnCl2 浸渍。因此,可以得出结论,ZnCl2 在增加表面积和多孔体积方面起着至关重要的作用。如前所述,ZnCl2 用于活性炭制备过程中的活性剂,会导致纤维素材料降解和脱水,从而导致碳骨架的魅力和芳构化以及孔隙结构的产生[25]。此外,MCM 样品 (c) 和 (d) 都浸渍了 1 小时,唯一的区别是它们的煅烧温度,这导致表面积和多孔体积发生了显着变化。温度越高,表面积和多孔体积越大。因此,MCM样品(d)因其最大的表面积和多孔体积而被选择用于以下磁性能和吸附研究。
MCM 的磁性
使用振动样品磁力计 (VSM) 研究了 MCM 的磁性能,Fe3O4 纳米/微球 (a) 和 MCM 在 600°C 温度下煅烧 1 小时 (b) 的磁滞回线如图 4 所示。使用 VSM 在室温 (300 K) 下测量。
<图片>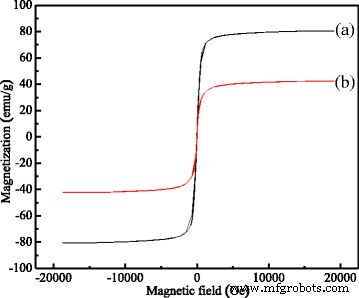
MCM 的磁性。 (a ) 纯 Fe3O4 纳米/微球的饱和磁化强度。 (b ) MCMs的饱和磁化
如图 4 所示,纯 Fe3O4 纳米/微球的饱和磁化强度为 80.3emu/g,小于 92.0emu/g,块状 Fe3O4 的饱和磁化强度 [19],而 MCM 的饱和磁化强度为 42.3 emu/g,远低于纯 Fe3O4 纳米/微球和块状 Fe3O4。这种急剧下降表明有很多碳附着在 Fe3O4 纳米/微球的表面。然而,MCMs中的磁芯具有高饱和磁化强度,附着在Fe3O4纳米/微球表面的碳几乎对其磁责任没有影响。发现它们的剩余磁化强度和矫顽力为零,表明Fe3O4纳米/微球和MCMs是超顺磁性的,这意味着MCMs可以通过外加磁场控制和分离。
吸附等温线
Langmuir 和 Freundlich 方程常用于吸附平衡以说明吸附相互作用,这些方程列于方程。 (2) 和 (3) [26, 27]:
$$ \frac{C_{\mathrm{e}}}{Q_{\mathrm{e}}}=\frac{1}{Q_{\mathrm{m}}{K}_L}+\frac{C_{ \mathrm{e}}}{Q_{\mathrm{m}}} $$ (2) $$ \ln {Q}_{\mathrm{e}}=\ln {K}_F+\frac{1}{1}{ \mathrm{n}}\ln {C}_{\mathrm{e}} $$ (3)其中 C e (mg/L) 是磺胺的平衡浓度,Q e (mg/g) 是平衡状态下每克吸附剂 MCM 吸附的磺胺量,Q m (mg/g) 是 MCMs 对磺胺的理论最大吸附容量,K L(L/mg)是描述朗缪尔吸附过程中亲和力的常数;其中 K F是表征MCMs相对吸附能力的Freundlich经验常数,1/n是表征Freundlich吸附强度的常数[27]。
Langumir和Freundlich吸附等温线如图5所示,其特征吸附参数列于表2中。
<图片>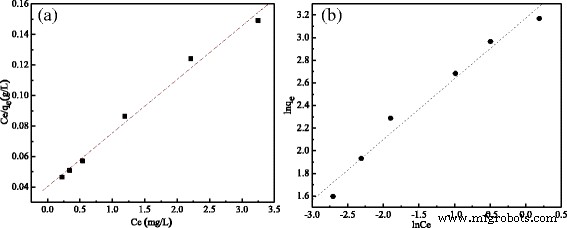
MCMs 的吸附等温线。 一 兰古米尔模型。 b 弗洛因德利希模型
如图 5 和表 2 所示,Langumir 和 Freundlich 等温线模型之间存在线性关系,两个模型之间没有太大差异。在Langumir模型中,MCMs对磺胺类药物的最大理论吸附容量为Q m =27.8551 毫克/克。在 Freundlich 模型中,常数 K 的值 F 和 1/n 分别计算为 3.0564 L/g 和 0.476。由于1/n的值小于1,表明吸附良好。至于线性系数值 (R 2 ) 关注,与 Freundlich 模型相比,线性系数值 (R 2 )的Langmuir等温线模型大于另一个,说明平衡吸附数据更符合Langmuir等温线。
吸附动力学
为了深入了解 MCM 和磺胺之间的吸附过程及其关系,并进一步阐明吸附类型和影响因素,两个动力学模型,准一级方程和准二级方程,分别为用于研究 MCM 的吸附动力学,由方程给出。 (4)和(5)[28,29,30]:
$$ \ln \left({Q}_e-{Q}_t\right)=\ln {Q}_e-{K}_1t $$ (4) $$ \frac{t}{Q_t}=\frac{ 1}{K_2\times {Q_e}^2}+\frac{t}{Q_e} $$ (5)其中 Q e 和 Q t 表示在平衡状态和 t 时间的磺胺吸附能力; K 1 (min −1 ) 和 K 2 (g mg −1 min −1 ) 分别是拟一级和拟二级吸附的模量。 ln(Q e - Q t ) 与 t 给出 − K 的斜率 1 和 lnQ 的截距 e . (t/Q t ) 与 t 给出斜率 (1/Q e ) 和截距 1/(K 2 × 问 e 2 ).
模型的动力学曲线和计算参数及其线性系数(R 2 ) 列在表 3 中。
如表 3 所示,伪二阶方程的相关系数大于伪一阶模型的相关系数并显示出良好的线性,这表明 MCM 对磺酰胺的吸附可能是动力学控制的二级反应而不是一级反应,吸附限速步骤可能包括化学吸附。
pH 值对 MCM 吸附能力的影响
发现 25 mg/L 磺胺溶液的自然 pH 值为 6.0。通过用 0.1 mol/L NaOH 和 0.1 mol/L HCl 调节,pH 值从 4.0 变为 10.0。考察了pH值对MCMs吸附能力的影响,结果如图6所示。
<图片>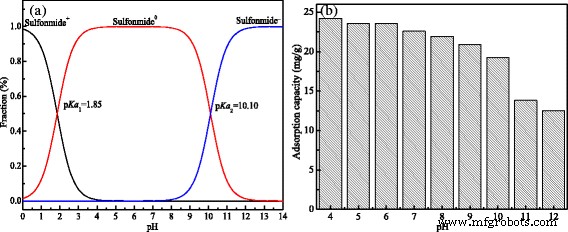
pH 值对磺胺类药物形态和吸附能力的影响。 一 磺胺类物质的形成随 pH 值而变化。 b MCMs的吸附能力随pH值变化
MCM 的吸附能力受磺胺类物质形成和 MCM 表面电荷的影响。如图 6 所示,当 pH 从 4 增加到 12 时,MCMs 的吸附容量从 24.22 降低到 12.48 mg/g。在酸性溶液中的吸附性能高于在碱性溶液中的吸附性能可能与磺胺的 pKa 值有关和 MCM 的零点电位。当pH在4.0~6.0范围内处于酸性条件下时,其zeta电位为2.96 mV,MCMs表面主要带正电荷,磺胺主要以天然分子状态存在(磺胺 0 ) 同时 [28, 29]。因此,磺胺很容易被MCMs吸收,表明MCMs的去除效率高于碱性条件下的MCMs;而在碱性条件下,其zeta电位为- 4.01 mV,MCMs表面的正电荷变为负电荷,磺胺形态变为负电荷(磺胺 - ),这导致了磺胺类物质和 MCMs 之间的静电排斥效应,因为它们的电荷类型相同。此外,磺胺很容易溶解在碱性溶液中 [30],这使得它更倾向于溶解在溶液中而不是被 MCM 吸收。因此,吸附容量显着下降,说明MCMs在pH=10等碱性溶液中可以有效解吸。
温度和离子强度对 MCM 吸附能力的影响
研究了温度和离子强度(KCl作为离子调节剂)对MCMs吸附能力的影响,结果列于表4中。
如表 4 所示,随着温度和离子强度的增加,MCMs 的吸附能力下降,这可能是由于 KCl 与磺胺的吸附竞争。 MCMs与其他吸收剂对水溶液中磺胺的吸附能力比较见表5。
这种比较表明 MCM 可以作为去除磺胺的替代吸收剂。在相同的吸附条件下,所得MCMs和Fe3O4纳米颗粒的吸附容量分别为24.22和10.83 mg/g,表明其对MCMs的吸附容量主要来自碳。
MCM 的可重用性
MCMs的重复使用频率如图7a所示,重复使用4次后MCMs的形貌和微观结构如图7b所示。
<图片>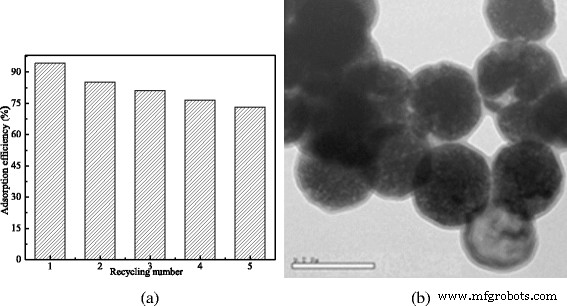
MCMs的重复使用频率及其重复使用四次后的形态。 一 重用频率。 b 重复使用4次后MCM的形貌
如图 7 所示,吸附去除率为 94.28%,计算其对磺胺的吸附量为 23.6 mg/g。用稀NaOH溶液洗涤后重复使用,其吸附效率随着循环次数的增加而降低。第二次、第三次、第四次和第五次吸附获得的吸附去除效率分别为85.23、81.17、76.53和73.23%,分别对应21.31、20.29、19.13和18.31mg/g的吸附去除率。吸附能力。将图 7b 与图 1b 进行比较,重复使用四次后 MCM 的形态和微观结构没有变化。因此,MCMs可重复用于磺胺去除。
结论
通过简便的水热法成功合成了具有灵敏磁责任和高比表面积的MCMs,其比表面积和孔体积达到1228 m 2 /g 和 0.445 m 3 /g,分别。 MCMs对磺胺的吸附符合Langmuir等温线模型并遵循准二级动力学。用NaOH溶液解吸后,MCMs的吸附剂可以回收利用。本工作的主要发现将有助于设计和合成新型吸附剂,并有助于更好地了解其吸附理化过程。
纳米材料


