负载青蒿琥酯和近红外染料偶联的白蛋白纳米颗粒作为高效肿瘤靶向光化学治疗剂
摘要
在此,使用简便的方法合成了一种靶向肿瘤的多功能治疗诊断剂,结合了四种临床批准的材料:青蒿琥酯 (Arte)、人血清白蛋白 (HSA)、叶酸 (FA) 和吲哚菁绿 (ICG)。获得的纳米复合材料(FA-IHA NPs)显示出优异的光稳定性和生理稳定性。 FA-IHA NPs 中的 ICG 不仅用于近红外 (NIR) 荧光成像,还用于单次 NIR 照射下的光热和光动力 (PTT-PDT) 治疗。此外,近红外辐射 (808 nm, 1 W/cm 2 ) 可以触发 Arte 释放,显示出增强的化疗效果。通过荧光成像,在体外和体内观察 FA-IHA NPs 的细胞摄取和肿瘤积累,通过共聚焦显微镜和近红外荧光成像在肿瘤异种移植小鼠中进行分析。根据诊断结果,FA-IHA NPs 在注射后 24 小时并结合 NIR 照射(808 nm,1 W/cm 2 )可以通过光化学联合治疗有效抑制肿瘤生长,在体外和体内均无肿瘤复发。所得结果表明FA-IHA NPs是未来临床转化的有前途的光化学治疗药物。
背景
在最近的几十年中,成像引导的光化学疗法 (IGPC) 引起了许多研究人员的极大兴趣,因为它是实现个性化肿瘤治疗的有前途的策略 [1, 2]。 IGPC 允许准确定位肿瘤并在体内追踪药物,确保有效治疗并减少副作用 [3, 4]。为了有效,IGPC 应具有以下特点: (i) 需要具有成像和治疗功能的多功能治疗诊断剂; (ii) 治疗诊断试剂应具有生物相容性、稳定性和特异性针对肿瘤 [5,6,7,8]。 IGPC 中的成像诊断方式通常包括磁共振成像、光声成像和荧光成像 [9,10,11,12,13,14]。荧光成像具有灵敏度高、时间分辨率好、信噪比高等优点,常被应用于基础研究和临床[15, 16]。
光化学疗法主要包括光热疗法(PTT)、光动力疗法(PDT)和化学疗法。由于近红外(NIR)照射是相同的,PTT和PDT功能可以合二为一,从而可以通过激光束选择性有效地破坏肿瘤。然而,据报道,光热和光动力 (PTT-PDT) 治疗通常具有不完全肿瘤抑制的局限性,这可能会导致肿瘤复发 [17,18,19]。化疗是一种广泛使用的抗癌治疗方法,可通过全身给药有效杀死肿瘤细胞,但由于其非特异性对附近正常细胞的毒性限制了其应用[20,21,22]。因此,IGPC组合可能是克服上述限制的一个很好的策略。
随着纳米医学的发展,IGPC 治疗诊断剂得到了发展,包括吲哚菁绿(ICG)、金属基纳米粒子、碳纳米材料和聚合物纳米材料 [23,24,25,26,27]。其中,ICG 已获得 FDA 批准,据报道其在临床实践中用于检测心输出量、肝功能、血流量和眼科血管造影 [28, 29]。此外,ICG 在 NIR 区域具有高吸收效率,因此在单次 NIR 照射下可产生高 PTT-PDT 效应 [30]。但其水溶液不稳定、体内清除快、易自漂白、缺乏靶向性等缺点严重阻碍了其广泛应用[31, 32]。为了克服这些限制,游离的 ICG 分子通常由包括胶束、聚合物纳米颗粒和自组装蛋白质纳米结构在内的载体携带,以形成纳米复合材料 [33, 34]。尽管已有相关工作,但体内成像和光疗仍需要更多生物相容性和新型ICG纳米复合材料。
在这项工作中,我们报道了一种靶向 IGPC 试剂,该试剂将叶酸 (FA) 和 ICG 与人血清白蛋白 (HSA) 纳米粒子共价结合,该纳米粒子还封装了抗癌药物青蒿琥酯 (Arte) (FA-IHA NPs)。据报道,FA 可以通过受体介导的内吞作用将纳米颗粒连接起来,以提高它们的细胞摄取效率 [17]。 HSA 是一种内源性蛋白质。由于其良好的生物相容性、无毒和非免疫原性,HSA 已成为递送不溶性抗癌药物的最令人兴奋的载体之一 [12, 17, 31]。 Arte,一种从青蒿中提取的天然药物 已被证明在治疗各种癌症方面具有显着疗效,如肝癌、肺癌和乳腺癌[35]。制备的 FA-IHA NPs 由这四种临床批准的材料组成,并显示出良好的生物相容性和稳定性。作为多功能治疗诊断纳米复合材料,ICG 因其 PTT-PDT 特性而被用作 NIR 荧光成像剂和光疗剂。 Arte 被高度加载到 NPs 中,并通过近红外辐射释放用于化疗。在 NIR 成像结果的指导下,靶向 IGPC 组合的高效果在体外和体内都得到了证明。根据我们的研究结果,我们相信FA-IHA NPs可能是一种潜在的多功能治疗诊断剂,用于控制药物递送和成像引导的肿瘤靶向联合光化学治疗。
方法
材料
N-(3-二甲氨基丙基)-N'-乙基碳二亚胺盐酸盐 (EDC)、N-羟基琥珀酰亚胺 (NHS) 和青蒿琥酯 (Arte,≥ 99%) 购自 Sigma-Aldrich (USA)。 4', 6'-二脒基-2-苯基吲哚(DAPI)和细胞计数试剂盒-8(CCK-8)购自阿拉丁(中国上海)。 NH2-PEG2000-COOH 和 NH2-PEG2000-FA 购自西安瑞熙生物科技有限公司(中国西安)。 DMEM 培养基和磷酸盐缓冲液 (PBS) 由 Gibco BRL (NY, USA) 提供。 ICG的磺基-NHS衍生物(ICG-NHS)购自Dojindo Laboratories(日本熊本)。
FA-IHA NPs 的合成和表征
青蒿琥酯溶解在 DMSO 中,然后加入 15 mL 水中。将 10 毫克 HSA 粉末加入上述溶液中,并在室温下轻微搅拌 3 小时。搅拌后,通过与 150 μL 0.5% 戊二醛交联处理混合物。为了去除多余的化学试剂,将混合物用蒸馏水(MW 截止值 =8,000–12,000 Da)透析 1 天,得到载有 Arte 的 HSA 纳米复合材料 (Arte-HSA)。
为了激活 HSA 的羧基,将化学试剂 EDC 和 NHS 添加到 Arte-HSA 溶液中。之后,将混合物与 NH2-PEG2000-FA 在 4°С 反应 3 小时。接下来,在室温下轻微搅拌 30 分钟将 ICG-NHS 添加到混合物中。通过在去离子水中透析 24 小时获得纯化的 FA 和 ICG 结合的 HSA 纳米粒子(FA-ICG-HSA@Arte,FA-IHA NPs)。通过紫外-可见分光光度计检测加载的 Arte 和 ICG 的量。加载效率 =W1 / W2 × 100%,其中W1代表FA-IHA NPs中Arte或ICG的重量,W2是加入的Arte或ICG的重量。
透射电子显微镜(Hitachi,Tokyo,Japan)用于检测样品的形态。 Zetasizer (Zetasizer 3000; Malvern Instruments, Worcestershire, UK) 用于测量样品的尺寸和 zeta 电位。紫外-可见分光光度计(UV-1601PC,Shimadzu,Kyoto,Japan)用于测量吸收光谱。应用808 nm单波长连续波激光器(北京镭波光电科技有限公司)进行光热实验,温度由热电偶温度计(美国Fluke)检测。
热和 pH 触发的艺术释放
为了确定热和 pH 触发的 Arte 释放,FA-IHA NPs (50 μg/mL) 分为三组:(a) pH 6.5,(b) pH 7.4,和 (c) pH 6.5,近红外辐射 (808纳米,1 W/cm 2 , 1 分钟脉冲)在 36 小时内的选定时间点。根据上清液中Arte在287 nm处的UV-vis吸收确定Arte的释放量。
单线态氧产生的检测
1, 3-二苯基异苯并呋喃 (DPBF) 用于检测单线态氧。将 15 μL DPBF 乙腈溶液加入原始 ICG 或 FA-IHA NPs 溶液(1.0 mL,10 μg/mL)中并充分混合,然后照射 5 分钟(808 nm,1.0 W/cm 2 )。记录不同时间点的紫外-可见吸收光谱,410 nm处吸收的减少率与单线态氧的产生量成正比。
细胞培养和细胞摄取
HepG2 细胞购自美国典型培养物保藏中心,25 cm 2 细胞培养瓶中分别加入1%青霉素链霉素和10%胎牛血清(FBS)的DMEM培养基。 HepG2 细胞在 5% CO2 气氛中保持在 37°C。
为了观察细胞摄取,HepG2 细胞与游离 ICG、IHA NP 和 FA-IHA NP(含有 0.05 mg/mL ICG)一起培养 6 小时。之后,用PBS清洗处理过的细胞3次。然后用 200 μL 戊二醛固定细胞并用 DAPI 染色 10 分钟。采用共聚焦激光扫描显微镜(FV300,Olympus,Japan)检测细胞内纳米颗粒的荧光信号。
为了进一步评估细胞摄取,使用流式细胞仪(FCM,BD,Franklin Lakes,NJ,USA)。如上所述,游离 ICG-、IHA NPs-和 FA-IHA NPs 处理的细胞用 PBS 洗涤 3 次,并用胰蛋白酶-EDTA 消化。将悬浮细胞直接导入FCM中分析细胞摄取率。
细胞内活性氧的产生
HepG2细胞在12孔板中培养,密度为2 × 10 5 每毫升细胞并孵育 24 小时,然后加入 1 mL 各种样品,包括 (1) PBS、(2) Arte、(3) FA-HA-NP、(4) 游离 ICG、(5) IHA- NPs,和 (6) FA-IHA NPs 解决方案。进一步孵育 12 小时后,将细胞照射 5 分钟(808 nm,1.0 W/cm 2 ),然后用 DCFH-DA (5 μg/mL) 再处理 30 分钟。最后用PBS彻底清洗细胞,细胞内ROS的产生采用细胞计数仪定量检测,徕卡倒置荧光显微镜定性检测。
体外肿瘤联合光化学疗法
HepG2 细胞接种于 96 孔板 (2 × 10 4 细胞/孔)培养 24 小时。将游离 ICG、Arte、IHA NP 和 FA-IHA NP(含 0、5、10、20 和 30 μg/mL Arte)添加到细胞中。孵育 6 小时后,丢弃旧培养基。使用或不使用 808 nm 激光 (1.0 W/cm 2 , 5 分钟)并在接下来的 24 小时内培养。根据方案通过经典的CCK-8测定法测量细胞活力。
为了进一步确认NIR处理后的活细胞和死细胞,将处理过的细胞用calcein-AM/PI共染色。 HepG2 细胞以 1 × 10 6 的密度预接种在 35 mm 平板中 每板一个细胞,并用 PBS、PBS + NIR、FA-IHA NPs 或 FA-IHA NPs + NIR 处理。孵育 6 小时后,用 808 nm 激光(1 W/cm 2 ) 并在接下来的 24 小时内培养。细胞用钙黄绿素-AM/PI 染色 30 分钟,用 PBS 洗涤以去除多余的染料溶液,然后使用共聚焦激光扫描显微镜成像(钙黄绿素-AM lex =488 nm,lem =515 nm;PI lex =535 nm , lem =617 nm).
动物模型和体内荧光成像
Balb/c 裸鼠获自广东省实验动物科学中心,并在广州医科大学批准的方案下使用。为了建立HepG2皮下肿瘤,1 × 10 6 将 HepG2 细胞(100 μL PBS)注射到 Balb/c 裸鼠背部。
荷瘤小鼠 (n =5) 在静脉注射游离 ICG、IHA NPs 和 FA-之前和之后 10 分钟、6 小时、12 小时、24 小时和 48 小时,通过市售的 IVIS 光谱系统(Caliper LifeSciences,美国)成像IHA NP。
体内肿瘤联合光化学疗法
荷瘤小鼠随机分为不同组(n =5) 并分别用 PBS、Arte、FA-IHA NPs、ICG + NIR、IHA NPs + NIR 和 FA-IHA NPs + NIR(具有相同的游离 Arte 剂量)处理。五分钟 NIR 激光(808 nm,1 W/cm 2 ) 用于在静脉注射这些样品后 24 小时(第 0 天)和 48 小时(第 1 天)照射肿瘤区域。记录照射小鼠的热图像和温度。在治疗过程中,每4天记录一次肿瘤大小并根据公式计算:体积 =(肿瘤长度) × (肿瘤宽度) 2 / 2. 结果显示为相对肿瘤体积,即肿瘤体积除以初始肿瘤体积。处理后,取PBS和FA-IHA NPs + NIR组小鼠的心、肝、脾、肺、肾等主要器官,4%福尔马林固定,石蜡包埋,H&E染色,记录数码显微镜。
结果与讨论
FA-IHA NPs 的合成和表征
图 1 说明了 FA-IHA NP 的示意图及其在成像引导的肿瘤靶向联合光化学疗法中的应用。通过简单且具有生物相容性的自组装方法制备了多功能治疗诊断剂 FA-IHA NPs。由于其 PTT-PDT 特性,共轭 ICG 被用作 NIR 荧光成像剂和光疗剂。此外,负载的Arte发挥了化疗作用。
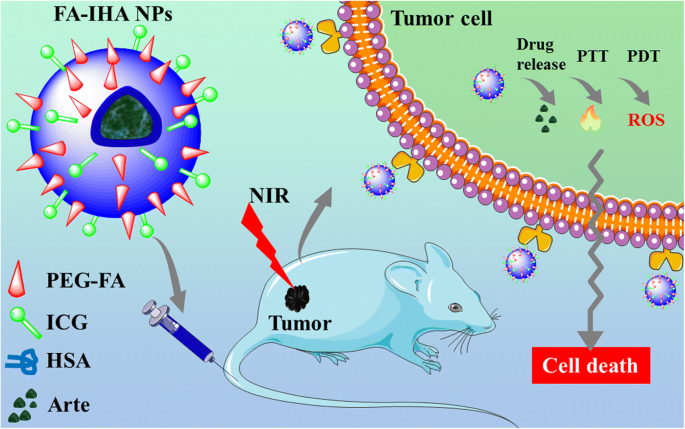
FA-IHA NPs用于体外和体内成像引导的肿瘤靶向联合光化学治疗的示意图
FA-IHA NPs 的 TEM 图像显示直径约为 131.2 nm 的单分散球形结构(图 2a)。根据 DLS 分析,该流体动力学直径在水、磷酸盐缓冲盐水 (PBS) 和细胞培养基中被证实为 131 ± 2.3 nm 长(图 2b)。在这三种介质中,131.2 ± 2.12 的 zeta 电位也被检测为 - 29.2 ± 1.13 mV(图 2c)。此外,在这三种培养基中,FA-IHA NPs 直径在 7 天内没有显着变化(图 2d)。这些结果表明制备的 FA-IHA NPs 具有良好的稳定性,可能是由于 PEG 和 HSA 涂层。 FA-IHA NPs 的 UV-vis-NIR 光谱显示了 Arte 和 ICG 的吸收峰(图 2e),表明 FA-IHA NPs 中存在 Arte 和 ICG。 Arte负载率为98.6 ± 3.1%,ICG负载率为56.9 ± 2.4%。图 2f 显示 FA-IHA NPs 与游离 ICG 具有相似的荧光特性。
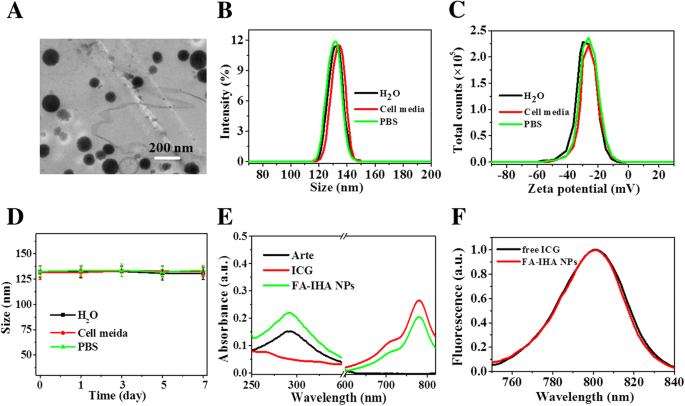
一 FA-IHA 纳米粒子的 TEM 图像。 b , c FA-IHA NPs 在水、细胞培养基和 PBS 中的大小和 zeta 电位分布。 d FA-IHA NPs 在水、细胞培养基和 PBS 中的大小变化。 e 游离 ICG、Arte 和 FA-IHA NP 的吸收光谱。 f 游离ICG和FA-IHA NPs的荧光光谱
受 FA-IHA NPs 强近红外光吸收的鼓舞,评估了 FA-IHA NPs 的光热性能。水、游离 ICG 和 FA-IHA NP(具有相同的 ICG 浓度)用 808 nm 激光 (1 W/cm 2 )。 FA-IHA NPs 和游离 ICG 的温度在辐照 5 分钟内升高了大约 36°C(图 3a),而水的温度增量小于 4°C,表明含有 ICG 的纳米颗粒具有显着的光热效果并具有治疗癌症的潜力。此外,附加文件 1:图 S1 显示了 FA-IHA NPs 在 0.5、1 和 1.5 W/cm 2 的 808 nm 激光照射下 5 分钟的光热加热曲线 ,表明最佳激光强度为 1 W/cm 2 .对 FA-IHA NPs 和游离 ICG 进行了光稳定性测试。与 FA-IHA NP 相比,游离 ICG 在五个循环后显示出显着的温度下降(图 3b)。图 3c 显示了游离 ICG 和 FA-IHA NPs 在五次 NIR 照射(808 nm,1 W/cm 2 )前后的吸收强度变化 )。结果表明,游离 ICG 在 808 nm 处的吸光度强度在 5 个 NIR 照射周期后降低,而 FA-IHA NPs 保持原始的吸光度强度。此外,我们比较了游离 ICG 和 FA-IHA NPs 的荧光稳定性(图 3d)。在 4°C 下储存 30 天后,FA-IHA NPs 在 800 nm 处的荧光强度与其初始强度 1 相比为 0.72,而游离 ICG 的荧光与其初始强度相比下降至 0.12,这是由于聚集诱导-光漂白 [36]。这些结果表明共价结合的 ICG 比游离 ICG 更稳定,这可能是由于 HSA 和 PEG 自组装保护 ICG 免受内部环境诱导的聚集,如热或光。因此,这些结果表明FA-IHA NPs具有优异的光热效应和光热稳定性。
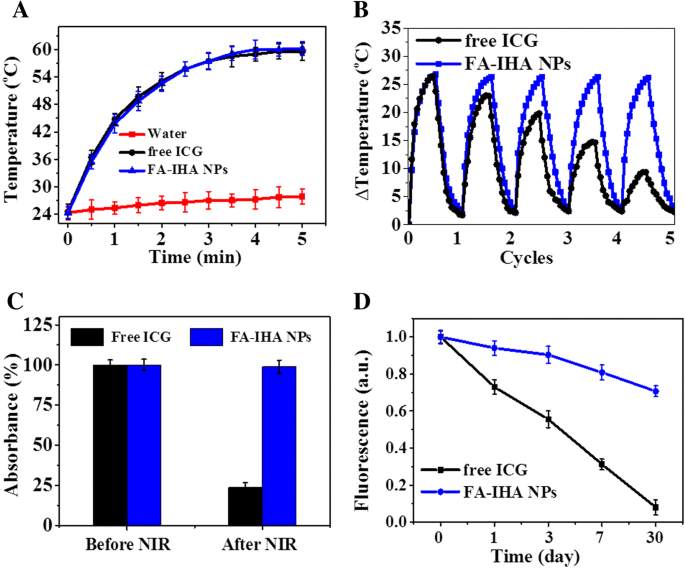
一 水、ICG 和 FA-IHA NPs 在 5 分钟 808 nm 激光照射下的光热加热曲线 (1 W/cm 2 )。 b 用 808 nm 激光连续照射 5 分钟 5 个周期后,ICG 和 FA-IHA NP 的温度变化。 c FA-IHA NPs 在 780 nm 处的吸收变化在用 808 nm NIR 激光照射 5 个周期之前和之后。 d ICG 和 FA-IHA NPs 荧光变化超过 30 天
接下来,使用 ROS 特异性探针 1,3-二苯基异苯并呋喃 (DPBF) 检测近红外辐射后 FA-IHA NPs 的 ROS 产生。如图 4a 所示,与游离 ICG (0.35) 相比,FA-IHA NPs 在 NIR 照射 5 分钟内产生了显着的 ROS 量(标准吸光度为 0.58),这可能归因于 FA-IHA NPs 联合治疗。
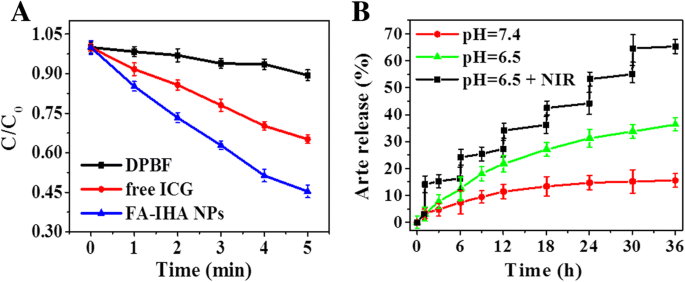
一 存在 ICG、FA-IHA NP 和空白样品时在 808 nm 激光照射下的归一化 DPBF 吸光度 (1 W/cm 2 )。 b FA-IHA NPs在pH =7.4和pH =6.5下分别有或没有NIR激光照射的Arte释放动力学
在近红外激光照射下(808 nm,1 W/cm 2 ) 和 pH 条件,研究了释放性能(图 4b)。相比之下,在没有 NIR 照射的情况下,FA-IHA NPs 在 pH 7.4 和 pH 6.5 下分别显示出 11.61% 和 34.2% 的 Arte 释放,而在 NIR 照射 6 次下,FA-IHA NPs 在pH 6.5,表明 NIR 照射和酸性条件都可以显着触发 FA-IHA NPs 的 Arte 释放。 NIR 照射和酸响应药物释放可能是由于 HSA 纳米粒子的热诱导膨胀,此外,在酸性环境下,H + 可以改变HSA的表面电荷,从而改变纳米颗粒的亲水/疏水平衡[37, 38]。
细胞摄取和细胞内活性氧的检测
由于 ICG 的荧光特性,通过荧光显微镜可以直接在 HepG2 细胞中观察到 FA-IHA NPs 的吸收。如图 5a 所示,在用 FA-IHA NPs 处理细胞后,细胞质显示出比在用游离 ICG 和 IHA NPs 处理的细胞中观察到的更强的红色 ICG 荧光。此外,FA-IHA NPs 细胞摄取率被 FCM 量化为 52.3%,高于 IHA NPs (25.2%) 和游离 ICG (3.9%)(图 5b)。结果表明共轭FA促进纳米颗粒靶向肿瘤细胞上的FA受体,从而增强FA-IHA NPs细胞摄取[39, 40, 41]。
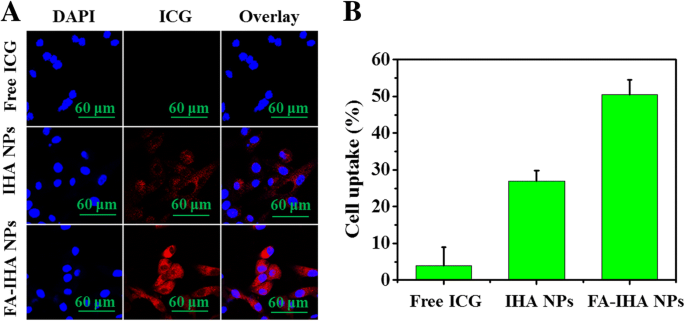
一 HepG2 细胞与游离 ICG 和 IHA NP 以及 FA-IHA NP 孵育后的共聚焦荧光图像。红色和蓝色分别代表 ICG 荧光和 DAPI 染色的细胞核。 b 流式细胞术检测HepG2细胞与游离ICG、IHA NPs和FA-IHA NPs孵育后ICG荧光强度
通过使用荧光显微镜,我们观察了 Arte-、ICG-和 FA-IHA NPs 处理的细胞在有或没有 NIR 照射的情况下的内在光动力活性。 ROS 探针 2, 7-二氯二氢荧光素二乙酸酯用于可视化细胞 ROS 的产生。结果表明,在 NIR 照射 5 分钟后,与其他样品相比,FA-IHA NPs 可以诱导显着增强的 ROS 产生(图 6a)。相应的荧光值如图 6b 所示。
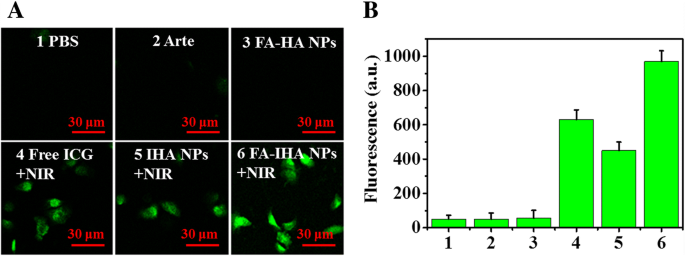
一 用各种药物处理的癌细胞中 ROS 产生的荧光图像,以及 b 相应的荧光强度:(1)PBS,(2)Arte,(3)FA-HA NPs,(4)游离ICG + NIR,(5)IHA NPs + NIR,和(6)FA-IHA NPs + NIR
体外肿瘤联合光化疗
图 7a 显示了 PBS-、游离 ICG-、IHA NPs-和 FA-IHA NPs 处理的细胞(具有相同的 ICG 浓度)在 NIR 照射 5 分钟后的温度变化(1.0 W/cm 2上> )。 FA-IHA NPs处理的细胞温度显示出最高的升高(ΔT =31°C) 与 PBS-、游离 ICG-和 IHA NPs 处理的细胞相比。在没有 NIR 照射的情况下,用不同浓度的 Arte、IHA NP 和 FA-IHA NP 处理 24 小时的细胞活力随着浓度的增加而降低,而这些浓度的游离 ICG 没有显示任何细胞毒性(图 7b)。同时,药物载体 FA-IH NPs(没有 Arte 的 FA-IHA NPs)也没有显示出明显的细胞毒性(附加文件 1:图 S2)。相比之下,在 NIR 照射后 (1.0 W/cm 2 ,5 分钟),在用游离 ICG、IHA NP 和 FA-IHA NP 处理的细胞中观察到显着的浓度依赖性细胞死亡(图 7c)。这种效果在 FA-IHA NPs 处理的细胞中尤为显着。优异的抗癌效果可能归因于靶向组合光化学疗法,例如释放的Arte的化学治疗作用和ICG的PTT-PDT治疗作用。此外,通过钙黄绿素-AM/PI 双染色研究了有或没有 NIR 照射的 FA-IHA NPs 的细胞毒性。与其他处理组相比,用 FA-IHA NPs 和辐射处理的细胞几乎完全死亡(图 7d)。
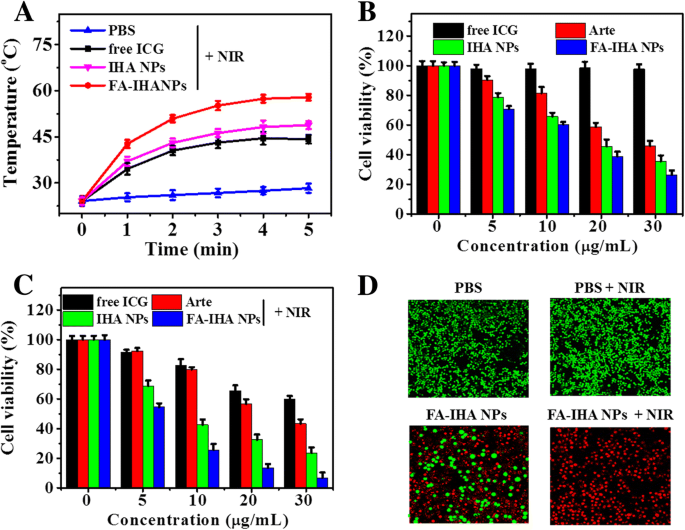
一 NIR 照射 5 分钟后,PBS-、游离 ICG-、IHA NPs-和 FA-IHA NPs 处理的细胞在 96 孔板中的温度变化曲线。 b, c 用游离 ICG、Arte、IHA NPs 和 FA-IHA NPs 处理的细胞在没有或有 808 nm 激光照射(5 分钟,1 W/cm 2 )的情况下的细胞活力 ), 分别。 d 分别用PBS(对照)、PBS + NIR、FA-IHA NPs和FA-IHA NPs + NIR处理后细胞的钙AM/PI双染色图像
体内荧光成像
如图 8a 和 b 所示,在注射游离 ICG、IHA NP 和 FA-IHA NP 后 0.1 小时,可以在荷瘤小鼠的整个身体中看到强烈的荧光信号。荧光信号在肿瘤区域随着时间的增加而增加,在注射后 24 小时达到峰值。在所有测试点,FA-IHA NPs 组的肿瘤荧光信号均高于 ICG 和 IHA NPs 组(图 8b),表明 FA-IHA NPs 可以由于 FA 在肿瘤区域高度积累-诱导的肿瘤靶向作用。此外,主要组织(包括心脏、肝脏、脾脏、肺和肾脏)中的生物分布是通过注射后 24 小时的离体荧光定量分析进行的。在所有测试组中,在肝脏组织中检测到强荧光信号(图 8c),表明这些化合物的主要代谢转化遵循肝脏途径。这些结果表明FA-IHA NPs可以在体内选择性地在肿瘤中积累,这可能是由FA靶向作用诱导的[37]。
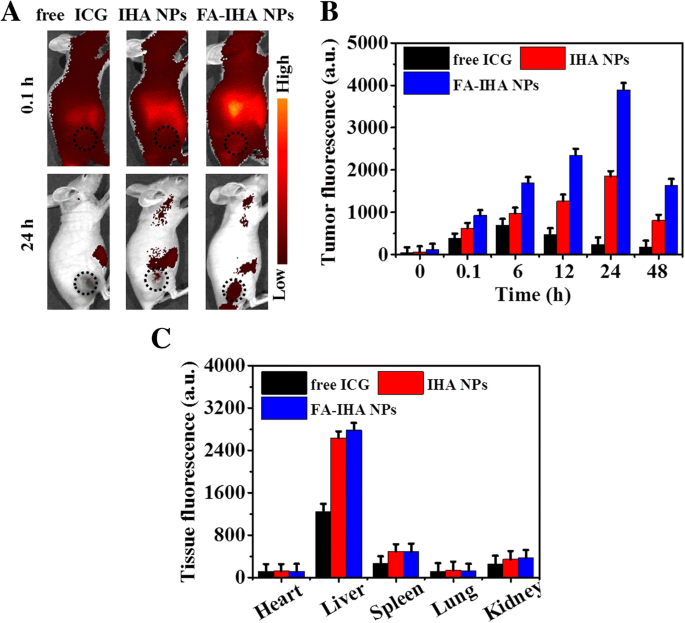
一 尾静脉注射游离 ICG、IHA NPs 和 FA-RIPNPs 后荷瘤小鼠的代表性荧光图像。黑色虚线圆圈表示肿瘤区域。 b 用游离 ICG、IHA NPs 和 FA-IHA NPs 治疗的小鼠肿瘤区域荧光信号的体内定量分析作为注射时间的函数。 c 心、肝、脾、肺、肾等主要器官的荧光信号
体内肿瘤联合光化疗
如图 9a 和 b 所示,在注射后 24 小时,在近红外辐射 5 分钟(1 W/厘米 2 ) 由热像仪记录。在 FA-IHA NPs 治疗组中检测到肿瘤区域增加了大约 22.1°C,这是最高的。在两个周期的 NIR 照射后(第 0 天和第 2 天),FA-IHA NPs + NIR 组表现出显着的肿瘤生长抑制而没有复发(图 9c),而用 PBS、Arte、FA-IHA NPs 处理的组, PBS + NIR、ICG + NIR和IHA NPs + NIR没有表现出明显的肿瘤抑制迹象。此外,在 90 天后,FA-IHA NPs + NIR 组中的小鼠显示出 100% 的存活率(图 9d)。这些结果表明近红外光照射的FA-IHA NPs具有优异的体内肿瘤治疗效果,这可能是由于主动靶向和联合光化学疗法。
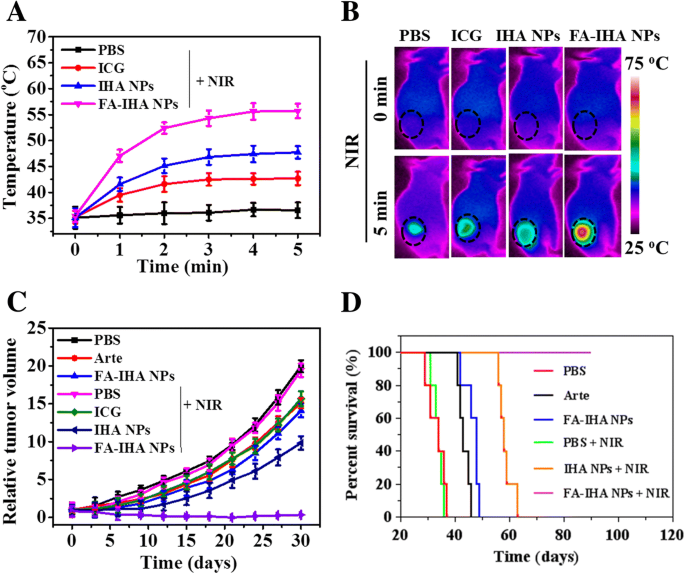
一 荷瘤小鼠在尾静脉注射 PBS、ICG、IHA NPs 和 FA-RIPNPs 后,在 5 分钟 NIR 照射(808 nm,1 W/cm 2 )下 24 小时的肿瘤区域温度 )。 b 荷瘤小鼠在尾静脉注射 PBS、ICG、IHA NPs 和 FA-RIPNPs 后,在 5 分钟 NIR 照射(808 nm,1 W/cm 2 )下 24 小时的热图像 )。 c 静脉注射 PBS、Arte、ICG、IHA NPs 和 FA-RIPNPs 后的 HepG2 异种移植肿瘤生长曲线,有或没有 5 分钟的 NIR 照射(808 nm,1 W/cm 2 )。 d 用 PBS、游离 Arte、ICG、IHA NPs 和 FA-RIPNPs 尾静脉注射 5 分钟近红外辐射(808 nm,1 W/cm 2 )后荷瘤小鼠的存活率 )
最后,苏木精和伊红 (H&E) 染色用于评估 FA-IHA NPs 的毒性。切片图像与 PBS 处理组相比没有明显的组织学病变(图 10),表明 FA-IHA NPs 具有可忽略的毒性,这可能是由于 FA-IHA NPs 成分的安全性,因此有利于未来在临床实践中的应用。
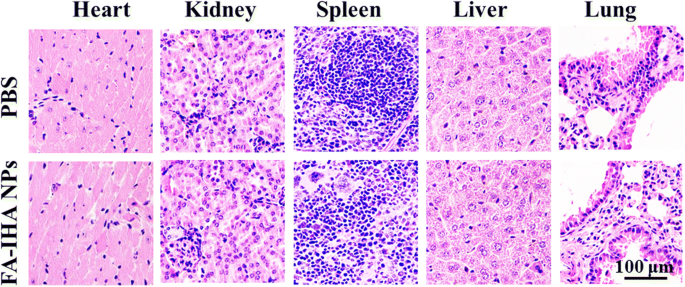
PBS 和 FA-IHA NPs 处理的小鼠心脏、肝脏、脾脏、肺和肾脏等主要器官的 H&E 染色组织切片
结论
总之,制备了一种多功能治疗诊断剂,将 FA 和 ICG 共价结合,并封装 Arte,用于体外和体内成像引导的肿瘤靶向联合光化学治疗。 The prepared FA-IHA NPs showed excellent colloidal- and heat-stabilities and fluorescence property. Under NIR irradiation, FA-IHA NPs showed great photothermal effect which could trigger Arte release and produce much more ROS after NIR irradiation than free ICG that exhibited photodynamic performance. The conjugated FA facilitated a highly efficient cellular uptake and tumor accumulation in vitro and in vivo. Moreover, the highly effective anticancer efficacy of FA-IHA NPs combined active targeting thermal drug chemotherapy, such as PTT-PDT therapy, which was demonstrated in vitro and in vivo. Overall, the results obtained indicated that FA-IHA NPs might be a promising tumor-targeted system feasible for future nanomedicine applications.
缩写
- Arte:
-
Artesunate
- FA:
-
Folic acid
- HSA:
-
人血清白蛋白
- ICG:
-
Indocyanine green
- 近红外:
-
Near infrared
- PDT:
-
Photodynamic therapy
- PEG:
-
聚乙二醇
- PTT:
-
Photothermal therapy
纳米材料
- 制造和成像环碳
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 钴掺杂 FeMn2O4 尖晶石纳米粒子的制备和磁性
- 加载白藜芦醇的白蛋白纳米颗粒具有延长血液循环和改善生物相容性的高效靶向胰腺肿瘤治疗
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 用于光热疗法和光声成像的聚吡咯涂层铁铂纳米粒子的合成和体外性能
- 酸性胶溶剂对 TiO2 纳米颗粒锐钛矿-金红石比和光催化性能的影响
- 磁性金纳米粒子标记乙酰肝素酶单克隆抗体及其在肿瘤磁共振成像中的后续应用
- 纳米粒子和超声波控制的水过冷
- 加载姜黄素的壳聚糖-牛血清白蛋白纳米颗粒可能增强阿尔茨海默病中的 Aβ 42 吞噬作用和调节巨噬细胞极化
- 双整合素 αvβ 3 和 NRP-1 靶向顺磁性脂质体,用于磁共振成像中的肿瘤早期检测
- 肿瘤靶向和生物相容性 MoSe2 纳米点@白蛋白纳米球作为协同光热放射治疗的双模态治疗剂


