一种基于磁性纳米颗粒的新型造影剂,用于检测胆固醇作为阿尔茨海默病生物标志物
摘要
背景
考虑到多年来阿尔茨海默病在世界人口中的高发病率,以及该病在卫生和社会方面给各国带来的成本,有必要开发非侵入性诊断测试,以检测该疾病的早期生物标志物。在早期诊断方法中,磁共振成像造影剂的开发变得特别有用。
越来越多的证据表明胆固醇可能在阿尔茨海默病的发病机制中发挥作用,因为在动物转基因模型和阿尔茨海默病患者中已经描述了围绕老年斑的胆固醇异常沉积。体内实验还表明,饮食诱导的高胆固醇血症会促进β-淀粉样蛋白在神经元内的积累,并伴有小胶质细胞增生,并加速脑内β-淀粉样蛋白的沉积。
假设陈述
在本研究中,我们首次提出合成由与抗胆固醇抗体结合的磁性纳米粒子组成的新纳米缀合物,以通过磁共振成像检测在阿尔茨海默病老年斑中观察到的异常胆固醇沉积。纳米平台还可以揭示与这种病理相关的神经元质膜中观察到的胆固醇降低。
检验假设
验证假设的实验设计将首先在体外进行,然后在第二阶段进行体外和体内研究。
假设的含义
因此,设计的纳米平台可以检测大脑水平的胆固醇沉积。在与老年斑块堆积一致的区域检测这种生物标志物可以提供阿尔茨海默病发病和进展的早期信息。
背景
多项研究表明,神经元质膜中存在适量的胆固醇 (CHO) 在保护神经细胞免受 β-淀粉样蛋白在阿尔茨海默病 (AD) 中的毒性方面起着关键作用,从而抵消了这种蛋白质的过度产生[1,2,3];富含CHO的神经元更能抵抗氧化应激和β-淀粉样蛋白的毒性[4, 5]。
因此,可以假设神经元质膜中存在的 CHO 量,而不仅仅是其血浆水平,可能在神经退行性疾病的发病机制中发挥作用 [6]。事实上,实验数据支持细胞膜中最佳数量的 CHO 是建立抵御有毒物质的保护屏障所必需的想法。质膜中细胞 CHO 量的减少会改变这种保护屏障,从而降低对有毒物质(包括 β-淀粉样蛋白)的保护作用 [7]。有趣的是,转基因AD小鼠大脑皮层神经元质膜中的CHO含量低于野生型小鼠[8]。
森等人。 [9] 表明,在人类和转基因淀粉样前体蛋白 (APP) 小鼠中,CHO 在成熟淀粉样斑块中异常积累,但在弥散或未成熟斑块中没有,表明 CHO 可能在老年斑的形成和进展中发挥作用。随后的其他研究发现,CHO 和载脂蛋白 E 存在于纤维状斑块的核心,但在早期不存在于弥漫性斑块中。在疾病的更晚期阶段,描述了更多数量的胆固醇氧化酶免疫阳性的纤维状斑块 [10]。通过质谱法测定的每个老年斑的游离 CHO 量与 β-淀粉样蛋白负荷相似 [8]。 AD 中 CHO 和老年斑浓度的这种相互增加可能表明该疾病的新致病机制 [11]。此外,在 AD 患者的脑组织中,已经使用抗斯托克斯拉曼散射和 2 光子荧光显微镜在硫磺素 S 染色的样品中描述了与纤维状老年斑共定位的脂质沉积物 [10]。可以观察到两种脂质形态:层状结构和亚微米尺寸的聚结大聚集体。由于整个斑块的脂质组成/组织各不相同,有明确证据表明纤维状老年斑中淀粉样蛋白-脂质密切相互作用,使它们的组成比以前认为的更具动态性 [12]。
此外,为了在疾病的早期检测 AD 的生物标志物,一些研究提出使用功能化磁性氧化铁纳米粒子 (MNP) 作为老年斑磁共振成像 (MRI) 的特异性造影剂 [13,14, 15]和铁蛋白[16]检测。这些粒子在 T2 和 T2* 加权序列中表现出的低信号效应在 MRI 图像中提供了更大的对比度。因此,使用MNPs作为MRI造影剂是一种有前景的AD早期诊断方法。
目前的工作提出了使用基于生物功能化 MNP 的新对比剂的假设,通过 MRI 检测老年斑中 CHO 的异常积累,可用作 AD 的潜在生物标志物。
据我们所知,目前的工作首次提出了一种基于生物功能化 MNP 的新型造影剂的设计,用于通过 MRI 检测老年斑中 CHO 的异常积累,可用作 AD 的潜在生物标志物.
假设
由于多年来世界人口中 AD 的高发病率 [17],以及国家在健康和社会方面的病理学相关成本 [17],迫切需要开发无创工具,以便检测早期生物标志物疾病的诊断和演变。
在早期诊断方法中,用于分子成像 (MI) 的造影剂的开发变得特别有用。 MI 将传统成像技术与分子探针相结合,旨在检测生物化学和细胞生物学方面的疾病进展和治疗反应 [18,19,20]。
我们建议合成一种基于用聚乙二醇 (PEG) 包被的 MNP 并用链霉亲和素功能化的造影剂(图 1a),以允许定向连接生物素化抗体,该抗体特异性识别老年斑中存在的 CHO(NANOCHOAD)(图 1b)。该抗体还将识别细胞质膜中存在的 CHO,从而检测神经元质膜中 CHO 的减少。 MNPs将被PEG链包覆以提高纳米平台的胶体稳定性,促进其在血流中的分散和通过血脑屏障(BBB)[21]。
<图片>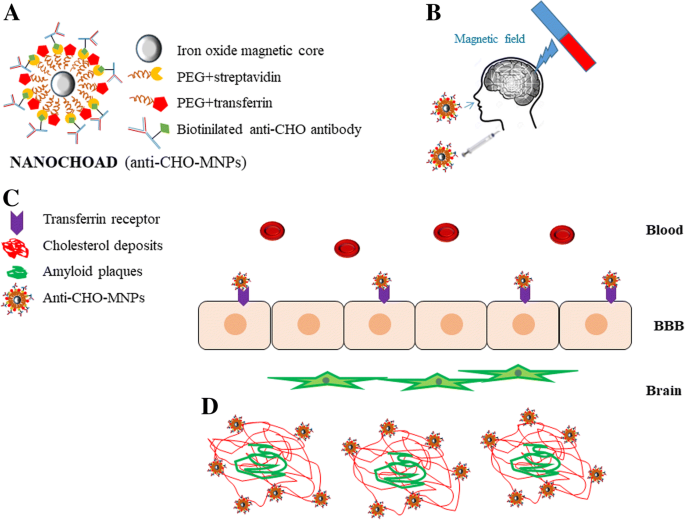
设计的纳米平台示意图及其作用机制。 一 MNP的结构,以及抗CHO抗体(NANOCHOAD)的功能化,b 通过 BBB 渗透纳米平台的策略,c 通过 NANOCHOAD 的 BBB 的穿越机制。 d 靶向淀粉样斑块上CHO沉积物的纳米缀合物抗CHO-MNP
BBB 是神经系统疾病治疗和诊断中遇到的最独特的生物障碍之一,限制了大多数诊断和治疗药物通过全身途径进入大脑 [22, 23]。因此,诊断和治疗大量脑部疾病的挑战在于克服通过 BBB 将治疗剂和造影剂输送到大脑特定区域的困难。幸运的是,脑毛细血管内皮细胞显示出一些特定的受体介导的转运机制。已有研究表明,大量转铁蛋白受体由脑毛细血管内皮细胞表达,参与受体介导的 BBB 胞吞作用 [24]。
因此,为了解决造影剂通过 BBB 的问题,我们提出了三种替代策略:(i) 将抗 CHO-MNP 与转铁蛋白结合 [25],使其通过 BBB; (ii) 抗 CHO-MNPs 偶联物的鼻内给药。鼻内途径是一种非侵入性的绕过 BBB 的途径,是将纳米缀合物输送到大脑的另一种途径 [26, 27]; (iii) 施加外部磁场以促进纳米共轭物穿过 BBB(图 2c)。这种新型递送技术可以通过 BBB [28,29,30](图 1c)向大脑(嗅觉区、皮层、海马...)递送临床相关剂量。此外,使用 PEG 包覆的 MNPs 和由于病理本身导致的 BBB 恶化也有利于纳米缀合物通过 BBB。纳米偶联物将通过抗原抗体亲和力特异性识别老年斑中 CHO 的异常沉积物(图 1c、d)。纳米颗粒在脑实质病理结构中作为老年斑的积累表明 AD 脑实质中 CHO 定位的变化。因此,与老年斑相关的抗 CHO-MNP 的存在将在 T2* 加权 MRI 中显示低信号,允许检测与 AD 的其他既定标志(如老年斑)相关的 CHO,从而进行 MR 成像脑CHO可能成为该疾病的新生物标志物。此外,由于 CHO 质膜减少,MRI 会发生变化。
<图片>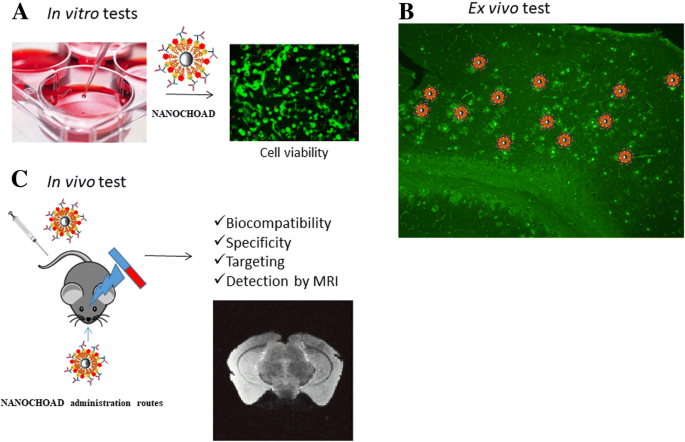
测试假设的实验设计。一、体外(a ):确定合成的纳米缀合物的生物相容性。体外试验 (b ):通过在来自 5XFAD 转基因小鼠的固定脑切片上孵育纳米平台来测试抗 CHO-MNPs 纳米偶联物的特异性。体内研究 (c ):纳米平台将通过静脉注射或替代途径作为鼻内给药/外磁场应用,其有效性(靶向)将通过 MRI 进行评估
如先前的研究所证明的那样,可以通过小胶质细胞对 MNP 的内化及其随后的溶酶体加工来实现从脑实质中清除造影剂 [16, 31, 32]。 MNP 将通过用于内源性铁代谢的常见途径消除。尽管如此,在拟定假设的发展过程中,将根据造影剂的大小和表面电荷及其潜在毒性确定造影剂的消除途径,详情如下。
检验假设
磁性纳米粒子的合成与表征
根据 Predescu 等人的工作,将使用受控共沉淀法合成氧化铁纳米粒子,通过在碱性溶液中混合亚铁离子 (Fe2+) 和三价铁离子 (Fe3+)。 [33]。 MNP 将按照 Liu 等人先前建立的协议涂上 PEG 壳。 [34].
将使用 X 射线衍射 (XRD)、扫描电子显微镜 (SEM)、透射电子显微镜 (TEM)、傅里叶变换红外光谱 (FTIR) 和超导量子干涉仪(SQUID)磁力仪。
在对合成的磁性纳米材料进行表征后,它将通过 NHS/EDC 方法用 (1) 链霉亲和素蛋白进行功能化。此后,它将与生物素化的抗 CHO 抗体和 (2) 转铁蛋白偶联。转铁蛋白的结合是通过将配体表面的羧基与PEG涂层上的羟基偶联来实现的[35]。
体外测试
第一步,将在体外测试纳米平台的生物相容性(图 2a)。纳米偶联物将被添加到神经元和星形胶质细胞的共培养物以及内皮细胞培养物中 [36],以确定纳米偶联物与典型脑细胞的相容性。如果功能化 MNP 的细胞相容性是正确的,系统的有效性将在疾病的离体模型中进行测试(图 2b)。所选模型为 APP/(presenilin-1) PS1 双转基因小鼠,共表达 5 个家族性 AD 突变 (5XFAD),并表现出类似于 AD [37] 中发现的淀粉样斑块病理。
5XFAD转基因模型中老年斑周围CHO的积累将通过免疫组织化学进行评估。
如果模型有效,一旦证明 CHO 在老年斑中积累,建议测试合成纳米缀合物的特异性。为此,首先,将从 5XFAD 转基因小鼠中获得固定的脑切片,然后,将在它们上试用纳米偶联物的结合,在 5XFAD 小鼠的固定脑切片上孵育抗 CHO-MNP。纳米缀合物的特异性将通过评估抗 CHO-MNP 与 CHO 沉积物和 5XFAD 脑切片中存在的老年斑的共定位,进行适当的对照来确定。如果在 5XFAD 中没有检测到明显的胆固醇积累,则将使用淀粉样前体蛋白小鼠模型 (APPsw)、AD 小鼠模型的另一种瑞典突变,因为在该模型中,与淀粉样蛋白斑块明显相关的 CHO 积累具有已在海马体中进行了描述 [9]。
体内测试
一旦证明偶联物的特异性,将进行纳米偶联物的体内生物相容性分析。纳米平台将以不同的剂量(范围从 25 到 100 mg/kg [38])静脉注射(图 2c),研究过程中的亚急性毒性将通过观察死亡率、萎缩证据来分析、充血、炎症或小鼠的任何严重行为变化。将计算每个器官对身体的权重系数。肾毒性取决于血液中尿素氮和肌酐的水平。可以测试血液中总胆红素和碱性磷酸酶的水平,作为衡量肝脏和胆汁功能的指标。此外,还将确定尿酸水平和血液学研究,以评估红细胞、白细胞和血红蛋白水平的变化。最后,为了更详细地寻找可能的毒性作用,将对各种组织(肾、肝、脾、脑或肺)进行组织学检查 [39]。在抗CHO-MNPs注射后24 h、72 h、1 周、2 周和1 个月,分析功能化MNPs在血液、尿液和不同器官中的位置。
一旦确定了合适的 MNP 浓度,纳米平台将被注射到对照和 5XFAD 小鼠中,其有效性将通过 MRI 进行评估(图 2c)。如果来自纳米平台的抗体不能识别体内系统中的抗原,那么 MNP 可以用苯基二炔胆固醇进行功能化,苯二炔胆固醇是一种化合物,在之前的研究中已经发现能够在体内结合 CHO 积累 [40] .该纳米缀合物的生物相容性将按照上文针对 MNP-CHO 纳米缀合物的描述进行评估。如果静脉给药途径不能有效穿过 BBB,则建议替代给药途径为鼻内给药或施加外部磁场(图 2c)。
假设的含义
通过将 MNP 与不同肽结合,使用生物功能化 MNP 通过 MRI 在体内检测 AD 已得到广泛证明:Aβ 1-40 [41]、Aβ1-30 [42]、Aβ1-42 [15]和抗 Aβ-1-42 抗体 [43]。在 AD 动物模型中静脉给药后,通过 MRI 检测到老年斑和血管淀粉样蛋白沉积物(嗜刚果红血管病)。然而,这些纳米缀合物本身是有毒的,因为所使用的淀粉样肽片段具有神经毒性(Aβ1-40、Aβ1-42)。此外,由于它们的大小,它们需要共同给药促进它们通过 BBB 的化合物。
NANOCHOAD 将用作造影剂,允许同时定位两种 AD 特异性生物标志物:淀粉样斑块和大脑白质中 CHO 的丢失 [44],避免毒性。由于其结构中存在 PEG,它也将促进纳米平台通过 BBB [43]。
可以看出,对这些特征的大多数研究都是针对老年斑的检测,老年斑是 AD 的主要生物标志物之一,但不是唯一的。最近,发表了一篇论文,其中通过基于 MNP 的纳米缀合物检测铁蛋白和铁沉积物 [16]。然而,这种用于检测铁蛋白的造影剂灵敏度低,因为它不能被 MRI 检测到,只能在大脑的特定位置进行量化。大脑中白质的丢失是一个巨大的现象 [44],而不是局部的;因此,认为所提出的造影剂对于 AD 生物标志物的早期检测可能更敏感。有必要推动新型造影剂的开发,以在疾病早期有效检测与AD相关的其他生物标志物。
另一方面,所提出的纳米缀合物的组成可以解决克服静脉注射造影剂功效的两个主要障碍:血流中的胶体稳定性和成功穿过 BBB 到达目标的能力。具有 PEG 链的纳米平台的功能化将确保纳米缀合物在血流中的胶体稳定性 [15, 21]。另一方面,作为穿越 BBB 的策略,MNP 与肽转铁蛋白的结合 [25] 将促进位于 BBB 中的特定受体识别转铁蛋白,从而允许纳米偶联物穿过 BBB 并与其最终目标结合.这一事实结合纳米系统尺寸的减小和 AD 患者血脑屏障的改变,将促进纳米缀合物通过血脑屏障。
由于所描述的纳米偶联物设计的新颖性,有必要深入研究纳米平台的生物相容性和给药剂量,特别是确定生物体造影剂的消除途径。
缩写
- 广告:
-
阿尔茨海默病
- BBB:
-
血脑屏障
- CHO:
-
胆固醇
- MI:
-
分子成像
- MNP:
-
磁性氧化铁纳米粒子
- MRI:
-
磁共振成像
- PEG:
-
聚乙二醇
纳米材料
- 用于磁性传感器的纳米金刚石
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 使用聚(4-苯乙烯磺酸-共-马来酸)增强金磁性纳米颗粒的稳定性:用于蛋白质检测的定制光学特性
- 用于细胞内蛋白质递送的二氧化硅纳米颗粒:一种使用绿色荧光蛋白的新型合成方法
- 用于氧化还原刺激触发释放的新型双线粒体和 CD44 受体靶向纳米颗粒
- 适体修饰的磁性纳米增敏剂,用于表达 HER2 的癌症的体内 MR 成像
- 加载姜黄素的壳聚糖-牛血清白蛋白纳米颗粒可能增强阿尔茨海默病中的 Aβ 42 吞噬作用和调节巨噬细胞极化
- 一种用于高灵敏度检测阿特拉津的新型磁弹性纳米生物传感器
- 使用基于智能手机的阅读器灵敏检测疾病生物标志物的等离子体 ELISA
- 带有 Ag 纳米颗粒的对齐良好的 TiO2 纳米管阵列,用于高效检测 Fe3+ 离子
- 基于铂和镍锯齿状纳米线的用于检测咖啡酸的超稳定电化学传感器
- 使用新型均匀磁场改善磁性聚乙烯亚胺纳米颗粒向 MG-63 成骨细胞的磁转染


