构建具有增强光催化性能的 ZnTiO3/Bi4NbO8Cl 异质结
摘要
构建异质结是提高光催化剂光催化性能的有效策略。在此,我们通过典型的机械混合方法制备了性能提高的 ZnTiO3/Bi4NbO8Cl 异质结。在氙弧灯照射下,异质结上的罗丹明 (RhB) 降解率高于单独的 ZnTiO3 或 Bi4NbO8Cl。 ZnTiO3 与 Bi4NbO8Cl 结合可以抑制光激发载流子的复合。瞬态光电流响应 (PC)、电化学阻抗谱 (EIS)、光致发光 (PL) 光谱和时间分辨 PL (TRPL) 光谱证明了量子效率的提高。该研究对光催化剂的工业应用具有一定的参考价值。
介绍
近年来,光催化引起了人们极大的兴趣,已经在太阳能电池、水分解和水净化等领域得到了应用[1,2,3,4]。据报道,基于氧化物的半导体是活性光催化剂 [5],以 TiO2 [6, 7]、ZnO [8] 等为代表。然而,单独的原始 ZnO 或 TiO2 并没有表现出令人满意的光催化性能。特别是,ZnTiO3 在钙钛矿型氧化物中表现出更好的性能。 ZnTiO3 已被用于气体传感器和光催化等领域[9, 10]。然而,ZnTiO3 的宽带隙(3.1 ~ 3.65 eV)[9,10,11,12,13]限制了其对太阳能的利用。另一方面,光生电荷的高复合率是另一个限制因素。有必要采取措施提高其光催化性能。一种可行且方便的途径是将 ZnTiO3 与一种窄带隙半导体耦合形成异质结结构 [14]。窄带隙半导体可以作为敏化剂来提高捕光能力和光催化性能。
Bi4NbO8Cl 是一种有希望增加光捕获的候选者,具有多种优点,包括窄带隙 (~ 2.38 eV)、分层结构、合适的能带势 [15,16,17],出现在研究人员的视线中。由于其低带隙能量和分层结构,这种材料可以吸收波长低于 520 nm 的光,并有利于电荷转移 [18]。已经制备了一些基于 Bi4NbO8Cl 的异质结,例如 Bi2S3/Bi4NbO8Cl [17] 和 g-C3N4/Bi4NbO8Cl [19]。因此,构建ZnTiO3/Bi4NbO8Cl异质结可能是提高光催化性能的有效措施。
在这项研究中,我们制造了一系列 ZnTiO3/Bi4NbO8Cl 异质结,并评估了氙弧灯照射下 RhB 降解的光催化性能。我们的结果表明异质结的性能优于单个组件的性能。异质结的形成可以减缓电子和空穴的结合,从而增强 RhB 的降解活性。详细讨论了可能的光催化机理。
实验
材料
氧化铋(Bi2O3)、乙醇(C2H6O)、钛酸四丁酯(C16H36O4Ti)、醋酸(CH3COOH)、硝酸锌(Zn(NO3)2•6H2O)均购自国药集团化学试剂有限公司;氯氧化铋 (BiOCl) 和五氧化二铌 (Nb2O5) 购自 Energy Chemical(中国上海)。本工作所用试剂均为分析纯,未经进一步纯化。
Bi4NbO8Cl 的制备
Bi4NbO8Cl是通过球磨混合和固态反应法合成的。材料的混合在配备刚玉研磨罐和刚玉球的行星式球磨机(Grinoer-BM4,中国)中进行。将 Bi2O3(18g)、BiOCl(12g)和 Nb2O5(6g)称重并使用乙醇(30mL)作为研磨罐中的分散溶液混合,加入 50 个球(10mm 直径),然后球以 300 rpm 研磨 2 小时。研磨后,混合试剂在 60°C 下干燥 12 小时,并在 600°C(加热速率为 5°C/分钟)下在空气中煅烧 10 小时。最终得到Bi4NbO8Cl黄色粉末。
ZnTiO3 的制备
采用溶胶-凝胶法制备 ZnTiO3 粉末。在典型的合成中,将 34 mL 钛酸四丁酯(0.1 mol)溶解在 35 mL 乙醇中形成溶液 A。5 mL 去离子水、15 mL 乙酸 (CH3COOH) 和一定量的 Zn(NO3 )2•6H2O 依次溶解在 35 mL 乙醇中形成溶液 B。然后,在磁力搅拌下将溶液 B 滴加到溶液 A 中。在加入搅拌 30 分钟后获得透明溶胶,其在 24 小时的静止时间内形成凝胶。凝胶在 105°C 下干燥 12 小时,然后将所得产物在 600°C 下以 2°C/min 的加热速率煅烧 3 小时,以获得最终的 ZnTiO3 粉末。
ZnTiO3/Bi4NbO8Cl异质结的制备
在典型实验中,将 400 mg Bi4NbO8Cl 和一定量的 ZnTiO3(ZnTiO3:Bi4NbO8Cl 的质量比 =10%、20%、30%)混合研磨 10 分钟,然后将它们分散在 10 mL 乙醇中,然后超声 30 分钟。所得混合物在 60°C 下干燥 12 小时,然后在 300°C 下煅烧 2 小时。制成的样品分别表示为 10% BNZ、20% BNZ 和 30% BNZ。
特征化
X 射线粉末衍射 (XRD) 测量是用 D-max 2500 XRD 光谱仪 (Rigaku) 记录的,扫描范围为 10-80°,速度为 10°/min。通过扫描电子显微镜(SEM,JSM-6700F,JEOL,日本)和透射电子显微镜(TEM,JEM-2100,JEOL,日本)表征所制备样品的形态。能量色散谱和元素映射分析是用配备在扫描电子显微镜上的 X 射线光谱仪进行的。 UV-vis 漫反射光谱 (UV-vis DRS) 使用带有积分球的 Agilent Technologies Cary 5000 分光光度计获得,其中使用 BaSO4 粉末作为参比。光致发光 (PL) 和时间分辨瞬态 PL 衰减光谱分别在 Hitachi FL-4600 和 Edinburgh FLS1000 荧光分光光度计上记录,激发波长为 365 nm。
光催化实验
将 RhB 光降解作为模型反应进行检查,以评估样品的光催化性能。将 50 毫克光催化剂在 50 毫升 RhB 溶液 (5 毫克/升) 中分散到石英光反应器容器中。放置在距离反应器 15 厘米处的 500 瓦氙弧灯用作光源。最初,将混合物在磁力搅拌下在黑暗中保持 30 分钟以达到吸附-解吸平衡。随后,以 30 分钟的给定间隔时间对悬浮液的等分试样 (4 mL) 进行取样和离心。染料浓度采用Agilent Technologies Cary 5000分光光度计分析。
为了比较,将一定量的Bi4NbO8Cl和ZnTiO3(ZnTiO3:Bi4NbO8Cl的质量比 =20%)直接加入石英光反应器容器中进行光催化活性评价实验。该样品的结果命名为20% BNZ-C(“C”表示比较)。
捕获剂实验过程与光催化活性评价相同,分别加入40 μL异丙醇(IPA)作为羟基自由基清除剂,0.005 g对苯醌(BQ)作为超氧自由基清除剂,0.0158 g乙二胺四乙酸二钠盐(EDTA-2Na) 作为空穴捕获剂,0.078 g 溴酸钾 (KBrO3) 作为电子捕获剂。
电化学测量
光电化学性能在 CHI760E 电化学系统(中国上海晨华)上在标准三电极上测量,其中催化剂沉积的 FTO 玻璃、Pt 板和 Ag/AgCl 电极分别作为光阳极、对电极和参比电极。同时,使用 0.5 M Na2SO4 作为电解质溶液。使用 500 瓦氙灯作为光源进行瞬态光电流测量。 Mott-Schottky 测量在 1000 Hz 的频率下进行。如下制备工作光阳极:通过搅拌 20 分钟混合 30 毫克样品、300 微升壳聚糖 (1% wt%) 和乙酸 (1% wt%) 混合溶液以制成悬浮液。然后,将上述混合物滴加到 FTO 玻璃(3 × 1 cm)上并在 40°C 下干燥。
结果与讨论
样品的晶体结构可以从 XRD 结果 [20] 中检测到,如图 1a 所示。 23.7°、26.0°、29.6°、32.6°、46.7°和56.3°的特征衍射峰可以索引到(112)、(114)、(116)、(020)、(220)和( 316) 裸 Bi4NbO8Cl 平面(JCPDS 卡 84-0843)。晶面(220)、(311)、(400)、(422)、(511)和(440)与立方钙钛矿ZnTiO3结构(空间群R-3,晶胞常数a =b =c =0.841 nm,JCPDS 卡 39-0190)。 BNZ样品的XRD图谱与Bi4NbO8Cl相似,ZnTiO3在35.4°处的反射衍射峰强度随着ZnTiO3含量的增加而增加。此外,从 ZnTiO3/Bi4NbO8Cl 异质结的 EDX 映射图像(图 1d)中观察到与 Zn、Ti、Bi、Nb、O 和 Cl 相关的信号。
<图片>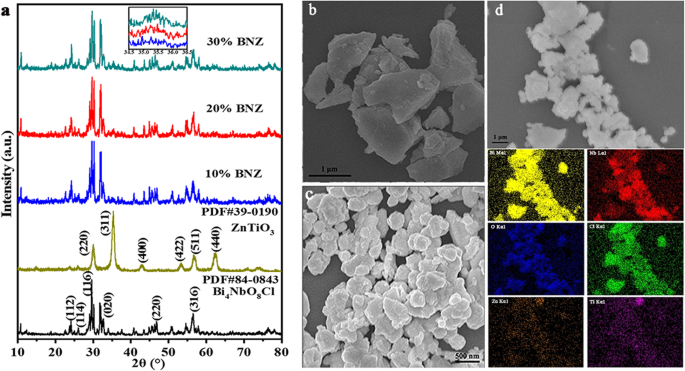
一 ZnTiO3、Bi4NbO8Cl和BNZ样品的XRD图谱; b 的 SEM 图像 Bi4NbO8Cl,c ZnTiO3,d SEM图像,以及20% BNZ的EDX映射图像
通过SEM研究了ZnTiO3、Bi4NbO8Cl和BNZ样品的形貌。图 1b 显示 ZnTiO3 样品为微米级不规则块状结构。原始 Bi4NbO8Cl 产品由不规则的椭球颗粒组成,由于颗粒聚集在一起,因此显示出堆叠结构,如图 1c 所示。对于20%的BNZ化合物(图1d),可以发现经过研磨、超声混合和煅烧处理后,ZnTiO3被粉碎并附着在Bi4NbO8Cl表面。
图 2 显示了 20% BNZ 样品的 TEM 和 HRTEM 图像,以及相应选择区域的快速傅里叶变换 (FFT) 模式和逆 FFT (IFFT) 图像。可以清楚地观察到 ZnTiO3 块和 Bi4NbO8Cl 块之间存在紧密的界面接触(图 2a)。在图 2b 中用红色线框标记,测量的 0.375 nm 晶格条纹对应于 Bi4NbO8Cl (112) 晶面,其相应的 FFT 和 IFFT 显示在图 2c 中。如图 2b 所示,测得的 0.301 nm 和 0.293 nm 晶格条纹与 Bi4NbO8Cl(116)晶面(绿色区域)和 ZnTiO3(311)晶面(橙色区域)匹配良好,它们的 FFT 和 IFFT 图像为分别如图 2d 和图 2e 所示。 HRTEM分析表明Bi4NbO8Cl和ZnTiO3结合良好。
<图片>
一 , b 20% BNZ 的 TEM 和 HRTEM 图像; c Bi4NbO8Cl (112) 晶面的 IFFT 和 FFT 图像; d Bi4NbO8Cl (116) 晶面的 IFFT 和 FFT 图像; e ZnTiO3(311)晶面的IFFT和FFT图像
通过氙弧灯照射下 RhB 染料水溶液的降解来评估原始 Bi4NbO8Cl、ZnTiO3 和 BNZ 异质结的光催化性能。如图 3a 所示,所有样品在黑暗中的 RhB 吸附率为 0-11%。曝光 5 小时后,裸 Bi4NbO8Cl 和 ZnTiO3 的降解率分别为 89% 和 61%。此外,BNZ复合材料表现出提高的光催化活性,染料去除效率首先随着ZnTiO3含量的增加而增加,然后当ZnTiO3含量从20wt%增加到30wt%时光降解性能略有下降。 20% BNZ 复合材料显示出最高的光催化活性,降解率几乎为 100%。对于 20% BNZ-C,反应 5 小时后,RhB 去除率为 81%。由于异质结形成后载流子的有效分离,20%的BNZ表现出更高的光催化性能。
<图片>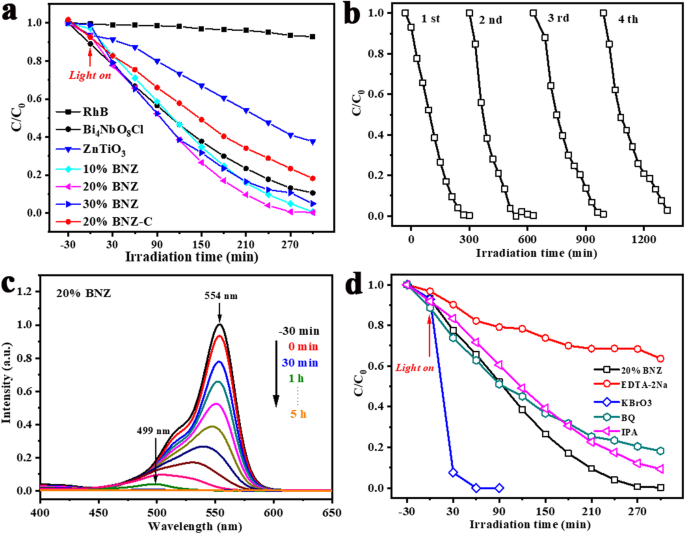
一 氙弧灯照射下 ZnTiO3、Bi4NbO8Cl 和 BNZ 异质结对 RhB 的光催化降解效率; b 循环运行 20% BNZ; c 在氙弧灯照射下,20% BNZ 对 RhB 的紫外可见吸收光谱的变化; d 氙弧灯照射下20% BNZ的捕集实验结果
光催化剂的可回收性也是其实际应用中的一个重要方面。在相同条件下进行去除 RhB 染料的循环实验,以研究 20% BNZ 样品的可回收性,如图 3b 所示。经过四次重复实验,光催化活性仅略有下降,表明20%的BNZ是一种稳定的降解RhB的光催化剂。图3c显示了20% BNZ后RhB的UV-vis吸收光谱的变化,随着照射时间的增加,特征峰的强度降低。此外,在光催化反应过程中,吸收峰的位置从 554 nm 移动到 499 nm。这种吸收最大值的蓝移是由 N -RhB的去乙基化[21,22,23]。
为了阐明导致 20% BNZ 复合材料降解 RhB 的主要活性物质,进行了捕获实验。乙二胺四乙酸二钠盐 (EDTA-2Na)、溴酸钾 (KBrO3)、苯醌 (BQ) 和异丙醇 (IPA) 作为空穴清除剂 (h + ), 电子 (e − ), 超氧自由基 (•O2 − ) 和羟基自由基 (•OH),分别。如图 3d 所示,在光催化反应体系中加入 EDTA 会严重影响并降低光降解速率,加入 BQ 或 IPA 时光催化活性受到轻微抑制。因此, h + 是主要的优势反应物种,而 •O2 − 或•OH参与了RhB在20% BNZ体系中的降解过程。
如图 4a 所示,在光照射下以间歇性开关循环测量所制备的光催化剂的瞬态光电流响应,以评估光生载流子的产生和迁移。光电流强度越高,光生载流子的产生能力越强[24, 25]。光电流密度在亮处比在暗处高,表现出典型的开关循环模式。光电流响应强度遵循以下顺序:20% BNZ> 30% BNZ> 10% BNZ> Bi4NbO8Cl> ZnTiO3。这意味着20% BNZ的光生载流子的生产能力是最好的。 20% BNZ 样品的光电流密度明显提高,这归因于异质结中的密切接触,这有利于电荷的产生、分离和转移。此外,采用电化学阻抗谱(EIS)来研究催化剂界面电荷转移的能力。 EIS Nyquist 图的圆弧半径越小,电荷转移电阻越小[26]。从结果(图 4b)可以看出,20% BNZ 表现出最小的半圆弧,这表明 20% BNZ 具有较小的转移电阻,并且与其他相比,电荷载流子过程非常快,如- 准备好的样品。为了研究光生载流子的复合行为,获得了室温下激发波长为 365 nm 的 PL 光谱(图 4c)[27]。与裸 Bi4NbO8Cl 相比,所制备的 20% BNZ 的 PL 强度较弱,表明光生载流子的复合率较低。这些结果表明 ZnTiO3 的引入可以有效抑制光生电子 (e − ) 和孔 (h + )。如图 4d 所示,时间分辨 PL 光谱可以提供有关光激发载流子寿命的信息。样品的时间分辨 PL 衰减曲线由方程拟合。 (1):
$$ I(t)={A}_1{e}^{\frac{-t}{\tau_1}}+{A}_2{e}^{\frac{-t}{\tau_2}} $$ (1)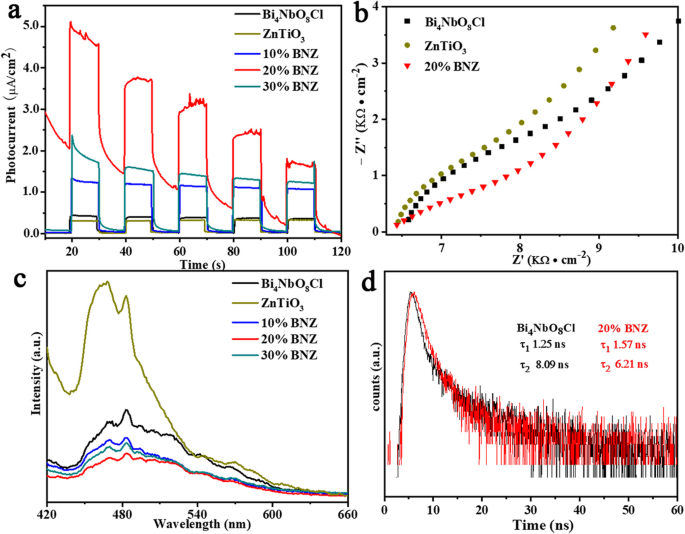
一 ZnTiO3、Bi4NbO8Cl 和 BNZ 样品的瞬态光电流响应。 b ZnTiO3、Bi4NbO8Cl 和 20% BNZ 的电化学阻抗谱。 c ZnTiO3、Bi4NbO8Cl 和 BNZ 样品的光致发光光谱。 d Bi4NbO8Cl和20% BNZ的时间分辨PL光谱
其中 τ 1 和 τ 2 分别是快速衰减常数(寿命较短)和较慢衰减常数(寿命长)。 A 1 和 A 2是对应的幅度。平均寿命通过等式计算。 (2) [17]:
$$ \uptau =\frac{A_1{\tau}_1^2+{A}_2{\tau}_2^2}{A_1{\tau}_1+{A}_2{\tau}_2} $$ (2 )20% BNZ 的平均寿命比 Bi4NbO8Cl 短(τBiNb =3.66 ns 和 τ20%BNZ =2.72 ns)。 τ ZnTiO3改性后的值从3.66降低到2.72,表明异质结的形成可以提高载流子的转移效率,促进光生电子和空穴的分离[28,29,30]。
在 300-800 nm 范围内测量 Bi4NbO8Cl、ZnTiO3 和 20% BNZ 的漫反射光谱 (DRS) 以研究它们的光学特性。如图 5a 所示,可以发现 ZnTiO3 的吸收边为 375 nm,而 Bi4NbO8Cl 在 505 nm 附近有一个吸收边陡峭的强吸收带。此外,吸收边 20% BNZ 约为 510 nm。此外,半导体的带隙能量 (Eg) 可以通过 Tauc 方程计算, (αhv) n =A (hv − Eg), 其中 Eg, A , α , h , 和 v 分别是带隙、吸收常数、吸收系数、普朗克常数和光频率 [31]。此外,n 代表直接过渡材料 (n =2) 或间接过渡材料 (n =1/2)。众所周知,Bi4NbO8Cl和ZnTiO3都是间接过渡半导体,因此n 等于 4。如图 5b 所示,所制备的 Bi4NbO8Cl、ZnTiO3 和 20% BNZ 样品的带隙值分别为 2.33 eV、3.10 eV 和 2.31 eV。
<图片>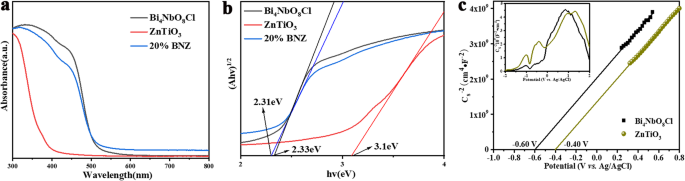
一 ZnTiO3、Bi4NbO8Cl 和 20% BNZ 样品的 DRS 光谱。 b ZnTiO3、Bi4NbO8Cl 和 20% BNZ 样品的 Tacus 曲线。 c ZnTiO3和Bi4NbO8Cl的Mott-Schottky曲线
导带 (CB) 电位和价带 (VB) 电位是了解纳米复合材料异质结形成和电子转移机制的最重要因素。已知CB底部靠近平带位置;因此,进行了莫特-肖特基测试来估计样品的平带电位 (Efb) [32]。使用以下方程从 M-S 图中获得电极的相应平带电位。 (3) 和 (4) [31, 33]:
$$ \mathrm{For}\ \mathrm{an}\ \mathrm{n}-\mathrm{type}\ \mathrm{semiconductor}\frac{1}{C^2}=\frac{2}{e\ varepsilon {\varepsilon}_o ND}\left(E-{E}_{fb}-\frac{KT}{e}\right) $$ (3) $$ \mathrm{For}\ \mathrm{an} \ \mathrm{p}-\mathrm{type}\ \mathrm{semiconductor}\frac{1}{C^2}=\frac{2}{e\varepsilon {\varepsilon}_0 NA}\left(E- {E}_{fb}-\frac{KT}{e}\right) $$ (4)其中 ε , ε o, e , C , E , E fb, K , T , N D 和 N A代表材料的介电常数、自由空间的介电常数、电子的电荷数(1.60 × 10 −19 C),空间电荷区的电容,分别施加到电位、平带电位、玻尔兹曼常数、绝对温度、施主和受主密度。如图 5c 所示,所有曲线都显示正斜率,这清楚地证实了所制备的样品作为 n 型半导体行为 [34, 35]。可以从线性电位曲线的交点到 X 测量平带电位 -轴在点 1/C 2 =0,并且可以根据公式(5)[36]转换为归一化氢电极标度(NHE):
$$ E\left(\mathrm{NHE}\right)=E\left(\mathrm{Ag}/\mathrm{AgCI}\right)+0.197\mathrm{V} $$ (5)根据 M-S 结果,Bi4NbO8Cl 和 ZnTiO3 的平带电位分别为 - 0.60 eV 和 - 0.40 eV(相对于 Ag/AgCl)。因此,Bi4NbO8Cl 和 ZnTiO3 的 ECB 分别为 - 0.403 eV 和 - 0.203 eV。因此,Bi4NbO8Cl 的 EVB 为 1.927 eV,ZnTiO3 的 EVB 为 2.897 eV。
Bi4NbO8Cl、ZnTiO3 和 20% BNZ 的比 BET 表面积如表 1 所示。20% BNZ 的 SBET 为 0.87 m 2 /g 超过 Bi4NbO8Cl 的 SBET。从表 1 可以看出,ZnTiO3 的 SBET 为 5.34 m 2 /G。 SBET 增加 20% BNZ 是由于引入了 ZnTiO3。 ZnTiO3 的带隙较宽,利用光的能力较弱。因此,增加的 SBET 可能无法提供许多有效的活性位点。相比之下,ZnTiO3 可能覆盖 Bi4NbO8Cl 表面的活性位点或成为新的电子和空穴复合中心。因此,增加 20% BNZ 的 SBET 可能仅对增强的光催化性能产生轻微影响。性能的提高主要是由于异质结的形成。
为了解释增强的光催化性能,方案 1 中提出了一种可能的光催化机制。在氙弧灯照射下,电子 (e − ) 在 Bi4NbO8Cl 中生成,它们从 VB 转移到 CB 留下相应的孔 (h + ) 在 VB 上。同时,同样的过程发生在 ZnTiO3 中。通过Bi4NbO8Cl和ZnTiO3能带电位的比较,ECB(Bi4NbO8Cl)比ECB(ZnTiO3)更负,EVB(ZnTiO3)比EVB(Bi4NbO8Cl)更正。因此,它们可以形成 II 型异质结。由于内部电场,e − Bi4NbO8Cl的CB转移到ZnTiO3的CB上,h + ZnTiO3 的 VB 转移到 Bi4NbO8Cl 的 VB,实现了光激发 e − 的分离 -h + 对,从而提高性能。由于20%的BNZ具有较高的VB正电位,因此其空穴具有较高的氧化能力。因此,VB 上的空穴可以直接氧化 RhB 等有机污染物。然而,BNZ异质结中ZnTiO3比例过高会覆盖Bi4NbO8Cl表面的活性位点,降低其捕光能力。此外,过量的ZnTiO3可能成为新的电子和空穴的复合中心。因此,异质结中ZnTiO3的用量有一个最佳值。
<图片>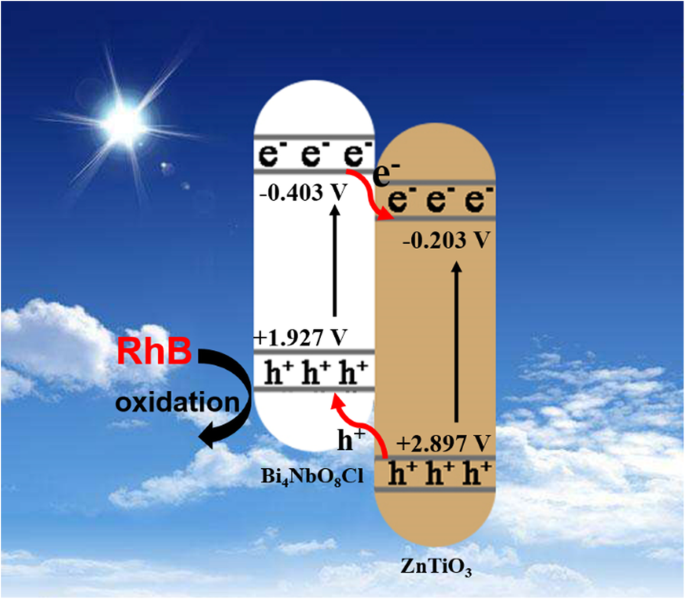
氙弧灯照射下ZnTiO3/Bi4NbO8Cl异质结光催化剂降解RhB的机理示意图。
结论
在这项工作中,通过典型的机械混合方法成功制备了 ZnTiO3/Bi4NbO8Cl 异质结催化剂。在氙弧灯照射下,与单独的 ZnTiO3 或 Bi4NbO8Cl 相比,异质结表现出增强的光催化性能。特别是20%的ZnTiO3/Bi4NbO8Cl异质结性能最好。该报告可能对异质结结构在催化剂改性和应用方面的发展具有启发意义。
数据和材料的可用性
当前研究中使用的数据集可根据合理要求从通讯作者处获得。
缩写
- BNZ:
-
ZnTiO3/Bi4NbO8Cl
- BNZ-C:
-
ZnTiO3/Bi4NbO8Cl-对比
- SBET:
-
BET比表面积
- PL:
-
光致发光
- CB:
-
导带
- VB:
-
价带
纳米材料
- 通过自动焊接提高性能
- 博客:具有出色性能的医疗可穿戴设备
- LiNi0.8Co0.15Al0.05O2/碳纳米管的机械复合材料具有增强的锂离子电池电化学性能
- Au-Plasmonic 纳米粒子在涂有 MoO3 的 TiO2 纳米管光电极上增强光催化活性
- N 掺杂 ZnO/g-C3N4 纳米复合材料的可见光驱动光催化性能
- 中空结构LiNb3O8光催化剂的制备和光催化性能
- 具有增强光催化性能的新型 Bi4Ti3O12/Ag3PO4 异质结光催化剂
- Ag 纳米颗粒/BiV1-xMoxO4 与增强的光催化活性的协同效应
- 通过快速硒化方法增强 Sb2S3 平面异质结太阳能电池的光伏特性
- 用于染料降解的新型 p-Ag3PO4/n-BiFeO3 异质结复合材料的简便合成和增强的可见光光催化活性
- 具有增强有效光吸收的针结纳米锥阵列太阳能电池的光伏性能
- 电动建筑设备与柴油机性能比较


