利用柠檬汁通过水热反应制备的荧光碳量子点的材料和光学特性
摘要
以柠檬汁为碳源,通过简单的水热反应合成水溶性荧光碳量子点(CQDs)。获得的 CQD 的平均尺寸为 3.1 nm。它们显示出均匀的形态和良好的结晶,并且在紫外线或蓝光照射下可以产生明亮的蓝绿色光发射。我们发现这些 CQDs 的荧光主要是由 CQDs 表面和边缘上含氧基团的存在引起的。此外,我们证明所制备的 CQD 可用于对植物细胞进行成像。本研究涉及新开发的碳纳米结构的制备、研究和应用。
背景
碳量子点(CQD)是一类新的碳基纳米材料,其空间尺寸通常小于 20 nm,由 Xu 等人发现。 2004 年 [1]。荧光碳纳米粒子由 Sun 等人制造。 2006 年通过激光烧蚀石墨粉 [2] 并从那时起被命名为“碳量子点 (CQDs)”。荧光碳量子点在光催化、光电器件、生物医学、薄膜显示、健康照明和其他实际应用学科中具有巨大的应用潜力。与传统的基于半导体的量子点相比,CQDs可以通过低成本的制造技术获得,并具有良好的生物相容性、精确的生物靶点、低毒性和更强的量子尺寸效应等迷人而重要的特点。近年来,荧光 CQDs 因其优异的结构和光学特性而引起了极大的关注 [3, 4] [5]。它们已被提议作为传统半导体量子点的替代材料,应用于生物成像、生物标记、量子点 LED (QLED)、环境保护和其他相关领域 [6,7,8,9]。 CQDs 的研究在凝聚态物理、材料科学、电子学和光电子学领域发展迅速。相关基础和应用研究已在世界范围内广泛开展[3,4,5,6,7,8,9]。
目前,合成碳量子点的技术有多种[10, 11],如水热法[11, 12]、微波法[13]等。 CQDs 由各种碳前体合成,如葡萄糖 [14]、柠檬酸 [15] 和抗坏血酸 [16]。然而,大规模生产生物相容性荧光 CQD 的有效制造技术仍然需要,并已成为 CQD 实际应用的挑战。已经注意到,从食品 [17,18,19] 和/或副产品 [20] 直接合成 CQDs 是一种有前途和重要的策略。通过加热无果肉柠檬汁的乙醇溶液,在水中合成了平均直径为 4 nm 且量子产率 (QY) 为 28% 的发红光碳点 (R-CD) [21]。添加到 R-CD 中的强还原剂 NaBH4 被用作增加 R-CD 光发射强度的手段。但是,我们知道 NaBH4 是有毒的。最近,我们在不添加任何有毒物质的情况下,从豆腐废水中制造了发绿光和蓝光的 CQD [22]。由食品和/或副产品制成的 CQD 被认为对生物应用是安全的,因为这些天然碳资源几乎没有已知的毒性。近年来,针对无毒碳资源一步法合成碳量子点的研究开展了多项认真的研究,并在这些碳量子点的合成、研究和应用方面取得了重大进展。例如,大蒜被用作合成 CQDs 的绿色来源 [23]。详细的结构和成分研究表明 [23] N 的含量以及 C-N 和 C=N 的形成是提高光致发光 (PL) QY 的关键。此外,CQDs 在较宽的 pH 范围和高 NaCl 浓度下表现出优异的稳定性,使其适用于复杂和恶劣的条件 [23]。
目前工作的主要动机是开发一种简单有效的实验方法,通过在相对较低的温度下使用水热处理和耗时较少的过程,从柠檬汁中低成本制造 CQD。众所周知,柠檬汁可以轻松且廉价地获得,因此,它是基于 CQD 的样品和设备制造的良好碳源。与之前的研究 [21] 相比,我们工作中获得的无毒 CQDs 更适合于生物成像和细胞标记。在本研究中,我们还对柠檬汁实现的CQDs的基本材料和光学性质进行了研究,并将CQDs应用于植物细胞成像。
方法
预备材料
在这项研究中,碳前体材料取自新鲜柠檬汁。主要成分及其百分比通过高效液相色谱(HPLC)测定得到,如表 1 所示。样品制备以新鲜柠檬为碳源,用于细胞成像的新鲜洋葱购自当地超市。乙醇为分析纯,用作分散剂。实验使用去离子水(18.25 MΩ cm)。
CQD 的合成
CQDs 是从柠檬汁中通过简单的水热处理在相对较低的温度和耗时较少的过程中合成的。典型的样品制备过程如图 1 所示。将 80 毫升无果肉柠檬汁与 60 毫升乙醇混合。然后将混合物转移到配备聚四氟乙烯的不锈钢高压釜中,并在约 120°C 的恒温下加热 3 小时。反应结束后自然冷却至室温,得到深棕色产物。用过量的二氯甲烷洗涤深棕色溶液以除去未反应的有机部分,此步骤可重复 2-3 次。加入去离子水直到棕色溶液的体积增加到溶液的三分之一,并以 10000 rpm 离心 15 分钟以分离大颗粒。因此,CQD 样品可以通过柠檬汁的碳化获得,柠檬汁含有碳水化合物和有机酸,如葡萄糖、果糖、蔗糖、抗坏血酸、柠檬酸等作为碳前体。与报道的方法 [24] 相比,我们简便的水热反应温度较低 (120 °C),耗时更短 (3 h)。
<图片>
柠檬汁水热处理制备碳量子点
特征化
通过在 300 KV 下操作的透射电子显微镜(JEM 2100,日本)分析从柠檬汁中获得的 CQD 的形态和微观结构。使用 Cu-Kα 辐射(λ =0.15418 纳米)。 UV-Vis吸收光谱通过UV-Vis分光光度计(Specord200)测量。通过荧光分光光度计(IHR320,HORIBA Jobin Yvon,USA)针对 330 至 490 nm 范围内的不同激发波长检查光子诱导的光发射。 X射线光电子能谱(XPS)光谱由PHI5000 Versa Probe II光电子能谱仪记录,Al Kα为1486.6 eV。
结果和讨论
CQDs 的透射电子显微镜 (TEM) 图像如图 2 所示。所制备样品的低倍 TEM 图像表明 CQDs 具有均匀的分散性。 CQD 呈球形,尺寸分布范围为 2.0 至 4.5 nm,平均尺寸为 3.1 nm,如图 2b、c 所示。图 2d 显示了 0.215 nm 的晶格间距,对应于石墨碳的 [100] 面,相应的 CQD 的快速傅立叶变换 (FFT) 模式进一步显示了高度结晶的结构,与之前的报告 [25] 一致。与之前的研究 [19, 21,22,23] 相比,如图 2 所示,我们工作中获得的 CQD 不仅具有良好的质量,而且表现出更好的均匀形态。因此,可以通过简单的水热处理工艺制造具有均匀圆形形态和良好结晶的 CQD。 CQDs的产率(PY)可以根据定义PY =(m /M ) × 100%,其中 m 是 CQD 的质量,M 是新鲜柠檬汁的质量。根据测定结果,本研究制备的CQDs的产率约为0.1%,即100 g液体与6.30%的柠檬酸可得到约0.1 g CQDs(见表1)。
<图片>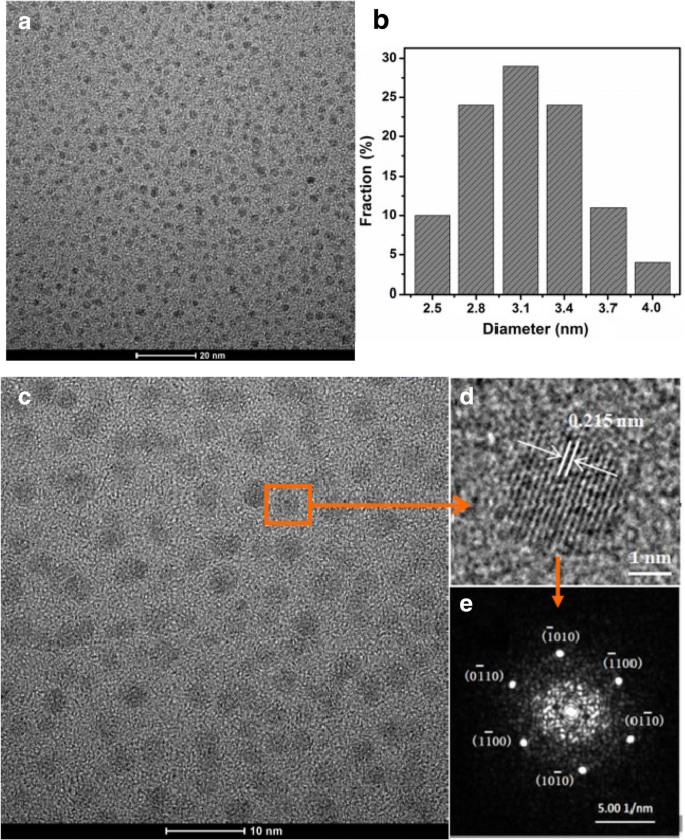
一 , c , d 透射电镜图像。 b CQD 的粒径分布。 e CQDs对应的FFT模式
CQDs 的典型 X 射线衍射 (XRD) 和 XPS 分布如图 3 所示。有一个宽 (002) 峰集中在 2θ ~21.73°,计算出的层间距为 0.409 nm,对应于石墨结构,如图 3a 所示,这与报道的其他方法制备的 CQD 的贬值相似 [15, 26]。层间距的变化可能是由于在制备 CQD 的水热反应过程中引入了更多的含氧基团,例如在 CQD 表面和边缘存在 -OH 和 -COOH。 XPS 和 FTIR 被用来检测 CQDs 的组成。如图 3b、c 所示,XPS 光谱显示 CQD 的主要石墨 C1s 峰位于 284.5 eV,O1s 峰位于 531.4 eV。在 C1s XPS 光谱的高分辨率扫描中,284.7、286.5 和 288.9 eV 的典型峰(图 3c 分别归因于 C=C/C-C、C-O 和 C=O/COOH)。这清楚地表明,CQDs 被羟基、羰基和羧酸基团官能化,有利于表面改性和官能化,也有利于在水中的溶解性。图 3d 显示了傅里叶变换红外光谱 (FTIR) 光谱CQDs。通过 3450 cm -1 处的峰证实 CQDs 中存在不同类型的氧官能团 (O–H 伸缩振动),2927 cm −1 , 1407 厘米 −1 (C–H 伸缩振动),1726 cm −1 (C=O 伸缩振动),1639 cm −1 (C=C 伸缩振动),1227 cm −1 (C–OH 伸缩振动)和 1080 cm −1 (C-O 伸缩振动)。注意到 FTIR 分析与上述 XPS 结果一致。最重要的是,C-O-C(环氧树脂)峰在 1290 cm -1 处完全消失 .这些结果暗示了 CQDs 的形成机制,环氧基断裂并形成下面的 C-C 键,随后形成 sp 2 通过进一步脱水或碳化,从葡萄糖、果糖、抗坏血酸和柠檬酸等小分子前体中提取结构域,最终形成 CQD。因此,周围氧基团的键断裂有助于CQDs的形成[15, 27]。
<图片>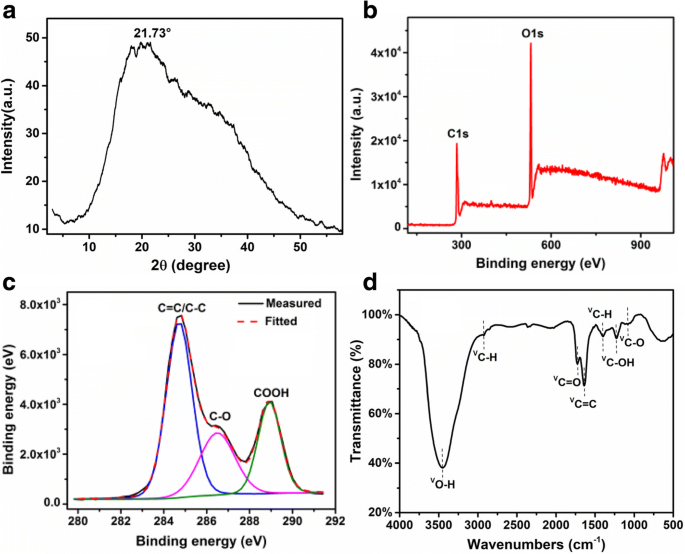
一 XRD 图。 b 低范围 XPS 光谱。 c C1s 区域的 XPS 高分辨率扫描。 d CQDs的FTIR光谱
目前,已经提出并研究了通过水热法从碳前驱体形成 CQD 的可能机制 [28]。基于这些已发表的结果,我们可以了解柠檬汁中 CQDs 的合成机制。无果肉柠檬汁经加热脱水形成主要由CQDs组成的C=C/C-C基本骨架,其余分子到达核表面生成新的C=C/ C-C 键,然后以这种形式不断增长。随着加热时间的延长,CQDs的形貌逐渐形成。同时,在水热处理形成CQDs的过程中,CQDs的表面和边缘可能含有大量的羟基(-OH)、羧基(-COOH)和羰基(-C=O)或其他氧-含有官能团;这些基团中的一部分H和O原子可以通过水热环境中的脱水去除。
为了检查 CQD 的光学特性,相应地测量了 CQD 的紫外-可见 (UV-Vis) 吸收和光致发光 (PL) 光谱。如图 4a 所示,在紫外区观察到 CQD 的光学吸收峰,最大吸收在 283 nm,这是由于 n -π * C=O 带的转变 [29]。图 4b 中的 PL 光谱显示 CQD 的 PL 发射波长在 482 nm 处达到峰值,激发波长为 410 nm。当激发波长从 330 nm 增加到 490 nm 时,发射波长从 430 nm 移动到 530 nm。随着激发波长的增加,荧光发射峰发生红移,表示发生光子重吸收。结果表明 CQD 具有依赖于激发的 PL 特征 [30]。绿色荧光 CQD 还显示出一个宽的 PL 峰,该峰随着激发波长的变化而移动,这与量子限制效应和边缘缺陷有关。使用标准 PL 测量 [22],CQD 的荧光量子产率为 16.7%,激发波长为 410 nm,其中硫酸奎宁已用作参考。该值明显优于之前报告中由柠檬汁制成的 CQD 的 QY (8.95%) [24]。众所周知,在表面改性或钝化后,CQD 的 QY 可以显着提高 [30]。在合成过程中加入乙醇可以引入更多的官能团,从而导致 CQD 的 QY 更高。然而,本研究中 CQDs 的 QY 明显低于使用柠檬酸 (CA) 和乙醇胺 (EA) 作为模型分子合成的 CQDs 的 QY。在这里,在 180 °C 下热解产生了具有强烈 PL 和 50% 高 QY 的分子前体,这是由于合成过程中的 N 掺杂 [30]。
<图片>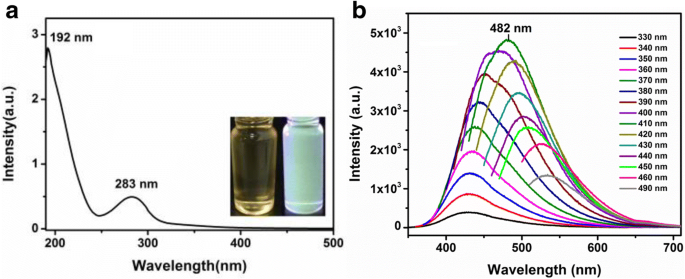
一 CQD 的紫外-可见吸收光谱,插图:日光(左)和紫外光(右)下的光学图像。 b CQDs在不同激发波长下的PL光谱
由于无毒和环境友好,CQDs 被认为是半导体量子点的替代品,可应用于体外和体内生物系统。将合成的 CQD 应用于洋葱表皮细胞的光学图像中,如图 5 所示。荧光显微镜显示洋葱内表皮细胞的细胞壁和细胞核可以清楚地看到,层状良好且立体感很强。结果表明,碳量子点的染色和成像效果非常好,对生物体没有不利影响,也没有观察到细胞的形态学损伤,进一步证明了碳量子点具有低细胞毒性。图 5 中的共聚焦图像表明柠檬汁合成的 CQDs 可作为荧光指示剂用于植物细胞成像,进一步展示了 CQDs 生物成像的潜在应用。
<图片>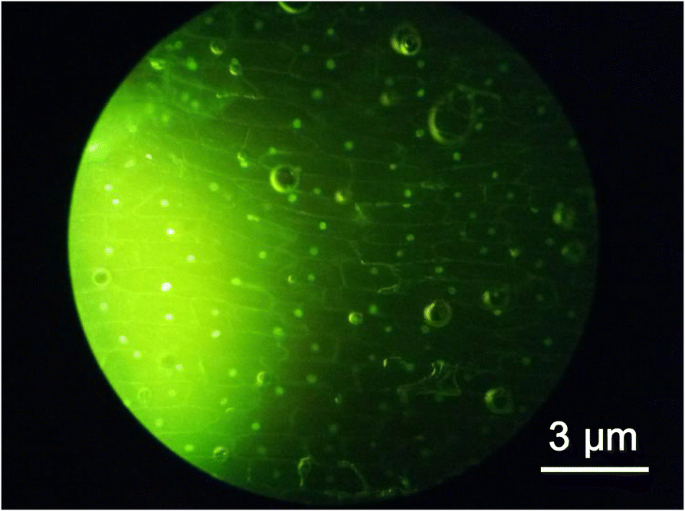
蓝色光源照射下CQDs染色洋葱表皮细胞的光学图像
结论
本研究以柠檬汁为碳源,通过简单的水热反应合成了水溶性荧光碳量子点。这些 CQD 具有良好的材料和光学性能。在紫外线或蓝光照射下,它们可以发出明亮的蓝绿色荧光。我们已经证明 CQD 可用于植物细胞的成像。我们希望这些重要且意义重大的发现能够帮助我们深入了解 CQD,并探索新型碳基纳米结构的更多实际应用。
缩写
- CQD:
-
碳量子点
- FFT:
-
快速傅里叶变换
- HPLC:
-
高效液相色谱
- PL:
-
光致发光
- QLED:
-
量子点LED
- QY:
-
量子产率
- R-CD:
-
发红碳点
- TEM:
-
透射电子显微镜
- 紫外可见光:
-
紫外可见
- XPS:
-
X射线光电子能谱
- XRD:
-
X射线衍射
纳米材料
- H2/NH3 混合气体中基于 GaN 的多量子阱的原子重排以改善结构和光学性能
- 垂直电场对 ML-GaS 的电子和光学各向异性特性的调制
- 小型硒纳米晶体和纳米棒的简便合成和光学特性
- 合成富含吡啶的 N、S 共掺杂碳量子点作为有效的酶模拟物
- 化学蚀刻制备的硅纳米线的光学和电学特性
- 从豆腐废水中合成荧光碳量子点的简单方法
- 水溶性硫化锑量子点的合成及其光电特性
- 石墨烯/Ag3PO4 量子点复合材料的简便一步声化学合成和光催化性能
- 溶胶-凝胶法合成的 Pr 掺杂钙钛矿锰酸盐 La0.67Ca0.33MnO3 纳米颗粒的微观结构、磁性和光学性能
- 水溶性蓝色发光锰合金碲化碲化镉量子点的合成和性质
- 碱金属吸附的 g-GaN 单层:超低功函数和光学特性
- 通过生长掺杂方法实现双发射和颜色可调的 Mn 掺杂 InP/ZnS 量子点


