Pr2CuO4 纳米片的可控合成和选择性吸附特性:机理讨论
摘要
使用配位化合物法 (CCM) 合成了厚度约为 60 nm 的四方相 Pr2CuO4 纳米片,然后用作对水溶液中孔雀石绿 (MG) 的高效选择性吸附剂。使用 X 射线衍射 (XRD)、扫描电子显微镜 (SEM)、高分辨率透射电子显微镜 (HRTEM)、X 射线光电子能谱 (XPS)、紫外-可见漫反射光谱 (DRS)、和标准的 Brunauer-Emmett-Teller (BET) 方法。最大吸附容量(Q 米 ) 所制备样品的吸附等温线通过不同吸附剂剂量 (m ) 在 298、318 和 338 K 下为 0.03–0.07 g,基于 Langmuir 模型。当 m <0.03 g 或> 0.07 g,系统质量损失和颗粒聚集的影响在 298 K 时与朗缪尔模型的数据偏差进行了讨论。基于氢键和配位键,Pr2CuO4 选择性吸附 MG 的可能机制是CuO和Pr2O3对MG的吸附实验和竞争离子实验进一步证实了这一点。最后,在DFT水平上进行了理论研究,揭示了可能的吸附过程。
背景
在过去的几十年里,工业排放的含染料废水是特别危险的污染物,因为染料,如甲基橙(MO)、亚甲蓝(MB)、罗丹明 B(RhB)、孔雀石绿(MG)等,在人体内不可生物降解 [1,2,3,4,5,6]。其中,MG作为一种常用的染料,最近被用作鱼卵的杀菌剂[7, 8]。因此,它常常与其他废水一起出现在地表水中,对人类健康构成严重威胁[9、10]。因此,许多吸附剂,例如纳米氧化物(即 ZnO 和 ZrO)[11,12,13]、介孔材料(即有序介孔碳和介孔聚(丙烯酸)/SiO2)[14, 15] 和据报道,一些金属有机框架 (MOF) [1] 可用于吸附 MG。据报道,在这些吸附剂中,花状 ZnO 具有最大的 Q 米 (最大吸附容量)为 2587 毫克/克。然而,它们对MG的吸附能力在实际水中大大降低,因为这些吸附剂很容易被各种有机化合物覆盖。因此,关注大容量和选择性吸附剂的研究对于有机染料的吸附具有重要意义[7, 8, 16, 17]。令人鼓舞的是,稀土铜酸盐对 MG 具有最大的特殊吸附容量(即 Q 米 Dy2Cu2O5 高于 5.54 g/g) [17];但是,机制还不是很清楚。
这种对稀土铜酸盐的选择性吸附应根据MG不同于其他染料的特定分子结构进行研究。正如 Y. Li 等人报道的那样。 [4],MG在水溶液中具有异构体(隐色孔雀石绿,LMG),含有可配位的氧原子。因此,我们提出了一种基于吸附过程中配位键的机制,如MOFs [1, 2, 17]。
在这项工作中,我们更深入地了解了 MG 在 Pr2CuO4 吸附剂上的吸附过程中吸附数据与 Langmuir 模型的偏差。另一个目标是解释 Ln-Cu-O 化合物对 MG 的大选择性吸附以及多层吸附机制的可能性。针对吸附过程中形成氢键和配位键的可能性,进行了DFT水平的理论研究。
与过渡金属氧化物和稀土氧化物的众多催化剂和吸附剂相比,关于 Ln2CuO4 型稀土铜酸盐的化学性质的报道很少[18,19,20]。据我们所知,这是关于 Pr2CuO4 对 MG 的吸附机制的第一份报告,伴随着大的 Q 米 室温下的值。
方法/实验
材料
Cu(OAc)2·4H2O、Pr(NO3)3·5H2O、3,4-pdc 和三乙胺购自国药集团化学试剂有限公司(中国上海)。孔雀石绿(MG)购自上海阿拉丁实业公司。本研究所用试剂均为分析纯,未经进一步处理直接使用。
综合
CCM 前体 [PrCu(3,4-pdc)2(OAc)(H2O)2] •10.5H2O 根据我们之前的研究制备 [21, 22]。将相应化学计量比的Cu(OAc)2·4H2O、Pr(NO3)3·5H2O、3,4-pdc和三乙胺以1:1的体积比溶解在水-甲醇混合物中。将溶液搅拌 3 小时,然后过滤并静置直至形成蓝色多晶。然后将所得晶体在 N2 气氛下在不同温度下煅烧 1 小时,得到 Pr2CuO4。
特征化
在 D/Max-RB X 射线衍射仪(日本理学)上使用 Cu Kα 获得所制备样品的 XRD 图 以扫描速率 (2θ ) 为 0.05°/s,从 10 到 90°。使用 SEM(Zeiss Supra 55,德国)和 HRTEM(FEI Tecnai F30,美国)表征粉末形态。获得选区电子衍射 (SAED) 图案和高角度环形暗场 (HAADF) 成像以测量单个纳米粒子。使用激光粒度仪(Mastersizer 2000,英国)检测制备的 Pr2CuO4 的粒度分布。所制备样品的比表面积通过 N2 吸附/解吸实验使用 Builder SSA-4300 进行测量。 DRS 是通过紫外-可见(PERSEE T9,中国)分光光度法以 BaSO4 作为参考样品测量的。通过高分辨率 X 射线光电子能谱 (XPS) 在 PHI 5000 C ESCA 系统(日本)上用 Mg K 获得催化剂元素的氧化态 电源在 14.0 kV 和 25 mA 下运行。
吸附实验
使用 Pr2CuO4 颗粒作为吸附剂,采用 100 rpm 的顶部搅拌器,在批量实验中从水溶液中吸附 MG。将各种吸附剂剂量 (0.03–0.07 g) 添加到 1000 mL 0.1 g/L MG 水溶液中。一旦建立平衡,将溶液过滤并使用紫外-可见光 (RF 5301) 分析滤液以确定 MG 的残留浓度。吸附量使用方程式计算。 (1).
$$ {q}_e=\frac{\left({C}_0-{C}_e\right)\times V}{m} $$ (1)其中 q e (mg/g) 是平衡浓度和 C 下的吸附容量 0 (mg/L) 和 C e (mg/L) 分别是水溶液中 MG 的初始浓度和平衡浓度。 V (L) 是初始溶液体积,m (g) 代表所用干吸附剂的质量。
线性形式的Langmuir方程和Freundlich方程表示为
$$ \frac{1}{q_e}=\frac{1}{K^{\theta}{Q}_m}\times \frac{1}{C_e}+\frac{1}{Q_m} $$ ( 2) $$ \ln {q}_e=\ln {K}_F+\frac{1}{n}\ln {C}_e $$ (3)其中 K θ 是朗缪尔常数,K F 和 n 是 Freundlich 常数。使用上述等温吸附实验的时间响应分析平衡之前吸附过程的动力学特性。为了进行比较,竞争离子(与 O-Pr 和 O-Cu 配位键相关)实验,包括甲基橙 (MO) 和罗丹明 B (RhB),在相同条件下进行。竞争离子的初始浓度设置为 0.02 g/L。
理论研究
DFT 计算使用 DMol 3 Materials Studio 包(7.1 版)。所有核心电子都是使用有效核心电位计算的,以降低计算成本。具有极化函数 (DNP) 的双数值质量基组用于系统中的所有原子。通过在广义梯度近似 (GGA) 中使用 PerdewWang (PW91) 交换相关函数来实现吸附剂表面的几何优化。平面波函数的截止能量和自洽场 (SCF) 容差设置为 340 eV 和 1 × 10 − 6 eV/原子,分别。所有计算均在倒易空间中进行。
结果与讨论
特征
在不同温度下合成的 Pr2CuO4 样品的 XRD 谱如图 1 所示。在 600-700°C 时,出现 Pr2O3 和 CuO 的微晶而没有 Pr2CuO4,这表明温度太低而无法激活 Pr2O3 和 CuO 形成 Pr2CuO4 [21]。在 800°C 时,可以在 23.5° 和 31.5° 的布拉格角处观察到与四方相 Pr2CuO4(PDF #22-0245)相关的一些特征峰;然而,样品中仍然存在大量的 Pr2O3 和 CuO。在 900 °C 时,更多的 Pr2O3 和 CuO 反应形成 Pr2CuO4,并有少量 CuO 残留。衍射峰尖锐而强烈,表明样品的结晶度高。没有观察到其他杂质峰,证实了 Pr2CuO4 的高纯度。随着温度升高到 1000 °C,样品仍保持完美的纯度。当温度超过 1100°C 时,由于样品的分解,会明显出现更多的 CuO 杂质相。因此,吸附实验中研究的所有样品均在900℃下合成。
<图片>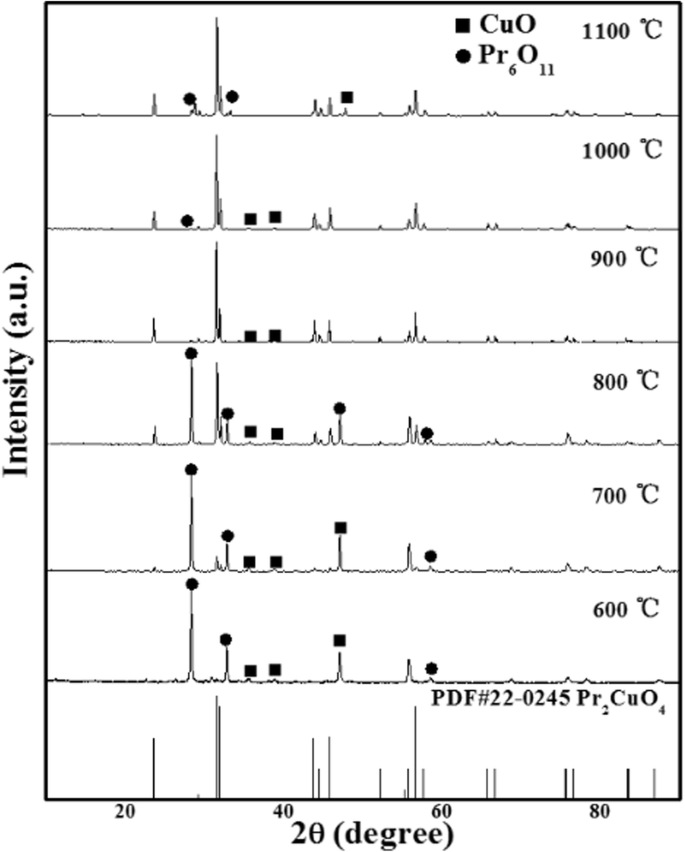
在 600-1100°C 和 PDF#22-0245 合成的 Pr2CuO4 的 XRD 图
图 2a、b 显示了在 900°C 下制备的 Pr2CuO4 颗粒的 SEM 图像。可以看出,Pr2CuO4 颗粒是分散良好的纳米片,平均厚度约为 60 nm。大多数纳米片像熔岩一样堆叠在一起,但仍能清晰地观察到层状结构。很少有结晶良好的纳米片显示规则的八边形片结构(在图 2b 中的黄色圆圈中)。纳米片相互连接以构建一个三维孔,该孔大到足以让有机分子通过,这表明其具有完美的吸附剂性质。如参考文献中所述。 [20],配位前体在 300°C 以上的温度下不断熔化,形成小的流动相,然后固化成氧化物,最终破碎成重叠的薄片(图 2b)。由于金属离子均匀分布在配位前体中,产品由多晶颗粒组成,通过在较低温度(<900 °C,与固态烧结方法相比)下煅烧而成。
<图片>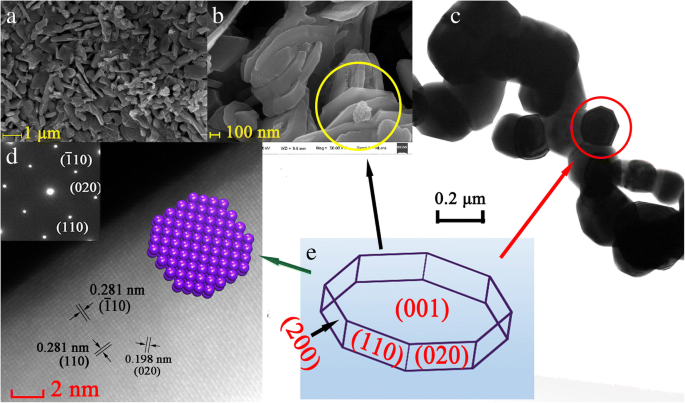
在 900 °C 下制备的 Pr2CuO4 样品的 SEM 图像 (a , b ), 透射电镜 (c )、SAED 和 HAFFD 图像 (d )、八边形结构图(e )
Pr2CuO4 的详细结构通过高分辨率 TEM 图像、SAED 和 HAADF 进一步揭示。图 2c 再次显示了八边形结构(红色圆圈),这与 SEM 图像一致。图 2d 中的 HAADF 图像显示 Pr2CuO4 样品显示出清晰的晶格间距,表明其单晶。 0.281、0.281 和 0.198 nm 的晶格面间距分别与四方 Pr2CuO4 的 (- 110)、(020) 和 (110) 面很好地匹配。图 2b、c 中的八角片状结构示意图如图 2e 所示,多面体边的刻面指数由相应的二面角和 XRD 结果推测。首先,发现八边形薄片侧面的两个晶面指数为(110)和(020)(图 2d)。其次,考虑到八边形相邻边的二面角约等于 45°,观察到的晶面如图 1 所示,推导出 (200) 晶面为一侧。最后,考虑上表面垂直于侧表面,确定上表面的晶面指数为(001)。由于八边形薄片的厚度较小,{006}的X射线衍射强度必定较弱,如图1所示,间接支持了上述假设。因此,据信所制备的样品很可能被{110}、{020}、{200}和{001}包围。考虑到(001)面的暴露面积最大,DFT建模中选择(001)晶面作为吸附面。
图 3 显示了 Pr2CuO4 吸附剂的氮吸附-解吸等温线和相应的孔径分布。可以看出,根据IUPAC分类,等温线显示出III型等温线,该等温线凸向p/p 0 轴在其整个范围内没有明确的点来确定多层吸附的开始 [23, 24]。没有观察到明显的滞后回线,表明 N2-Pr2CuO4 相互作用较弱。此外,其比表面积经计算为 11.6 m 2 /g,根据 Brunauer-Emmet-Teller (BET) 方法,孔径为 10-100 Å,表明颗粒之间的间距非常窄,这与 SEM 结果一致。
<图片>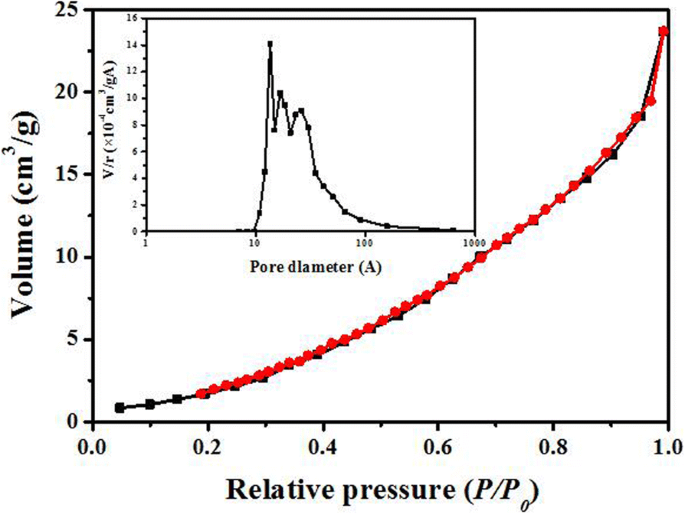
氮吸附-解吸等温线及相应的Pr2CuO4孔径分布(黑线为吸附支线,红线为解吸支线)
通过 XPS 研究了 Pr2CuO4 吸附剂的表面化学成分和元素状态。图 4a 显示了 XPS 调查光谱,表明样品包含 Pr、Cu、O 和 C 元素。考虑到自旋轨道耦合,对 Pr、Cu、O 和 C 的高分辨率 XPS 光谱进行了珍贵的解卷积。 Pr 3d 的高分辨率 XPS 光谱如图 4b 所示。在 1073.1 和 1091.5 eV 处观察到的 3d5/2 和 3d3/2 峰分别证实了具有 + 3 正式电荷的化学等价 Pr 离子的存在 [25,26,27]。如图 4c 所示,Cu 2p XPS 光谱显示了具有一个自旋轨道双峰的 Cu 2p 光谱区域的核心能级。主峰代表 953.8 eV 的 Cu 2p1/2 和 933.6 eV 的 Cu 2p3/2,能量差约为 20 eV,这可能归因于 CuO4 组中的 Cu 离子,其形式电荷为 + 2 [28]。同时,在 929.5 eV 处观察到的一个小峰可归因于 Cu 2p 的卫星峰,这可能是由吸附剂表面具有较低对称配位环境的 Cu 离子引起的。图 4d 分别显示了 531.3 eV 和 535.6 eV(更正)的两种不同价态的 O,表明存在两种不等价的 O 原子。以 531.3 eV 为中心的峰代表在 Pr2CuO4 晶格的 CuO2 层中被两个 Cu 原子和四个 Pr 原子包围的 O 原子,而在 535.6 eV 处的峰被指定为与 Pr2CuO4 的 Pr2O2 层中的四个 Pr 原子配位的 O 原子格[29]。在图 4e 中,不定碳的结合能 (284.7 eV) 用于电荷校正。然而,289.5 eV 的峰值可归因于 C-O 物种,表明存在 C 残留,这可以被视为 CCM 的特征之一。
<图片>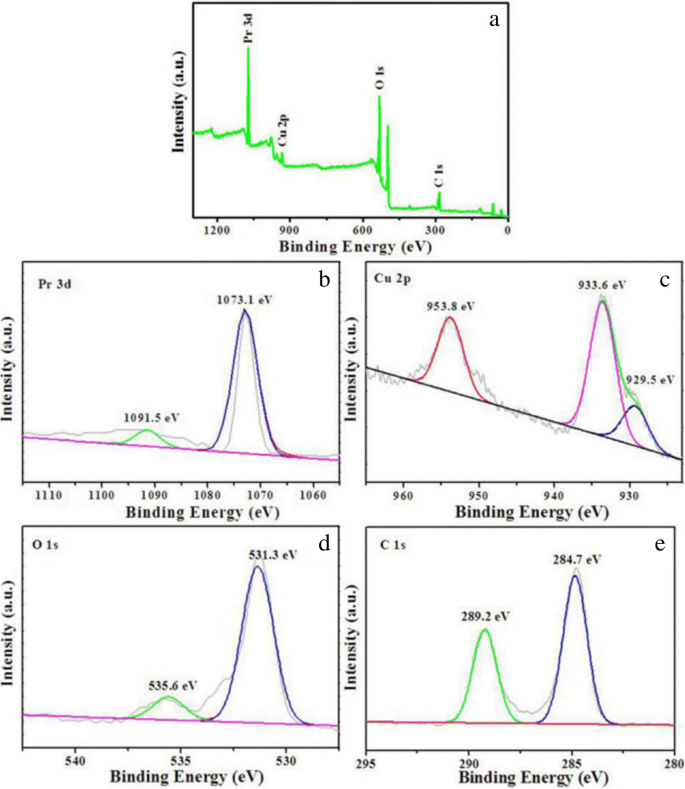
总 XPS 光谱 (a ) 和 Pr 3d (b ), Cu 2p (c ), O 1 s (d ) 和 C 1 s (e ) Pr2CuO4
图 5 显示了 Pr2CuO4 的 UV-Vis 吸收光谱。由于 Cu-O 和 Pr-O 的强 d-d 电子跃迁和电荷转移跃迁,可以清楚地观察到从 750 到 300 nm 的强而宽的光谱吸收带 [30, 31]。因此,样品呈现深蓝色。对光的强吸收使 Pr2CuO4 成为一种潜在的光催化剂,但尚未观察到光催化现象。这间接意味着 Pr2CuO4 的光生电子-空穴对的复合是强烈的。计算出的直接带间能隙为 0.51 eV(图 5 中的插图),表明光生电子可以通过晶格振动轻松松弛。因此,未观察到Pr2CuO4的光催化性能。
<图片>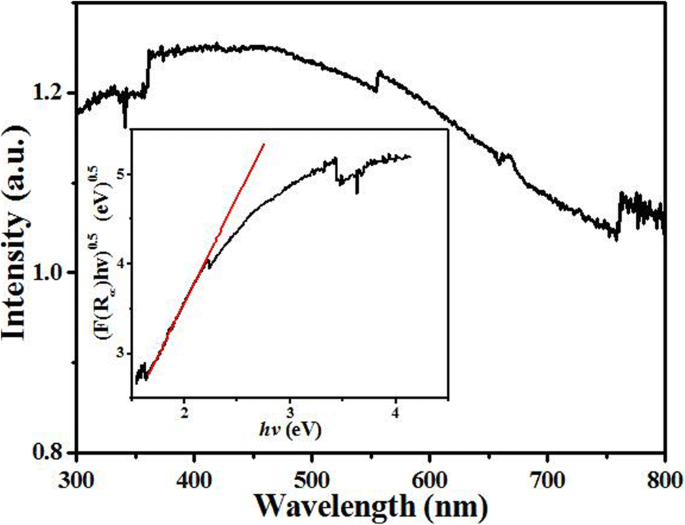
Pr2CuO4样品的UV-Vis漫反射光谱和确定的直接带间跃迁能
最大吸附容量及机理
通过在 298、318 和 338 K 下的平衡吸附实验评估 Pr2CuO4 的吸附能力,如图 6a-c 所示。当吸附反应在 298 K 达到平衡时,MG 的平衡浓度随着吸附剂用量的增加而显着降低(图 6a)。随着温度的升高,在相同剂量吸附剂的情况下,MG的平衡浓度逐渐增加,表明温度升高对MG的解吸有积极影响(图6b,c)。根据 Langmuir 模型(方程 2)和 Freundlich 模型(方程 3)[32],图 6a-c 的数据如图 6d、e 所示。相关参数的值和对应的R 2 列于表 1。结果表明,当 R 值较高时,等温线更符合朗缪尔模型 2 与 Freundlich 模型相比。因此,Q 米 根据朗缪尔模型计算的 Pr2CuO4 吸附剂在 298 K 时的吸附量高达 3.52 g/g。为了比较,表 2 总结了一些选定吸附剂的最大 MG 吸附容量。据我们所知,问 米 Pr2CuO4 对 MG 的吸附仅略低于模拟 Sm2CuO4,但比物理吸附剂如竹基活性炭大得多,表明吸附机制可能与普通物理吸附不同。 Q 米 随着温度升高到 338 K,Pr2CuO4 的含量下降到 2.17 g/g。同时,平衡常数 (K θ ) 从 906 降至 667 L·mol − 1 随着温度从 298 K 升高到 338 K,表明吸附过程是放热的 [33]。
<图片>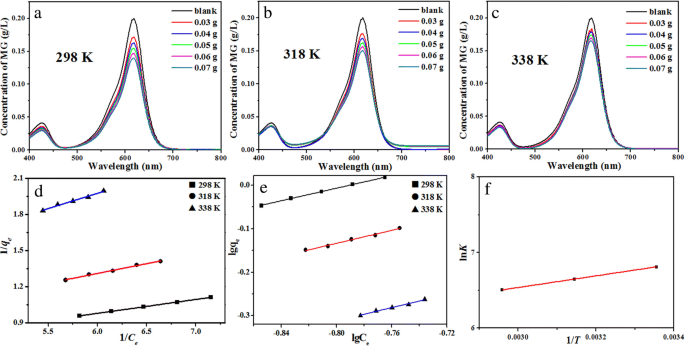
CCMs在298 (a ), 318 (b ) 和 338 K (c ) 和相应的拟合线根据方程。 (2)、(3) 和 (4) 在 (d , e , 和 f ),分别
热力学参数根据等式从表 1 中的数据拟合。 (4) 结果如图 6f [34] 所示:
$$ \ln {K}^{\uptheta}=\frac{-{\Delta}_r{G_m}^{\theta }}{RT}=-\frac{\Delta_r{H_m}^{\theta }} {R}\times \frac{1}{T}+\frac{\Delta_r{S_m}^{\theta }}{R} $$ (4)其中Δ r G 米 θ , Δ r H 米 θ , 和 Δ r S 米 θ 分别为吸附 1 mol MG 的标准吉布斯自由能变化、标准焓变和标准熵变。
Δ r G 米 θ , Δ r H 米 θ , 和 Δ r S 米 θ 分别计算为 - 16.9 kJ/mol、- 6.41 kJ/mol 和 35.1 J/mol·K。 Δ的负值 r G 米 θ 表明吸附反应是自发的。 Δ的负值 r H 米 θ 进一步解释平衡常数随温度升高而降低。 Δ的正值 r S 米 θ 可能意味着吸附剂表面最初被水分子覆盖,吸附的MG分子在表面占据了很大的面积[33]。
偏差分析
1/q 的情节 e 与 1/c e 根据方程。 2 与 q e 由方程修改。 5 与 m' 图 7a 中描绘了 298 K 下从 0 到 0.009 g 的范围。可以清楚地观察到,当 m' =0,表明与 Langmuir 模型的显着偏差 (0.01 g <m <0.03 克和 0.07 克 <米 <0.10 克)。因此,1/q 的图 e 与 1/c e 需要通过引入因子m’进行校准 根据方程。 5. 如图 7b 所示,当 0.001 g <m' <0.003 克,R 2 随着 m’ 稳定增加 , 而 R 2 当 m’ 时迅速减小 超过 0.004 克。因此,m’的最优值 为 0.003 g,表明可能由于某些原因存在系统误差,例如吸附剂颗粒的团聚。吸附剂颗粒的团聚可能是由于吸附剂颗粒在吸附MG分子后粘度增加所致。相应的机制和过程将在下一节中演示。
$$ {q}_e=\frac{\left({C}_0-{C}_e\right)\times V}{m-{m}^{\hbox{'}}} $$ (5) <图片>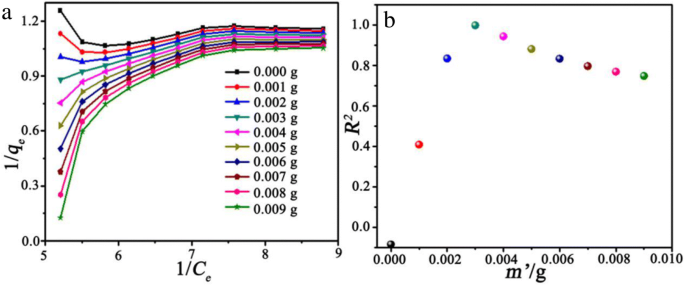
1/q 的情节 e 与 1/c e 根据方程。 2(其中,m’ =0 ) 与 q e 由方程修改。 5 具有不同的 m’ 值 在 298 K (a )。对应的R 2 作为 m' 的函数 (b )
上述修正方法可以很好地解释m情况下的偏差 <0.04 g,但是当 m> 0.07 g,解释偏差变得非常困难。 m 的高阶项的加法 到 m' 是解释 m 偏差的一个选项> 0.07 克;然而,它的物理意义变得模棱两可。另一种方法是采用多层吸附理论。一个明显的实验现象,即容器壁上出现深蓝色斑点,支持了这一理论。这表明吸附剂颗粒聚集的可能性。可能是由于MG吸附过程中H原子的重排[4],如图8所示。氢原子的迁移产生O − 离子和NH3 + 离子,产生偶极MG。由于MG分子的极化极大地增加了分子间相互作用,吸附了MG分子的吸附剂颗粒倾向于聚集在一起并附着在容器壁上。以1:1体积比的水/乙醇混合溶液为溶液,在298 K重复上述等温线实验。水/乙醇混合溶液中的聚集程度明显下降,这可以用去极化来解释MG分子在弱极性溶剂中的反应。
<图片>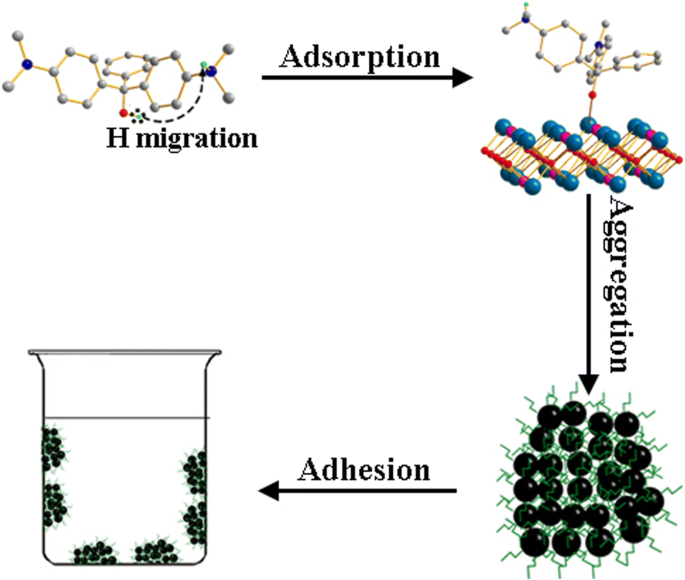
具有巨大Q的Pr2CuO4颗粒团聚过程示意图 米 在水和水/乙醇混合物中
DFT 层面的理论分析
通过DFT方法进一步分析上述假设。正如 Li 等人报道的那样。 [4],MG的异构体(图9)含有配位氧原子,具有与吸附剂的Cu和Pr原子连接的能力。这种模式在图 9 中被描述为路线 1。根据 DFT 水平的 O-Pr 配位键计算,路线 1 的吸附能为 62.5 kJ/mol,比 O 大 6.46 eV/mol –铜。基于此,路线2由两个阶段表示:(i)MG分子的H原子从羟基迁移到氨基,能量上升28.8 kJ/mol,活化能为309.8 kJ/mol,接近于 O-H 的键能。然而,O 的电离通过更强的 O-Pr 配位键增强了吸附强度,更大的吸附能为 83.3 kJ/mol。路线 2 的产物比路线 1 稳定 20.8 kJ/mol。 OMG-Pr 配位键的长度计算为 2.99 Å,略大于 Cu-Pr 配位配合物(即 CCDC 中的 2.36 Å) :1524771),表明 Pr 和 OMG 之间有很强的相互作用。 (ii) 电离的MG分子可以引起相邻MG分子的极化,从而增加MG分子之间的静电相互作用并进一步形成H…N键。因此,获得了能量降为 26.4 kJ/mol 的多层吸附。路线 2 的值与上述热力学结果更一致,说明路线 2 更可靠。形成氢键后(图 10),O-H 的键长被拉伸至 1.07 Å,比游离 MG 分子长 0.10 Å。 H…N 的 H 键长度约为 1.60 Å,这意味着 MG 分子之间的共价相互作用在氢键的形成中起着关键作用。在路线 2 中,大量吸附在 Pr2CuO4 表面的电离 MG 分子具有静电粘性,这可能解释了吸附过程中吸附剂颗粒的团聚(图 8)。因此,多层吸附路线可能是主要模式,这可以解释大Q 米 Pr2CuO4 很好。上述机理与Tang[35]报道的可电离化合物的pH依赖性吸附相似。
<图片>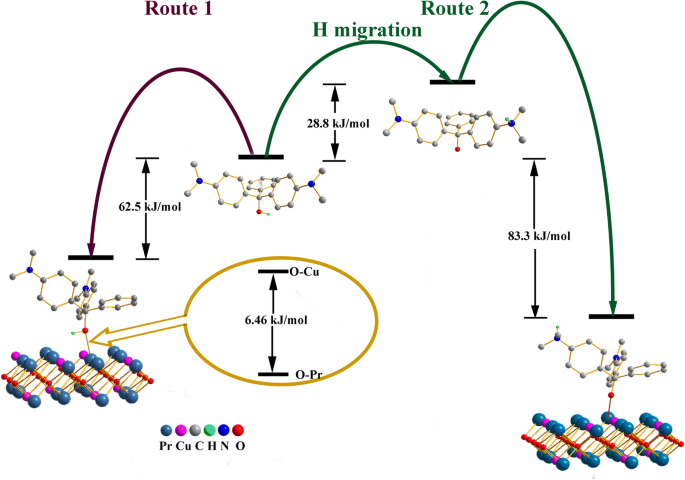
基于DFT研究的路线1和2能量变化示意图
<图片>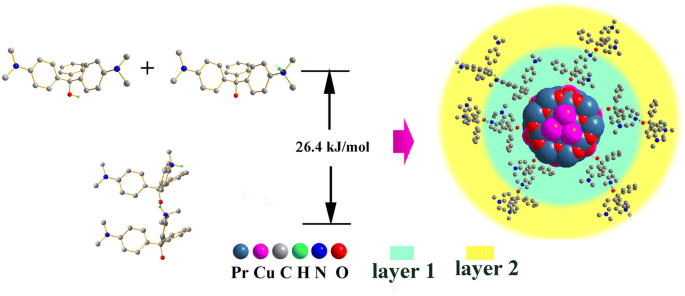
偶极MG分子间氢键多层吸附能量变化示意图
为了更好地了解吸附机制,还进行了不同竞争性离子、染料和氧化物的等温吸附实验,数据如图 11 所示。MO 和 RhB 等染料对吸附过程的影响很小,表明 Pr2CuO4 是一种选择性吸附剂。离子 (Cl − 阴离子和 Na + 阳离子)对吸附过程也显示出很小的影响,表明选择性吸附不同于静电吸附。 OAc的作用 − 强于 Cl − ,部分原因是 O-Cu 和 O-Pr 配位键的形成。类似地,Cu 2+ 和 Pr 3+ 可以通过配位键有效地阻止MG的吸附。同时,CuO 和 Pr2O3 显着提高了吸附容量,表明它们可能具有与 Pr2CuO4 相同的吸附机制。这些实验结果与DFT分析一致,进一步支持了配位吸附的观点。
<图片>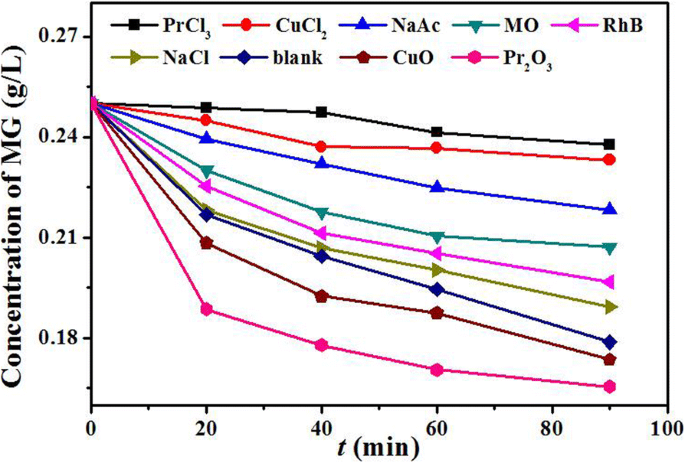
竞争离子、染料、CuO、Pr2O3对MG吸附Pr2CuO4的影响
结论
通过具有大Q的CCMs成功制备了Pr2CuO4吸附剂 米 3.52 g/g at 298 K. 吸附数据与 Langmuir 模型的偏差是由于系统质量损失 0.003 g,当 m <0.04。当 m> 0.07 g,颗粒团聚对吸附容量的影响不容忽视。根据多层吸附模型讨论了 Pr2CuO4 吸附剂的大吸附容量:(i)MG 分子的 H 原子从羟基迁移到氨基以增强吸附强度,吸附能为 83.3 kJ/mol。 (ii) 极化的 MG 分子在多层吸附过程中通过氢键相互结合,能量降为 26.4 kJ/mol。此外,DFT研究和竞争离子实验证实了这种多层吸附机制。
缩写
- 3,4-pdc:
-
3,4-吡啶二羧酸
- CCM:
-
配位复合法
- HAADF:
-
高角度环形暗场
- MG:
-
孔雀石绿
- MOF:
-
金属有机骨架
- Qm :
-
最大吸附量
- RhB:
-
罗丹明B
- SAED:
-
选区电子衍射
纳米材料
- 小型硒纳米晶体和纳米棒的简便合成和光学特性
- 通过溶胶-凝胶工艺制备的纳米结构二氧化硅/金-纤维素-键合氨基-POSS 混合复合材料
- 接触非平衡等离子体对 Mn Х Fe3 − X О4 尖晶石结构和磁性能的影响
- 水溶性α-NaGdF4/β-NaYF4:Yb,Er核壳纳米粒子的合成和发光特性
- 水溶性硫化锑量子点的合成及其光电特性
- 通过蒸发诱导自组装和增强的气敏特性简便合成虫孔状介孔氧化锡
- 石墨烯/Ag3PO4 量子点复合材料的简便一步声化学合成和光催化性能
- 改性 BiOCl 的合成和表征及其在从水溶液中吸附低浓度染料中的应用
- 表面功能化磁性纳米复合材料的简便合成,可有效选择性吸附阳离子染料
- 纳米粒子和超声波控制的水过冷
- 水溶性蓝色发光锰合金碲化碲化镉量子点的合成和性质
- 钒原子在清洁和石墨烯覆盖的 Cu(111) 表面吸附的电子特性


