在金纳米粒子功能化中对 ELISA 和叉指电极表面的补充,以有效检测人类血液凝固缺陷
摘要
使用生物传感器进行增强的诊断对于在疾病并发症出现之前治疗患者很重要。改进生物传感器将使检测各种低丰度疾病生物标志物成为可能。在传感表面上有效固定探针/受体是增强检测的有效方法之一。在此,我们引入了具有胺功能化的预碱性传感表面,用于捕获与人凝血因子 IX (FIX) 结合的金纳米颗粒 (GNP),并证明了该策略的优异性能。我们选择了广泛使用的酶联免疫吸附测定 (ELISA) 和叉指电极 (IDE) 来演示我们的方法。已发现硅烷化的最佳量为 2.5%,并且 15 纳米大小的 GNP 是理想的和表征的。 FIX 检测的极限是在 100 pM 与预混合 GNP 和 FIX 的 ELISA 中达到的,与传统的 ELISA 相比,这显示灵敏度提高了 60 倍而没有生物污染。此外,在 1:1280 稀释度的人血清中检测到 FIX 具有更高的特异性,这相当于 120 pM FIX。这些结果得到了 IDE 分析的补充,其中在 25 pM 下实现了改进的检测,并且在稀释为 1:640 的人血清中检测到 FIX。这些优化的表面有助于提高对不同传感表面上不同疾病的检测。
介绍
医学前沿的各个方面的改进对于维持健康的人类生活和延长寿命是必不可少的。疾病诊断是医学领域的主要领域之一,应进一步改进,以便更容易地识别疾病和治疗。另一方面,流感和登革热等流行病必须在开始阶段被发现,以避免传播[1,2,3]。有不同的诊断方法已被证明能够通过广泛的生物标志物进行真正的检测 [4, 5]。在先前生成的诊断系统中,酶联免疫吸附试验 (ELISA) 被广泛认为是识别主要病毒和细菌疾病及分子种类的“金标准” [6, 7]。 ELISA 开发了不同的策略,具有吸引人的特性,例如易用性、精确度和较低的检测限。此外,同时检测多种疾病并用于筛查主要疾病在实践中很常见[8,9,10]。 ELISA 是一种免疫测定法,用于在聚苯乙烯 (PS) 96 孔板上使用适当的抗体检测感兴趣的目标。目标分子的灵敏度和选择性在 ELISA 中高度依赖于各种因素,例如目标与抗体的结合亲和力、一抗和二抗的相互作用以及目标在 ELISA 表面的有效固定。特别是,将目标固定在 PS 板上对限制检测起着至关重要的作用。通过疏水基团与抗体的相互作用,抗体或蛋白质可以物理吸附到 PS 表面 [11]。有一些可能性,例如涉及抗体(或蛋白质)的弱结合或抗体在PS板上的不稳定性以及抗体(或蛋白质)的不均匀分布导致检测缺陷。已经证明,与随机固定的分子相比,固定化板上抗体的正确定向可将检测提高 64 倍以上 [12, 13]。因此,找到将蛋白质或抗体有效固定在 PS 板上且均匀的合适程序是至关重要的。不同的研究人员正在利用化学或物理过程将蛋白质固定在 PS ELISA 板上,例如由聚乙烯苄基内酯酰胺辅助的光化学反应和在洗涤剂存在下固定蛋白质 [14,15,16]。迪克西特等人。 [8] 将抗体固定在胺修饰的 PS 板上以提高检测限,他们证明在固定步骤之前(3-氨基丙基)三乙氧基硅烷 (APTES) 和抗体的预混物将灵敏度提高了 54 倍。与常规ELISA相比,检测限达到10 pM [8, 17]。
在目前的工作中,我们介绍了一种在金纳米粒子 (GNP) 辅助下将蛋白质固定在 PS ELISA 板上的新方法。 GNP 是传感器开发领域最强大的工具之一。它们具有积极的特性,例如易于在水中分散、生物惰性以及与表面功能化的良好相容性,并且它们可以定制为均匀的纳米尺寸 [18,19,20,21,22,23]。已经证明,GNP 偶联抗体提高了波导模式传感器上流感病毒和 FIX 的检测限 [21,22,23]。 GNP 用于各种传感器,包括波导模式传感器、表面等离子体共振和用于高性能检测的拉曼光谱。此外,GNPs 也被用于比色分析,其中适体或抗体在 GNP 表面的结合被跟踪以通过肉眼检测分析物。研究人员还关注在 ELISA 方法中使用 GNP 来增强检测 [24]。以前,GNP 偶联的抗小鼠 IgG-HRP 改进了 Pb(II) 的检测并达到了 9 pg/mL 的检测限 [25]。拉克什米普里亚等人。已经发现 GNP 上的一级和二级抗体的结合提高了 ESAT-6 蛋白的检测,该蛋白与引起结核病有关 [9, 26]。在这里,我们使用 GNP 通过 APTES 辅助的化学修饰将蛋白质固定在 PS ELISA 表面上。这种方法包括两个步骤:使用 APTES 用胺基团对 PS 表面进行功能化,然后将 GNP 结合蛋白固定在胺修饰的 PS 板上。 APTES 的胺基团可以与 PS ELISA 表面上的 COOH 基团结合。另一方面,用阴离子柠檬酸离子稳定的 GNP 偶联蛋白质可以通过静电相互作用与阳离子 APTES 结合 [11, 27, 28]。 APTES 中的氨基末端基团取代了 GNP 上的柠檬酸盐基团,并以化学方式固定在 PS 板上 [29]。 APTES 中带正电的胺基团也吸引带负电的 GNP。此外,APTES处理改变了PS底物,使其更具疏水性[30]。
化学修饰的 ELISA 板和 GNP 偶联物用于检测来自人类凝血级联反应的因子 IX (FIX)。 FIX 是凝血系统中的一种重要蛋白质,血液中较低浓度的 FIX 会导致凝血缺陷。通过 GNP 在 ELISA 板上增强的 FIX 固定为检测较低水平的 FIX 提供了潜在途径。 GNP 修饰的 ELISA 板在 FIX 检测中显示出显着改善。此外,我们还展示了人血清中 FIX 的检测,目前的策略可与 ELISA 结合使用以检测其他生物标志物。为了用 ELISA 底物补充上述研究,我们还在电化学介电传感器中另一个广泛使用的叉指电极表面 (IDE) 上应用了上述策略,以检测人稀释血清样品中的纯 FIX 和 FIX(图 1a、b) .
<图片>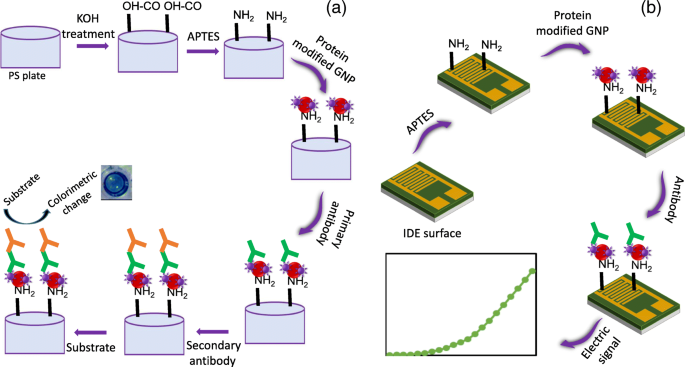
一 GNP 辅助 ELISA 的示意图。 GNP 与蛋白质预混合并固定在 APTES 修饰的 ELISA 表面。然后加入抗体。最后,使用 HRP 的底物来检测目标。 b GNP辅助IDE示意图
材料和方法
试剂和生物分子
(3-氨基丙基)三乙氧基硅烷 (APTES) 和人血清购自 Sigma-Aldrich(美国)。 FIX 蛋白和抗 FIX 抗体来自 Abcam(马来西亚)。抗小鼠 IgG 偶联辣根过氧化物酶(抗小鼠免疫球蛋白 HRP)购自 Thermo-Scientific(美国)。 ELISA 板购自 Becton Dickinson (France)。 ELISA 5x 包被缓冲液购自 BioLegend (UK)。牛血清白蛋白 (BSA) 和 HRP 底物购自 Promega (USA)。金纳米粒子 (GNP)(10、15 和 80 纳米)来自 Nanocs(美国)。分析ELISA阅读器来自Fisher Scientific(马来西亚)。
使用硅烷试剂和 GNP 进行优化
为了优化 APTES 和 GNP 的合适浓度,我们在 ELISA 板上用不同的 APTES 和 GNP 组合进行了固定过程。最初,ELISA板用1% KOH羟基化1 小时。然后,在室温 (RT) 下将 1.25、2.5 和 5% APTES 连接到 ELISA 板的单独孔上 5 小时。之后,将稀释的 GNP(在蒸馏水中)以 25%、50% 和 100% 的浓度固定在 APTES 修饰的表面上。然后允许 FIX 在 200 nM 下结合到 GNP 表面。然后使用 2% BSA 封闭剩余的结合位点,然后引入 1:1000 稀释的 FIX 抗体,然后添加 1:1000 稀释的抗小鼠-IgG-HRP。最后,添加底物以检测 FIX 相互作用。在每个步骤之间使用洗涤缓冲液(含有 0.05% Tween 20 的 PBS 缓冲液,pH 7.4)将孔洗涤 5 次。最后,通过ELISA读数器在405 nm处测量光密度(OD)。本实验使用15 nm大小的GNP。
确定 GNP 的必要规模
在最佳条件下确定合适的APTES浓度和GNP稀释度后,尝试10、15和80 nm GNPs进行FIX固定,以确定最合适的尺寸。使用与上述相同的实验条件。 FIX 固定使用 2.5% 的 APTES 和 50% 的 GNP 稀释液。
FIX的特异性和选择性检测
我们还证实了蛋白质和抗体在 ELISA 板上的特异性结合。为此,我们使用了三种不同的对照实验。我们将以下生物分子顺序固定在ELISA板上作为对照和特定条件:对照1(C1),FIX-BSA-抗小鼠IgG-底物;对照 2 (C2),FIX-BSA-FIX 抗体-底物;对照 3 (C3),BSA-FIX 抗体-抗小鼠 IgG-底物,特异性 (S),FIX-BSA-FIX 抗体-抗-小鼠 IgG-底物。
ELISA 板上 GNP 偶联 FIX 的检测与传统 ELISA 的比较
使用 GNP 修饰的 ELISA 板通过两种不同的方法检测 FIX,例如 APTES-GNP-FIX 和 APTES-GNP 预混 FIX,并将这些方法与常规 ELISA 进行比较。以下步骤构成了程序。常规 ELISA:(i) FIX 蛋白在 1x 包被缓冲液中稀释,浓度为 0 到 200 nM,(ii) 用 2% BSA 封闭,(iii) 加入 1:1000 稀释的 FIX 抗体,(iv) 1:加入1000稀释的抗小鼠IgG-HRP,(v)加入HRP的底物并在405 nm处测量。
APTES-GNP-FIX(方法 1):(i)PS 板被 1% KOH 激活,(ii)2.5% APTES 在 RT 下添加到 ELISA 板上 5 h,(iii)25% 的接收到的 15 nm添加 GNP 并在 4 °C 下保持过夜,(iv) 允许浓度为 0 到 200 nM 的 FIX 独立结合到 GNP 表面,(v) 剩余表面被 2% BSA 封闭,(vi) 1:加入 1000 稀释的 FIX 抗体,(vii) 加入 1:1000 稀释的抗小鼠-IgG-HRP,(vii) 加入 HRP 底物并在 405 nm 处测量。
APTES-GNP 预混 FIX(方法 2):(i)PS 板用 1% KOH 活化,(ii)在室温下加入 2.5% APTES 5 h,(iii)不同浓度的 25% 15 nm GNP 溶液的预混的 FIX(在室温下孵育 30 分钟;0 到 200 nM)被固定在 APTES 修饰的表面上,(iv)剩余的表面被 2% BSA 封闭,(v)加入 1:1000 稀释的 FIX 抗体, (vi) 加入 1:1000 稀释的抗小鼠-IgG-HRP,(vii) 加入 HRP 的底物并在 405 nm 处测量。
检测人血清中和加标 FIX 后的 FIX
为了检测人血清中的 FIX,我们在此处将血清与 GNP 而不是 FIX 预混合。滴定从 20 到 1280 的血清稀释度并与 GNP 混合以评估 FIX 的检测。使用其他实验条件和浓度,与之前的实验类似。
通过将不同浓度的 FIX(0 至 8 nM)加入优化的人血清稀释液中并在固定在 ELISA 板上之前与 GNP 预混合来进行加标实验。其他实验条件和浓度同前面的实验。
叉指电极表面制造
交叉指状电极 (IDE) 表面制造工艺包括晶片清洁、氧化层生长、负光刻胶旋涂、光刻胶图案化、铝金属沉积、光刻胶去除和晶片切割。该工艺开始于缓冲氧化物蚀刻剂清洁的晶片,然后在高温 (1000 °C) 下对硅晶片 (310 nm) 进行氧化,然后使用铝进行蚀刻工艺。负光刻胶通过旋涂机以2000 rpm的旋转速度沉积。在暴露于紫外线(240 s)后,通过 RD-6 使抗蚀剂显影。然后,通过热蒸发器(Edwards Auto 306)在 3.0E-5 Torr 下沉积 240 nm 铝。使用丙酮剥离光刻胶直到出现固体 IDE,然后切成小块以创建单个 IDE。最后,氧化锌层覆盖在顶部以实现最终的生物分子固定 [31]。在进行氧化锌附着之前,首先用1 M氢氧化钾(pH 9.0)清洗传感表面。
在 GNP 修改表面上检测 FIX
在用 GNP 修饰的 ELISA 底物对 FIX 的检测效率进行优化和确认后,在 IDE 表面进行相同的表面修饰以补充上述检测。最初,IDE 氧化锌表面通过添加 2.5% APTES 在乙醇中稀释 3 小时在室温下用胺改性。之后,将表面用乙醇洗涤 5 次,并加入 GNPs (25%) 和 FIX 的预混物。然后,剩余的表面用乙醇胺封闭,然后加入 FIX 抗体以检测 FIX。注意到电流信号的伴随变化。为了检查检测限,将不同浓度的 FIX 与 GNP 独立混合,固定在胺修饰的 IDE 表面,然后由抗体检测;检测限由3σ计算确定。与 GNP 混合的稀释人血清中 FIX 的丰度被固定在胺修饰的 IDE 表面,然后由其抗体检测。上述表面的制造按照[31]之前所述。
结果与讨论
PS ELISA 表面预处理
蛋白质或抗体在聚苯乙烯 (PS) ELISA 表面上的有效固定显然提高了目标-探针相互作用的检测限。 ELISA 板上的蛋白质或抗体附着使用了不同的固定方法。在这项工作中,我们引入了带有 GNP 的化学修饰 ELISA 表面,用于固定蛋白质或抗体。我们希望使用一种重要的凝血因子,例如因子 IX (FIX),它已被广泛报道为重要 [32,33,34,35,36]。图 1 显示了蛋白质固定在聚苯乙烯 ELISA 表面上的示意图。首先,ELISA 表面被 1% KOH 激活。在没有 KOH 预处理的情况下,要结合在 PS 表面上的 APTES 分子的数量是最少的。这是因为缺乏极性和氢键接受基团,这有助于 APTES 在聚合物上的初始吸附 [11]。 KOH处理后,通过适当浓度的APTES用胺修饰表面以捕获GNPs。
GNP 的特征
在进一步进行之前,我们通过光学、形态学和尺寸分布测量来表征原样的 GNP(15 nm)。图 2a 显示了 GNP 的紫外-可见分光光度计分析,显然在 550 nm 处显示了峰值最大值。透射电子显微镜观察显示 GNP 的大小为 ~ 15 nm,形状良好(图 2b 和插图)。从波数500到4000 cm -1 进行傅里叶变换红外光谱分析 (图2c)。在 1650 cm −1 处有一个明显的单峰 注意到金以及另一个小峰,而存在代表 APTES 附着的胺基峰。体积分布和 zeta 电位分析提供了进一步的支持。基于此分析,体积分布表明尺寸分布略有变化(图 2d)并且 zeta 电位为 - 6.9,代表本研究中使用的 GNP 的稳定性(图 2e)。
<图片>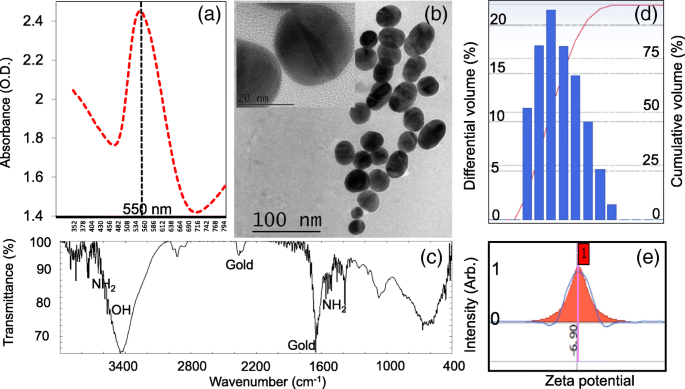
金纳米粒子的表征。以最佳尺寸 15 nm 进行。 一 紫外-可见分光光度法分析。在 550 nm 处发现了一个突出的单峰。 b 透射电镜观察。图插图显示了放大的图像。显示比例尺。 c 傅里叶变换红外光谱分析。标出了金和 NH2 的表观峰位置。 d GNP 的体积分布分析。显示了获得的分布。 e Zeta电位分析。发现该值为- 6.9
胺表面捕获 GNP 的制备和优化
APTES 的量极大地影响了 GNP 或抗体在 PS 表面上的固定化。一般来说,高度拥挤的 APTES 分子有可能产生假阳性结果。由于已使用 1% 至 2% 的 APTES 将抗体固定在多个传感器表面,因此我们在这里滴定了 1.25% 至 5% 的 APTES,在无水乙醇中制备。接下来,我们的目标是将 GNP 固定在 APTES 修饰的表面上。较高数量的 GNP 有可能产生拥挤效应,因此在 APTES 修饰的表面上测试了 25%、50% 或 100% 的 15 nm 的 GNP,以优化合适的稀释度。在这些修饰的表面上,用 FIX 抗体检测到 250 nM 的 FIX。如图 2a 和 b 所示,1.25% APTES 在 GNP 的所有稀释度(25、50 和 100%)下显示出较低的吸光度(OD),而 2.5% 和 5% APTES 在 50% 和 100% 的 GNP 下显示出更高的吸光度国民生产总值。同时,信噪比随着 APTES 和 GNP 浓度的增加而提高(图 3a、b)。具有 50% 和 100% GNP 的 5% APTES 显示出非特异性结合,而具有 2.5% APTES 的 50% 和 100% GNP 显示出相似的吸光度。基于这些获得的值,我们选择了2.5%的APTES和25%的GNP稀释液进行进一步的实验。
<图片>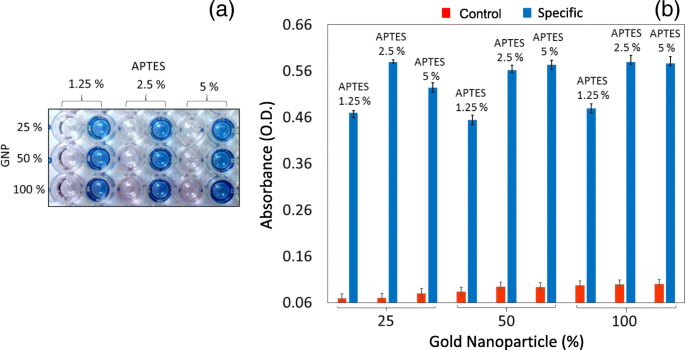
确定 APTES 和 GNP 的数量。三种不同浓度(1.25、2.5 和 5%)的 APTES 与 GNP 的三种稀释液(25、50 和 100%)一起使用。 一 添加底物后 FIX 的视觉检测。包括没有 FIX 的对照泳道。 b 最佳 APTES 水平的图形表示。发现 2.5% APTES 和 25% GNP 是最佳的
潜在 GNP 规模的确定
在 APTES 和 GNP 稀释优化之后,我们接下来评估了 GNP 的合适大小。由于表面积在蛋白质固定中起着至关重要的作用,在这里,我们尝试固定三种不同大小的 GNP,包括 10、15 和 80 nm。不同大小的 GNPs 具有不同的表面积和不同的电荷来吸引蛋白质,在 APTES 修饰的表面上的结合能力也不同。如图 4a 所示,使用 10、15 和 80 nm GNP 修饰的 ELISA 表面检测到 250 nM FIX。发现对于检测 250 nM 的 FIX,15 和 80 nm GNP 显示几乎相同的 0.4 (OD) 吸光度,但 10-nm 大小的 GNP 仅显示 0.34 OD。从这个实验中,我们确认了 15 或 80 nm GNPs 适合进一步的实验,我们继续使用 15 nm GNPs。
<图片>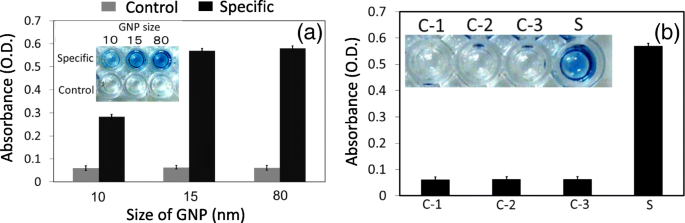
一 确定理想的 GNP 规模。在10、15和80 nm中,15和80 nm表现出相似的结果。 15 纳米用于确定 FIX 的检测限。 b 检测 FIX 的对照实验。进行了三个不同的对照实验(C1——没有 FIX 抗体;C2——没有抗小鼠 IgG;C3——没有 FIX)。在任何对照实验中均未发现显着信号。图插图显示视觉效果
确认无污染和高性能的实验策略
在检测 GNP 修饰的 ELISA 表面上的 FIX 之前,我们进行了三种不同类型的对照实验,如“材料和方法”部分所述。如图 4b 所示,我们无法在对照实验 1、2 和 3(C1、C2 和 C3)的孔中观察到显着的吸光度。在特定实验 (S) 中,较高的吸光度水平与明显的颜色变化明显相关。在 C1 的情况下,我们没有添加 FIX 抗体,这证实了 FIX 抗体与 FIX 特异性相互作用(在 S 中)。在 C2 中没有抗小鼠 IgG 的情况下没有发现可观察到的信号,这为 FIX 和抗体的正确相互作用提供了进一步的锚定,然后是抗小鼠 IgG。在 C3 中,在没有 FIX 的情况下,我们无法测量显着的吸光度。从这些结果可以证实 FIX 与其抗体在 ELISA 表面的正确相互作用,没有非特异性结合。
GNP 辅助 ELISA 与传统 ELISA:灵敏度的确定
进行对照实验后,我们用 GNP 修饰的表面检测 FIX,并将结果与常规 ELISA 方法进行比较。我们进行了三个不同的实验来检测 FIX。首先,将 GNP 固定在 APTES 修饰的表面上,然后通过静电相互作用将 FIX 连接到 GNP 表面。由于静电相互作用,大多数蛋白质有可能结合到 GNP 表面;这样,我们就可以将 FIX 固定在 ELISA PS 表面上。蛋白质固定还取决于氨基酸和 GNP 产生的电荷。戈皮纳特等人。 [37] 已经证明了 FIX 在 GNP 表面上的强结合,并且他们还发现它在高盐条件下是稳定的。在第二种方法中,GNP 和蛋白质在固定在胺化 ELISA PS 表面之前首先预混合。预计更多的蛋白质可以以这种方式结合,因为蛋白质分子更有可能在溶液状态下结合到 GNP 表面。然后将预混溶液固定在 APTES 改性的胺表面上。这些方法与传统的ELISA方法进行了比较。如图 5a 所示,当我们将 FIX 浓度从 0 滴定到 200 nM 时,常规 ELISA(方法 1)显示检测限为 6 nM。 APTES-GNP-FIX 方法(方法 2)显示的检测限为 200 pM,与传统 ELISA 相比,灵敏度提高了 30 多倍。通过正确定向固定在 ELISA PS 板上的大量抗原,可以提高灵敏度,最终更多的抗体将相互作用。在这项研究中,金纳米粒子被用于通过 ELISA 板的胺修饰来固定更多的抗原。在传统的 ELISA 中,抗原直接固定在 ELISA 板上,这导致结合在表面上的分子数量减少,并导致与当前金纳米颗粒介导的策略相比灵敏度降低。此外,正如对 GNP 的研究所揭示的那样,局部表面等离子体共振进一步提高了灵敏度。当我们将 GNP 与 FIX 预混合时,正如预期的那样,检测限得到了极大的提高,达到了 100 pM 的水平,这是比传统 ELISA 灵敏度高 60 倍的水平。如图 5a 所示,可以清楚地看到,当我们使用 GNP 进行蛋白质固定时,GNP 表面上预混和直接固定的蛋白质的最大吸光度达到 ~ 0.6,但使用常规 ELISA 发现的吸光度为 ~ 0.4。 FIX 的相似浓度 (200 nM)。即使在其他浓度下,方法 3 的吸光度差异也比常规 ELISA 更高,这也合理地高于方法 2。 在常规 ELISA 的情况下,在 25 nM 和 3 nM 处发现可见检测在方法 2 中。使用方法 3,由于吸光度较高,我们可以明显地看到从 200 pM FIX 开始的颜色变化(图 5a)。在方法 3 中,吸光度在 25 nM 处饱和。由于我们可以看到从 200 pM FIX 开始的颜色变化,我们评估了检测限并使用较低浓度的 FIX 进行滴定。很明显,当我们预先混合 GNP 和 FIX 时,检测限达到了 100 pM(图 5b)。
<图片>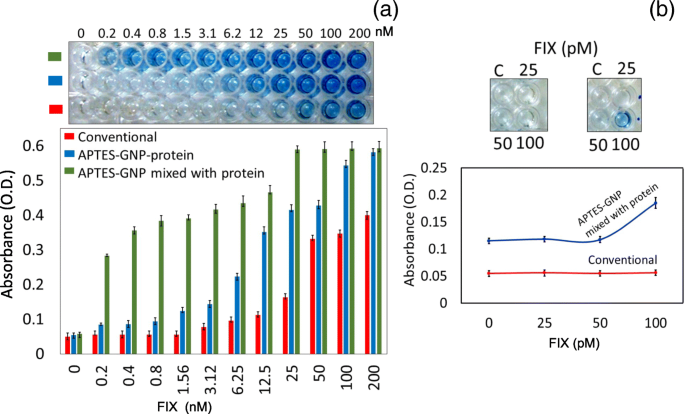
一 比较 FIX 在 GNP 修饰的 ELISA 与常规 ELISA 中的灵敏度。 FIX 从 0.2 滴定到 200 nM。传统 ELISA 的检测限为 6 nM。在 GNP 修饰的 ELISA 中,观察到信号直到 200 pM。图插图显示了视觉结果。 b FIX 在 GNP 修饰的 ELISA 板上的检测限。 FIX 从 25 到 100 pM 滴定。发现检测限为100 pM。图插图显示视觉效果
检测人血清中的 FIX 并通过 Spiking FIX 进行增强
由于发现 FIX 在凝血级联反应中发挥重要作用 [38, 39],在检查检测限后,我们还在人血清中检测到 FIX。对于此分析,我们在 1:1280 和 1:20 稀释度范围内滴定了人血清。稀释的血清与 GNP 预混合并固定在 APTES 修饰的 ELISA 表面上,如上所述。很明显,从 1:640 稀释的血清中检测到 FIX,相当于 125 pM FIX(图 6a)。健康人血清通常含有大约 87 nM FIX,以及其他主要蛋白质,如白蛋白和球蛋白。通过我们的策略,我们在人血清中达到了 125 pM 的特定检测限,这对于识别凝血缺陷非常有用。另一方面,当我们将 FIX 从 1 到 8 nM 添加到 1:640 稀释的人血清中时,它显示出吸光度的增加,并且随着 FIX 浓度的增加而增加(图 6b)。
<图片>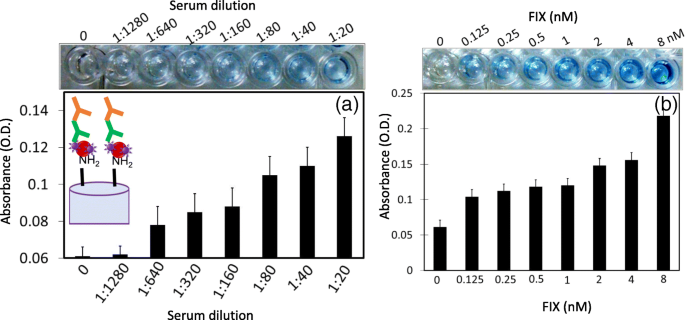
一 检测人血清中的 FIX。人血清从 1:20 稀释到 1:1280。在 1:640 稀释的人血清中检测到 FIX(内图为示意图)。 b 将 FIX(0.125 至 8 nM)加入 1:640 稀释的人血清中。随着 FIX 浓度的增加,吸光度增加。图插图显示视觉效果
IDE Surface 检测 GNP-FIX:互补分析
由于发现 GNP 共轭 FIX 提高了检测限,我们应用了类似的策略,使用具有 IDE 表面的电化学传感器来补充这些发现。我们将 FIX 滴定为 25 到 200 pM(与 GNP 混合),将其固定在胺修饰的 IDE 表面,然后通过 FIX 抗体进行检测。如图 7a 所示,随着 FIX 浓度的增加,电流水平也从基线同时增加。 FIX 水平从 200 pM 开始饱和,检测限为 25 pM。与 ELISA (100 pM) 相比,这种检测增强了四倍。此外,在稀释的人血清中证实了 FIX 检测(图 7b)。在本实验中,人血清从 1:80 稀释到 1:1280。如图所示,1:1280的稀释度(红色曲线)与基线(黑色曲线)3σ估计有明显差异,说明1:1280稀释度的人血清中FIX检测明显匹配ELISA 结果(检测时间为 1:640)。稀释度较低的IDE检测显示灵敏度增加。
<图片>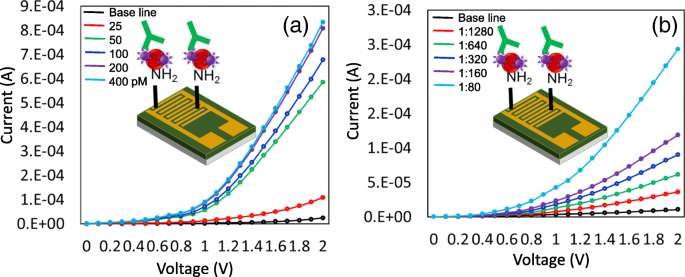
一 Limit of detection of FIX-conjugated GNP on IDE sensing surface. FIX was titrated from 25 to 400 pM. The limit of detection was found to be 25 pM. b Detection of FIX in human serum on the IDE sensing surface. Human serum was diluted from 1:80 to 1:1280. FIX was detected in human serum diluted 1:1280
结论
Efficient immobilization of protein or antibody on the PS ELISA surface is a crucial step to improve the limit of detection. Here, we introduced a new and easy protein immobilization strategy on the PS ELISA surface assisted by GNPs. Two different methods were used:one is the direct immobilization of FIX on the GNP-modified surface, and another one is premixing of FIX with GNPs before attachment. It was found with the former method that improvement of the limit detection is 30-fold higher compared with the conventional ELISA. The latter method showed a 60-fold improved limit of detection compared to the conventional ELISA. We also demonstrated the detection of FIX in 1:650 diluted human serum, which is equivalent to 125 pM. Obviously, these strategies proved that the higher binding of proteins on the ELISA surface was able to improve the sensitivity and to be useful for detecting a wide range of biomarkers on the ELISA surface.
数据和材料的可用性
All of the data are fully available without restriction.
缩写
- APTES:
-
(3-氨基丙基)三乙氧基硅烷
- BSA:
-
牛血清白蛋白
- COOH:
-
Carboxyl
- ELISA:
-
酶联免疫吸附试验
- Fc:
-
Fragment crystallizable
- GNP:
-
Gold nanoparticle
- HRP:
-
辣根过氧化物酶
- IDE:
-
Interdigitated electrode
- IgG:
-
Immunoglobulin
- OD:
-
光密度
- PEG:
-
Polyethylene glycol
- 附注:
-
聚苯乙烯
- PVLA:
-
Polyvinyl benzyl lactonoylamide
- TMB:
-
3,3′,5,5′-Tetramethylbenzidine
纳米材料
- 用于灵敏快速检测卵巢癌细胞的柔性石墨烯生物传感器的演示
- 用于改进诊断和治疗应用的多功能金纳米粒子:综述
- 基于局部表面等离子体共振的金纳米生物传感器能够诊断人类布鲁氏菌病,介绍一种快速且经济的方法
- 加载白藜芦醇的白蛋白纳米颗粒具有延长血液循环和改善生物相容性的高效靶向胰腺肿瘤治疗
- 通过激光脉冲和溅射技术合成导电二氧化硅纳米纤维/金纳米粒子复合材料
- 通过镀金和等离子处理调整聚醚醚酮的表面化学
- 改性超支化聚甘油作为分散剂,用于控制和稳定碳氢化合物中的金纳米粒子
- 用于最大太阳能收集的高效且有效的 InP 纳米线设计
- 用于新型隐球菌诊断和光热治疗的抗体偶联二氧化硅修饰金纳米棒:体外实验
- 金纳米团簇的生物医学应用:最新发展和未来展望
- 电子表面散射对金纳米壳光吸收和散射消光比的影响
- 使用基于智能手机的阅读器灵敏检测疾病生物标志物的等离子体 ELISA


