Co/CoP 纳米颗粒封装在 N、P 掺杂碳纳米管中,用于纳米多孔金属-有机骨架纳米片上,用于氧还原和氧析出反应
摘要
在此,通过煅烧和随后的磷化获得源自原子层沉积的六方金属有机骨架 (MOF) 的 N、P 掺杂碳纳米管包裹的 Co/CoP 纳米粒子,并用作电催化剂。电催化性能评估表明,所制备的电催化剂在10 mA cm −2 的电流密度下表现出342 mV的过电位。 和 74 mV dec −1 的 Tafel 斜率 用于析氧反应(OER),优于最先进的氧化钌电催化剂。电催化剂还表现出比基准 RuO2 更好的稳定性。 9 h后,电流密度仅下降10%,远小于RuO2的损失。此外,其氧还原反应 (ORR) 的起始电位为 0.93 V,并且遵循理想的 4 电子方法。稳定性测试后,电催化剂的电流密度保持初始值的94%,优于Pt/C。上述结果表明该电催化剂对 OER 和 ORR 均具有双功能活性和优异的稳定性。相信该策略可为磷化钴/碳基电催化剂的合成提供指导。
介绍
现代社会的发展在很大程度上依赖于能源供应,但随着化石燃料燃烧引发的环境问题和能源短缺的加剧,需要寻找新的转换系统或可再生能源[1,2,3, 4]。燃料电池和金属空气电池被认为是很有前景的能源系统;然而,它们较差的能量转换效率和较短的寿命是限制其广泛使用的主要瓶颈[5,6,7,8,9]。这些缺陷主要是由于析氧反应 (OER) 和氧还原反应 (ORR) [10,11,12,13] 固有的缓慢动力学。特别是,OER 在金属-空气电池和水分解中起着非常重要的作用。然而,它的缓慢动力学通常导致低反应速率和高电极过电位,阻碍了此类能源系统的发展。目前,对碱性条件下OER过程的解释最多的理论如下:
$$ \mathrm{M}+\mathrm{OH}\to \mathrm{M}-\mathrm{OH}+{\mathrm{e}}^{-} $$ (1) $$ \mathrm{M} -\mathrm{OH}+{\mathrm{O}\mathrm{H}}^{-}\to \mathrm{M}-{\mathrm{O}}^{-}+{\mathrm{H}} _2\mathrm{O} $$ (2) $$ \mathrm{M}-{\mathrm{O}}^{-}\to \mathrm{M}-\mathrm{O}+{\mathrm{e} }^{-} $$ (3) $$ 2\mathrm{M}-\mathrm{O}\to 2\mathrm{M}+{\mathrm{O}}_2 $$ (4)ORR作为燃料电池的阴极反应是制约电池效率的关键因素。反应过程中会产生多种中间氧物种,反应过程相对复杂。在碱性条件下,有两种反应方式:
2e − 路径:
$$ {\mathrm{O}}_2+{\mathrm{H}}_2\mathrm{O}+2{\mathrm{e}}^{-}\to \mathrm{H}{\mathrm{O}} _2+\mathrm{O}{\mathrm{H}}_2^{-} $$ (5) $$ \mathrm{H}{\mathrm{O}}_2^{-}+\mathrm{O}{\ mathrm{H}}^{-}+2{\mathrm{e}}^{-}\to 3\mathrm{O}{\mathrm{H}}^{-}\ \mathrm{or}\ \mathrm {H}{\mathrm{O}}_2^{-}+\mathrm{O}{\mathrm{H}}^{-}+2{\mathrm{e}}^{-}\to 3\mathrm {O}{\mathrm{H}}^{-} $$ (6)4e − 路径:
$$ {\mathrm{O}}_2+2{\mathrm{H}}_2\mathrm{O}+4{\mathrm{e}}^{-}\to 4\mathrm{O}{\mathrm{ H}}^{-} $$ (7)因此,有必要探索廉价、高效、耐用的电催化剂,以促进这些可再生资源的实际应用[14, 15]。目前,贵金属被认为是活性最高的电催化剂,如 Pt、Ru、Ir 及其合金,但成本高、稀缺、缺乏双功能催化等严重阻碍了其商业化[16,17,18,19, 20]。因此,商业化的需求迫切需要追求双功能、稳定且廉价的电催化剂。过渡金属磷化物 (TMP) 是有前景的替代候选者,其中 Co 2+ 在 CoxPy 中提供 OH − 吸附中心并将其转化为产物,而负 P 中心加速 OH − 对 Co 2+ 的吸附 ,从而导致成本低、性能优异、效率高和耐用性好 [21,22,23,24]。许多研究人员付出了巨大努力来设计具有多样化和高电催化活性的 CoPx 纳米结构。由于活性在很大程度上取决于它们的表面性质,因此许多研究集中在电催化剂的结构工程上,以尽可能多地暴露催化活性位点,例如各种纳米结构的 TMP,包括纳米颗粒 [25, 26]、纳米线 [27, 28]、纳米管 [29, 30] 和纳米棒 [31, 32] 被开发出来,其中大部分表现出良好的电催化性能。近年来,有许多报道认为高效强钴基材料因其高效、高丰度和良好的稳定性而被认为是一种很有前途的 OER 电催化剂。磷化钴 (CoP) 是 TMP 家族之一。由于CoP的新颖特性,其在电池电催化和光催化中的应用受到了广泛关注。它为电化学反应提供了大量的活性位点,以促进电催化活性[33]。 CoP不仅解决了Ru和Ir电催化剂储量不足、价格高、稳定性差的问题,而且对OER具有良好的催化性能[34, 35]。此外,CoP具有中性耐碱性,有利于电化学稳定性。然而,CoP的导电性较差,严重影响了其电催化活性[36]。
金属有机框架 (MOF) 是一系列具有可调结构的可调有机-无机杂化材料 [37, 38]。简而言之,金属离子在原子水平上均匀分散在 MOFs 前驱体中,并且 MOFs 中有机配体的存在使它们能够在不引入外部碳源的情况下被煅烧成各种碳材料 [39]。作为制备 TMP 的通用前体,MOF 化合物由于其大比表面积、高孔隙率和结构协调性而被广泛研究 [40, 41]。一般来说,MOFs 碳化过程需要高温煅烧,这会破坏原有的 MOFs 结构并导致金属中心的团聚[42]。 MOFs直接用作电催化剂可以利用其良好的结构,但其稳定性相对较低,催化活性较差,尤其是在强碱性和酸性溶液条件下[43, 44]。如果设计合理,将 TMPs 和 MOFs 结合的混合电催化剂不仅提高了内在催化活性,而且利用了 MOFs 明确的多孔结构。更重要的是,配位不饱和金属MOFs的中心更有利于吸附含氧物质,这将进一步提高催化性能[45]。
在此,我们报告了通过原子层沉积 (ALD) 技术制备源自 N 掺杂多孔 MOF 纳米片 (NPM) 的纳米管 (CNT),其中 Co/CoP 纳米颗粒封装在纳米管的尖端。 Co-MOF 的受控部分在磷化过程中产生 Co/CoP 物种,从而产生具有大比表面积的混合纳米结构。所制备的产品用作电催化剂,在 OER 和 ORR 的电化学性能方面表现出双功能特征。 ORR的起始电位为0.93 V,而过电位约为342 mV,塔菲尔斜率为74 mV dec −1 对于 OER。此外,该电催化剂对两种反应均表现出优异的稳定性。
方法
材料
氢氧化钾 (KOH)、2-甲基咪唑 (C4H6N2)、次磷酸钠 (NaH2PO2) 和六水硝酸锌 (Zn(NO3)2·6H2O) 购自上海麦克林生化科技有限公司。钴茂 ((η5-C5H5 )2Co) 购自苏州福纳诺有限公司。以上化学品均为分析纯。 Nafion溶液(5 wt%)购自上海和森有限公司
电催化剂的合成
首先,将包含0.33 g亚硝酸锌六水合物的90 mL去离子水缓慢加入另一种制备的包含0.985 g 2-甲基咪唑的90 mL去离子水溶液中,然后在25 °C下连续搅拌24 小时。将此混合物用无水乙醇离心数次,在70 ℃环境空气中干燥,最终得到白色粉末,记为NPM。
通过使用KEMICRO PEALD-200A(Kemin Co. Ltd,China)的设备沉积电催化剂(表示为NPMCNT)。在 PE-ALD 过程中,Cobaltocene (CoCp2) 用作 Co 源,氧等离子体 (O2, 99.999%) 用作 O 源。该沉积过程在真空反应室中在 200 °C 下沉积,氩气(Ar,99.999%)作为载气用于吹扫多余的源。 Co 源温度为 100 °C。第二个源(氧等离子体)保持在 25 °C。沉积过程包括 200 个循环,每个循环包括 4 个步骤:Co 源、Ar、氧等离子体和 Ar。 Co源和氧等离子体的剂量时间分别为3和20 s,Ar吹扫时间为50 s。将得到的粉末在925 ℃下在N2下退火2 h,升温速率为2 ℃ min -1 .收购的产品名为NPMCNT。
将上述得到的10 mg NPMCNT电催化剂置于管式炉上游,300 mg次磷酸钠置于管式炉下游,然后在350 ℃下在N2下退火2 h,升温速率为2 ℃ min -1 .收购的产品命名为NPMCNT-300。 NPMCNT-50、NPMCNT-100、NPMCNT-200和NPMCNT-400的制备方法相同,但次磷酸钠用量分别改为50、100、200和400 mg。
物理特性
通过使用 Cu Kα 辐射的 X 射线粉末衍射(XRD,Empyrean,PANalytical)获得微晶结构。通过场发射扫描电子显微镜(FESEM,JSM-7800F)确认形态。通过透射电子显微镜(FETEM,JEM-200)观察微观结构。元素分布通过能量色散X射线光谱法(EDS,JEM-F200)测量。通过X射线光电子能谱(XPS,K-Alpha+)收集键能的关系。在BELSORP-max II仪器上收集氮吸附-解吸等温线。
电化学测量
将 5 mg NPMCNT-300 电催化剂加入到含有 100 μm Nafion(5 wt%,杜邦公司)和 1 mL 无水乙醇的混合溶液中,然后用超声波处理 30 分钟以形成均匀的混合物。将12微升均质混合物滴在预先抛光的玻碳电极上数次,然后在室温下自然干燥。
所有电化学测量均由 CHI760E 工作站(中国)与三电极系统测量。使用旋转环盘电极(RRDE,Φd =4 mm,ΦPt 环 =内/外环直径 5.0/7.0 mm,ALS,日本)在 0.1 M KOH 中研究 ORR 和 OER 活性。带有沉积电催化剂的光滑碳电极、铂丝和 Ag/AgCl 电极分别用作工作电极、反电极和参比电极。采用线性扫描伏安(LSV)技术测试电化学催化活性,电压范围为1.1653~0.1653 V(vs. RHE),电极转速1600 rpm,扫描速率5 mV s -1 在 0.1 M KOH 电解液中。所有电位值通过以下公式转换为可逆氢电极 (RHE) 的电位值:
$$ {E}_{\mathrm{RHE}}={E}_{\mathrm{Ag}/\mathrm{AgCl}}+0.0591\times \mathrm{pH}+0.197\ \left(\mathrm{V }\对)。 $$ (8)在不同的各种转速下(400、625、900、1225、1600和2025 rpm),转移电子数的值(n ) 由 RDE 获得的 ORR 期间的 LSV 曲线的可通过以下 Koutecky-Levich (K-L) 方程计算:
$$ \frac{1}{j}=\frac{1}{j_k}+\frac{1}{j_d}=\frac{1}{nFK{C}_{O_2}}+\frac{1} {B{\omega}^{\raisebox{1ex}{$1$}\!\left/ \!\raisebox{-1ex}{$2$}\right.}} $$ (9) $$ B=0.2{ nFC}_{O_2}{D}_{O_2}^{\raisebox{1ex}{$1$}\!\left/ \!\raisebox{-1ex}{$3$}\right.}{V}^{ \raisebox{1ex}{$-1$}\!\left/ \!\raisebox{-1ex}{$6$}\right.} $$ (10)其中 j 是测得的电流密度,j k 是估计的动力学极限电流密度,n 是每个氧分子转移的电子总数。 F 是法拉第常数 (F =96,485 C mol −1 ), 和 ω 是圆盘的角速度 (ω =2πN, N 是线性转速),\( {C}_{{\mathrm{O}}_2} \) 是电解质中 O2 的整体浓度(0.1 M KOH,1.2 × 10 −6 mol cm −3 ), \( {D}_{{\mathrm{O}}_2} \) 是 O2 在电解质中的扩散系数 (1.9 × 10 −5 厘米 2 s −1 ), ν 是电解质的运动粘度 (0.01 cm 2 s −1 ), k 是电子转移速率常数。当转速以 rpm 表示时,通常接受常数 0.2。电子转移数 (n ) 和通过 RRDE 测量测试的 H2O2 产率,并通过以下公式通过环和盘电流计算:
$$ n=4\times \frac{I_{\mathrm{disk}}}{I_{\mathrm{disk}}+{I}_{\mathrm{ring}}/N} $$ (11) $$ {\mathrm{HO}}_2^{-}\left(\%\right)=100\times \frac{2{I}_{\mathrm{ring}}/N}{I_{\mathrm{disk} }+{I}_{\mathrm{ring}}/N} $$ (12)其中我 环和我 盘分别是环电流和盘电流。 N 使用 [Fe(CN)6] 4−/3− 将值调整为 0.43 氧化还原对。
电化学活性表面积 (ECSA) 在不同扫描速率 (5–35 mV s -1 ) 和 0~0.15 V (vs. Ag/AgCl) 通过循环伏安法 (CV) 测量。
结果与讨论
XRD 和 SEM 表征
在图 1a 中,在不同磷源摄入量下 NPMCNT 复合材料的 XRD 图中显示了 Co(PDF no.15-0806)和 CoP(PDF no.29-0497)的典型图案。值得注意的是,磷化过程中不同磷源的摄入会导致形成不同的产物。当磷源为50、100、200 mg时,明显出现了Co2P在40.7°的特征峰。但当磷源摄入量增加到300和400 mg时,Co2P的特征峰消失。因此,当使用后者质量的磷源时,获得了 Co/CoP 杂化物。 20°和30°之间显示的特征峰是由于MOFs煅烧后形成的碳布。在图 1b 中可以观察到,NPM 在高温热解后呈现六边形片状结构,图 1c 显示在 NPM 片材表面均匀生成 CNT。在此,根据我们之前的工作 [1],在 200 °C 下通过 ALD 在 NPM 表面沉积 CoOx,在 925 °C 下将其还原为 Co,并生长纳米管。当磷源摄入量为400 mg时,纳米管已经结合在一起,而不是如图1d所示的单个分布。
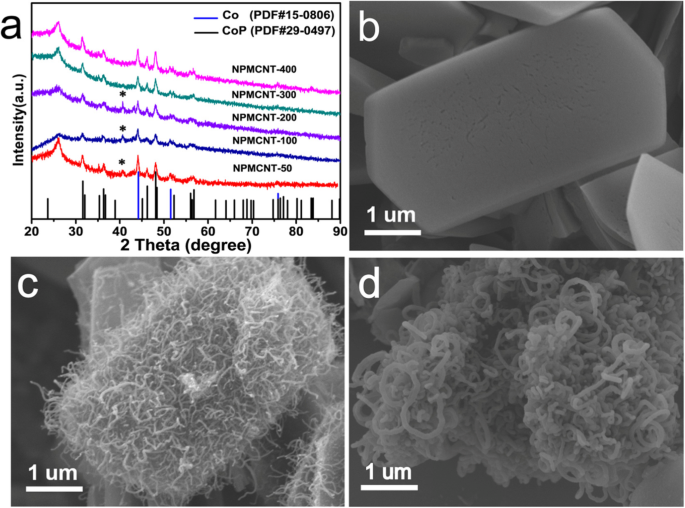
a XRD图谱。 b 的 SEM 图像 NPM,c NPMCNT-300,d NPMCNT-400
TEM 表征
TEM 观察显示了整个 NPMCNT-300 的全貌。显然,MOF 的整体形态得以保留,并且在边缘清晰可见大量纳米管,并且纳米颗粒被封装在碳纳米管中(图 2a)。图 2b 中的高分辨率 TEM 进一步证明了纳米颗粒封装在碳纳米管尖端。 Co纳米粒子将催化从MOFs衍生出CNTs,这可以提高整个混合结构的导电性。很少有石墨碳层可以防止嵌入的 Co 和 CoP 纳米粒子在电催化过程中受到腐蚀、聚集和氧化,从而在恶劣的环境中具有出色的耐久性和稳定性。此外,源自MOFs的N掺杂CNTs结构提供了一种有效的方式来调整电催化剂的电子结构,从而提高催化性能。图2c中的平面间距确定为0.244和0.231 nm,分别与CoP纳米颗粒的(102)和(201)晶面相同。 EDS 分析(图 2d)进一步证实纳米颗粒被封装在 CNT 的尖端,映射图像还显示 P 不仅存在于 CoP 纳米颗粒中,而且还存在于 CNT 中。 N掺杂的碳负载纳米材料可以由有机单体(2-甲基咪唑)通过热处理获得,无需任何外部来源。对于磷掺杂,NaH2PO2 作为磷源,通过在 350 °C 的热处理将掺杂到碳结构中。在这项工作中,不同杂原子的掺杂可以改变电催化剂的化学结构和电子结构,从而使衍生的纳米管表面具有更多的催化活性位点。一些报道表明,碳缺陷可以通过调整碳的电子结构和表面极性来产生活性位点,从而提高电催化性能。因此,掺杂多个杂原子的碳基磷化钴纳米复合材料具有更优异的电催化活性[46,47,48]。
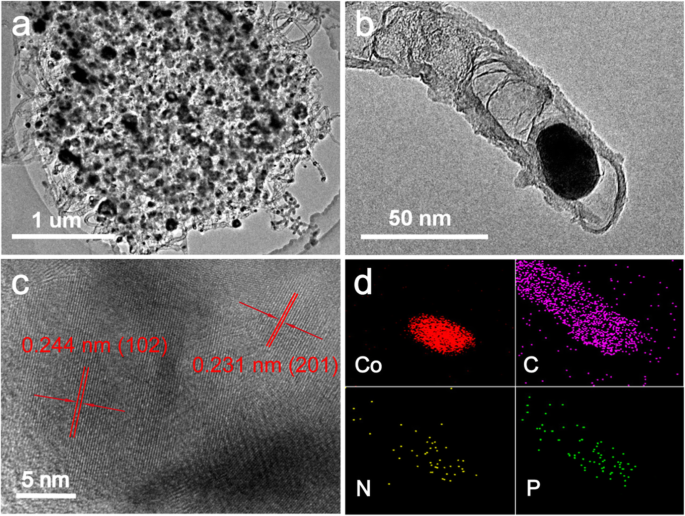
a 的 TEM 图像 NPMCNT-300 电催化剂和 b 封装在源自碳层的 CNT 尖端中的 CoP 纳米粒子。 c NPMCNT-300 电催化剂的 HRTEM 图像。 d NPMCNT-300电催化剂TEM图像区域对应的EDS元素映射
XPS 表征
NPMCNT-300 电催化剂的种类和元素组成由 XPS 确定,图 3a 显示了调查光谱中 Co、P、N、C 和 O 元素的存在。图 3b 中的 Co 2p 光谱显示以 778.6 和 781.6 eV 为中心的峰连接到 Co 2p3/2,793.9 和 797.5 eV 分别归因于 Co 2p1/2。集中在 778.9 eV 和 793.9 eV 的峰与 Co 3+ 相关 , 其他峰集中在 781.6 eV 和 797.5 eV 连接到 Co 2+ .此外,以 786.2 和 803 eV 为中心的强卫星峰归因于 Co 3+ [21, 49,50,51]。如图 3c 所示,在 P 2p 光谱中,129.8 eV 的波段与 P 2p3/2 相连,而 130.3 eV 的波段对应于 P 2p1/2。 129.8 和 130.3 eV 的两个峰值与 CoP 相关。 134.0 eV 处的另一个峰归因于 P-C,而位于 134.8 eV 处的峰与 P-O 相关 [41, 52, 53]。这些结果证实了 NaH2PO2 作为磷源掺杂到 CNTs 中并形成 CoP。在图 3d 中,C1 s 光谱分为四个峰(284.7、285.2、286.4 和 288.4 eV)。强峰集中在 284.7 eV,对应 sp 2 C =热解石墨的 C 能量。峰值 (285.2 eV) 与 C-P 矩阵相关联到 sp 2 C与芳环中的P键合。此外,286.4 eV 的峰值归属于 C-O 带。此外,288.4 eV 的峰值与 C =O [30, 50, 54, 55] 相关。 NPMCNT-300 的高分辨率 N1 s 峰如图 3e 所示,它可以由位于 398.8、400.3 和 401.2 eV 的三个峰拟合,分别与吡啶 N、吡咯 N、石墨 N [56, 57 ]。上述XPS结果表明P和N通过取代O或C原子掺杂到CNTs的缺陷位。
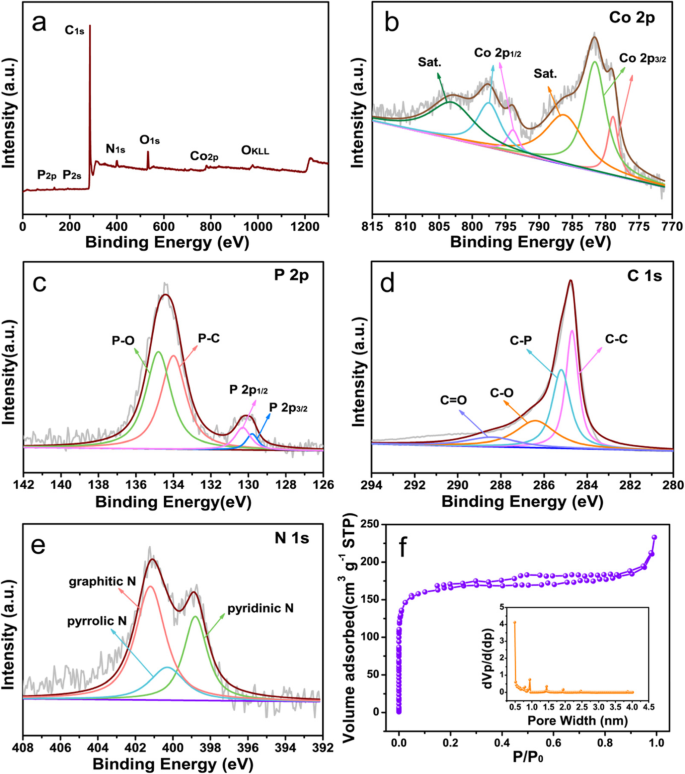
一 NPMCNT-300 电催化剂的 XPS 光谱。 b NPMCNT-300 电催化剂的 Co 2p XPS 光谱。 c NPMCNT-300 电催化剂的 P 2p XPS 光谱。 d NPMCNT-300 电催化剂的 C1 s XPS 谱。 e NPMCNT-300 电催化剂的 N1 s XPS 谱。 f N2吸附-解吸等温线及相应的孔径分布曲线
Brunauer–Emmett–Teller (BET) 表征
NPMCNT-300 的氮吸附/解吸等温线如图 3f 所示。值得一提的是,等温线显示出 IV 型滞后环,这表明 NPMCNT-300 中存在大量介孔/微孔 [58, 59]。 NPMCNT-300电催化剂的BET表面积值为641 m 2 g −1 这些结果表明,在 NPMCNT-300 合成过程中纳米管的存在可以大大增加电催化剂的比表面积和孔体积。这种具有大比表面积的独特多孔结构被认为对反应物分子的氧吸收和运输以及最活性物质的暴露很重要。
电催化性能和讨论
使用 ORR 的三电极系统测试电催化活性。在图 4a 中,LSV 曲线是在 O2 饱和电解质中检查的。 NPMCNT、NPMCNT-50、NPMCNT-100、NPMCNT-200、NPMCNT-300 和 NPMCNT-400 的起始电位分别为 0.80、0.89、0.91、0.90、0.93 和 0.89 V(相对于 RHE)显然,NPMCNT-300 表现出最高的电催化活性。与40% Pt/C(0.993 V vs. RHE)相比,前者的性能稍弱,但NPMCNT-300s的扩散限制电流密度接近6 mA cm -2 , 优于 Pt/C (5.1 mA cm −2 )。图 4b 显示了 NPMCNT-300 在不同旋转速度(从 625 到 2025 rpm)下的典型 LSV 曲线。 NPMCNT-300 ORR过程的电子转移数在电位为0.35~0.65 V时计算接近4,证实了四电子转移途径(图4c)。为了估计 ORR 动力学,通过 RRDE 方法测量了电子转移的数量和 H2O2 的产率。相应的环电流是用铂环电极同时测量的,用于检测圆盘电极处的过氧化物物质(图 4d)。 NPMCNT-300 的电子转移数(图 4e)约为 3.7,这与 K-L 方程计算的数据非常吻合,表明 ORR 过程遵循有效的四电子方法。在这些电催化剂的存在下,中间的 H2O2 形成率很低,约为 17%。为了测量电催化剂的稳定性,我们在0.5 V的电压和1600 rpm的转速下,在O2饱和的0.1 M KOH电解液中使用i-t法对电催化剂进行表征。图 4f 显示了相对电流密度。在连续运行 40,000 s 后,NPMCNT-300 保持了 94% 的高相对电流密度,而在连续运行 10,000 s 后,Pt/C 的初始电流密度仅保留了 91%,这表明 NPMCNT-300 的稳定性300电催化剂优于40% Pt/C电极。
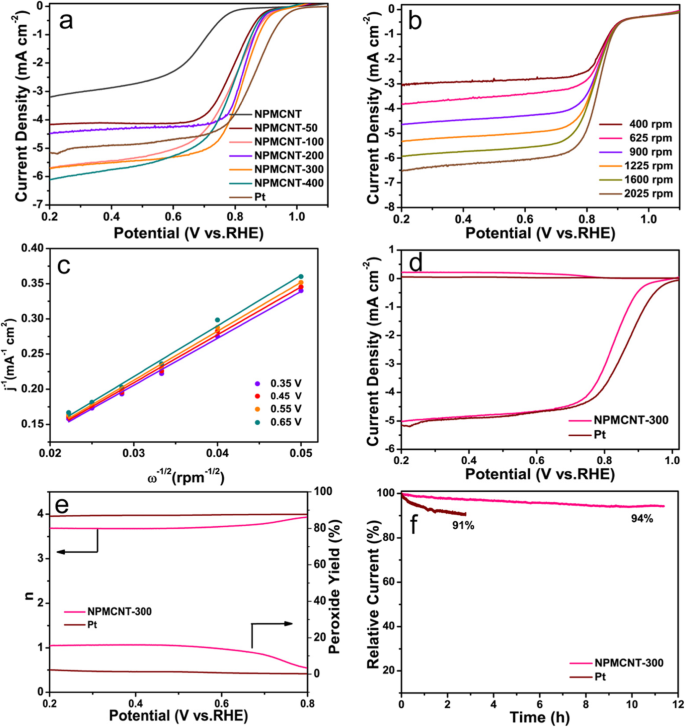
一 NPMCNT、NPMCNT-50、NPMCNT-100、NPMCNT-200、NPMCNT-300、NPMCNT-400 和 20% Pt/C 电催化剂的线性扫描伏安曲线。 b NPMCNT-300电催化剂在不同转速下的转盘电极伏安图。 c Koutecky-Levich 图 (j 是测得的电流密度,ω 是圆盘的角速度 (ω =2πN , N 是线性转速),d 旋转环盘电极伏安图,e 电子转移的估计值 (n ) 和过氧化物产率,以及 f NPMCNT-300和Pt/C电催化剂的耐久性测试
为了评估NPMCNT-300的OER电催化性能,在5 mV s -1 的扫描速率下测试了LSV曲线 .在图 5a 中,NPMCNT-300 电催化剂的过电位为 342 mV,相当于 RuO2 电催化剂的电位(340 mV)。而对于 NPMCNT,NPMCNT-50、NPMCNT-100、NPMCNT-200 和 NPMCNT-400 分别为 579、488、461、418 和 430 mV。图5b表明NPMCNT-300电催化剂的Tafel斜率为74 mV dec -1 对于 NPMCNT、NPMCNT-50、NPMCNT-100、NPMCNT-200 和 NPMCNT-400,分别为 266、170、190、137、156 mV dec -1 , 分别。虽然 NPMCNT-300 电催化剂低于 RuO2 (88 mV dec −1 ),因此证明了 NPMCNT-300 电催化剂的优异 OER 动力学。该结果表明,NPMCNT-300 对于 OER 具有与 RuO2 一样优异的电催化性能。为了研究 NPMCNT-300 电催化剂的耐久性,使用了两种方法。首先,NPMCNT-300 在 KOH 电解质中进行了 1000 次循环 CV 测试(图 5c)。测试后,它显示降解略有减少(5 mV)。另一项稳定性测试是使用计时电流法。计时电流法是在未搅拌的状态下向工作电极施加一个大的阶跃电位(从法拉第反应中发生的电位跳变到电极表面电活性成分的有效电位接近零)来记录电流随时间的变化。解决方案。初始电位基于图 5d 的结果,这使得 NPMCNT-300 和 RuO2 产生 10 mA cm -2 在 iR 补偿范围内。 NPMCNT-300 电催化剂的电流在连续 9 小时内保持约 90%,而 RuO2 仅在 1 h 内损失超过 50% 的电流。两项稳定性测试均表明 NPMCNT-300 对 OER 具有出色的稳定性。 CoP与各种已报道的Co基非贵金属电催化剂在碱性介质中的电催化性能比较见表1。
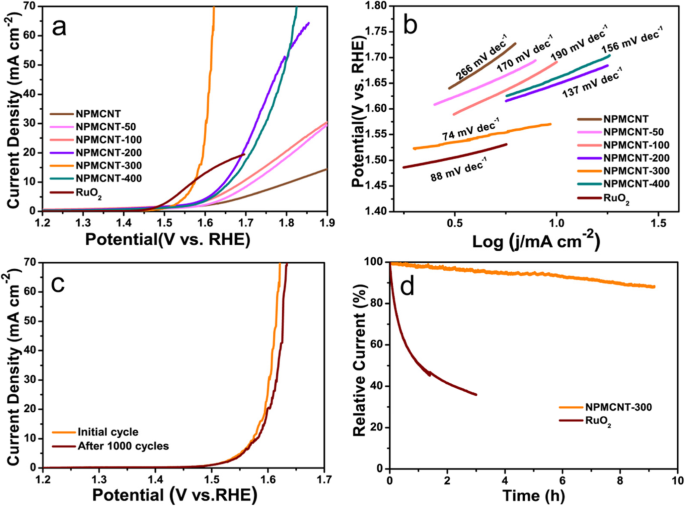
一 具有 iR 补偿的电催化剂的线性扫描伏安曲线。 b 从图a计算的电催化剂的塔菲尔图 . c 初始和 1000 循环循环伏安法后的线性扫描伏安法曲线。 d 电流型 i-t 曲线
<图>以上结果总结了不同产品对应的OER和ORR电化学性能,表明不同磷源的摄入会影响电催化剂的性能。一方面,虽然 NPMCNT-50、NPMCNT-100 和 NPMCNT-200 的电催化剂具有相似的结构,但磷含量较低,这会导致 CoP 的形成量较少。另一方面,虽然NPMCNT-400的磷含量最高,但由于碳纳米管原有结构被破坏,碳纳米管聚集在一起,电催化活性相对较差。 NPMCNT-300的特殊形貌提供了更大的比表面积和更高的CoP含量,从而提高了电化学性能。
电催化剂的电化学活性表面积(ECSA)可以进一步表明其优异的电化学活性的原因。 NPMCNT-50、NPMCNT-100、NPMCNT-200、NPMCNT-300和NPMCNT-400的双层电容(Cdl)在不同的扫描速率(0.005、0.01、0.15、0.20、0.25、0.30和0.30)下计算V s −1 ) 在图 6a-e 中。为了通过 CV 测量电化学双层电荷,从静态 CV 确定不发生显着法拉第过程的电位范围。该范围通常是以系统开路电位 (OCP) 为中心的 0.1 V 电位窗口。在此非法拉第电位区域中测量的所有电流都被认为是由于双层充电。图 6 f 显示了各种扫描速率与电催化剂在 0.1 V (vs. 银/氯化银)。双层充电电流等于扫描速率的乘积,v ,以及电化学双层电容,C dl,由方程给出。 (1):
$$ ic=v\ {C}_{\mathrm{dl}} $$ (13)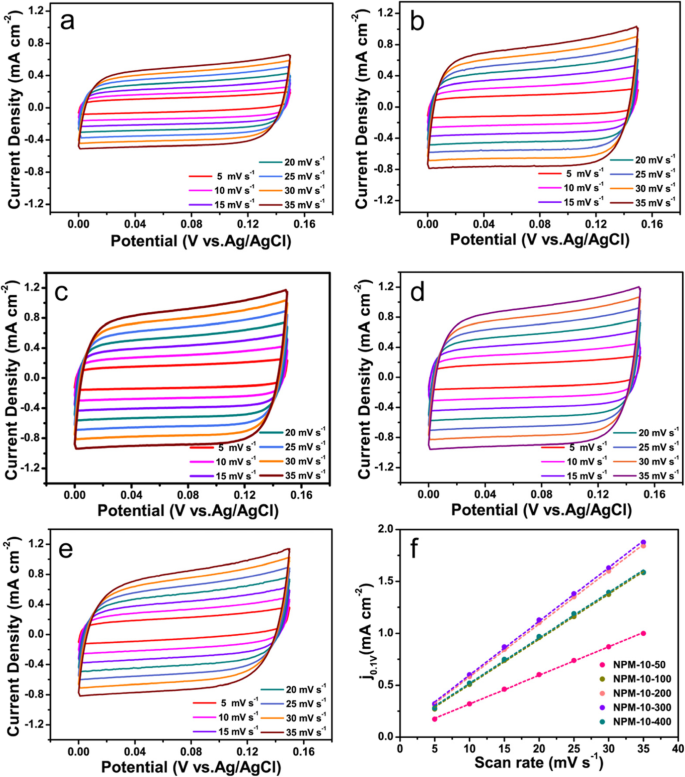
a 的循环伏安扫描 NPMCNT-50,b NPMCNT-100,c NPMCNT-200,d NPMCNT-300 和 e NPMCNT-400。 f 电催化剂电流密度与扫描速率的关系图
因此,ic 的情节 作为 v 的函数 产生斜率等于 C 的直线 dl。通过在 0.1 V(vs. Ag/AgCl)下将 Δj 与扫描速率作图,斜率是 C 的两倍 dl 可以得到如图 6f 所示。 C 线性拟合斜率的 dl 为 27.55、43.55、51、51.75 和 43.73 mF cm −2 分别用于 NPMCNT-50、NPMCNT-100、NPMCNT-200、NPMCNT-300 和 NPMCNT-400。电催化剂样品的 ECSA 由 Cdl 根据方程计算。 (2):
$$ \mathrm{ECSA}={C}_{\mathrm{dl}}/{C}_{\mathrm{s}} $$ (14)其中 C s 是样品的比电容或在相同电解质条件下每单位面积材料的原子级光滑平面的电容。通过考虑真实表面积为 1.0 cm 2 的原子级光滑平面的比电容 , 比电容 (C s) 一般在 20–60 μF cm −2 在碱性介质中。对于表面积的估计,我们使用 Cs =0.04 mF cm −2 的一般比电容 在 0.1 M KOH 中。由此,我们估计 ECSA 为 0.0689、0.1089、0.1275、0.1294 和 0.1093 m 2 用于 NPMCNT-50、NPMCNT-100、NPMCNT-200、NPMCNT-300 和 NPMCNT-400 电催化剂。因此,NPMCNT-300电催化剂表现出优异的OER和ORR性能。
结论
我们充分利用 MOFs 的有效比表面积和 CoP 的高活性来生产优异的双功能电催化剂。报道了通过原子层沉积 (ALD) 技术在 MOF 纳米片表面均匀引入钴源,以及在高温煅烧过程中衍生 N 掺杂纳米管,以及在纳米管尖端封装 Co/CoP。证实纳米管的存在为电催化剂提供了更大的比表面积。当用作双功能电催化剂时,NPMCNT-300 对 OER 和 ORR 均表现出非凡的电化学性能。它表明 ORR 的起始电位为 0.925 V,过电位约为 342 mV,塔菲尔斜率为 74 mV dec −1 对于 OER。此外,该电催化剂对OER和ORR均表现出显着的稳定性。
数据和材料的可用性
在当前研究期间生成和/或分析的数据集可根据合理要求从相应作者处获得。
缩写
- OER:
-
析氧反应
- ORR:
-
氧还原反应
- TMP:
-
过渡金属磷化物
- CoP:
-
磷化钴
- MOF:
-
金属有机骨架
- 碳纳米管:
-
碳纳米管
- NPM:
-
N掺杂多孔MOFs纳米片
- PE-ALD:
-
等离子体增强原子层沉积
- XRD:
-
X射线衍射
- FESEM:
-
场发射扫描电子显微镜
- TEM:
-
透射电子显微镜
- EDS:
-
能量色散X射线光谱
- XPS:
-
X射线光电子能谱
- RRDE:
-
旋转环盘电极
- LSV:
-
线性扫描伏安图
- RHE:
-
可逆氢电极
- K-L:
-
Koutecky-Levich
- ECSA:
-
电化学活性表面积
- 简历:
-
循环伏安法
- Cdl:
-
双层电容
纳米材料
- 用于改进诊断和治疗应用的多功能金纳米粒子:综述
- 用于癌症治疗的纳米粒子:当前的进展和挑战
- 用于超级电容器应用的石墨烯和聚合物复合材料:综述
- 用于体内 CT 成像和肾脏清除特性的新型生物相容性 Au Nanostars@PEG 纳米颗粒
- 用于电催化氧还原反应的重石墨-氮自掺杂高孔隙率碳
- 桔梗皂苷(桔梗)用于金和银纳米颗粒的绿色合成
- 分层多孔 Silicalite-1 封装的 Ag NP 的制备及其对 4-硝基苯酚还原的催化性能
- 铂钴纳米催化剂上的氧还原反应:(双)硫酸盐阴离子中毒
- Mg 掺杂对用于增强光催化评估和抗菌分析的 ZnO 纳米颗粒的影响
- 用于提高溶解度的蝌蚪形和球形血红素纳米颗粒的制备和表征
- 用碳纳米管和石墨烯改性的 FeF3·0.33H2O 高性能正极材料,用于锂离子电池
- 碳纳米管-Cu2O 纳米复合材料的简便制备作为还原对硝基苯酚的新催化剂材料


